Peptidi, proteine ed e nzim i i 1
|
|
|
- Livia Damiano
- 8 anni fa
- Visualizzazioni
Transcript
1 Peptidi, proteine ed enzimi 1
2 Gli amminoacidi possono formare catene Due amminoacidi possono unirsi tra loro attraverso il legame ammidico detto legame peptidico, tra il gruppo NH 2 di un amminoacido e quello COOH dell'altro amminoacido, con liberazione di una molecola d'acqua. L'unione di due amminoacidi genera un dipeptide. Più amminoacidi uniti tra di loro generano un biopolimero detto polipetide. 2
3 Le proteine sono polipeptidi strutturati (I) Le catene polipeptidiche possono ripiegarsi dando origine alle proteine, che sono quindi costituite da polimeri di amminoacidi. La differenza tra un polipeptide e una proteina propriamente detta, consiste nel fatto che la catena polipeptidica della proteina assume una particolare conformazione spaziale che le conferisce le sue caratteristiche funzionali (ad esempio un enzima, un anticorpo, un recettore di membrana). 3
4 Le proteine sono polipeptidi strutturati (II) La struttura della proteina è determinata dalla sua composizione amminoacidica. In particolare, la natura delle catene laterali R determina il ripiegamento dei diversi segmenti della catena secondo strutture precise. 4
5 I diversi livelli strutturali delle proteine (I) In una proteina si distinguono: la struttura primaria, ovvero la sequenza lineare degli amminoacidi della catena polipeptidica; la struttura secondaria, determinata da forme di ripiegamento assunte spontaneamente da segmenti della catena polipeptidica, in funzione della loro composizione amminoacidica; 5
6 I diversi livelli strutturali delle proteine (II) la struttura terziaria, costituita da ulteriori ripiegamenti e interazioni tra le strutture secondarie delle varie porzioni della catena. Anche questa dipende dalla natura dei gruppi R degli amminoacidi; la struttura quaternaria, costituita dall'associazione di più catene polipeptidiche a formare proteine con più subunità. 6
7 I diversi livelli strutturali delle proteine (III) 7
8 Struttura primaria: il legame peptidico (I) Il legame peptidico CO-NH- è rigido. Per questo, in una catena polipeptidica, il legame tra due amminoacidi adiacenti giace sullo stesso piano. Il carbonio centrale a cui è legata la catena laterale R (detto carbonio alfa) che non è impegnato nel legame, è l'unico elemento dello scheletro peptidico che può ruotare attorno ai suoi legami con l'atomo di azoto amminico e con il carbonio carbossilico, rispettivamente. 8
9
10 Struttura primaria: il legame peptidico (II) Quindi il legame peptidico impone una limitazione alle possibili conformazioni delle catene peptidiche. 10
11 Il legame peptidico è rigido e planare Gli atomi di Cα di amminoacidi adiacenti sono separati da tre legami covalenti: Cα C N Cα PROPRIETA DEL LEGAME PEPTIDICO 1. I 6 atomi del gruppo peptidico giacciono sullo stesso piano l ossigeno legato al carbonio del gruppo carbonilico e l atomo di idrogeno legato all azoto amminico, si trovano in trans. 2. L ossigeno carbonilico ha una parziale carica negativa e l azoto amminico ha una parziale carica positiva ciò genera un parziale dipolo elettrico. 3. I legami ammidici C-N hanno un parziale carattere di doppio legame per effetto della risonanza non possono ruotare liberamente. 4. La rotazione è permessa solo attorno ai legami N-Cα e Cα-C.
12 Il legame peptidico è rigido e planare φe ψsonodi180 quandoilpolipeptideènellaconformazionecomplanareestesae tutti i gruppi peptidici sono sullo stesso piano. φ e ψ possono assumere tutti i valori compresi tra -180 e +180, ma molti valori risultano proibiti per interferenze steriche tra gli atomi dello scheletro del polipeptide e quelli delle catene laterali.
13
14
15 Risonanza del legame peptidico Le parziali caratteristiche di doppio legame impediscono la libera rotazione attorno al legame peptidico, C-N, che costituisce così un punto di rigidità della catena polipeptidica. La barriera energetica che si oppone alla libera rotazione è circa 20 kcal/mole (84 kj/mole).
16 Studi di diffrazione ai raggi X hanno mostrato che nel gruppo peptidico il legame C-N è più breve (1.33 Å) di un normale legame C-N (1.46 Å) il legame C=O è leggermente più lungo (1.24 Å) di un normale doppio legame C=O (1.20 Å). Il legame peptidico ha quindi parziali caratteristiche di doppio legame (oltre il 40%), mentre il doppio legame C=O si comporta in parte (40%) come un legame singolo. Tutto ciò trova giustificazione nel fenomeno della risonanza del gruppo peptidico fra due strutture limite
17
18
19 peptidi, polipeptidi e proteine gli aminoacici sono uniti tra loro da legami peptidici energia di legame 100 Kcal/mol # aminoacidi peptide (oligopeptide) <20 polipeptide <60 proteina >60 non vengono rotti con l ebollizione, ma solo con l azione prolungata di acidi o basi concentrate gli enzimi proteolitici sono in grado di rompere tali legami esistono sequenze lunghe da pochi aminoacidi a migliaia di aminoacidi con peso molecolare da 5 a 1000 KDalton (1 Dalton = 1/12 massa 12 C)
20 Struttura secondaria: l'alfa-elica Nel 1951 Linus Pauling e Robert Corey, studiando la cheratina (una proteina fibrosa presente ad esempio nei capelli e nella lana) dimostrarono che le catene polipeptidiche possono avvolgersi lungo il proprio asse formando una struttura elicoidale detta alfa elica. Nella cheratina della lana, sette alfa eliche sono avvolte una sull'altra formando una fibra. α-cheratina dei capelli umani 20
21 Alfa elica: struttura (I) Tutti gli amminoacidi naturali hanno conformazione L. Si è visto che L-amminoacidi formano preferenzialmente alfa eliche destrogire. L'alfa elica ha uno scheletro elicoidale, in cui ogni giro d'elica comprende 3,6 amminoacidi e costituisce un' unità ripetitiva. Tra due unità successive si formano legami idrogeno tra l'atomo di idrogeno legato al gruppo NH- del legame peptidico e l'atomo di ossigeno legato al gruppo -CO- del legame peptidico posto a quattro amminoacidi di distanza (cioè sul giro d'elica successivo). 21
22 Alfa elica: struttura (II) 22
23 Alfa elica: struttura (III) Il gruppi R degli amminoacidi, orientati verso l'esterno dell'elica, determinano la tendenza di un segmento peptidico a formare un alfa elica. Polipeptidi formati da amminoacidi privi di carica (come l'alanina) formano spontaneamente alfa eliche, mentre polipeptidi di amminoacidi con la stessa carica (come la lisina) non lo fanno a causa della repulsione tra le cariche delle catene R. Catene ingombranti (come quella dell'isoleucina) impediscono la formazione di alfa eliche se si ripetono a distanza ravvicinata in una stessa catena polipeptidica, a causa della collisione tra le catene R e i carboni alfa. 23
24 Struttura secondaria: il foglietto beta Studiando i cambiamenti di conformazione della cheratina al calore, Pauling e Corey dimostrarono l'esistenza di una seconda struttura secondaria: il foglietto beta. La cheratina dei capelli, ad esempio, normalmente assume una conformazione ad alfa elica (detta alfa-cheratina) che le conferisce elasticità. Se si scalda l'alfa-cheratina, si rompono i legami idrogeno tra le unità dell'elica e la proteina assume una forma più allungata e rigida: la beta-cheratina, fatta di foglietti beta. Per questo i parrucchieri per "stirare" i capelli li scaldano prima. 24
25 Il foglietto beta: struttura (I) Nel foglietto beta le catene polipeptidiche si dispongono parallelamente. A causa della rigidità del legame peptidico, le catene non sono planari ma assumono una conformazione "a fisarmonica". Ciascun gruppo NH del legame peptidico forma un legame idrogeno con il gruppo CO del legame peptidico a lui corrispondente sulla catena parallela. 25
26 Il foglietto beta: struttura (II) Nel foglietto beta le catene laterali R si dispongono sopra e sotto il piano del foglio. Generalmente richiede catene polipeptidiche ricche di amminoacidi con gruppi R piccoli senza carica (come glicina e alanina), poiché catene ingombranti andrebbero a collidere tra di loro. Similmente, se gruppi R con la stessa carica si susseguissero a distanza ravvicinata, la repulsione impedirebbe la formazione del foglietto. L'alfa elica è una struttura elastica ma il foglietto beta è rigido. La fibroina (proteina della seta) è formata da foglietti beta: questo spiega perché la lana è elastica e la seta no. 26
27 Struttura terziaria Le proteine sono costituite da catene polipeptidiche molto lunghe: una proteina "media" ha amminoacidi, ma ci sono proteine con migliaia di amminoacidi. Diversi segmenti di queste lunghe catene possono assumere conformazioni a foglietto beta, alfa elica o anche rimanere non strutturate. Le diverse strutture secondarie, a loro volta, si ripiegano in complesse conformazioni spaziali, caratteristiche di ciascuna proteina. È questa la struttura terziaria. 27
28 Il ripiegamento delle proteine (I) Le proteine assumono la struttura terziara in un processo detto ripiegamento (folding). Un primo ripiegamento avviene già durante la sintesi proteica nella cellula, mano a mano che la catena polipeptidica esce dal ribosoma. In questa fase, ad esempio, nell'ambiente acquoso i segmenti con amminoacidi idrofobici tenderanno a ripiegarsi all'interno, lasciando all'esterno i gruppi idrofili. Nelle proteine solubili, gli amminoacidi con gruppi idrofili (rappresentati dai quadrati) si dispongono sulla superficie. 28
29 Il ripiegamento delle proteine (II) Una volta sintetizzata, la proteina parzialmente ripiegata entra nel reticolo endoplasmatico della cellula, dove il ripiegamento si completa grazie alla presenza di particolari proteine dette ciaperoni (chaperons), che avvolgono la catena polipeptidica e favoriscono il processo di ripiegamento. Il funzionamento delle proteine chaperoniche DnaK e DnaJ nel batterio Escherichia coli 29
30 Il ripiegamento delle proteine (III) La struttura terziaria è stabilizzata da legami intramolecolari tra le catene R degli amminoacidi. Oltre ai legami idrogeno e alle interazioni elettrostatiche tra amminoacidi con carica opposta, sono spesso presenti ponti disolfuro -S-S-. Si tratta di legami covalenti dovuti all'ossidazione dei gruppi tiolici -SH delle cisteine. 30
31 Struttura terziaria e funzione La struttura terziaria conferisce le principali proprietà funzionali alle proteine, per questo proteine con proprietà simili hanno spesso una struttura terziaria simile. Ad esempio, proteine fibrose come la cheratina o il collagene hanno forma allungata, sono insolubili in acqua e formano strutture robuste. Le proteine solubili invece tendono ad una forma sferica e sono dette globulari. Proteine ancorate alla membrana della cellula ma che devono anche sporgere nel mezzo acquoso, come i recettori, hanno un dominio idrofobico esteso che attraversa la membrana e uno globulare che sporge all'esterno. 31
32 Struttura terziaria e funzione: i recettori I recettori proteici sono proteine presenti alla superficie della cellula in grado di legare molecole o altre proteine presenti nello spazio extracellulare. Il sito di legame assume una struttura terziaria specifica per accogliere un certo ligando. Ad esempio il recettore dell'ormone adrenalina è selettivo per la forma enantiomerica L, grazie alla disposizione nel sito attivo di gruppi di amminoacidi idrofobici e carichi negativamente in grado di interagire con la porzione idrofobica e carica positivamente della molecola di adrenalina. 32
33 Legame ormone-recettore Un recettore è selettivo nei confronti di un solo enantiomero, come una mano che interagisce con un altro oggetto chirale. 33
34 Struttura terziaria e funzione: gli enzimi Un'altra importante classe di proteine le cui funzioni dipendono strettamente dalla struttura terziaria sono gli enzimi. Gli enzimi sono dei catalizzatori biologici la cui funzione è rendere possibile lo svolgimento delle reazioni chimiche del metabolismo cellulare. 34
35 Le reazioni chimiche richiedono energia In ogni reazione chimica, due o più molecole (i substrati) si combinano per generare una o più nuove molecole (i prodotti). Questo processo comporta la rottura di legami chimici dei substrati e la formazioni di nuovi legami nei prodotti. L'energia richiesta per rompere i legami dei substrati e generare i prodotti è detta energia di attivazione, in quanto serve a portare le molecole dei substrati in uno stato di transizione o stato attivato, in cui possono combinarsi nei prodotti. 35
36 A cosa servono gli enzimi Alcune reazioni hanno una bassa energia di attivazione, per cui il calore presente nell'ambiente cellulare (circa 37 C) è sufficiente ad attivare i substrati. Un esempio è la reazione spontanea tra gruppi aldeidici e alcolici degli zuccheri, a formare la forma chiusa semiacetalica. La maggior parte delle reazioni metaboliche (ad esempio la glicolisi o l'ossidazione degli acidi grassi) tuttavia ha un'energia di attivazione elevata e non avverrebbe praticamente mai spontaneamente nelle condizioni cellulari. 36
37 Profilo energetico di reazione Gli enzimi servono ad abbassare l'energia di attivazione per passare dai substrati ai prodotti, rendendo possibili le reazioni del metabolismo cellulare. Come si vede dall'immagine, il salto di energia necessario per attivare i substrati è minore in presenza degli enzimi (curva blu). 37
38 Come funzionano gli enzimi Gli enzimi possiedono tasche di legame altamente specifiche per i substrati di una certa reazione. Possono così avvicinare i due substrati in modo che i loro gruppi reattivi siano nella posizione ottimale. Inoltre, gli enzimi possiedono una tasca detta sito attivo, in cui le catene R degli amminoacidi prendono contatto con i gruppi reattivi dei substrati facilitando la sintesi dei prodotti. 38
39 Legame enzima-substrato L'enzima forma con il substrato il complesso ES (enzima-substrato), grazie alla complementarietà del suo sito di legame in cui catene laterali R degli amminoacidi sono posizionate in maniera ottimale per interagire con le porzioni corrispondenti della molecola di substrato. 39
40 Il complesso ES è un sistema dinamico La formazione del complesso ES procede solitamente attraverso due passaggi: il substrato entra nel sito di legame attraverso la complementarietà strutturale (modello chiave- serratura); l'interazione del substrato con l'enzima causa una modificazione della struttura terziaria di quest'ultimo che assume la conformazione attiva in cui i substrati sono correttamente posizionati per la catalisi (adattamento indotto). 40
41 Gli enzimi sono regolati (I) Oltre a rendere possibile le reazioni metaboliche, gli enzimi sono importanti punti di regolazione. La loro attività può essere regolata: dalla concentrazione dei substrati e dei prodotti; dal ph; da cofattori essenziali per la reazione come gli ioni metallici Ca 2+, Mg 2+, Mn 2+, Zn 2+ ; dalla temperatura. 41
42 Gli enzimi sono regolati (II) Esistono inoltre molecole o addirittura piccole proteine che, legandosi ad un enzima lo possono attivare o inibire. Agendo sugli enzimi, la cellula è in grado di operare una fine regolazione della velocità delle sue vie metaboliche. Schema generale della regolazione enzimatica: C e R indicano rispettivamente la subunità catalizzatrice e quella regolatrice dello stesso enzima 42
43 Nomenclatura degli enzimi (I) Le migliaia di enzimi esistenti possono essere raggruppati in 6 classi principali in base al tipo di reazione che catalizzano. A loro volta queste classi sono divise in sotto- e sotto-sottoclassi. 43
44 Nomenclatura degli enzimi (II) Ad ogni enzima è assegnato (oltre ad un nome comune) un numero che lo identifica. Il codice assegnato all enzima lattato deidrogenasi 44
45 Struttura quaternaria (I) Molte proteine ed enzimi sono in realtà complessi formati da più subunità. Ogni subunità è una proteina essa stessa, ma solo la loro associazione conferisce al complesso le sue proprietà funzionali. Questa associazione è detta struttura quaternaria. 45
46 Struttura quaternaria (II) Un esempio è l'emoglobina, che ha quattro subunità di due tipi differenti. Grazie ai loro gruppi eme, le quattro subunità insieme generano il principale trasportatore di ossigeno cellulare. 46
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale:
 Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 2
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Macromolecole Biologiche. I domini (I)
 I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B
 Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Laura Beata Classe 4 B Concorso Sperimento Anch io Silvia Valesano Classe 4 B RELAZINI DI LABRATRI (Italiano) Titolo: : Cosa mangiamo veramente? Scopo: 1. Scoprire in quali alimenti ci sono o non ci sono
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
BIOLOGIA GENERALE. Alessandro Massolo Dip. Biologia Animale e Genetica c/o Prof. F. Dessì-Fulgheri (Via Romana 17) massolo@unifi.
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Macromolecole Biologiche. I domini (II)
 I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 9
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 9 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 9 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
DNA - RNA. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi.
 DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
NUCLEOTIDI e ACIDI NUCLEICI
 NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
La biochimica è anche definita la chimica del C :
 Tutte le cellule viventi sono composte da macromolecole simili, costituite dalle stesse piccole molecole di base. La grande diversità è data dalle diverse combinazioni di 4 principali elementi C H O N
Tutte le cellule viventi sono composte da macromolecole simili, costituite dalle stesse piccole molecole di base. La grande diversità è data dalle diverse combinazioni di 4 principali elementi C H O N
Elettroforesi. Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita.
 Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Elettroforesi Elettroforesi: processo per cui molecole cariche si separano in un campo elettrico a causa della loro diversa mobilita. A qualunque ph diverso dal pi le proteine hanno una carica netta quindi,
Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che
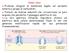 Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini.
 I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
Regione cerniera monomero regione cerniera
 Regione cerniera Tutte le Ig, sia quelle secrete che quelle presenti sulla membrana plasmatica dei linfociti B, sono costituite da quattro catene proteiche, due pesanti (H, da heavy, in rosso nel disegno)
Regione cerniera Tutte le Ig, sia quelle secrete che quelle presenti sulla membrana plasmatica dei linfociti B, sono costituite da quattro catene proteiche, due pesanti (H, da heavy, in rosso nel disegno)
Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine.
 Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
LA CHERATINA. CORSO COSMETOLOGIA- DOTT.SSA B. SCARABELLI (www.cosmesinice.it) PROTEINA: unione di più aminoacidi
 PROTEINA: unione di più aminoacidi LA CHERATINA AMINOACIDO: molecola unità di base; ce ne sono 20 di cui 8 sono essenziali (da introdurre solo con i cibi) La struttura delle proteine vien suddivisa in
PROTEINA: unione di più aminoacidi LA CHERATINA AMINOACIDO: molecola unità di base; ce ne sono 20 di cui 8 sono essenziali (da introdurre solo con i cibi) La struttura delle proteine vien suddivisa in
«Macromolecole» Lipidi
 LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas
 1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
1 Tratto dal libro Come vivere 150 anni Dr. Dimitris Tsoukalas Capitolo 7 Enzimi, le macchine della vita Piccole macchine regolano la funzione del corpo umano in un orchestrazione perfetta e a velocità
Dall RNA alle proteine. La traduzione nei procarioti e negli eucarioti
 Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Dall RNA alle proteine La traduzione nei procarioti e negli eucarioti Codice genetico La sequenza dell mrna viene decodificata a gruppi di tre nucleotidi, e tradotta in una sequenza di amminoacidi 4 x
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca
 INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
INTERVENTO DI CLAUDIA RICCARDI PLASMAPROMETEO - Dipartimento di Fisica Università degli Studi di Milano - Bicocca La ricerca come strumento per lo sviluppo aziendale: sinergia tra università e industria
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
aa 2013-14 Proteine Struttura delle Proteine α Amminoacidi
 Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
la struttura tridimensionale può essere ottenuta solo per Un intero dominio in genere da 50 a 300 residui
 Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
BIOMOLECOLE STRUTTURA E FUNZIONE
 BIOMOLECOLE STRUTTURA E FUNZIONE Lo studio delle relazioni tra struttura e funzione nelle biomolecole è uno degli aspetti più importanti per la comprensione del funzionamento dei processi biologici La
BIOMOLECOLE STRUTTURA E FUNZIONE Lo studio delle relazioni tra struttura e funzione nelle biomolecole è uno degli aspetti più importanti per la comprensione del funzionamento dei processi biologici La
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
4x4x4=4 3 =64 codoni. 20 aminoacidi
 4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
Figura 1. Rappresentazione della doppia elica di DNA e struttura delle differenti basi.
 Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
Sommario La molecola di DNA è deputata a conservare le informazioni genetiche necessarie per lo sviluppo ed il funzionamento degli organismi viventi. Poiché contiene le istruzioni per la costruzione delle
Le proprietà periodiche degli elementi LA LEZIONE
 Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
Le proprietà periodiche degli elementi LA LEZIONE Le proprietà degli elementi mostrano delle tendenze che possono essere predette usando il sistema periodico ed essere spiegate e comprese analizzando la
SINTESI PROTEICA. Replicazione. Trascrizione. Traduzione
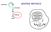 Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Replicazione SINTESI PROTEICA Trascrizione Traduzione 61 codoni codificanti 3 triplette non senso (STOP) AUG codone di inizio codone per Met Caratteristiche del codice genetico Specificità Il codice genetico
Le proteine. Polimeri composto da 20 diversi aminoacidi
 Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
SISTEMI ENERGETICI. L ATP privato di uno dei suoi 3 radicali fosforici diventa ADP (adenosindifosfato).
 SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
SISTEMI ENERGETICI LE FONTI ENERGETICHE MUSCOLARI I movimenti sono resi possibili, dal punto di vista energetico, grazie alla trasformazione, da parte dei muscoli, dell energia chimica ( trasformazione
Mediatore chimico. Recettore. Trasduzione del segnale. Risposta della cellula
 Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
Mediatore chimico Recettore Trasduzione del segnale Risposta della cellula I mediatori chimici sono prodotti da cellule specializzate e sono diffusi nell organismo da apparati di distribuzione Sistemi
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 7
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 7 La struttura delle proteine Concetti chiave: La struttura terziaria di una proteina descrive il ripiegamentodei suoi elementi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 7 La struttura delle proteine Concetti chiave: La struttura terziaria di una proteina descrive il ripiegamentodei suoi elementi
che è caratteristico degli alcoli (es CH 3 -CH 2 -OH etanolo) gruppo carbonilico che si trova in composti detti chetoni;
 LE BIOMOLECOLE 1. IL CARBONIO E I SUOI COMPOSTI Il carbonio è l'elemento base del mondo vivente. Ciò si deve alla sua particolare capacità di formare 4 legami covalenti, in genere molto forti, o con altri
LE BIOMOLECOLE 1. IL CARBONIO E I SUOI COMPOSTI Il carbonio è l'elemento base del mondo vivente. Ciò si deve alla sua particolare capacità di formare 4 legami covalenti, in genere molto forti, o con altri
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa
 Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
Metabolismo: Introduzione
 Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Metabolismo: Introduzione METABOLISMO Insieme delle reazioni chimiche coordinate e integrate che hanno luogo in tutte le cellule C A T A B O L I S M O Ossidazioni esoergoniche Alimenti: Carboidrati Lipidi
Caratteristiche chimiche e nutrizionali dei pascoli toscani e aspetti della loro digestione nei ruminanti
 Caratteristiche chimiche e nutrizionali dei pascoli toscani e aspetti della loro digestione nei ruminanti M. Antongiovanni Dipartimento di Scienze Zootecniche 1 Indice degli argomenti La dieta dei ruminanti
Caratteristiche chimiche e nutrizionali dei pascoli toscani e aspetti della loro digestione nei ruminanti M. Antongiovanni Dipartimento di Scienze Zootecniche 1 Indice degli argomenti La dieta dei ruminanti
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione
 REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
REAZIONI ORGANICHE Variazioni di energia e velocità di reazione Abbiamo visto che i composti organici e le loro reazioni possono essere suddivisi in categorie omogenee. Per ottenere la massima razionalizzazione
I Composti Organici. Le Biomolecole
 I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
LE MOLECOLE INFORMAZIONALI. Lezioni d'autore Treccani
 LE MOLECOLE INFORMAZIONALI Lezioni d'autore Treccani Introduzione (I) I pionieri della biologia molecolare, scoperta la struttura degli acidi nucleici, pensarono di associare al DNA una sequenza di simboli,
LE MOLECOLE INFORMAZIONALI Lezioni d'autore Treccani Introduzione (I) I pionieri della biologia molecolare, scoperta la struttura degli acidi nucleici, pensarono di associare al DNA una sequenza di simboli,
isomeria di struttura isomeria di posizione isomeria di catena stereoisomeria isomeria di conformazione isomeria di configurazione 'isomeria ottica
 ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
ISOMERIA L'isomeria di struttura è connessa al diverso modo in cui gli atomi di due o più composti si legano tra loro in sequenza. Ci sono due forme: isomeria di posizione e isomeria di catena. La stereoisomeria
Rappresentazione dei Dati Biologici
 Rappresentazione dei Dati Biologici CORSO DI BIOINFORMATICA C.d.L. Ingegneria Informatica e Biomedica Outline Proteine ed Amminoacidi Rappresentazione di Amminoacidi Rappresentazione delle strutture Proteiche
Rappresentazione dei Dati Biologici CORSO DI BIOINFORMATICA C.d.L. Ingegneria Informatica e Biomedica Outline Proteine ed Amminoacidi Rappresentazione di Amminoacidi Rappresentazione delle strutture Proteiche
Prof.ssa Gamba Sabrina. Lezione 7: IL DNA. Duplicazione e sintesi delle proteine
 Prof.ssa Gamba Sabrina Lezione 7: IL DNA Duplicazione e sintesi delle proteine concetti chiave della lezione Costituzione fisico-chimica del DNA Basi azotate Duplicazione Concetto di geni Rna Trascrizione
Prof.ssa Gamba Sabrina Lezione 7: IL DNA Duplicazione e sintesi delle proteine concetti chiave della lezione Costituzione fisico-chimica del DNA Basi azotate Duplicazione Concetto di geni Rna Trascrizione
Capitolo 17. Risposte alle domande interne al capitolo. 17.1 (p. 501) a. glicina. b. prolina. c. treonina. d. aspartato
 apitolo 17 Risposte alle domande interne al capitolo 17.1 (p. 501) a. glicina b. prolina c. treonina d. aspartato e. 17.2 (p. 501) a. La glicina è un aminoacido idrofobico. b. La prolina è un aminoacido
apitolo 17 Risposte alle domande interne al capitolo 17.1 (p. 501) a. glicina b. prolina c. treonina d. aspartato e. 17.2 (p. 501) a. La glicina è un aminoacido idrofobico. b. La prolina è un aminoacido
Struttura delle proteine
 Struttura delle proteine Nelle proteine vi sono quattro livelli di organizzazione strutturale Struttura Primaria: sequenza di aminoacidi legati tra loro da legami peptidici Tutte le proteine esistenti
Struttura delle proteine Nelle proteine vi sono quattro livelli di organizzazione strutturale Struttura Primaria: sequenza di aminoacidi legati tra loro da legami peptidici Tutte le proteine esistenti
Forza. Forza. Esempi di forze. Caratteristiche della forza. Forze fondamentali CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA
 Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
Forza CONCETTO DI FORZA E EQUILIBRIO, PRINCIPI DELLA DINAMICA Cos è una forza? la forza è una grandezza che agisce su un corpo cambiando la sua velocità e provocando una deformazione sul corpo 2 Esempi
Le Ig sono glicoproteine costituite da 4 catene polipeptidiche:
 Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
EMOGLOBINA ... www.pianetachimica.it
 EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
EMGLBIA www.pianetachimica.it L'emoglobina è una proteina specializzata nel trasporto di ossigeno, si trova all interno dei globuli rossi del sangue ai quali conferisce il caratteristico colore rosso intenso.
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
I L I P I D I. Lipidi complessi: fosfolipidi e glicolipidi; sono formati da CHO e altre sostanze.
 I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
I L I P I D I ASPETTI GENERALI I Lipidi o grassi sono la riserva energetica del nostro organismo; nel corpo umano costituiscono mediamente il 17% del peso corporeo dove formano il tessuto adiposo. In generale
strutture di Proteine
 Laboratorio di Bioinformatica I Database di strutture di Proteine Dott. Sergio Marin Vargas (2014 / 2015) Dal gene alla proteina La funzione della proteina è nella sua struttura 3D. Struttura delle proteine
Laboratorio di Bioinformatica I Database di strutture di Proteine Dott. Sergio Marin Vargas (2014 / 2015) Dal gene alla proteina La funzione della proteina è nella sua struttura 3D. Struttura delle proteine
Helena Curtis N. Sue Barnes
 Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Helena Curtis N. Sue Barnes LA RESPIRAZIONE CELLULARE INDICE Demolizione del glucosio Glicolisi Fermentazione lattica Fermentazione alcolica Respirazione cellulare Ciclo di Krebs Catena di trasporto degli
Trasformazioni materia
 REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
REAZIONI CHIMICHE Trasformazioni materia Trasformazioni fisiche (reversibili) Trasformazioni chimiche (irreversibili) È una trasformazione che non produce nuove sostanze È una trasformazione che produce
Classificazione della materia: Sostanze pure e miscugli
 Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
Classificazione della materia: Sostanze pure e miscugli la composizione e quindi le proprietà intensive sono le stesse in ogni parte del sistema La composizione e le proprietà intensive variano da una
Dal DNA all RNA. La trascrizione nei procarioti e negli eucarioti
 Dal DNA all RNA La trascrizione nei procarioti e negli eucarioti DOGMA CENTRALE DELLA BIOLOGIA MOLECOLARE Gene Regione di DNA che porta l informazione (= che CODIFICA) per una catena polipeptidica o per
Dal DNA all RNA La trascrizione nei procarioti e negli eucarioti DOGMA CENTRALE DELLA BIOLOGIA MOLECOLARE Gene Regione di DNA che porta l informazione (= che CODIFICA) per una catena polipeptidica o per
La classificazione dei lipidi
 La classificazione dei lipidi Concetti chiave Le proprietà fisiche di un acido grasso sono determinate dalla sua lunghezza e dal suo grado di saturazione. I triacilgliceroli e i glicerofosfolipidi contengono
La classificazione dei lipidi Concetti chiave Le proprietà fisiche di un acido grasso sono determinate dalla sua lunghezza e dal suo grado di saturazione. I triacilgliceroli e i glicerofosfolipidi contengono
materia atomi miscugli omogenei e eterogenei sostanze elementari composti
 Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Elementi e Composti materia miscugli omogenei e eterogenei sostanze elementari composti atomi Gli atomi sono, per convenzione, le unità costituenti le sostanze Le sostanze possono essere costituite da
Farmaci del sistema nervoso autonomo
 Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Farmaci del sistema nervoso autonomo Farmaci colinergici Esercitano i loro effetti farmacologici sul sistema nervoso parasimpatico che utilizza Acetilcolina come mediatore chimico L acetilcolina (Ach)
Il magnetismo nella materia
 Le orbite degli elettroni in atomo di idrogeno Forma spaziale degli Orbitali elettronici di atomo di idrogeno Un solido Il magnetismo nella materia ferrimagnetismo Dr. Daniele Di Gioacchino Istituto Nazionale
Le orbite degli elettroni in atomo di idrogeno Forma spaziale degli Orbitali elettronici di atomo di idrogeno Un solido Il magnetismo nella materia ferrimagnetismo Dr. Daniele Di Gioacchino Istituto Nazionale
La propagazione delle onde luminose può essere studiata per mezzo delle equazioni di Maxwell. Tuttavia, nella maggior parte dei casi è possibile
 Elementi di ottica L ottica si occupa dello studio dei percorsi dei raggi luminosi e dei fenomeni legati alla propagazione della luce in generale. Lo studio dell ottica nella fisica moderna si basa sul
Elementi di ottica L ottica si occupa dello studio dei percorsi dei raggi luminosi e dei fenomeni legati alla propagazione della luce in generale. Lo studio dell ottica nella fisica moderna si basa sul
Domande relative alla specializzazione in: Biochimica clinica
 Domande relative alla specializzazione in: Biochimica clinica Domanda #1 (codice domanda: n.403) : Nell'ibridazione fluorescente in situ (Fluorescent in situ hybridization "FISH"), che tipo di sonde fluorescenti
Domande relative alla specializzazione in: Biochimica clinica Domanda #1 (codice domanda: n.403) : Nell'ibridazione fluorescente in situ (Fluorescent in situ hybridization "FISH"), che tipo di sonde fluorescenti
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA
 LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
LA MOLE : UN UNITA DI MISURA FONDAMENTALE PER LA CHIMICA Poiché è impossibile contare o pesare gli atomi o le molecole che formano una qualsiasi sostanza chimica, si ricorre alla grandezza detta quantità
tecnologia PROPRIETÀ DEI METALLI Scuola secondaria primo grado. classi prime Autore: Giuseppe FRANZÈ
 tecnologia PROPRIETÀ DEI METALLI Scuola secondaria primo grado. classi prime Autore: Giuseppe FRANZÈ LE PROPRIETÀ DEI MATERIALI DA COSTRUZIONE Si possono considerare come l'insieme delle caratteristiche
tecnologia PROPRIETÀ DEI METALLI Scuola secondaria primo grado. classi prime Autore: Giuseppe FRANZÈ LE PROPRIETÀ DEI MATERIALI DA COSTRUZIONE Si possono considerare come l'insieme delle caratteristiche
TEST BIOLOGIA 1 ANNO ABEI Da inviare a connesso@alice.it entro e non oltre il 6 novembre 2015
 1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
1) I batteri sono organismi: a- bicellulari b- monocellulari c- pluricellulari 2) I virus: a- possono riprodursi solo nell acqua b- possono riprodursi solo sulla superficie di una cellula c- possono riprodursi
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
GIROSCOPIO. Scopo dell esperienza: Teoria fisica. Verificare la relazione: ω p = bmg/iω
 GIROSCOPIO Scopo dell esperienza: Verificare la relazione: ω p = bmg/iω dove ω p è la velocità angolare di precessione, ω è la velocità angolare di rotazione, I il momento principale d inerzia assiale,
GIROSCOPIO Scopo dell esperienza: Verificare la relazione: ω p = bmg/iω dove ω p è la velocità angolare di precessione, ω è la velocità angolare di rotazione, I il momento principale d inerzia assiale,
STEREOISOMERIA carbonio ibridizzato sp3 è legato a quattro atomi o gruppi tutti diversi fra loro
 STEREOISOMERIA i sono oggetti che sono sovrapponibili alla loro immagine speculare: tutti gli oggetti di forma piana, ad esempio. osì, se prendo un alchene e lo confronto con la sua immagine allo specchio:
STEREOISOMERIA i sono oggetti che sono sovrapponibili alla loro immagine speculare: tutti gli oggetti di forma piana, ad esempio. osì, se prendo un alchene e lo confronto con la sua immagine allo specchio:
SINTESI DELL RNA. Replicazione. Trascrizione. Traduzione
 SINTESI DELL RNA Replicazione Trascrizione Traduzione L RNA ha origine da informazioni contenute nel DNA La TRASCRIZIONE permette la conversione di una porzione di DNA in una molecola di RNA con una sequenza
SINTESI DELL RNA Replicazione Trascrizione Traduzione L RNA ha origine da informazioni contenute nel DNA La TRASCRIZIONE permette la conversione di una porzione di DNA in una molecola di RNA con una sequenza
Formazione del legame peptidico:
 Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Il metabolismo dell RNA. Prof. Savino; dispense di Biologia Molecolare, Corso di Laurea in Biotecnologie
 Il metabolismo dell RNA I vari tipi di RNA Il filamento di DNA che dirige la sintesi dello mrna è chiamato filamento stampo o filamento antisenso. L altro filamento che ha sequenza identica a quella dello
Il metabolismo dell RNA I vari tipi di RNA Il filamento di DNA che dirige la sintesi dello mrna è chiamato filamento stampo o filamento antisenso. L altro filamento che ha sequenza identica a quella dello
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
CHIMICA COMBINATORIALE
 CHIMICA COMBINATORIALE La sintesi di composti chimici come insiemi (librerie) e lo screening di queste librerie per composti singoli con proprietà desiderate Studio combinatoriale per ottimizzare una reazione
CHIMICA COMBINATORIALE La sintesi di composti chimici come insiemi (librerie) e lo screening di queste librerie per composti singoli con proprietà desiderate Studio combinatoriale per ottimizzare una reazione
Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE
 Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale
Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale
La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di
 La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di un solido (polvere) che diverrà il ceramico, con un
La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di un solido (polvere) che diverrà il ceramico, con un
Ogni globina ha una tasca in cui lega un gruppo EME, quindi l Hb può legare e trasportare 4 molecole di O 2
 Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Emoglobina (Hb): tetramero (le globine si associano formando due copie di dimeri αβ (α 1 β 1 e α 2 β 2 ) che si associano a formare un tetramero attraverso interazioni idrofobiche, legami H e ponti salini
Metabolismo degli aminoacidi
 Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Metabolismo degli aminoacidi Quando gli aminoacidi provenienti dalla digestione gastrica e intestinale, non vengono utilizzati per la costruzione di nuove proteine vengono demoliti Transaminazione Per
Regolazione della trascrizione. Operoni catabolici nei procarioti (controllo negativo)
 Regolazione della trascrizione Operoni catabolici nei procarioti (controllo negativo) I geni possono essere accesi e spenti In un organismo pluricellulare adulto, vi sono molti tipi di cellule differenti,
Regolazione della trascrizione Operoni catabolici nei procarioti (controllo negativo) I geni possono essere accesi e spenti In un organismo pluricellulare adulto, vi sono molti tipi di cellule differenti,
Si tratta di corpiccioli di natura ribonucleoproteica che nel citoplasma di tutte le cellule presiedono ai processi di sintesi proteica.
 I R I BOSOM I I RIBOSOMI sono organuli citoplasmatici presenti in tutte le cellule, sia procariotiche che eucariotiche. Sono visibili al M.O. solo quando presenti in gran numero, (come capita nelle cellule
I R I BOSOM I I RIBOSOMI sono organuli citoplasmatici presenti in tutte le cellule, sia procariotiche che eucariotiche. Sono visibili al M.O. solo quando presenti in gran numero, (come capita nelle cellule
