Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE
|
|
|
- Ferdinando Marconi
- 8 anni fa
- Visualizzazioni
Transcript
1 Dipartimento Di Scienze Della Vita STRUTTURA DELLE PROTEINE
2 LE PROTEINE possono assumere 4 LIVELLI DI ORGANIZZAZIONE STRUTTURA PRIMARIA SEQUENZA degli amminoacidi STRUTTURA SECONDARIA Ripiegamento locale dello scheletro polipeptidico STRUTTURA TERZIARIA Ripiegamento complessivo 3D STRUTTURA QUATERNARIA Associazione di più catene polipeptidiche
3
4 AMMINOACIDI I. Amminoacidi A. Strutture (scrittura) B. Proprietà acido-basiche 1. Acidità e basicità degli -gruppi 2. acidità e basicità dei gruppi laterali 3. Punto isoelettrico II.Polipeptidi e proteine A. Struttura primaria 1. Analisi degli amminoacidi 2. Determinazione della sequenza 3. Struttura secondaria, terziaria e quaternaria
5 AMMINOACIDI Tutti gli amminoacidi hanno la stessa struttura generale. La catena laterale (gruppo R) differenzia gli amminoacidi. + 3 Amminoacido
6 AMMINOACIDI NON-POLAR AMINO ACIDS Amminoacidi con catena laterale apolare
7 AMMINOACIDI Amminoacidi POLAR con catena AMINO laterale POLARE, ACIDS priva di carica netta Amminoacidi con catena laterale POLARE, con carica netta negativa Amminoacidi con catena laterale POLARE, con carica netta positiva
8 AMMINOACIDI I. Amminoacidi A. Strutture (scrittura) B. Proprietà acido-basiche 1. Acidità e basicità degli -gruppi 2. acidità e basicità dei gruppi laterali 3. Punto isoelettrico II.Polipeptidi e proteine A. Struttura primaria 1. Analisi degli amminoacidi 2. Determinazione della sequenza 3. Struttura secondaria, terziaria e quaternaria
9 AMMINOACIDI Zwitterioni Gli amminoacidi esistono come ioni dipolari. -COOH perde H +, -NH 2 acquista H + La struttura dipende dal ph
10 AMMINOACIDI Struttura e ph
11 AMMINOACIDI Punto isoelettrico ph al quale gli amminoacidi esistono (elettricamente neutri) Depende dal tipo di catena laterale Per gli amminoacidi acidi: pi ~3 Per gli amminoacidi basici: pi ~9 Per gli amminoacidi neutri: il pi è debolmente acido (5-6)
12 AMMINOACIDI I. Amminoacidi A. Strutture (scrittura) B. Proprietà acido-basiche 1. Acidità e basicità degli -gruppi 2. acidità e basicità dei gruppi laterali 3. Punto isoelettrico II.Polipeptidi e proteine A. Struttura primaria 1. Analisi degli amminoacidi 2. Determinazione della sequenza 3. Struttura secondaria, terziaria e quaternaria
13 POLIPEPTIDI Struttura primaria peptide bond H 3 N + CH R O C O - + H 3 N + CH R' O C O - enzyme -H 2 O H 3 N + O CH C NH R a dipeptide CH R' O C O - N-terminus O O O C-terminus H 3 N + CH C NH CH C NH CH 2 C O - CH 3 CH 2 OH ala-ser-gly (a tripeptide)
14 LEGAME PEPTIDICO Il legame peptidico è un un legame ammidico ed ha un parziale carattere di doppio lagame; Le ammidi sono molto stabili e neutre.
15 NATURA PLANARE DEL LEGAME PEPTIDICO I quattro atomi del legame peptidico giacciono nello stesso piano e così pure i C dei due amminoacidi che lo formano.
16 LE PROTEINE: STRUTTURA PRIMARIA La struttura primaria delle proteine consiste nella successione (sequenza) nella catena polimerica di una proteina, degli amminoacidi che la costituiscono.
17 AMMINOACIDO Legami peptidici Parziale carattere di doppio legame
18 LE PROTEINE: STRUTTURA PRIMARIA La struttura primaria delle proteine si può rappresentare come una successione di piani
19 La disposizione della catena carboniosa (scheletro peptidico) di una proteina e delle catene laterali rappresenta la conformazione della proteina. NELLA CONFORMAZIONE DI UNA PROTEINA IDENTIFICHIAMO: STRUTTURE PERIODICHE che sono alla base della STRUTTURA SECONDARIA Sono caratterizzate da paradigmi strutturali altamente ordinati e ripetitivi dello scheletro peptidico. STRUTTURE NON PERIODICHE: non si ripetono con regolarità.
20 Struttura secondaria -elica 3,6 13
21 Struttura secondaria Struttura beta
22 Struttura secondaria: anse beta
23
24 LA STRUTTURA ad -ELICA Fu la prima ad essere identificata tra le strutture regolari che lo scheletro peptidico può assumere nelle proteine. Fu scoperta da L. Pauling. E il tipo di struttura secondaria più frequente e quindi, probabilmente, anche la più stabile.
25 LA STRUTTURA AD -ELICA Questo tipo di struttura secondaria si forma quando lo scheletro peptidico si avvolge ad elica con un passo di 5,4 Å in senso destrorso, con angoli e che si susseguono con valori, pari a circa -60 e 45/-50, rispettivamente. L elica è mantenuta da legami a idrogeno tra l ossigeno carbonilico di un gruppo peptidico e l azoto ammidico di un altro gruppo, 4 residui più avanti nella catena: Legame a idrogeno Legame idrogeno Un giro dell elica comprende 3,6 residui amminoacidici e il ciclo formato formato dal legame a idrogeno comprende 13 atomi. Da qui la notazione (3,6 13 ) per questa elica. Per ogni residuo l -ELICA progredisce di 1,5Å.
26 RAPPRESENTAZIONE DELLA STRUTTURA ad -ELICA
27 4. I gruppi R si orientano verso l esterno dell elica, che così assume l aspetto di un cilindro al cui interno corrono i legami a idrogeno, e dalla cui superficie sporgono le catene laterali dei residui amminoacidici.
28 L analisi di numerose proteine di cui è nota la struttura ha consentito di classificare gli amminoacidi proteici in varie classi in relazione alla loro capacità ad interferire con la conformazione ad -elica: RESIDUI FAVORENTI RESIDUI INDIFFERENTI RESIDUI DESTABILIZZANTI FAVORISCONO LA STRUTTURA AD A-ELICA NON SEMBRANO INFLUENZARE L ELICA INTERROMPONO L ELICA La destabilizzazione dell elica può anche essere provocata dall adiacenza di residui con catene laterali alifatiche ramificate (Thr, Val, Ile, gli ultimi due capaci di interazioni idrofobiche), o ionizzate, con carica dello stesso segno (Glu -, Asp - e Lys +, Arg + )
29 La conformazione ad -elica è presente, anche se in misura più o meno rilevante, nella maggioranza delle proteine globulari. In alcune il suo contributo alla struttura della proteina risulta rilevante, come nella mioglobina e nella emoglobina, dove costituisce il 75% della struttura. Mioglobina Emoglobina
30 -cheratina È inoltre presente anche in proteine fibrose, come l -cheratina, dove due lunghi cilindri di -elica si avvolgono l uno sull altro in senso sinistrorso realizzando una superelica.
31 Tripla elica del collagene -Tre catene polipeptidiche avvolte ad elica in senso sinistrorso
32 LA STRUTTURA AD -ELICA: il grafico di Ramachandran
33 LA STRUTTURA PUO ANCHE ESSERE INDICATA COME: 1. Nella STRUTTURA la catena risulta più estesa di quella organizzata ad -elica, con una distanza tra residui adiacenti pari a 3.3 Å, rispetto al valore di 1,5 Å dell -elica; 7, 04Å.
34 STRUTTURA A LAMINE, A STRATI PIEGHETTATI O A FOGLIETTO RIPIEGATO perché essendo la struttura costituita da due o più catene affiancate, il suo motivo dominante risulta quello di un piano che si piega su se stesso seguendo lo zig-zag dei piani peptidici che si susseguono. Come l -elica, è stabilizzata da legami a idrogeno tra l azoto ammidico e l ossigeno carbonilico di tutti i gruppi peptidici dei tratti di catena organizzati in tale struttura, di due distinte catene o di segmenti anche distanti della stessa catena (intercatena).
35 LA STRUTTURA DUE CATENE ORDINATE NELLA STRUTTURA beta POSSONO ESSERE DISPOSTE IN: DIREZIONE PARALLELA DIREZIONE ANTIPARALLELA Le due catene hanno la stessa polarità H 2 N COOH Le due catene hanno polarità opposta H 2 N COOH una catena e COOH H 2 N quella adiacente
36
37 LA STRUTTURA : Il grafico di Ramachandran
38 LE INVERSIONI DI CATENA Nelle proteine globulari la catena polipeptidica può invertire bruscamente la sua direzione, ripiegando su se stessa, in vari modi. Nella maggioranza dei casi il ripiegamento è stabilizzato da un legame a idrogeno tra il carbonile peptidico dell ultimo residuo prima del ripiegamento e l azoto peptidico del quarto residuo che segue. Le inversioni di catena si trovano sulla superficie delle proteine, per cui contengono spesso residui idrofilici. Esse sono determinanti nella costruzione dei siti di riconoscimento proteina-proteina.
39 LE STRUTTURE SUPERSECONDARIE Alcuni schemi strutturali costruiti con più segmenti di catena ordinati in strutture secondarie sono particolarmente frequenti nella proteine. Tra queste, quelle più frequenti sono: SUPERELICA DI -ELICHE Si forma quando due catene di -elica si avvolgono l una sull altra in senso sinistrorso. È stata osservata in proteine fibrose e globulari. La sua particolare stabilità deriva dall accurato reciproco incastrarsi dei gruppi R dell una e dell altra elica lungo la linea di contatto tra le due eliche. UNITA X La notazione indica una catena ordinata con struttura mentre x può essere: 1. un tratto di catena non ordinata ( c ); 2. un cilindro di -elica ( ); 3. una catena appartenente ad una distinta struttura ( ). La struttura costituita di due unità consecutive ( ), nota come avvolgimento di Rossman, è stata osservata in un notevole numero di proteine enzimatiche.
40 LE PROTEINE: STRUTTURA TERZIARIA Il termine struttura terziaria riguarda in genere le proteine globulari, dato che la costruzione di una proteina fibrosa prevede lo sviluppo preferenziale della struttura in una sola dimensione nello spazio realizzandosi mediante la ripetizione regolare di un certo motivo strutturale.
41 LE PROTEINE: STRUTTURA TERZIARIA La struttura terziaria di una proteina è tenuta insieme da: FORZE NON COVALENTI LEGAMI A IDROGENO INTERAZIONI IDROFOBICHE FORZE DI WAN DER WAALS LEGAMI IONICI FORZE COVALENTI PONTI DISOLFURICI TRA CISTEINE ANCHE LONTANE NELLA SEQUENZA AMMINOACIDICA
42
43 STRUTTURA TERZIARIA: I PONTI DISOLFURICI I PONTI DISOLFURICI SI FORMANO PER OSSIDAZIONE delle CATENE LATERALI DI DUE CISTEINE - Controllo Cinetico: Proteina disolfuro Isomerasi (PDI)
44 Segue controllo Cinetico - Prolina Isomerasi (PI) Configurazione cis-trans a livello di sequenze X-Pro - Chaperonine
45 Controllo termodinamico
46 LE PROTEINE: STRUTTURA TERZIARIA Un altro contributo alla struttura terziaria viene dal fatto che i residui polari sono quasi tutti disposti sulla superficie del globulo proteico, mentre quelli apolari puntano quasi tutti verso l interno, a costituire quello che viene chiamato nucleo idrofobico della proteina. Residui polari possono essere presenti all interno di una proteina e stabilire ponti a idrogeno. E anche frequente che la superficie di una proteina globulare si ripieghi in alcuni punti, generando fessure o cavità ricche di residui apolari formando le tasche idrofobiche che rispondono a precise esigenze funzionali (es. siti catalitici degli enzimi).
47 STRUTTURA TERZIARIA: TERMODINAMICA LEGAMI NON COVALENTI FORZE NON COVALENTI - LEGAMI A IDROGENO - FORZE DI WAN DER WAALS - LEGAMI IONICI INTERAZIONI IDROFOBICHE E COVALENTI - PONTI DISOLFURICI CONTRIBUTO ENTALPICO CONTRIBUTO ENTROPICO G = H - T S
48 STRUTTURA TERZIARIA: I DOMINI STRUTTURALI Le proteine globulari risultano spesso costituite di più domini strutturali, regioni tridimensionali della proteina dotate di autonomia strutturale, nel senso che la loro struttura si definisce autonomamente rispetto al resto della proteina. I DOMINI STRUTTURALI SONO STRUTTURE COMPATTE, COLLEGATE TRA LORO DA BREVI E FLESSIBILI SEGMENTI DI CATENA PROTEICA
49 STRUTTURA TERZIARIA: I DOMINI FUNZIONALI In molte proteine i domini strutturali costituiscono domini funzionali. I DOMINI FUNZIONALI SONO ENTITA FUNZIONALI AUTONOME ALLE QUALI COMPETONO FUNZIONI SPECIFICHE DELLA PROTEINA. DOMINI FUNZIONALI CON FUNZIONI IDENTICHE O SIMILI SONO COSTITUITI DA DOMINI STRUTTURALI OMOLOGHI, LE CUI SEQUENZE AMMINOACIDICHE SONO OMOLOGHE, E CIOE EVOLUTIVAMENTE CORRELATE.
50 LE PROTEINE: STRUTTURA QUATERNARIA Quando una proteina risulta costituita da più catene polipetidiche, l organizzazione nello spazio di queste catene, dette subunità o protomeri, rappresenta un ulteriore livello di complessità strutturale cui si dà il nome di struttura quaternaria. LE PROTEINE CON STRUTTURA QUATERNARIA SONO ANCHE DETTE PROTEINE OLIGOMERICHE. Le forze che mantengono un struttura quaternaria sono le stesse di cui si è discusso trattando la struttura terziaria delle proteine. I protomeri di una proteina oligomerica possono essere assimilati ai domi strutturali di una proteina monomerica.
51
52
53 LIVELLI STRUTTURALI Struttura primaria Struttura secondaria a -elica filamento random coil SEQUENZA ELICHE E FILAMENTI Strutt. super-secondarie MOTIVI ( autonomia strutturale ) elica-ansa-elica foglietto motivo - a - Struttura terziaria DOMINI ( autonomia funzionale ) domini a (fascio di 4 eliche, strutt. ripiegate) domini a/ (botte, foglietto aperto) domini (botte, chiave greca, "jelly-roll" )
54 Motivi STRUTTURALI
55 RIPIEGAMENTI FOGLIETTI BETA Motivo a greca
56 Motivi beta a forcina ed a chiave greca 40% 5 % 5% 25% 25%
57 Motivi beta-alpha-beta
58 Motivi beta-alpha-beta struttura "a botte" struttura "a foglietto aperto"
59 Classi strutturali delle proteine
60 Domini alpha : il "fascio di 4 eliche" Fasci di quattro eliche spesso compaiono nelle proteine con struttura a costruire domini. a) Rappresentazione schematica del dispiegamento della catena polipeptidica in un dominio costituito da un fascio di quattro eliche. b) Visione schematica della proiezione di a) su un piano perpendicolare all asse del fascio.
61 Domini alpha : il "fascio di 4 eliche" Due alpha-eliche adiacenti di solito sono disposte in modo antiparallelo l una rispetto all altra. a) Catena polipeptidica della proteina ROP (Cole 1 Repressor Of Primer) legante l RNA. b) La molecola della proteina ROP è formata da due catene polipeptidiche in cui le due -eliche presenti in ciascuna catena sono disposte a formare un fascio di quattro -eliche
62 Domini alpha : il "fascio di 4 eliche" Le catene polipeptidiche della mioemeritrina e del citocromo b 562 formano entrambe strutture a fascio di quattro eliche; i loro siti attivi sono localizzati in regioni della molecola simili.
63 Domini alpha : il "fascio di 4 eliche" I margini di una a-elica si adattano nei solchi presenti su un elica adiacente
64 Dominio della globina
65 La molecola dell emoglobina è costituita da quattro catene polipeptidiche: due catene e due catene
66 Domini / : la struttura "a botte"
67 L enzima triosofosfatoisomerasi è costituito da quattro motivi - - consecutivi sia nella sequenza aminoacidica (a) che nella struttura tridimensionale (b)
68 Domini / : la struttura "a botte" Glicolato ossidasi Metilmalonilcoenzima A mutasi
69 Domini / : la struttura "a botte" Piruvato chinasi
70 Domini / : la struttura "a botte : sito attivo RuBisCo Ribulosio Bisfosfato carbossilasi
71 Motivi strutturali ricchi di leucina: ripiegamento / "a ferro di cavallo Inibitore della ribonucleasi
72 Domini / a foglietto aperto
73 Domini / a foglietto aperto: sito attivo
74 Sito di legame del coenzima FMN Flavodossina
75 Adenilato chinasi Sito di legame dell' ATP Sito di legame dell' AMP
76 Esochinasi Fosfoglicerato mutasi
77 Domini : la struttura a "botte testa-coda" Superossido dismutasi
78 Domini : la struttura a "botte testa-coda" RBP (Proteina legante il retinolo)
79 Motivo a chiave greca
80 FUNZIONI delle PROTEINE -Proteine strutturali - Proteine di trasporto - Proteine di protezione difesa - Proteine di controllo e regolazione - Proteine catalitiche (enzimi) - Proteine per il movimento - Proteine di riserva
81 1- Proteine strutturali Il Collagene- sono stati descritti almeno ventotto tipi di collagene - Il tipo I rappresenta il 90% del collagene totale ed entra nella composizione dei principali tessuti connettivi, come pelle, tendini, ossa e cornea. -Il tipo IV va a comporre la membrana basale
82 -La fibra del collagene consiste di 3 catene polipepdiche, avvolte l una intorno all altra a formare una tripla elical elica del collagene. -Ognuno di queste tre catene ha, in prevalenza, una sequenza di 3 AA che si ripetono: -X-Pro-Gly- oppure -X-Hyp-Glydove X= qualsiasi amminoacido; Hyp, 3 oppure 4 Idrossiprolina.
83
84 1- Proteine strutturali Gli istoni
85 2- Proteine di trasporto Canale ionico Emoglobina
86 3- Proteine di protezione e difesa Anticorpi
87 3- Proteine di protezione e difesa Fibrinogeno-> Fibrina
88 4- Proteine di controllo e regolazione Insulina
89
90
91 5- Proteine catalitiche Gli enzimi
92 6- Proteine di Movimento Lunghezza
93
94 6- Proteine di riserva Fagiolo: fino al 40% di proteine
95 Grandezza e forma di proteine
96 Relazione struttura-funzione
97
98 α cheratina La proteina alfa-cheratina é presente: nei capelli, nelle penne degli uccelli, nelle unghie. Struttura a corda dell alfa-cheratina Due catene polipeptidiche (ogni catena ad alfaelica destrorsa) superavvolte sono stabilizzate da ponti disolfurici, formando il dimero. Due dimeri si associano testa coda, generando i protofilamenti; i protofilamenti dimerizzano a protofibrille; l associazione di 4 di esse forma la Microfibrilla; le protofibrille sono stabilizzate da ponti disolfurici.
99 La permanente è una operazione di ingegneria biochimica -S-S- -SH HS- HS- Ondulazione -SH H-S- -S -S- HS- -S-S- -S-S- -S-S- Riduzione Tioli -SH HS- -SH HS- -SH HS- -SH -SH -S-S- Ossidazione -SH H-S- -SH -SH HS- HS-
100 L α cheratina è presente nella lana. La lana è estensibile
101 Fibroina della seta - Unità polipeptidiche Ripetitive (59 residui AA); - Ciascuna contenente sequenze ripetitive Gly-Ala-Gly-Ala-Gly-Ser-Gly-Ala-Ala-Gly- (Ser-Gly-Ala-Gly Ala-Gly)8-Tyr Ala 32,89%; Gly 48%, Ser 15%
102 Per la presenza della struttura, la seta e molto meno estensibile della lana.
103 Mioglobina Emoglobina
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 9
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 9 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 9 Funzioni delle proteine Concetti chiave: La varietà strutturale delle proteine consente loro di svolgere un enorme quantità
Le Biomolecole I parte. Lezioni d'autore di Giorgio Benedetti
 Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Le Biomolecole I parte Lezioni d'autore di Giorgio Benedetti LE BIOMOLECOLE Le biomolecole, presenti in tutti gli esseri viventi, sono molecole composte principalmente da carbonio, idrogeno, azoto e ossigeno.
Macromolecole Biologiche. I domini (I)
 I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
I domini (I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
Macromolecole Biologiche. I domini (III)
 I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
I domini (III) Domini α/β La cross over connection è l unità costitutiva su cui si basa la topologia di 3 tipi di domini α/β osservati nelle proteine: - α/β barrel - motivi ricchi di Leu (fold a ferro
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
Macromolecole Biologiche. I domini (II)
 I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
I domini (II) Domini β Nonostante l elevato numero di possibili disposizioni di filamenti β (a costituire foglietti β antiparalleli) connessi da tratti di loop, i domini β più frequentemente osservati
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 7
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 7 La struttura delle proteine Concetti chiave: La struttura terziaria di una proteina descrive il ripiegamentodei suoi elementi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 7 La struttura delle proteine Concetti chiave: La struttura terziaria di una proteina descrive il ripiegamentodei suoi elementi
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale:
 Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
Gli amminoacidi Gli amminoacidi sono dei composti polifunzionali che hanno formula generale: N 2 Il nome ordinario degli amminoacidi prevale su quello della nomenclatura IUPA. Si possono avere α-amminoacidi,
PROTEINE. sono COMPOSTI ORGANICI QUATERNARI
 PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
PROTEINE sono COMPOSTI ORGANICI QUATERNARI Unione di elementi chimici diversi Il composto chimico principale è il C (carbonio) Sono quattro gli elementi chimici principali che formano le proteine : C (carbonio),
Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica.
 Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
Concanavalina A Emoglobina subunità Trioso fosfato isomerasi Una proteina qualsiasi assume costantemente un unica conformazione ben definita, cui è legata la sua azione biologica. 1 La conformazione è
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini.
 I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita da uno o più domini. I domini sono definiti come una catena polipeptidica
Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine.
 Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
Struttura di proteine Gli amminoacidi Il legame peptidico Motivi strutturali classificazione, architettura topologia delle strutture tridimensionali di proteine. Correlazioni struttura-funzione Gli amminoacidi
2011 - G. Licini, Università di Padova. La riproduzione a fini commerciali è vietata
 Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
Ammino acidi Composto che contiene una funziome acida e amminica. Usualmente però con amminoacidi si intendono gli alfa- amminoacidi. Tra questi composti ve ne sono 20 che vengono definiti geneticamente
PROTEINE. Amminoacidi
 PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
PROTEINE Le proteine sono le macromolecole alla base delle attività cellulari. Sono oltre diecimila per cellula, dove svolgono differenti funzioni: Sono ad esempio: enzimi: aumentano la velocità delle
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Struttura delle proteine
 Struttura delle proteine Nelle proteine vi sono quattro livelli di organizzazione strutturale Struttura Primaria: sequenza di aminoacidi legati tra loro da legami peptidici Tutte le proteine esistenti
Struttura delle proteine Nelle proteine vi sono quattro livelli di organizzazione strutturale Struttura Primaria: sequenza di aminoacidi legati tra loro da legami peptidici Tutte le proteine esistenti
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA Email: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Biotecnologie Biochimiche DISPENSA
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
AMMINOACIDI E PROTEINE Vengono chiamate amminoacidi quelle molecole organiche in cui sono contemporaneamente presenti sia un gruppo acido carbossilico -COO che un gruppo amminico -N2. Una molecola appartenente
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
Modello del collasso idrofobico. Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60
 Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Modello gerarchico Modello del collasso idrofobico Il folding è facilitato dalla presenza di chaperons molecolari quali le Heat Shock Proteins, Hsp70 e Hsp60 Le Hsp70 si legano ai segmenti idrofobici di
Continua. Peptidasi H 2 O
 Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
Continua Peptidasi H 2 O Classificazione delle peptidasi 1. Meccanismo catalitico 2. Tipo di reazione catalizzata 3. Struttura molecolare e omologia 1. Meccanismo catalitico (mostrato per la chimotripsina)
La biochimica è anche definita la chimica del C :
 Tutte le cellule viventi sono composte da macromolecole simili, costituite dalle stesse piccole molecole di base. La grande diversità è data dalle diverse combinazioni di 4 principali elementi C H O N
Tutte le cellule viventi sono composte da macromolecole simili, costituite dalle stesse piccole molecole di base. La grande diversità è data dalle diverse combinazioni di 4 principali elementi C H O N
Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa
 Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
Gli amminoacidi Le proteine rappresentano gli elementi strutturali e funzionali più importanti nei sistemi viventi. Qualsiasi processo vitale dipende da questa classe di molecole: p. es. la catalisi delle
Rappresentazione dei Dati Biologici
 Rappresentazione dei Dati Biologici CORSO DI BIOINFORMATICA C.d.L. Ingegneria Informatica e Biomedica Outline Proteine ed Amminoacidi Rappresentazione di Amminoacidi Rappresentazione delle strutture Proteiche
Rappresentazione dei Dati Biologici CORSO DI BIOINFORMATICA C.d.L. Ingegneria Informatica e Biomedica Outline Proteine ed Amminoacidi Rappresentazione di Amminoacidi Rappresentazione delle strutture Proteiche
30/10/2015 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE
 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
DOMINI E MODULI 02/04/2014. Domini modulari delle proteine 2
 Domini modulari delle proteine 1 Proteine della matrice DOMINI E MODULI La maggior parte dei peptidi consiste in disposizioni lineari di regioni globulari, ripiegate in modo indipendente, dette domini,
Domini modulari delle proteine 1 Proteine della matrice DOMINI E MODULI La maggior parte dei peptidi consiste in disposizioni lineari di regioni globulari, ripiegate in modo indipendente, dette domini,
Seminario. Domini modulari delle proteine 1
 Seminario Proteine della matrice DOMINI E MODULI Domini modulari delle proteine 1 La maggior parte dei peptidi consiste in disposizioni lineari di regioni globulari, ripiegate in modo indipendente, dette
Seminario Proteine della matrice DOMINI E MODULI Domini modulari delle proteine 1 La maggior parte dei peptidi consiste in disposizioni lineari di regioni globulari, ripiegate in modo indipendente, dette
aa 2013-14 Proteine Struttura delle Proteine α Amminoacidi
 Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
Proteine Biopolimeri degli α-amino acidi. Amino acidi sono uniti attraverso il legame peptidico. Alcune funzioni: Struttura (collagene, cheratina ecc.) Enzimi (maltasi, deidrogenasi ecc) Trasporto (albumine,
BIOLOGIA GENERALE. Alessandro Massolo Dip. Biologia Animale e Genetica c/o Prof. F. Dessì-Fulgheri (Via Romana 17) massolo@unifi.
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LA CHERATINA. CORSO COSMETOLOGIA- DOTT.SSA B. SCARABELLI (www.cosmesinice.it) PROTEINA: unione di più aminoacidi
 PROTEINA: unione di più aminoacidi LA CHERATINA AMINOACIDO: molecola unità di base; ce ne sono 20 di cui 8 sono essenziali (da introdurre solo con i cibi) La struttura delle proteine vien suddivisa in
PROTEINA: unione di più aminoacidi LA CHERATINA AMINOACIDO: molecola unità di base; ce ne sono 20 di cui 8 sono essenziali (da introdurre solo con i cibi) La struttura delle proteine vien suddivisa in
Peptidi, proteine ed e nzim i i 1
 Peptidi, proteine ed enzimi 1 Gli amminoacidi possono formare catene Due amminoacidi possono unirsi tra loro attraverso il legame ammidico detto legame peptidico, tra il gruppo NH 2 di un amminoacido e
Peptidi, proteine ed enzimi 1 Gli amminoacidi possono formare catene Due amminoacidi possono unirsi tra loro attraverso il legame ammidico detto legame peptidico, tra il gruppo NH 2 di un amminoacido e
DNA - RNA. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi.
 DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
DNA - RNA Le unità fondamentali costituenti il DNA e l RNA sono i Nucleotidi. Nucleotide = Gruppo Fosforico + Zucchero Pentoso + Base Azotata. Esistono 4 basi azotate per il DNA e 4 per RNA Differenze
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 6
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 6 La struttura secondaria delle proteine Concetti chiave: Il carattere planare di un gruppo peptidico limita la flessibilitàconformazionale
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 6 La struttura secondaria delle proteine Concetti chiave: Il carattere planare di un gruppo peptidico limita la flessibilitàconformazionale
REPLICAZIONE DEL DNA
 REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
REPLICAZIONE DEL DNA La replicazione (o anche duplicazione) è il meccanismo molecolare attraverso cui il DNA produce una copia di sé stesso. Ogni volta che una cellula si divide, infatti, l'intero genoma
Le proteine. Polimeri composto da 20 diversi aminoacidi
 Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
Le proteine Polimeri composto da 20 diversi aminoacidi (D. Voet, J.G. Voet, Biochemistry, 3 ed., John Wiley & Sons, 2004) PROTEINE come ATTUATORI nella cellula Trasporto elettronico Trasporto di ioni e
La funzione delle proteine dipende dalla loro struttura tridimensionale
 La funzione delle proteine dipende dalla loro struttura tridimensionale La struttura dipende dal ripiegamento di particolari sequenze aminoacidiche La sequenza aminoacidica della catena polipeptidica è
La funzione delle proteine dipende dalla loro struttura tridimensionale La struttura dipende dal ripiegamento di particolari sequenze aminoacidiche La sequenza aminoacidica della catena polipeptidica è
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA
 PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
PROTEINE RESPIRATORIE DEI VERTEBRATI EMOGLOBINA E MIOGLOBINA Svolgono la loro funzione legando reversibilmente l OSSIGENO. Aumentano la solubilità dell ossigeno nel plasma, da 3ml/L a 220 ml/l. La mioglobina
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Le Ig sono glicoproteine costituite da 4 catene polipeptidiche:
 Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
Struttura delle Ig Le Ig sono glicoproteine costituite da 4 catene polipeptidiche: 2 catene pesanti H (heavy( heavy) di P.M. 50.000 D, formate da c/a 450 amminoacidi 2 catene leggere L (light) Di P.M.
Università di Roma Tor Vergata - Corso di Laurea in Scienze Biologiche - Immunologia Molecolare - dott. Claudio PIOLI - a.a.
 Anticorpi generalità Riconoscimento antigene Anticorpi Molecole MHC Recettore per l Ag dei linfociti T (TCR) Anticorpi riconoscono diversi tipi di strutture antigeniche macromolecole proteine, lipidi,
Anticorpi generalità Riconoscimento antigene Anticorpi Molecole MHC Recettore per l Ag dei linfociti T (TCR) Anticorpi riconoscono diversi tipi di strutture antigeniche macromolecole proteine, lipidi,
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
Regione cerniera monomero regione cerniera
 Regione cerniera Tutte le Ig, sia quelle secrete che quelle presenti sulla membrana plasmatica dei linfociti B, sono costituite da quattro catene proteiche, due pesanti (H, da heavy, in rosso nel disegno)
Regione cerniera Tutte le Ig, sia quelle secrete che quelle presenti sulla membrana plasmatica dei linfociti B, sono costituite da quattro catene proteiche, due pesanti (H, da heavy, in rosso nel disegno)
strutture di Proteine
 Laboratorio di Bioinformatica I Database di strutture di Proteine Dott. Sergio Marin Vargas (2014 / 2015) Dal gene alla proteina La funzione della proteina è nella sua struttura 3D. Struttura delle proteine
Laboratorio di Bioinformatica I Database di strutture di Proteine Dott. Sergio Marin Vargas (2014 / 2015) Dal gene alla proteina La funzione della proteina è nella sua struttura 3D. Struttura delle proteine
I gruppi R differenziano i 20 amminoacidi standard. Tratto da D. Voet, G. Voet e C.W. Pratt Fondamenti di biochimica
 Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
Gli aminoacidi NOMENCLATURA Aminoacido Abbr. tre lettere Abbr. una lettera Aminoacido Abbr. tre lettere Abbr. una lettera Alanina ALA A Lisina LYS K Arginina ARG R Metionina MET M Asparagina ASN N Fenilalanina
AMINOACIDI - 1 AMINOACIDI - 2
 AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
AMINOAIDI - 1 Proteine (gr. pròtos = primo) 50-80% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida o alcalina α-aminoacidi proteasi Struttura generale degli α-aminoacidi primari
Capitolo 17. Risposte alle domande interne al capitolo. 17.1 (p. 501) a. glicina. b. prolina. c. treonina. d. aspartato
 apitolo 17 Risposte alle domande interne al capitolo 17.1 (p. 501) a. glicina b. prolina c. treonina d. aspartato e. 17.2 (p. 501) a. La glicina è un aminoacido idrofobico. b. La prolina è un aminoacido
apitolo 17 Risposte alle domande interne al capitolo 17.1 (p. 501) a. glicina b. prolina c. treonina d. aspartato e. 17.2 (p. 501) a. La glicina è un aminoacido idrofobico. b. La prolina è un aminoacido
formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita i da unoo più domini.
 Idomini(I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita i da unoo più domini. I domini sono definiti come parte
Idomini(I) I domini I motivi generalmente si combinano a formare strutture globulari compatte, chiamate domini. Una proteina può essere costituita i da unoo più domini. I domini sono definiti come parte
in Terminazione Neurone Dendriti Soma Fessura sinaptica sinaptica Nucleo dendrite Segmento iniziale Sinapsi inibitoria Segmento mielinico Assone
 Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Le funzioni del sistema nervoso si basano sull attività dei neuroni che consiste nel generare, trasmettere ed elaborare informazioni nervose, che dipendono da modificazioni del potenziale di membrana,
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Biosintesi non ribosomiale di metaboliti peptidici bioattivi
 Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Biosintesi non ribosomiale di metaboliti peptidici bioattivi Principali bersagli degli antibiotici Gli antibiotici derivano per la maggior parte da composti naturali Strutture di alcuni peptidi bioattivi
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Energia nelle reazioni chimiche. Lezioni d'autore di Giorgio Benedetti
 Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
Energia nelle reazioni chimiche Lezioni d'autore di Giorgio Benedetti VIDEO Introduzione (I) L energia chimica è dovuta al particolare arrangiamento degli atomi nei composti chimici e le varie forme di
La spirale iperbolica: Fu descritta per la prima volta da Pierre Varignon (1654-1722). L equazione, espressa in coordinate polari, è del tipo:
 Esistono delle forme geometriche che sono in grado, per complessi fattori psicologici non del tutto chiariti, di comunicarci un senso d equilibrio, di gradimento e di benessere. Tra queste analizzeremo
Esistono delle forme geometriche che sono in grado, per complessi fattori psicologici non del tutto chiariti, di comunicarci un senso d equilibrio, di gradimento e di benessere. Tra queste analizzeremo
Parametri dell α-elica. residui/giro 3.6. passo dell elica
 GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
GRAFICO DI RAMACHANDRAN Parametri dell α-elica residui/giro 3.6 spazio/residuo passo dell elica 1.5 Å 5.4 Å 1 L α-elica può essere destabilizzata da interazioni tra i gruppi R: repulsione/attrazione elettrostatica
LE MOLECOLE INFORMAZIONALI. Lezioni d'autore Treccani
 LE MOLECOLE INFORMAZIONALI Lezioni d'autore Treccani Introduzione (I) I pionieri della biologia molecolare, scoperta la struttura degli acidi nucleici, pensarono di associare al DNA una sequenza di simboli,
LE MOLECOLE INFORMAZIONALI Lezioni d'autore Treccani Introduzione (I) I pionieri della biologia molecolare, scoperta la struttura degli acidi nucleici, pensarono di associare al DNA una sequenza di simboli,
BIOMOLECOLE STRUTTURA E FUNZIONE
 BIOMOLECOLE STRUTTURA E FUNZIONE Lo studio delle relazioni tra struttura e funzione nelle biomolecole è uno degli aspetti più importanti per la comprensione del funzionamento dei processi biologici La
BIOMOLECOLE STRUTTURA E FUNZIONE Lo studio delle relazioni tra struttura e funzione nelle biomolecole è uno degli aspetti più importanti per la comprensione del funzionamento dei processi biologici La
Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che
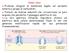 Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
Canali ionici Proteine integrali di membrana legate sul versante esterno a gruppi di carboidrati. Formati da diverse subunità che circoscrivono un poro acquoso che permette il passaggio selettivo di ioni.
BIOLOGIA GENERALE 22-24 ottobre 2007
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 22-24 ottobre 2007 Facoltà di Psicologia Tecniche di Psicologia Generale e Sperimentale Alessandro Massolo Dip.
Metalli in Biologia. Metalli e leganti bio
 Metalli in Biologia Metalli e leganti bio La struttura della mioglobina La struttura della emoglobina John Cowdery Kendrew MRC, Cambridge, UK Nobel Prize in 1962 Max Ferdinand Perutz MRC, Cambridge, UK
Metalli in Biologia Metalli e leganti bio La struttura della mioglobina La struttura della emoglobina John Cowdery Kendrew MRC, Cambridge, UK Nobel Prize in 1962 Max Ferdinand Perutz MRC, Cambridge, UK
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
AMINOACIDI. GENE PROTEINA EFFETTO. calore. idrolisi acida (o alcalina) Struttura generale degli α-aminoacidi primari (standard, normali):
 AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
AMINOAIDI. Proteine (gr. pròtos = primo) > 50% peso secco cellulare GENE POTEINA EFFETTO proteine calore idrolisi acida (o alcalina) α-aminoacidi Struttura generale degli α-aminoacidi primari (standard,
NUCLEOTIDI e ACIDI NUCLEICI
 NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
NUCLEOTIDI e ACIDI NUCLEICI Struttura dei nucleotidi Il gruppo fosfato conferisce carica negativa e proprietà acide FUNZIONI DEI NUCLEOTIDI MOLECOLE DI RISERVA DI ENERGIA L idrolisi dei nucleosidi trifosfato
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA. Angela Chambery Lezione 2
 Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Corso di Laurea in Farmacia Insegnamento di CHIMICA BIOLOGICA Angela Chambery Lezione 2 Versatilità del carbonio nel formare legami covalenti La chimica degli organismi viventi è organizzata intorno al
Grandezze scalari e vettoriali
 Grandezze scalari e vettoriali Esempio vettore spostamento: Esistono due tipi di grandezze fisiche. a) Grandezze scalari specificate da un valore numerico (positivo negativo o nullo) e (nel caso di grandezze
Grandezze scalari e vettoriali Esempio vettore spostamento: Esistono due tipi di grandezze fisiche. a) Grandezze scalari specificate da un valore numerico (positivo negativo o nullo) e (nel caso di grandezze
PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi
 POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
Chimotripsina Una proteina globulare. Glicina Un amminoacido
 Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Relazione struttura-funzione
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Relazione struttura-funzione Marco Nardini Dipartimento di Scienze
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Relazione struttura-funzione Marco Nardini Dipartimento di Scienze
dieta vengono convertiti in composti dei corpi chetonici.
 Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Metabolismo degli aminoacidi Metabolismo degli aminoacidi Gli aminoacidi introdotti in eccesso con la dieta vengono convertiti in composti precursori del glucosio, degli acidi grassi e dei corpi chetonici.
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
corta catena (meno di 20 ammino acidi) mancanza di una struttura spaziale organizzata lunga catena di ammino acidi struttura spaziale organizzata
 STRUTTURA DELLE PROTEINE Peptide: corta catena (meno di 20 ammino acidi) mancanza di una struttura spaziale organizzata Polipeptide (proteina): lunga catena di ammino acidi struttura spaziale organizzata
STRUTTURA DELLE PROTEINE Peptide: corta catena (meno di 20 ammino acidi) mancanza di una struttura spaziale organizzata Polipeptide (proteina): lunga catena di ammino acidi struttura spaziale organizzata
SUPERAVVOLGIMENTO DEL DNA (ORGANIZZAZIONE TERZIARIA DEL DNA)
 SUPERAVVOLGIMENTO DEL DNA (ORGANIZZAZIONE TERZIARIA DEL DNA) ORGANIZZAZIONE TERZIARIA DEL DNA Il DNA cellulare contiene porzioni geniche e intergeniche, entrambe necessarie per le funzioni vitali della
SUPERAVVOLGIMENTO DEL DNA (ORGANIZZAZIONE TERZIARIA DEL DNA) ORGANIZZAZIONE TERZIARIA DEL DNA Il DNA cellulare contiene porzioni geniche e intergeniche, entrambe necessarie per le funzioni vitali della
La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di
 La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di un solido (polvere) che diverrà il ceramico, con un
La base di partenza per la maggior parte dei processi produttivi di materiali ceramici sono le sospensioni. Queste si ottengono dalla miscelazione di un solido (polvere) che diverrà il ceramico, con un
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
4x4x4=4 3 =64 codoni. 20 aminoacidi
 4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
4x4x4=4 3 =64 codoni 20 aminoacidi 1 Le 20 diverse catene laterali (gruppo R) che costituiscono gli aminoacidi si differenziano considerevolmente per dimensioni, volume e per le loro caratteristiche fisico-chimiche,
Il legame peptidico è un ibrido di risonanza: scaricato da
 Il legame peptidico è un ibrido di risonanza: - O ha una parziale carica negativa - - la coppia di e - del legame C=O è parzialmente spostata verso O - N ha una parziale carica positiva + - la coppia di
Il legame peptidico è un ibrido di risonanza: - O ha una parziale carica negativa - - la coppia di e - del legame C=O è parzialmente spostata verso O - N ha una parziale carica positiva + - la coppia di
AMMINOACIDI. Gli amminoacidi si distinguono in base alla diversità della catena laterale R in ciascuno di essi.
 AMMINOACIDI Gli amminoacidi sono composti polifunzionali, infatti essi presentano sia un gruppo carbossilico, che conferisce loro caratteristiche acide, sia un gruppo amminico, che conferisce loro caratteristiche
AMMINOACIDI Gli amminoacidi sono composti polifunzionali, infatti essi presentano sia un gruppo carbossilico, che conferisce loro caratteristiche acide, sia un gruppo amminico, che conferisce loro caratteristiche
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
STRUTTURA TERZIARIA. H 3 N + COO - β-foglietto
 STRUTTURA TERZIARIA α-eliche H 3 N + COO - β-foglietto La catena polipeptidica delle proteine GLOBULARI oltre ad organizzarsi in strutture di tipo secondario va incontro ad un ulteriore ripiegamento sino
STRUTTURA TERZIARIA α-eliche H 3 N + COO - β-foglietto La catena polipeptidica delle proteine GLOBULARI oltre ad organizzarsi in strutture di tipo secondario va incontro ad un ulteriore ripiegamento sino
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
Le proteine. Le proteine sono macromolecole che presentano differenze funzionali e strutturali
 Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di
Le proteine Le proteine sono macromolecole che presentano differenze funzionali e strutturali LE PROTEINE HANNO FUNZIONI BIOLOGICHE DIVERSE enzimi proteine di trasporto proteine strutturali proteine di
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
la struttura tridimensionale può essere ottenuta solo per Un intero dominio in genere da 50 a 300 residui
 Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Durante la traduzione l informazione di ripiegamento codificata nella sequenza aminoacidica diventa disponibile in maniera vettoriale la struttura tridimensionale può essere ottenuta solo per Un intero
Domande relative alla specializzazione in: Biochimica clinica
 Domande relative alla specializzazione in: Biochimica clinica Domanda #1 (codice domanda: n.403) : Nell'ibridazione fluorescente in situ (Fluorescent in situ hybridization "FISH"), che tipo di sonde fluorescenti
Domande relative alla specializzazione in: Biochimica clinica Domanda #1 (codice domanda: n.403) : Nell'ibridazione fluorescente in situ (Fluorescent in situ hybridization "FISH"), che tipo di sonde fluorescenti
Gerarchia della struttura delle proteine
 Si indica con CONFORMAZIONE la disposizione tridimensionale degli atomi di una molecola, cioè la loro organizzazione spaziale. Gerarchia della struttura delle proteine struttura primaria: sequenza degli
Si indica con CONFORMAZIONE la disposizione tridimensionale degli atomi di una molecola, cioè la loro organizzazione spaziale. Gerarchia della struttura delle proteine struttura primaria: sequenza degli
Dal DNA all RNA. La trascrizione nei procarioti e negli eucarioti
 Dal DNA all RNA La trascrizione nei procarioti e negli eucarioti DOGMA CENTRALE DELLA BIOLOGIA MOLECOLARE Gene Regione di DNA che porta l informazione (= che CODIFICA) per una catena polipeptidica o per
Dal DNA all RNA La trascrizione nei procarioti e negli eucarioti DOGMA CENTRALE DELLA BIOLOGIA MOLECOLARE Gene Regione di DNA che porta l informazione (= che CODIFICA) per una catena polipeptidica o per
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
«Macromolecole» Lipidi
 LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
LIPIDI (1) «Macromolecole» Lipidi Biotecnologie Miscellanea di molecole biologiche che condividono la proprietà di non essere solubili in acqua. Molecole idrofobiche. Es: Grassi Oli (grasso liquido a temperatura
Costituzione dei viventi
 Costituzione dei viventi La materia e costituita da elementi chimici in forma pura o in combinazioni dette composti 25 dei 92 elementi naturali sono costituenti essenziali dei viventi 4 (C, O,, N) costituiscono
Costituzione dei viventi La materia e costituita da elementi chimici in forma pura o in combinazioni dette composti 25 dei 92 elementi naturali sono costituenti essenziali dei viventi 4 (C, O,, N) costituiscono
Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.
![Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro. Ke = ] = Kw = 10 = 10-7 moli/litro, ed in base a quanto avevamo affermato in precedenza: [H + ] = [OH - ] = 10-7 moli/litro.](/thumbs/27/12374782.jpg) Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
Prodotto ionico dell acqua e ph Prodotto ionico dell acqua L acqua è un elettrolita debolissimo e si dissocia secondo la reazione: H 2 O H + + OH - La costante di equilibrio dell acqua è molto piccola
