La gastroenterite acuta
|
|
|
- Gino Pagani
- 8 anni fa
- Просмотров:
Транскрипт
1 La gastroenterite acuta Dott. Gilberto Guindani Indice del corso Introduzione Definizione Epidemiologia Eziologia Diarrea infettiva Virus Batteri Parassiti Diarrea da antibiotici Fisiopatologia Diarrea osmotica Diarrea secretoria Diarrea di tipo infiammatorio Diarrea da disturbi della motilità intestinale Diarrea da Rotavirus: modello fisiopatologico per entrambi i meccanismi, osmotico e secretivo Meccanismo d azione delle enterotossine virali e batteriche Meccanismi endogeni di controllo della secrezione e dell assorbimento Altre forme di diarrea acuta Diarrea da Rotavirus Eziologia Epidemiologia Patogenesi Immunità Diagnosi Trattamento Misure generali e di profilassi Vaccino Sicurezza Efficacia Analisi costi/benefici Controindicazioni e precauzioni
2 Raccomandazioni Valutazione anamnestica Sospetto diagnostico e manifestazioni cliniche Il ruolo della diagnostica di laboratorio Gestione clinica Il bambino a rischio Valutazione della disidratazione Indicazioni al ricovero Trattamento La reidratazione L alimentazione (rialimentazione) La terapia con farmaci Micronutrienti Probiotici Antimicrobici Adsorbenti Antiperistaltici Antiemetici Antisecretori Tannato di gelatina Prevenzione Bibliografia
3 INTRODUZIONE La gastroenterite acuta rimane una frequente causa di morbilità e di ospedalizzazione particolarmente nelle prime epoche della vita e ha un impatto non trascurabile sulla spesa sanitaria. È uno dei sintomi più frequenti in età pediatrica, soprattutto nei paesi in via di sviluppo, dove rappresenta ancora oggi una frequente causa di morte. La diarrea è stata, infatti, riconosciuta dall OMS e dall UNICEF come la seconda causa di morte tra i bambini al di sotto dei 5 anni di età, dopo la polmonite. Anche in Italia, così come in altri paesi industrializzati, la gastroenterite acuta rappresenta un importante causa di morbilità ed è responsabile di gravi quadri di disidratazione, soprattutto nei primi anni di vita. La forma più comune di gastroenterite acuta in età pediatrica è la diarrea acuta infettiva; l agente eziologico maggiormente implicato è il Rotavirus, seguito da Norovirus e Adenovirus. Meno frequentemente vengono isolati dei batteri, tra cui principalmente la Salmonella e il Campylobacter. Dopo i 5 anni, soprattutto nei paesi del Nord Europa, il patogeno maggiormente identificato è il Campylobacter. Le strategie mediche hanno l obiettivo di tentare un ulteriore riduzione della percentuale di mortalità, e prevedono per i paesi in via di sviluppo la possibilità di diffondere in maniera capillare l utilizzazione della reidratazione per via orale ai primi segni clinici, mentre, per i paesi industrializzati, prevedono l identificazione delle categorie a rischio e una migliore conoscenza dei protocolli di reidratazione e di rialimentazione. La completa conoscenza e la corretta applicazione di protocolli e linee guida, sia nella pediatria del territorio sia in quella ospedaliera, appaiono necessarie per un adeguata gestione di tutti gli aspetti della gastroenterite acuta. Il pediatra ha quindi il compito di operare per ridurre la gravità delle infezioni intestinali e la durata della sintomatologia, limitando il numero dei ricoveri, spesso non necessari. Tali obiettivi sono raggiungibili attraverso l applicazione delle moderne strategie per l approccio al bambino con gastroenterite acuta.
4 DEFINIZIONE La gastroenterite acuta è definita come una riduzione nella consistenza delle feci (morbide o liquide) e/o un aumento nella frequenza delle evacuazioni (tipicamente 3 nelle 24 ore), con o senza febbre o vomito. L alterazione qualitativa della consistenza fecale si ritiene più indicativa di diarrea rispetto all aumento del numero di scariche, in quanto un aumentata frequenza delle evacuazioni può essere fisiologica in alcune epoche della vita (come nel lattante) e può essere influenzata dall alimentazione o dalla presenza di disordini funzionali, come la sindrome del colon irritabile. La gastroenterite acuta viene quindi identificata dalle variazioni dell alvo, intese soprattutto come consistenza delle feci e frequenza delle evacuazioni, anche se qualche autore tende a utilizzare l entità dell output fecale (emissioni di feci) in rapporto al peso corporeo (è considerato normale un output fecale < 5 ml/kg/die). Si parla di gastroenterite acuta quando il disturbo ha una durata inferiore a 7 giorni e comunque non superiore a 14 giorni; per diarrea cronica s intende, invece, una forma che persiste per oltre 14 giorni. Nella maggioranza dei casi, tale entità clinica rappresenta l espressione di un infezione gastroenterica. Tuttavia, la diarrea acuta può rappresentare anche la modalità di presentazione di patologie digestive non infettive ed extradigestive. La gestione del paziente con diarrea acuta richiederà pertanto una valutazione preliminare, che consenta di escludere tutte le potenziali cause diverse dalla gastroenterite e, successivamente, permetta un preciso inquadramento eziologico e clinico.
5 EPIDEMIOLOGIA La forma più comune di gastroenterite acuta in età pediatrica è la diarrea acuta infettiva, che in Europa presenta un incidenza variabile tra 0,5 e 1,9 episodi all anno nei bambini al di sotto dei 3 anni di età, con dati sovrapponibili anche in Italia. Il Rotavirus (RTV) è l agente eziologico più frequente di diarrea acuta. Il più comune agente batterico è il Campylobacter nel Nord Europa o la Salmonella nel Sud Europa. I parassiti sono cause infrequenti di gastroenterite nei bambini sani nei paesi occidentali. I parassiti che più spesso causano diarrea nei soggetti immunocompromessi, o nei bambini che vivono nei paesi in via di sviluppo, sono Cryptosporidium e Giardia. La massima incidenza di episodi di diarrea acuta si osserva nei bambini < 5 anni, in particolare nella fascia di età compresa tra 6 e 24 mesi. Per quanto riguarda la stagionalità, la diarrea acuta si verifica più frequentemente da ottobre a maggio, con picco di incidenza tra gennaio e marzo. Il picco di incidenza per la diarrea acuta da Rotavirus si colloca tra gennaio e marzo, tranne che in Svezia, dove l incidenza massima di Rotavirus presenta un picco più tardivo (aprile). Le forme batteriche presentano invece due picchi di incidenza: maggio-giugno; settembre-ottobre. Nella Tabella 1 vengono riportati i dati relativi all incidenza delle gastroenteriti da Rotavirus e da altri agenti eziologici, suddivisi per fascia di età, e i principali dati relativi all impatto delle gastroenteriti sull attività ospedaliera e ambulatoriale.
6 PATOGENI DIVERSI DA ROTAVIRUS ROTAVIRUS Incidenza annuale complessiva* mesi 6-11 mesi 5.60 (Norovirus, Adenovirus, Salmonella) (Norovirus, Adenovirus, Salmonella minori) mesi (Norovirus, Adenovirus, Salmonella, Campylobacter, Yersinia) mesi (Norovirus, Adenovirus, Salmonella, Campylobacter, Yersinia) mesi 5.73 (Norovirus, Adenovirus, Salmonella, Campylobacter, Yersinia) 2.10 numero ricoveri* numero accessi al DEA* numero visite* ambulatoriali * Numero di nuovi casi/100 bambini < 5 anni/anno Tabella 1. Incidenza delle gastroenteriti da Rotavirus e da altri agenti eziologici (Fonte: Romano C et al. Standard care in gastroenterologia pediatrica: la diarrea acuta. Società Italiana di Gastroenterologia Epatologia e Nutrizione Pediatrica, 2009). È stato calcolato che, in Italia, il costo medio per episodio di diarrea è pari a circa 110 euro, con significative differenze tra bambini con età inferiore o superiore a 36 mesi (116 euro vs 72 euro) (vedi Tabella 2). La stima del costo annuo sulla base dei dati ricordati è variabile tra 110 e 220 milioni di euro. Età > 36 mesi (n = 61) euro Età < 36 mesi (n = 412) euro Tutti (n = 473) euro Cibi speciali 0,40 4,80 4,25 Esami di laboratorio 1,80 1,97 1,97 Farmaci 11,35 11,35 11,35 Giorni di lavoro persi 54,91 87,26 82,06 Pannolini extra 1,24 5,10 4,58 Visite extra 2,41 5,93 5,50 Totale 72,11 116,41 109,71 Tabella 2. Costo di un singolo episodio di diarrea in base all età del bambino (Fonte: Guarino A, Albano F. La gastroenterite: fisiopatologia e correlati clinici diagnostici. Area Pediatrica, n. 2 anno 7, febbraio 2006).
7 EZIOLOGIA Molte patologie intestinali ed extraintestinali possono presentarsi con un quadro clinico di diarrea a insorgenza acuta. Le possibili cause di diarrea acuta in età pediatrica sono rappresentate da infezioni intestinali ed extraintestinali, assunzione di antibiotici, allergie alimentari e, più raramente, chemioterapia e radioterapia, patologie chirurgiche, deficit vitaminici e ingestione di metalli pesanti (vedi Tabella 3 per le principali cause di diarrea acuta non infettiva in età pediatrica). Farmaci Diarrea associata agli antibiotici Lassativi Antiacidi Astinenza da oppiacei Altri farmaci Allergie alimentari Allergia alle proteine del latte vaccino Allergia alle proteine della soia Allergie alimentari multiple Patologie digestive e/o dell assorbimento Deficit di saccarasi-isomaltasi Esordio tardivo (o tipo adulto ) di deficit di lattasi Fibrosi cistica Malattia celiaca Chemioterapia o radioterapia Patologie chirurgiche Appendicite acuta Invaginazione intestinale Sindrome dell intestino corto Patologie endocrine Diabete Ipertiroidismo Ipoparatiroidismo Malattia di Addison Deficienze vitaminiche Deficit di niacina Deficit di folati Ingestione di metalli pesanti Zinco, rame, stagno Tabella 3. Principali cause di diarrea acuta non infettiva in età pediatrica (Fonte: Guandalini S, Kahn S. Acute Diarrhea. In: Walker Textbook of Pediatric GI, 2008). Diarrea infettiva La principale causa di diarrea acuta, sia nei paesi in via di sviluppo sia in quelli industrializzati, è ancora oggi infettiva. La diarrea acuta infettiva, o gastroenterite acuta, è
8 una patologia molto comune in età pediatrica, responsabile di circa 2 milioni di decessi in tutto il mondo. Nell ultimo decennio, l elenco dei microrganismi responsabili di diarrea acuta nell infanzia è notevolmente aumentato. Nella Tabella 4 sono elencati i principali agenti patogeni responsabili di diarrea acuta. PATOGENI FREQUENZA (%) Virus Rotavirus Norovirus 2-20 Adenovirus 2-10 Batteri Campylobacter jejuni 4-13 Salmonella 5-8 Escherichia coli enteropatogeno Escherichia coli enteroaggreganti Escherichia coli enteroemorragico Escherichia coli enterotossigeno Shigella Parassiti Entamoeba 0-4 Giardia lamblia Non determinato Tabella 4. Principali agenti patogeni responsabili di diarrea acuta infettiva in età pediatrica (0-5 anni) in Europa (Fonte: Guarino A et al. ESPGHAN/ESPID Evidence-based Guidelines for the Management of Acute Gastroenteritis in Children in Europe. J Pediatr Gastroenterol Nutr, Vol. 46, Suppl. 2, May 2008). Definire il peso epidemiologico di ciascun microrganismo è difficile a causa delle notevoli differenze tra le varie aree geografiche, dovute a diversità climatiche, igienico-sanitarie (vedi Figura 1), della scarsità di studi che ricerchino tutti i possibili patogeni e delle differenze riguardanti l età dei vari gruppi studiati.
9 Figura 1. Distribuzione geografica dei principali agenti enteropatogeni in Europa (Fonte: Guarino A et al. ESPGHAN/ESPID Evidence-based Guidelines for the Management of Acute Gastroenteritis in Children in Europe. J Pediatr Gastroenterol Nutr, Vol. 46, Suppl. 2, May 2008). I batteri sono in genere più frequenti nei primi mesi di vita e successivamente nell età scolare; l infezione da Rotavirus, invece, ha un picco di incidenza tra i 6 e i 24 mesi di età. Una recente metanalisi effettuata dal National Institute for Health and Clinical Excellence ha verificato l incidenza di ogni singolo patogeno nell eziologia della diarrea acuta in età pediatrica. Sebbene i risultati di 3 studi hospital-based e di 5 studi di popolazione mostrassero una notevole variazione nella percentuale di bambini con gastroenterite in cui era stato isolato un organismo patogeno dall esame delle feci (45%-75%), il Rotavirus era l agente eziologico più comunemente riscontrato in tutti gli studi. Altri patogeni virali, sebbene singolarmente meno comuni, nell insieme sono responsabili di molti altri casi. Il virus di Norwalk presenta attualmente un ruolo epidemiologico crescente come agente eziologico di gastroenterite, insieme ad altri Calicivirus, agli Adenovirus e agli Astrovirus. In una minore percentuale dei casi, le infezioni batteriche (soprattutto da Salmonella e Campylobacter) e protozoarie (soprattutto da Cryptosporidium) possono essere causa di diarrea acuta. Nella Tabella 5 è riportata la distribuzione degli agenti patogeni per età dei soggetti colpiti.
10 Età < 1 anno Età 1-4 anni Età > 5 anni Rotavirus Norovirus Adenovirus Salmonella Rotavirus Norovirus Adenovirus Salmonella Campylobacter Yersinia Campylobacter Salmonella Rotavirus Tabella 5. Distribuzione degli agenti patogeni per età dei soggetti colpiti (Fonte: Guarino A et al. ESPGHAN/ESPID Evidence-based Guidelines for the Management of Acute Gastroenteritis in Children in Europe. J Pediatr Gastroenterol Nutr, Vol. 46, Suppl. 2, May 2008). VIRUS Adenovirus enterici Sono patogeni ubiquitari causa di numerose patologie, dalle infezioni respiratorie all epatite. L enterite da Adenovirus tende a essere più duratura (spesso più di 2 settimane) rispetto alla patologia causata dagli altri patogeni virali. I sierotipi implicati nella patogenesi della diarrea sono il 40 e il 41. La prevalenza di anticorpi anti-adenovirus enterici aumenta del 50% o più dopo il terzo-quarto anno di vita. L infezione ha un picco in estate. Astrovirus Sono importanti agenti causali di diarrea nei paesi in via di sviluppo e nelle epidemie nosocomiali. L infezione è caratterizzata da una diarrea acquosa che può durare 3 giorni. Il vomito è poco frequente. Calicivirus (Norovirus e Sapovirus) Virus di Norwalk Il virus di Norwalk è stato il primo virus identificato nelle feci tramite microscopia elettronica durante un epidemia di enterite verificatasi a Norwalk (USA). Successivamente, altri virus con una simile morfologia piccola e circolare sono stati denominati virus Norwalk-like, recentemente riclassificati come Norovirus, facenti parte della famiglia dei Calicivirus insieme ai Sapovirus. I Norovirus sono causa di epidemie in ambienti ristretti come la scuola, i campeggi, le navi da crociera. La trasmissione avviene tramite vari alimenti, tra cui crostacei e insalata lavata con acqua contaminata. I Norovirus sono agenti eziologici emergenti anche di diarrea nosocomiale. La sintomatologia è indistinguibile dalla gastroenterite da Rotavirus. Le infezioni si verificano durante tutto l anno, con una prevalenza che diminuisce nel periodo estivo. I Sapovirus provocano diarrea meno severa e di minor durata rispetto ai Norovirus e al Rotavirus.
11 Citomegalovirus È frequente in soggetti immunocompromessi, ma il suo ruolo come patogeno enterico non è ben definito. In bambini con infezione da HIV, il Citomegalovirus può causare lesioni ulcerative lungo tutto il tratto gastrointestinale, con prevalente localizzazione al colon, dolore addominale, vomito, diarrea e perdita ematica con le feci. Rotavirus Sono stati identificati vari gruppi di Rotavirus. Il gruppo A è il principale responsabile delle infezioni nell uomo. Il Rotavirus è l agente eziologico più frequente di diarrea in età pediatrica. Presenta un picco di incidenza nei paesi a clima temperato e nel periodo invernale. L età più colpita è tra i 6 e i 24 mesi. Il meccanismo fisiologico classico prevede, dopo la penetrazione del microrganismo per via orale o per via respiratoria, la localizzazione elettiva del virus nelle cellule mature dei villi del tenue. Queste, in seguito all invasione virale, muoiono rapidamente; di conseguenza i villi si accorciano e vengono velocemente ricoperti da cellule provenienti dall accresciuta attività rigeneratrice che si svolge nelle cripte. Queste cellule, però, non hanno avuto il tempo di maturare adeguatamente, per cui non solo non sono in grado di svolgere la funzione digestivo-assorbitiva delle cellule differenziate dei villi, ma anzi mantengono il fisiologico stato secretivo tipico delle cellule epiteliali poco differenziate delle cripte. Pertanto, da un lato i nutrienti non assorbiti richiamano acqua per osmosi, dall altro vi sono più cellule immature di tipo secretivo, con conseguente sbilanciamento tra assorbimento e secrezione a favore di quest ultima. Studi recenti hanno dimostrato che una glicoproteina non strutturale del virus può indurre secrezione di cloro attraverso un meccanismo calcio-dipendente. Pertanto, il Rotavirus induce diarrea con 3 diversi meccanismi: 1. meccanismo osmotico derivante dal danno cellulare, 2. meccanismo secretivo dovuto alla proliferazione di cellule delle cripte, 3. un secondo meccanismo secretivo mediato da un enterotossina. Classicamente, la sintomatologia consiste in una diarrea profusa, con vomito e febbre. La diarrea da Rotavirus è mediamente più grave di quella indotta da altri agenti, e costituisce una frequente causa di ricovero ospedaliero per l elevata incidenza di disidratazione. Altri virus Tra gli altri virus responsabili di gastroenteriti si ricordano: Parvovirus, Picobirnavirus, Breda virus, Pestivirus, Torovirus. BATTERI Aeromonas Si tratta di batteri gram-negativi di cui si riportano 3 specie:
12 1. Aeromonas hydrophila, 2. Aeromonas sobria, 3. Aeromonas caviae. Poiché molti laboratori clinici non possono fornire un identificazione precisa, la maggior parte delle specie isolate è segnalata come Aeromonas hydrophila. Il contagio è stato spesso attribuito all ingestione di acqua o di cibi contaminati da feci di animali. Sebbene sia stata dimostrata la produzione di enterotossine termolabili e termostabili da parte di alcuni ceppi, il meccanismo patogenetico è ancora in parte oscuro. Campylobacter È, insieme alla Salmonella, la principale causa di diarrea batterica nei paesi industrializzati. È un batterio le cui 2 specie predominanti, patogene per l uomo, sono: 1. Campylobacter jejuni, 2. Campylobacter coli. Il Campylobacter jejuni è un bacillo gram-negativo, sottile, mobile, a forma di virgola, a volte corto e a volte lungo, di cui si conoscono più di 90 sierotipi. Il serbatoio dell infezione è rappresentato dall intestino di animali selvatici e domestici. In particolare, il veicolo dell infezione è rappresentato dal pollame e dal consumo di latte non pastorizzato e di acqua contaminata. In natura esiste un serbatoio del bacillo, rappresentato dall intestino degli uccelli e di alcuni mammiferi domestici e selvatici, che è stato isolato nel % dalle feci di polli, tacchini e uccelli acquatici. Anche le carcasse dei polli sono contaminate con il Campylobacter jejuni, ma anche altri animali, come cani, gatti e uccelli, possono talvolta albergare il bacillo. La trasmissione all uomo del Campylobacter jejuni avviene per ingestione di cibi infettati, ma anche attraverso latte non pastorizzato, acqua non clorata o animali da cortile non sufficientemente cotti o, più di rado, per contatto diretto con le feci di animali o di persone infettate. Campylobacter Si sono verificate epidemie nelle scolaresche in seguito a gite in fattoria, dove i bambini hanno bevuto latte non pastorizzato. La trasmissione da persona a persona avviene di rado: essa sembra avvenire fra i bambini che non controllano ancora l emissione delle feci. Un esempio di trasmissione è dato dai neonati che sono stati infettati dalle loro madri. La durata dell escrezione del bacillo è breve: da 2 a 3 settimane nella maggioranza dei casi, si riduce a 2-3 giorni quando il soggetto viene adeguatamente trattato. La dose minima infettante è bassa: bastano poche centinaia di agenti per dare infezione o malattia. Altre volte, anche grandi inocula non danno malattia. Non esiste lo stato di portatore asintomatico. Il periodo di incubazione è da 1 a 7 giorni, ma può essere anche più lungo. Il quadro clinico dell infezione da Campylobacter jejuni è molto simile a quello delle enteriti dovute ad altri batteri enteropatogeni, come Shigella, Salmonella, Escherichia coli invasivo e Amebiasi. I sintomi fondamentali dell infezione da Campylobacter jejuni sono rappresentati da: diarrea, dolori addominali (fino a far sospettare un appendicite acuta), febbre, generico stato di malessere.
13 Le feci possono contenere sangue ben visibile o possono mostrare la presenza di sangue solo attraverso le prove specifiche (sangue occulto). Le forme più lievi assomigliano strettamente alle gastroenteriti da Rotavirus: la diarrea cessa in 1-2 giorni e tutto passa in meno di 1 settimana; tuttavia, il 20% dei pazienti presenta una ricaduta o una malattia prolungata o i segni di una grave infezione, tanto da far sospettare talvolta una malattia infiammatoria cronica dell intestino. Nel neonato è possibile trovare una setticemia. Se l infezione capita in un soggetto immunocompromesso, è più facile che l infezione da Campylobacter jejuni si presenti come una forma prolungata o con localizzazione extraintestinale. Fra le complicazioni vanno ricordate: la sindrome di Guillain-Barré, la sindrome di Miller-Fisher, l artrite reattiva, la sindrome di Reiter, l eritema nodoso. In generale, c è una buona correlazione tra sintomatologia e meccanismo patogenetico: la diarrea acquosa è legata a ceppi che colonizzano il tenue prossimale e che danno vita a un enterotossina termolabile simile a quella prodotta da Escherichia coli; la diarrea mucoematica è dovuta, invece, a ceppi invasivi, simili a Shigella, che colonizzano il grosso intestino. Si ritrovano leucociti nelle feci nel 75% dei soggetti con infezione. Una diagnosi rapida è possibile nel laboratorio mediante tecniche di microscopia in campo oscuro e mediante la colorazione di Gram. Il Campylobacter jejuni può essere coltivato dalle feci su terreni selettivi. Per l identificazione di specie si ricorre a sonde DNA e alla reazione polimerasica a catena (PCR). La diagnosi sierologica può essere fatta con metodi immuno-enzimatici, per misurare i livelli di anticorpi IgA, IgM e IgG. Oltre alle normali misure di profilassi, viene consigliata un attenta sorveglianza per i pannolini e le feci in generale dei bambini affetti da questo tipo di gastroenterite. Fra le regole generali sono da ricordare: lavaggio attento delle mani dopo aver toccato gli animali in cui abbiamo visto albergare di frequente il Campylobacter jejuni; accurata pulizia delle mani e degli utensili da cucina dopo aver tagliato pollame crudo; cottura corretta dei polli e degli altri animali; pastorizzazione del latte e trattamento con cloro delle acque; il personale ospedaliero e gli alimentaristi con infezione asintomatica non costituiscono un rischio per la trasmissione dell infezione, per cui non debbono essere allontanati dal lavoro, se sono scrupolosamente seguite le correnti norme igieniche; i bambini con infezioni sintomatiche vanno esclusi dalla frequenza negli asili nido e nelle scuole materne, oppure vanno mantenuti in aree separate; non sono raccomandate colture delle feci per bambini asintomatici, in precedenza positivi o in bambini asintomatici esposti al contagio. Clostridium difficile È l agente eziologico della colite pseudomembranosa, in genere secondaria all assunzione di antibiotici, soprattutto in pazienti ospedalizzati, ma può essere causa di una diarrea di lieve entità non collegata alla terapia antibiotica. Si tratta di un batterio anaerobio gram-positivo che forma spore, rendendo così difficile la sua eliminazione dall ambiente ospedaliero. Infatti, spesso viene isolato sulle tende, sulle porte, sui comodini delle stanze dei pazienti infetti, dove può persistere fino a 5 mesi.
14 La diarrea si verifica per la produzione di 2 tossine (A e B) nel lume intestinale. La tossina A ha effetto citotossico e facilita l interazione tra epitelio intestinale e tossina B, che ha un effetto secretivo. Il danno esteso che si verifica sulla mucosa per azione della tossina A e l intenso infiltrato infiammatorio probabilmente portano alla disseminazione sia della tossina A sia di quella B nella circolazione sistemica. Poiché queste tossine causano infiammazione e, talvolta, necrosi della mucosa senza invasione batterica, si può osservare diarrea profusa con o senza enterorragia. Clostridium perfringens Dà luogo a una sindrome di intossicazione da cibo di breve durata dovuta alla produzione di un enterotossina termolabile. La malattia si risolve in 24 ore. Escherichia coli È un bacillo gram-negativo della famiglia delle Enterobacteriaceae, che vive come saprofita nell intestino, ma di cui esistono ceppi in grado di causare diarrea. Sulla base del loro meccanismo patogenetico, sono stati definiti diversi gruppi di Escherichia coli: Escherichia coli enterotossigenici (ETEC), Escherichia coli enteroinvasivi (EIEC), Escherichia coli enteropatogeni (EPEC), Escherichia coli enteroaggregativi (EAggEC), Escherichia coli enteroemorragici (EHEC). Gli ETEC (Escherichia coli enterotossigenici) rappresentano una delle principali cause di diarrea infantile con importante disidratazione nei paesi in via di sviluppo e sono frequentemente responsabili della cosiddetta diarrea del viaggiatore. Gli ETEC causano diarrea attraverso la produzione di enterotossine termolabili e termostabili. Il motivo per cui la diarrea dovuta alla tossina termostabile risulta particolarmente grave nelle prime epoche della vita è da mettere in relazione a un più elevato numero di recettori intestinali nell età pediatrica rispetto a quelle successive. Le infezioni da EIEC (Escherichia coli enteroinvasivi) generalmente si verificano negli adulti. Analogamente alla Shigella, gli EIEC colonizzano la mucosa del colon producendo una diarrea di tipo dissenterico. Gli EPEC (Escherichia coli enteropatogeni) sono responsabili della diarrea nosocomiale neonatale. Il contagio in genere avviene tramite le mani del personale medico e paramedico nei paesi industrializzati, mentre nei paesi in via di sviluppo avviene tramite formule o alimenti del divezzamento contaminati. Gli EPEC si distinguono dagli altri ceppi di Escherichia coli in quanto inducono una caratteristica lesione a livello degli enterociti del duodeno e per la loro incapacità a produrre tossine. Gli EAggEC (Escherichia coli enteroaggregativi) sono associati a diarree persistenti, in particolare in paesi sudamericani. Gli EHEC (Escherichia coli enteroemorragici), infine, sono responsabili di gravi tossinfezioni alimentari che si manifestano con diarrea ematica o colite emorragica. Sono stati identificati diversi sierotipi, ma il prototipo resta l Escherichia coli 0157:H7, di cui è ben conosciuta una grave complicanza: la sindrome emolitico-uremica.
15 Tutti i sierotipi producono una potente citotossina, di cui si conoscono 3 varianti antigenicamente correlate, indicate anche come Verotossine per l effetto patogeno su cellule Vero. Mycobacterium avium-intracellulare Può essere causa di diarrea nel paziente immunocompromesso, in particolare quando la conta dei linfociti CD4 è inferiore a 50/mm 3. Plesiomonas shigelloides È un bacillo gram-negativo responsabile di infezioni intestinali in ospiti immunocompromessi ma anche negli immunocompetenti. È comune ai tropici e nelle aree subtropicali, da dove deriva la maggior parte dei casi segnalati. Salmonella La Salmonella è un batterio gram-negativo della famiglia delle Enterobacteriaceae. Comprende 3 specie patogene per l uomo: 1. Salmonella typhi, 2. Salmonella choleraesuis, 3. Salmonella enteritidis, che include a sua volta oltre sierotipi. È possibile distinguere 5 sindromi cliniche dovute alla Salmonella: 1. gastroenterite acuta (75% dei casi); 2. batteriemia, con o senza interessamento intestinale (10% dei casi); 3. febbre tifoidea o enterica legata alla specie Salmonella typhi o, molto raramente, alla Salmonella enteritidis; 4. infezioni localizzate (circa il 5% dei casi); 5. stato di portatore. I sintomi della gastroenterite da Salmonella sono causati dall invasione della mucosa con infiammazione, dalla produzione di un enterotossina simile a quella del colera e di una citotossina che inibisce la sintesi proteica. L infezione è molto comune durante il primo anno di vita, diminuisce nella prima infanzia e rimane relativamente costante fino all età adulta. La maggior parte delle epidemie è dovuta al consumo di alimenti contaminati (carne bovina, pollame, uova e molluschi), ma è ben documentata anche la trasmissione interumana: l elevata frequenza di portatori sani e la prolungata escrezione del germe dopo un episodio acuto rendono l uomo un importante serbatoio di infezione. La sintomatologia più comune consiste in diarrea, febbre, dolore addominale. Nella maggioranza dei casi sono presenti nelle feci muco, sangue occulto e granulociti, una minoranza presenta diarrea acquosa importante o una sindrome dissenterica. La Salmonella batteriemia può associarsi all infezione intestinale e i pazienti immunocompromessi sono ad alto rischio di batteriemia.
16 Shigella È relativamente rara nei paesi industrializzati al di fuori di aree endemiche circoscritte. La trasmissione interumana è la più comune. Esistono 4 specie: la Shigella dysenteriae, che è la più diffusa e quella che causa sintomi più gravi, la Shigella flexneri, la Shigella boydii, la Shigella sonnei. Tutte provocano dissenteria e il quadro classico è caratterizzato da diarrea muco-ematica, febbre, dolori addominali e, talvolta, tenesmo. Si possono osservare convulsioni, di natura verosimilmente febbrile. La sintomatologia nel bambino è generalmente di media gravità e di durata variabile da 1 a 3 giorni, mentre negli adulti tende a persistere per 7 giorni o più. In alcuni casi, sia nel bambino sia nell adulto, la malattia può continuare fino a 3 settimane. Il meccanismo patogenetico è legato alla capacità di aderire agli enterociti, prevalentemente del grosso intestino. Dopo l adesione, la Shigella penetra nella cellula, prolifera e provoca la morte della cellula attraverso una tossina che agisce sull RNA ribosomiale bloccando la sintesi proteica. Vibrio cholerae Il Vibrio cholerae è un gram-negativo a forma di virgola mobile di cui si conoscono molti sierogruppi. Fino a poco tempo fa, solo il sierogruppo 01 produttore di enterotossina aveva causato epidemie. Il Vibrio cholerae 01 è suddiviso in: 2 sierotipi, Inaba e Ogawa, 2 biotipi, quello classico e quello El Tor. Negli ultimi 30 anni, il biotipo El Tor si è diffuso dall India e dal Sudest asiatico all Africa, Medio Oriente, Europa del Sud e Oceania, provocando diverse pandemie. Il Vibrio colpisce tutte le età, ma particolarmente i bambini. La diarrea è il risultato dell azione di una tossina costituita da una subunità A e un unità pentamerica B. Quest ultima consente il legame della tossina a uno specifico ganglioside presente sugli enterociti e l ingresso di parte della subunità A all interno dell enterocita. La tossina A induce l attivazione irreversibile dell adenilato ciclasi con aumento della Vibrio cholerae concentrazione intracellulare di AMP ciclico (camp). L aumento di camp provoca un inibizione dell assorbimento del sodio con secrezione di cloro e di acqua nel lume intestinale. La sintomatologia è caratterizzata da una diarrea di estrema gravità con vomito e dolori addominali. Nei casi più gravi compaiono precocemente i segni dell acidosi, della disidratazione gravissima e quindi dello shock. Vibrio parahaemolyticus È largamente distribuito nelle acque costiere, nei crostacei e nel pesce; la sua infezione è particolarmente frequente in Giappone, dove è comune il consumo di pesce crudo. La patogenesi sembra essere attribuita all effetto di una citotossina simile a quella della Shigella.
17 Yersinia enterocolitica È responsabile dell 1-2% delle diarree infantili. Sono state descritte epidemie da alimenti contaminati. Casi sporadici sono la conseguenza di contatti con animali o portatori umani, facilitati dalla prolungata escrezione fecale (15-90 giorni). La sintomatologia nel bambino piccolo (< 2-3 anni) è relativamente aspecifica e modesta, ma spesso la durata della diarrea è nettamente superiore (in media 14 giorni) a quella tipica delle gastroenteriti acute indotte da altri patogeni. Particolarmente a rischio di batteriemia sono gli immunodepressi, in particolare i talassemici, probabilmente per il sovraccarico di ferro che rappresenta un importante fattore di crescita per il microrganismo. Altri batteri Altri batteri, come Klebsiella, Citrobacter, Bacteroides fragilis, sono stati implicati nell eziologia della diarrea per la produzione di enterotossine e di altri fattori di patogenicità. Una loro definizione come agenti eziologici richiede procedure diagnostiche molto complete e non disponibili nei comuni laboratori di microbiologia. PARASSITI Cryptosporidium L infezione da Cryptosporidium è veicolata tramite l acqua o con una trasmissione interumana. Il meccanismo con cui provoca diarrea non è noto, ma sono state descritte numerose anomalie morfologiche, tra cui una distruzione dei microvilli di membrana e una parziale atrofia dei villi. La criptosporidiosi enterica può presentarsi con un ampio spettro di sintomi che vanno da una escrezione asintomatica fino a una diarrea acquosa grave o cronica. Il Cryptosporidium è responsabile del 10% dei casi di gastroenterite acuta di modesta entità e autolimitata in bambini immunocompetenti. Nei bambini con AIDS, la criptosporidiosi enterica ha un quadro clinico caratterizzato da una diarrea cronica e grave. Giardia lamblia Protozoo flagellato, responsabile di diarrea in popolazioni ad alto rischio e in persone che viaggiano in aree endemiche. I bambini sembrano più suscettibili alla Giardia degli adulti. Condizioni predisponenti per la giardiasi, oltre all età, sono: l ipogammaglobulinemia, il deficit di IgA secretorie, l ulcera peptica, le malattie delle vie biliari, la pancreatite. Giardia lamblia Il parassita può presentarsi come forma cistica e come trofozoita. Dopo l ingestione, ogni ciste si divide in due trofozoiti, che in seguito maturano. I trofozoiti sono riscontrati in aspirati duodenali e nelle feci molli, mentre le cisti possono rimanere vitali e contagiose nell acqua per più di 5 mesi.
18 Le manifestazioni cliniche sono: una forma asintomatica; una malattia acuta con scariche improvvise di feci acquose, maleodoranti, flatulenza, distensione addominale, nausea; una diarrea cronica con malassorbimento, distensione addominale, flatulenza e dolore. La Giardia si trova nelle feci di soggetti sani con una prevalenza fino al 10%, pertanto il suo ruolo eziologico nel singolo bambino con diarrea va valutato con cautela. Diarrea da antibiotici Molti farmaci possono indurre diarrea come effetto collaterale, ma particolare importanza riveste la diarrea associata agli antibiotici. Ha un incidenza variabile tra l 11% e il 40%, con un tasso più elevato in età precoce, nei soggetti ospedalizzati e negli immunodepressi. Tutti gli antibiotici possono essere causa di diarrea, ma il rischio è più alto con: le cefalosporine, l associazione di amoxicillina e acido clavulanico la clindamicina. Il meccanismo eziopatogenetico è, nella maggior parte dei casi, da attribuirsi alle alterazioni della flora intestinale anaerobica che, da un lato comporta conseguenze metaboliche, quali la ridotta digestione di carboidrati e la minore degradazione dei sali biliari e la successiva diarrea osmotica e, dall altro consente la colonizzazione da parte di altre specie patogene tra cui Salmonella, Clostridium perfringens, Staphylococcus aureus, Candida albicans e Clostridium difficile in una minore percentuale di casi.
19 FISIOPATOLOGIA Acqua ed elettroliti sono indispensabili alla sopravvivenza di ogni individuo. Ogni giorno, circa 8-9 litri di liquidi entrano nell intestino tenue adulto, dei quali solo 1-2 litri sono costituiti da acqua ingerita con gli alimenti, mentre tutto il resto deriva da fonti endogene come le secrezioni salivari, gastriche, pancreatiche, biliari e intestinali. La maggior parte di questi liquidi viene assorbita nell intestino tenue, per cui solo 1,5 litri raggiungono il colon, che ne riassorbe la maggior parte: il contenuto idrico delle feci ammonta invece a circa ml al giorno. La diarrea è l inversione del normale stato di regolazione del trasporto di acqua ed elettroliti nell intestino, con passaggio da un assorbimento netto alla secrezione di elettroliti e acqua nel lume intestinale. La definizione del meccanismo può essere utile per un orientamento diagnostico differenziale tra forme dovute a germi invasivi e forme dovute a germi enterotossigeni. Infatti, alcuni microrganismi inducono danno cellulare e malassorbimento, altri prevalentemente o esclusivamente diarrea secretiva (vedi Tabella 6). Nel primo caso, la sintomatologia è caratterizzata da feci diarroiche con un contenuto di acqua relativamente modesto, ma con presenza di muco e sangue (micro o macroscopico). Nel secondo caso, la diarrea è caratterizzata da evacuazioni di grossi volumi di feci acquose, ma senza muco o sangue. Patogeni responsabili esclusivamente di diarrea secretiva Aeromonas Escherichia coli enterotossigeni (ETEC) Enterobatteri ST-produttori (Klebsiella, Citrobacter) Vibrio cholerae Patogeni responsabili di diarrea osmotica Campylobacter Clostridium difficile Entamoeba histolytica Escherichia coli enteroinvasivi (EIEC) Rotavirus Salmonella Shigella Yersinia Patogeni responsabili di diarrea infiammatoria Campylobacter jejuni Escherichia coli enteroinvasivi (EIEC) Salmonella Shigella Yersinia Patogeni in cui la diarrea si realizza con meccanismi secretivi e osmotici Bacteroides fragilis Campylobacter Cryptosporidium Escherichia coli enteroemorragici (EHEC) Escherichia coli enteroinvasivi (EIEC) Escherichia coli enteropatogeni (EPEC) Salmonella Shigella dysenteriae tipo I Virus (Rotavirus, Adenovirus, Coronavirus, Enterovirus, Astrovirus) Yersinia Tabella 6. Meccanismi patogenetici della diarrea in relazione all agente eziologico (Fonte: Guarino A, Albano F. La gastroenterite: fisiopatologia e correlati clinici diagnostici. Area Pediatrica, n. 2 anno 7, febbraio 2006).
20 Diarrea osmotica La diarrea osmotica è secondaria al danno cellulare con riduzione della superficie assorbente ed è riconducibile alla presenza nel lume intestinale di sostanze non riassorbibili e osmoticamente attive, che richiamano liquidi all interno dell intestino, con conseguente aumento del volume fecale. Il danno può essere causato sia dalla penetrazione del microrganismo nella mucosa, sia dall azione di citotossine elaborate dal microrganismo stesso. Ne deriva un alterazione delle funzioni di digestione e assorbimento dell enterocita. La presenza di soluti non assorbiti nel lume intestinale esercita una forza osmotica che richiama acqua nel lume con conseguente diarrea. Tra le condizioni caratterizzate da diarrea di tipo osmotico si possono citare l intolleranza al lattosio e le forme da malassorbimento di carboidrati, ma anche le diarree infettive in cui i microrganismi inducono lisi cellulare tramite penetrazione diretta o produzione di tossine, come nel caso dell infezione da Rotavirus. L ingestione di grandi quantità di exitoli, come il sorbitolo e il mannitolo, usati come sostituti dello zucchero, provoca una diarrea osmotica a causa del loro lento assorbimento e dell accelerazione della peristalsi intestinale. Questa forma di diarrea, causata di frequente dall abuso di succhi di frutta ipertonici, è facilmente correggibile modificando le abitudini alimentari del bambino. Nella diarrea osmotica, il volume fecale è proporzionato all assunzione del substrato non riassorbibile e di solito risulta inferiore ai 200 ml/die. Le feci sono acquose e caratterizzate da ph acido e osmolarità aumentata, perché influenzata, in questo caso, non solo dagli elettroliti, ma anche dalla presenza del soluto nel lume intestinale e dei suoi prodotti di degradazione. Diarrea secretoria La diarrea secretoria si verifica per l azione di tossine prodotte da alcuni microrganismi. Le enterotossine possono indurre un attivazione dell adenilato ciclasi o della guanilato ciclasi, con conseguente accumulo endocellulare di AMP o GMP ciclico. Un terzo e importante meccanismo coinvolge, invece, il sistema calcio-calmodulina, una proteina che lega il calcio e ha funzioni di regolazione. La concentrazione intracellulare di calcio, bassissima in condizioni fisiologiche, è aumentata da tossine che attivano una fosfolipasi calcio-dipendente che idrolizza alcuni fosfolipidi di membrana; i prodotti di tale idrolisi determinano l apertura dei canali del calcio e la liberazione dello ione dal reticolo endoplasmatico, aumentandone la concentrazione intracellulare. Alcuni di questi prodotti, infine, sono substrati per la produzione di acido arachidonico, precursore di prostaglandine e di leucotrieni, noti stimolatori della secrezione intestinale. A sua volta, il calcio è in grado di modificare, direttamente o attraverso l attivazione di chinasi specifiche o della calmodulina, la struttura delle proteine di trasporto di membrana e l azione di cgmp e di camp. Questi mediatori intracellulari sono responsabili di una riduzione dell assorbimento di sodio e di cloro (e di conseguenza di acqua) e di un aumento della secrezione attiva di elettroliti e liquidi. Lo squilibrio del rapporto tra assorbimento e secrezione di acqua e ioni è responsabile della diarrea. La diarrea secretoria è dovuta quindi alla secrezione nel lume intestinale di acqua ed elettroliti in eccesso rispetto alla capacità degli enterociti di riassorbirli. Nella diarrea secretoria tipica, quale quella indotta da alcune enterotossine batteriche, si verifica un aumentata secrezione di anioni provenienti principalmente dalle cellule delle cripte ghiandolari. Nella diarrea secretiva, i processi di trasporto elettrolitico degli enterociti passano a uno stato di secrezione attiva. La causa più comune è un infezione intestinale batterica nella quale possono intervenire diversi meccanismi. Dopo la colonizzazione, il patogeno può aderire all epitelio oppure invaderlo; può produrre enterotossine (cioè esotossine che inducono secrezione mediante l innesco di un secondo
21 messaggero intracellulare) o citotossine. Il patogeno può anche indurre il rilascio di citochine che attraggono cellule infiammatorie, le quali, a loro volta, contribuiscono alla secrezione attiva, inducendo il rilascio di agenti quali prostaglandine o fattore attivante le piastrine. L azione della tossina del Vibrio cholerae esemplifica il meccanismo della diarrea secretoria, in quanto il legame della tossina a recettori epiteliali causa l aumento di mediatori intracellulari come AMP ciclico, GMP ciclico e calcio, con conseguente aumento della secrezione di cloro da parte delle cripte e diminuito riassorbimento di sodio e cloro dai villi intestinali. Altri esempi di sostanze secretagoghe includono le tossine di Escherichia coli enterotossigeno, i virus enteropatogeni, gli acidi biliari, i grassi alimentari non assorbiti, alcuni farmaci come quelli prostaglandino-simili e gli ormoni peptidici, come il peptide intestinale vasoattivo (VIP) prodotto dai tumori neuroendocrini. Anche agenti infettivi classificati come cause di diarrea osmotica (cioè perdite di fluidi ed elettroliti dovute al malassorbimento di contenuto intestinale) possono aumentare la secrezione degli enterociti. Il Rotavirus, per esempio, danneggia l orletto a spazzola dei villi provocando diarrea osmotica, ma produce anche un enterotossina che provoca una diarrea secretiva Ca 2+ -mediata. L infezione da Vibrio cholerae si associa a una perdita fecale di sodio di circa meq/l, l infezione da Escherichia coli enterotossigeno a perdite di meq/l e la diarrea da Rotavirus a perdite di meq/l. Nella diarrea secretoria, le feci sono tipicamente voluminose (> 200 ml/die) con ph > 6 e osmolarità nella norma. I segni distintivi della diarrea secretiva includono un elevata frequenza di evacuazioni, la mancata risposta al digiuno e un normale gap ionico fecale (cioè 100 mosm/kg o meno), indicando così che l assorbimento dei nutrienti è intatto. Studi clinici hanno chiaramente dimostrato che, sebbene la natura secretiva della diarrea da enterotossine batteriche provochi considerevoli perdite fecali di acqua ed elettroliti, il meccanismo del co-trasporto di Na e soluti è intatto e consente un efficace riassorbimento di sali e acqua. La scoperta di questo meccanismo, e del fatto che esso rimane intatto anche in pazienti con diarrea secretiva severa, ha costituito il principale razionale per l aggiunta di glucosio alle soluzioni reidratanti orali. Soluzioni reidratanti orali addizionate con altri co-trasportatori di Na, hanno offerto risultati promettenti. Studi di perfusione nell intestino di ratto hanno mostrato che l assorbimento di acqua aumenta in proporzione diretta alla concentrazione di glucosio, ma il sistema è saturabile. Una volta superata una determinata concentrazione di glucosio nel liquido di perfusione (nel ratto circa 60 mmol/l), l assorbimento di acqua rimane stabile ma, se la concentrazione aumenta di oltre 2 volte, il flusso si inverte e l assorbimento di acqua diminuisce drasticamente. In effetti, studi clinici hanno chiaramente dimostrato che le soluzioni di minore osmolarità che mantengono inalterato il rapporto di 1-2:1 tra sodio e glucosio funzionano benissimo per il trattamento della diarrea, mentre le soluzioni reidratanti con un elevata concentrazione di co-trasportatori funzionano come soluzioni ipertoniche e comportano il rischio di ridurre piuttosto che migliorare l assorbimento di sodio e acqua. Diarrea di tipo infiammatorio La diarrea di tipo infiammatorio può essere acuta o cronica. Mentre la seconda è tipica delle malattie infiammatorie croniche intestinali, in particolare il morbo di Crohn e la colite ulcerosa, le forme acute di diarrea infiammatoria sono riconducibili all azione di patogeni enteroinvasivi, come Salmonella, Shigella, Amoeba, Yersinia enterocolitica ed Escherichia coli enteroinvasivo. Il processo infiammatorio in questi casi è la risposta all invasione diretta da parte del patogeno.
22 Dal punto di vista clinico, nella diarrea infiammatoria le feci si presentano miste a sangue, muco e leucociti, con sintomi di accompagnamento quali tenesmo. Il prototipo di questo meccanismo è quello della Shigella che, oltre a invadere l epitelio, elabora una citotossina in grado di avere multipli effetti patogeni sull epitelio intestinale: la stimolazione diretta della secrezione di ioni, un aumento della permeabilità cellulare, un danno diretto sulla cellula intestinale e l attivazione del sistema delle cellule infiammatorie, i cui prodotti possono a loro volta alterare i meccanismi di trasporto di elettroliti e dare danno cellulare. Diarrea da disturbi della motilità intestinale La diarrea da disturbi della motilità è conseguente a un accelerato transito intestinale, come avviene ad esempio nella sindrome del colon irritabile o nella tireotossicosi, in cui il ridotto tempo di contatto dei soluti con la mucosa intestinale ne riduce l assorbimento. Diarrea da Rotavirus: modello fisiopatologico per entrambi i meccanismi, osmotico e secretivo Il Rotavirus, l agente eziologico più frequente di diarrea in età pediatrica, rappresenta il classico modello che spiega come un microrganismo sia in grado di causare diarrea con entrambi i meccanismi, e questo rende ragione della particolare gravità della sintomatologia. Il Rotavirus induce diarrea con 2 diversi meccanismi: 1. quello osmotico, derivante dal danno cellulare legato alla localizzazione elettiva del virus nelle cellule mature dei villi del tenue; 2. quello secretivo, dovuto alla proliferazione di cellule delle cripte che si moltiplicano rapidamente per compensare l aumentata distruzione di cellule del villo intestinale causata dal Rotavirus. Esse migrano velocemente lungo l asse cripta/villo, senza avere il tempo di sviluppare le normali funzioni digestivo-assorbenti e mantenendo, invece, il fisiologico stato secretivo, tipico delle cellule epiteliali poco differenziate delle cripte. Il virus infetta principalmente gli enterociti maturi dell apice del villo intestinale e induce diarrea acquosa. La diarrea da Rotavirus è stata a lungo considerata una diarrea osmotica da malassorbimento, in quanto il Rotavirus altera l attività delle disaccaridasi intestinali e il cotrasporto Na + -soluti associato al trasporto di acqua. Tuttavia, la diarrea da Rotavirus può manifestarsi anche in assenza di danno tessutale intestinale visibile e, per contro, le lesioni istologiche indotte da Rotavirus possono essere asintomatiche. Nelle fasi iniziali della diarrea da Rotavirus non si osservano alterazioni istologiche nell intestino. Infatti, le fasi iniziali della diarrea sono il risultato dell azione di una glicoproteina non strutturale del virus, che induce secrezione di cloro attraverso un meccanismo calcio-dipendente (vedi Figura 2). La glicoproteina NSP4 (Non Structural Protein 4) è considerata la prima dimostrazione di un enterotossina prodotta da virus. La severità delle lesioni istologiche è chiaramente dipendente sia da fattori virali, sia da fattori inerenti l ospite. Nei modelli animali, anche quando vi erano piccole erosioni della superficie epiteliale, non vi erano né significativa perdita di enterociti, né appiattimento della mucosa. È quindi possibile che la diarrea da Rotavirus non sia necessariamente conseguenza di una lesione fisica ma, al contrario, la disfunzione cellulare sia la causa piuttosto che la conseguenza dell eventuale danno istologico. Nei topi, una diminuzione delle attività disaccaridasiche indotta da Rotavirus in vivo si verifica con una membrana dell orletto a spazzola relativamente intatta. In cellule umane Caco-2 sia l attività sia l espressione in vitro della saccarasi-isomaltasi sono ridotte dall infezione senza alcuna apparente distruzione degli enterociti, probabilmente a causa di un blocco del traffico delle proteine verso l orletto a spazzola.
23 Nell intestino di coniglio, l attività di trasporto combinato Na + -glucosio mediata da SGLT1, presente nell orletto a spazzola delle cellule dei villi e delle cripte, anche se più elevata nei villi che nelle cripte, è inibita dal Rotavirus in assenza di danno tessutale. Dalla scoperta dell enterotossina NSP4 sono emersi vari elementi che suggeriscono l esistenza di una componente secretiva nella patogenesi della diarrea da Rotavirus. Il Rotavirus induce una moderata secrezione netta di cloro all inizio della diarrea, ma il meccanismo sembra essere alquanto diverso da quelli utilizzati dalle enterotossine batteriche che causano diarrea secretiva pura. Il Rotavirus, infatti, non stimola la secrezione di Cl dalle cripte, mentre stimola il riassorbimento di Cl nei villi, mettendo quindi in discussione l origine della secrezione netta di Cl. Essendo assente nel virione infettante maturo, NSP4 deve essere sintetizzata negli enterociti infettati del villo intestinale, ed è stato mostrato che il prodotto di cleavage di NSP4 (NSP4- peptide ) viene secreto nel medium extracellulare e/o nel lume intestinale. Analogamente alla proteina NSP4 completa e al NSP4-peptide , il NSP4-peptide induce diarrea nel topo neonato in assenza di qualsiasi danno istologico della mucosa intestinale. Il peptide NSP sarebbe disponibile per legare un recettore della membrana apicale negli enterociti dei villi e forse anche delle cripte e delle cellule enterocromaffini, per innescare una sequenza di eventi che porta alla diarrea secretiva. La secrezione del cloro è regolata da un segnale del calcio fosfolipasi C-dipendente indotto da NSP4. La risposta complessiva, tuttavia, è debole, il che suggerisce che NSP4 possa esercitare entrambe le azioni, prima secretiva e successivamente anti-secretiva, limitando così la secrezione di Cl. Poiché SGLT1 favorisce il riassorbimento dell acqua in condizioni fisiologiche, il meccanismo della diarrea da Rotavirus può comprendere un inibizione generalizzata dei sistemi di trasporto abbinato Na + /soluti, e quindi del riassorbimento di acqua. È stato dimostrato che, nell orletto a spazzola dell intestino di coniglio, il NSP4-peptide inibisce direttamente e in modo praticamente istantaneo SGLT1, ma non le attività di trasporto abbinato Na + -leucina. Tutte queste osservazioni supportano il concetto che NSP4 possa agire come un enterotossina, funzionante però in modo alquanto diverso dalle enterotossine batteriche, inducendo una diarrea di tipo misto piuttosto che una diarrea secretiva. Figura 2. Effetti della NSP4 nella patofisiologia della diarrea da Rotavirus (Fonte: Guarino A, Albano F. La gastroenterite: fisiopatologia e correlati clinici diagnostici. Area Pediatrica, n. 2 anno 7, febbraio 2006).
24 Nella figura sono descritti gli effetti della NSP4 nella patofisiologia della diarrea, che possiamo così sintetizzare: il Rotavirus infetta le cellule epiteliali del piccolo intestino, si replica e induce lisi cellulare. La NSP4 (Non Structural Protein 4) è rilasciata dalle cellule infettate e funziona come enterotossina calcio-dipendente, provocando secrezione di cloro. La NSP4 diminuisce il trasporto di fluidi ed elettroliti mediante l inibizione della SGLT1 e probabilmente della Na-K ATPasi, e altera anche l espressione della disaccaridasi. Il Rotavirus e la NSP4 possono diffondersi al di là dell epitelio intestinale, attivando il sistema nervoso enterico, con ulteriore secrezione. Infine, durante l infezione si determina una risposta infiammatoria nella lamina propria con produzione di sostanze infiammatorie, in particolare di citochine che contribuiscono all aumento della permeabilità intestinale e, quindi, alla diarrea. Meccanismo d azione dell enterotossine virali e batteriche I meccanismi mediante i quali il Rotavirus e l enterotossina NSP4 causano diarrea sono quindi alquanto diversi da quelli descritti per le enterotossine batteriche, come la tossina colerica e le enterotossine termolabili e termostabili dell Escherichia coli, che provocano una diarrea secretiva pura. Sembra che l unica caratteristica comune delle enterotossine batteriche e virali sia che nessuna delle due causi un evidente danno morfologico. Nella Tabella 7 sono fornite le principali caratteristiche delle malattie diarroiche associate alle enterotossine batteriche e all enterotossina virale NSP4. ENTEROTOSSINE BATTERICHE Vibrio cholerae ed Escherichia coli ENTEROTOSSINE VIRALI NSP4 di Rotavirus Danno morfologico No No Assorbimento di D-glucosio via SGLT1 Assorbimento di Cl nelle cellule del villo Secrezione di Cl nelle cellule delle cripte Inalterato Ridotto Aumentata Ridotto Aumentato Inalterata Secrezione netta di Cl Notevole Moderata Mediatori intracellulari della secrezione di Cl Nucleotidi ciclici (camp, cgmp) Ca 2+ Tabella 7. Principali caratteristiche delle malattie diarroiche associate alle enterotossine batteriche e all enterotossina virale NSP4. Meccanismi endogeni di controllo della secrezione e dell assorbimento Numerosissimi fattori possono essere coinvolti nella regolazione endogena della secrezione e del (ri)assorbimento intestinale di elettroliti e acqua. Mediante l attivazione di secondi messaggeri quali camp, cgmp e Ca 2+, un effetto stimolante sulla secrezione è svolto da neurotrasmettitori quali peptide intestinale vasoattivo (VIP), ossido nitrico (NO), acetilcolina, istamina, serotonina, sostanza P, neurotensina, ma anche da adenosina, prostaglandine, bradichinina, guanilina e ATP. Citochine pro-infiammatorie come IFN-γ, TNF-α, IL-1 e il fattore di crescita epidermico 1 (EGF-1) inducono secrezione attraverso l attivazione di vie come la tirosina- e la MAP-chinasi o la regolazione dell espressione genica. L assorbimento di acqua e sali può essere stimolato anch esso in vari modi.
25 Catecolamine, neuropeptide Y (NPY), encefaline e somatostatina agiscono mediante l inibizione del camp intracellulare. Nutrienti quali glucosio, aminoacidi e oligopeptidi agiscono attraverso il co-trasporto di Na+ (SGLT1, vedi sopra), mentre gli ormoni steroidei promuovono l assorbimento di acqua e sali attraverso meccanismi diversi. Le encefaline sono neurotrasmettitori normalmente presenti nel sistema nervoso enterico, dotati di un elevata affinità per i recettori δ degli oppioidi. La loro stimolazione blocca l adenilciclasi enterocitaria, e quindi esercita un marcato effetto inibitorio sulla secrezione intestinale di elettroliti e acqua (e, in misura molto minore, sulla motilità intestinale). Le encefaline vengono rapidamente degradate dalle encefalinasi presenti nel lume intestinale. L inibizione delle encefalinasi da parte di sostanze come l acetorfano si è dimostrata in grado di ridurre rapidamente e significativamente la secrezione di acqua ed elettroliti e, quindi, il contenuto idrico delle feci. Altre forme di diarrea acuta La diarrea essudativa deriva da un danno esteso dovuto a infiammazione e/o ulcerazione della mucosa del tenue o del colon come avviene tipicamente nella malattia di Crohn e nella colite ulcerosa che porta a perdita di muco, proteine e sangue nel lume. In queste condizioni, l aumentata escrezione di acqua ed elettroliti nelle feci deriva dal ridotto (ri)assorbimento da parte della mucosa intestinale infiammata piuttosto che dall attiva secrezione nell essudato. Altre cause non infettive di diarrea acuta includono: la colite ischemica, l ostruzione intestinale, gli ascessi pelvici nell area retto-sigmoidea, l intossicazione acuta da alcol, l ingestione di zuccheri poco assorbibili come il lattulosio. Infine, la diarrea è uno dei più comuni effetti collaterali dei farmaci, soprattutto di alcuni antibiotici.
26 DIARREA DA ROTAVIRUS La diarrea è la causa principale di morte nei primi due anni di vita in tutto il mondo: si pensa che le siano attribuibili fra i 5 e i 10 milioni di morti ogni anno. La causa più frequente della grave diarrea, e quindi della disidratazione, è l infezione da Rotavirus. L enterite da Rotavirus varia ampiamente nei suoi aspetti clinici: da forme asintomatiche o molto lievi di malattia, a forme gravi con disidratazione e collasso circolatorio. La malattia è preceduta da scarsa febbre e da vomito, cui segue una diarrea acquosa, povera di muco, con scarsa partecipazione dei leucociti e perlopiù senza sangue. Le scariche possono essere anche nelle 24 ore. La febbre e il vomito si attenuano durante il secondo giorno di malattia, ma il quadro intestinale diarroico dura per 5-7 giorni, anche se tende a risolversi spontaneamente. La disidratazione può insorgere all improvviso, soprattutto nei lattanti, sia per le forti perdite di acqua e di sali (sodio, potassio e bicarbonati) con le feci, sia per l impossibilità di bere, a conseguenza del vomito. Un precedente stato di malnutrizione può influire negativamente sulla malattia. Possono associarsi manifestazioni a carico delle vie aeree superiori, come faringite o lieve arrossamento della membrana del timpano, senza isolamento del virus in quelle sedi. I bambini che hanno superato l infezione hanno molte probabilità di presentare nuove infezioni da Rotavirus nelle stagioni invernali successive. I neonati infettati dai Rotavirus sono in generale completamente asintomatici, ma talvolta sono state descritte epidemie di enterocolite necrotizzante, dovute alla comparsa di un nuovo Rotavirus nella nursery. I bambini immunodeficienti e malnutriti possono presentare talvolta forme particolarmente gravi e durature. Anche l adulto è colpito dall infezione da Rotavirus, attraverso la trasmissione oro-fecale del virus: tipicamente nell adulto, l infezione determina nausea, stato di malessere, cefalea, crampi addominali, diarrea e febbre; tuttavia, anche nell adulto, l infezione può avvenire senza sintomi. Eziologia Il Rotavirus causa malattia nell uomo e in quasi tutti gli animali. Tali virus costituiscono un genere distinto della famiglia delle Reoviridae: contengono una doppia elica di RNA, racchiusa in un doppio capside. Il loro diametro è di circa 70 nm; sono suddivisi in 7 gruppi daa a G, ognuno dei quali infetta varie specie animali, in sottogruppi e in sierotipi. L RNA codifica 6 proteine virali (VP), che formano le proteine del capside, e 6 proteine non strutturali (NSP)., Il gruppo tradizionale di Rotavirus è il gruppo A, responsabile delle diarree nei lattanti e nei bambini. Esso comprende una varietà di virus che danno infezioni anche negli animali. Il gruppo B è di rado causa di gravi malattie nei bambini e negli adulti ed è diffuso soltanto in Cina. Ancor più rado, il gruppo C può dare epidemie nell uomo, mentre di frequente è responsabile di infezione nei mammiferi (maiali, vitelli, agnelli). Gli altri gruppi (D e G) interessano solo gli animali (uccelli, polli e ancora maiali). La particella virale è composta da 3 strati concentrici che racchiudono l RNA a doppia Micrografia elettronica di Rotavirus elica, di cui lo strato esterno contiene 2
27 proteine strutturali, la VP7 (glicoproteina chiamata proteina G) e la VP4 (emoagglutinina sensibile alle proteasi, chiamata proteina P). La proteina VP4 costituisce le proiezioni a raggio, che danno l impressione di una ruota. Queste due proteine definiscono il sierotipo del virus e sono considerate basilari per lo sviluppo di un vaccino, perché sono il bersaglio degli anticorpi neutralizzanti, che possono dare protezione. Queste 2 proteine a loro volta si suddividono in diversi tipi: la proteina G (VP7) in 14 sierotipi, la proteina P (VP4) in 20 sierotipi. Gli anticorpi verso la proteina G e la proteina P sono neutralizzanti in vitro. 5 tipi della proteina G (1, 2, 3, 4 e 9) e 3 tipi della proteina P (1A, 1B e 2) sono responsabili più spesso delle malattie nell uomo. I ceppi sono indicati generalmente a seconda della specificità G (per esempio G1) e della specificità P. I differenti ceppi predominano in diverse parti del mondo. Le differenze virali si manifestano in natura grazie al fenomeno del riarrangiamento, cioè della mescolanza di geni di differenti sottotipi o ceppi, con la produzione di un nuovo ceppo, analogamente a quanto avviene per il virus dell influenza. Epidemiologia Le infezioni da Rotavirus si verificano in tutto il mondo: i Rotavirus sono responsabili di circa il 50% delle diarree acute epidemiche, in bambini al di sotto dei 3 anni. Dopo il terzo mese, la prima infezione si associa in genere a diarrea; entro i 3 anni di vita, quasi tutti bambini, di tutto il mondo, si sono infettati con i Rotavirus. All età di 5 anni, quasi tutti i bambini hanno avuto un episodio di gastroenterite da Rotavirus: 1 su 5 ha avuto una visita da un pediatra, 1 su 65 è stato ospedalizzato e 1 su 293 è morto. Figura 3. Malattia e morti nel mondo per Rotavirus (Fonte: Umesh D. Parashar et al. Global Illness and Deaths Caused by Rotavirus Disease in Children. Emerging Infectious Diseases, Vol. 9, n. 5, May 2003). La proporzione delle morti attribuibili alla diarrea nei bambini di 5 anni o meno è inversamente proporzionale al reddito: nei paesi a basso reddito la proporzione media della letalità è del 21%; nei paesi a reddito medio-basso è del 17%; nei paesi a reddito medio-alto è del 9%; nei paesi a reddito alto è dell 1% o meno.
28 In una statistica del Nord Italia, eseguita in ospedale, il 23,9% dei bambini ricoverati con gastroenterite aveva un istologia da Rotavirus (Medici MC et al. 2004): circa il 30% degli episodi avveniva in soggetti in età inferiore ai 4 anni. Negli Stati Uniti, i Rotavirus sono responsabili di circa visite mediche, ospedalizzazioni e da 20 a 40 morti ogni anno; il carico economico è di 1 miliardo di dollari fra costi diretti e indiretti (Clark HF et al. 2004). Nei primi 3 mesi di vita, le infezioni sono generalmente asintomatiche, probabilmente per la difesa conferita dal latte materno o per gli anticorpi trasmessi attraverso la placenta nell ultima parte della gravidanza, ma sono state rilevate anche modificazioni maturative dell epitelio intestinale, che, nei primi mesi di vita, sarebbe meno suscettibile all infezione e, quindi, alla malattia. Su questa base, è stata anche sospettata una possibile scarsa risposta immunologica alla vaccinazione, quando questa viene eseguita prima della fine del secondo mese di vita. Mentre nei paesi occidentali a clima temperato è difficile che l infezione da Rotavirus si accompagni a quadri clinici gravi, nei paesi in via di sviluppo i Rotavirus rappresentano un importante componente della mortalità infantile. Secondo l andamento epidemiologico, la malattia da Rotavirus si può presentare con quattro diverse modalità: malattia endemica, ondate epidemiche, gastroenterite del viaggiatore, infezioni trasmesse dal bambino all adulto. Il ruolo dell immunità nel proteggere contro l infezione da Rotavirus è convalidato dall osservazione che l incidenza e la gravità della malattia diminuiscono con l aumentare dell età, che le infezioni neonatali, anche asintomatiche, proteggono i bambini dalle malattie successive e, infine, che i bambini durante la loro vita hanno ripetute malattie da Rotavirus, progressivamente sempre più lievi, dovute a sierotipi diversi. Poco si sa sul modo in cui si diffondono i Rotavirus. L osservazione che in tutte le parti del mondo i bambini si infettano precocemente, suggerisce che i Rotavirus non siano trasmessi attraverso l acqua o cibi contaminati con le feci, tanto è vero che è difficile che i miglioramenti nell approvvigionamento dell acqua e nell igiene pubblica alterino l incidenza della malattia. Probabilmente basta un inoculum piccolo, come è possibile nella diffusione delle goccioline di saliva nel contatto fra una persona e un altra, o tramite oggetti. D altra parte, la malattia si manifesta nei climi temperati durante la stagione invernale (vedi Figura 4), proprio come avviene per tutti gli altri virus che colpiscono le vie aeree superiori, come l influenza, i virus parainfluenzali e gli altri. In ogni caso, la via oro-fecale viene riconosciuta come una via importante di infezione, proprio perché attraverso le feci (soprattutto fra il secondo e il quinto giorno di malattia) viene diffusa la maggiore quantità di virus. Viene calcolato che durante l infezione dei bambini sono eliminate con le feci particelle virali.
29 Figura 4. Mese di punta dell attività del Rotavirus negli Stati Uniti, giugno 2005-giugno 2009 (Fonte: Payne DC, Wikswo M, Parashar UD. Rotavirus. Manual for the Surveillance of Vaccine-Preventable Diseases. 5th Edition, CDC: Centers for Disease Control and Prevention). L uomo sembra sia la sola riserva di alcuni tipi di virus; per cui pare che il passaggio dagli animali all uomo avvenga molto difficilmente. Tuttavia, la grande diffusione delle infezioni da Rotavirus negli animali e il reperto di segmenti di genoma, comune nei Rotavirus umani e animali, indicano che una certa ricombinazione di ceppi possa avvenire in natura, e che questo riassetto genetico possa essere importante nell evoluzione del virus, analogamente a quanto dimostrato per il virus influenzale. La possibilità di riarrangiamento genico fra ceppi umani e ceppi animali è stata sfruttata per la preparazione di diversi vaccini. Come stiano effettivamente i rapporti fra immunità e trasmissione dei Rotavirus, si può meglio ricavare dagli studi epidemiologici. Mentre si pensava che l immunità potesse proteggere completamente un adulto dalla malattia, è stato visto che i genitori e il personale di assistenza dei bambini con diarrea da Rotavirus possono presentare una malattia lieve, probabilmente perché esposti a forti inocula, come è possibile nei contatti stretti figlio-genitore e quando si procede al cambio dei pannolini in corso di diarrea. Le epidemie di diarrea da Rotavirus negli asili nido, nelle scuole materne o in ospedale possono essere legate alla rapida diffusione fra lattanti e bambini piccoli non immuni, presumibilmente per contatto diretto da persona a persona, attraverso le goccioline di saliva o il contatto con giocattoli contaminati. Negli anziani, invece, le epidemie possono essere dovute alla progressiva riduzione delle difese immunitarie.
30 I viaggiatori nei paesi in via di sviluppo, che probabilmente sono già immuni, possono ugualmente presentare diarrea, forse perché il modo di diffondersi dei Rotavirus è diverso per l eccessiva grandezza dell inoculum. Infine, nei soggetti immunocompromessi, di qualsiasi natura, si può sviluppare una diarrea da Rotavirus ad andamento prolungato con eliminazione del virus per mesi. Molte differenze nell epidemiologia dei Rotavirus possono essere notate nella diffusione di questi virus e delle malattie a essi connessi, a seconda della situazione geografica e, quindi, della divisione in paesi sviluppati e in via di sviluppo. In primo luogo, nei climi temperati il periodo di ospedalizzazione per diarrea da Rotavirus è soprattutto la stagione invernale, mentre nei climi tropicali il periodo di ospedalizzazione si estende per tutto l anno. Ne consegue che un bambino nato in un paese a clima temperato affronterà una stagione di elevata diffusione dei Rotavirus, che si ripeterà solo nell anno successivo, mentre un bambino nato in un paese tropicale sarà esposto al Rotavirus ogni giorno per tutto l anno. Ne consegue che l età media alla prima infezione sarà più precoce nei climi tropicali e che in questi paesi il maggior numero di attacchi di diarrea da Rotavirus avverrà nel primo anno di vita, mentre nei paesi a clima temperato la malattia sarà presente principalmente nel secondo o terzo anno di vita. Le differenze riguardano poi anche l agente causale: mentre nei paesi sviluppati le epidemie sono dovute quasi sempre a un solo ceppo di Rotavirus, nei paesi in via di sviluppo a clima tropicale le infezioni da Rotavirus sono spesso miste, con due o tre ceppi in circa il 30% dei casi e, soprattutto, con sierotipi sconosciuti, al di fuori di quelli sopra ricordati. La maggior parte delle malattie che colpiscono l uomo derivano dal contatto con persone affette; non è infatti documentata la possibilità di passaggio dell infezione dagli animali all uomo. È frequente la diffusione all interno di famiglie e di comunità infantili; in corsia è una delle più comuni cause di enterite acuta. Patogenesi Il periodo di incubazione è di 1-2 giorni. Spesso, l infezione da Rotavirus non colpisce solo il lattante, ma la coppia madre-lattante, tanto è vero che frequentemente, durante la diarrea del lattante, si riscontra un aumento della concentrazione di anticorpi al Rotavirus nel latte della madre. È questo un ulteriore esempio dell importanza dell allattamento al seno per comprendere la collaborazione immunologica della diade madre-lattante. Le difese immunitarie della madre collaborano strettamente con quelle del proprio figlio nella lotta verso gli agenti infettivi presenti nell ambiente in cui vivono. Il latte del seno materno è il tramite di queste difese; gli anticorpi in esso contenuti collaborano con le difese intestinali, fornite dal lattante, per combattere l invasione da parte dei Rotavirus: è ovvio che questi anticorpi non vengono assorbiti dall intestino, ma esercitano la loro attività nel faringe e in tutto l intestino, cioè nelle sedi stesse in cui si moltiplica il Rotavirus. La dimensione dell inoculum è un altro elemento importante per la prima infezione, ma soprattutto per le reinfezioni, che richiedono, per insorgere, grandi quantità di virus. Sebbene i bambini possano essere infettati più volte dai Rotavirus durante la loro vita, è più facile che l infezione iniziale, dopo l età di 3 mesi, determini grave diarrea e disidratazione. Dopo una singola infezione, il 40% dei bambini è protetto contro ogni successiva infezione con Rotavirus, il 65% è protetto dalla diarrea per una successiva infezione da Rotavirus dello stesso tipo e l 88% è protetto contro una grave diarrea. La seconda, la terza e la quarta infezione conferiscono progressivamente una maggiore protezione. I Rotavirus entrano nel tenue dopo essere passati attraverso lo stomaco e il duodeno: la tripsina concorre a favorire l aggancio del Rotavirus all enterocita del tenue. L infezione avviene soprattutto a carico dei due terzi superiori del tenue, ma, dopo la moltiplicazione in queste sedi, i virus liberati nel lume intestinale vanno incontro a ulteriori moltiplicazioni nelle aree distali. La comparsa, fra i lattanti vaccinati, della complicanza dell invaginazione
31 intestinale, a livello soprattutto della valvola ileo-cecale, è probabilmente legata all ispessimento della mucosa in seguito all infezione delle parti più basse del tenue. I Rotavirus si moltiplicano all apice delle cellule cilindriche mature dell intestino tenue, nelle quali penetrano dopo che la proteina del capside, VP4, (attaccata dalla tripsina), si aggancia ai glicolipidi della superficie dell enterocita. La moltiplicazione segue dal tenue prossimale alla parete distale. I Rotavirus non sembrano in grado di moltiplicarsi nelle cellule epiteliali immature che si trovano nelle cripte dei villi. L invasione e la moltiplicazione degli enterociti determinano numerose modificazioni funzionali e morfologiche. In primo luogo, si ha un ridotto assorbimento del sodio, del glucosio e dell acqua e si ritrovano ridotti livelli di lattasi intestinali, fosfatasi alcalina e saccarasi a carico degli enterociti. Queste alterazioni determinano un difetto nell assorbimento, con un accelerata migrazione delle cellule epiteliali immature del villo dalla cripta alla punta. Poiché non sono state dimostrate modificazioni infiammatorie a carico della lamina propria, né delle placche del Peyer o della superficie della mucosa intestinale, le alterazioni sono da addebitare all invasione diretta da parte del virus, piuttosto che a una reazione immune dell ospite. L infezione da Rotavirus è più grave in bambini da 3 a 24 mesi, sia in confronto a lattanti di meno di 3 mesi, sia in confronto a bambini di età superiore e agli adulti. Quali sono le ragioni di questa differenza? I bambini oltre i 2 anni possono essere protetti dalle risposte immuni virus-specifiche in seguito alle ripetute infezioni precedenti. La scarsa sintomatologia dei lattanti nei primi 3 mesi può essere dovuta alle difese passive trasferite dalla madre. Le cellule epiteliali del tenue acquisiscono solo dopo il secondo mese la disposizione a essere invase da Rotavirus, per cui esiste una suscettibilità particolare, legata all età. L entrata del Rotavirus nelle cellule bersaglio è facilitata dalla rottura della proteina VP4, che avviene in presenza di tripsina, elastasi e pancreatina, tutti enzimi intestinali che sono poco presenti nei liquidi intestinali del neonato, in confronto a quelli che si trovano nel lattante di qualche mese, nel bambino e nell adulto. Non va dimenticato, infine, che qualche proteina del Rotavirus possa agire come una vera e propria enterotossina virale. La diarrea riconosce come meccanismo principale una diminuzione nell assorbimento di acqua e di sali da parte delle cellule intestinali, per cui risulta un eccessiva quantità di liquidi nel lume. Si ha contemporaneamente una depressione dell attività delle disaccaridasi nell orletto a spazzola: la lattasi è uno degli enzimi maggiormente compromessi, la cui deficienza si prolunga per giorni. La maggiore gravità delle infezioni da Rotavirus nei paesi in via di sviluppo può essere ricondotta alla situazione di scarse misure assistenziali, scarsa nutrizione e infezioni concomitanti con altri virus, con batteri o con parassiti. La principale causa di morte per gastroenterite da Rotavirus è rappresentata dalla disidratazione con sbilanciamento elettrolitico; tuttavia, recenti descrizioni suggeriscono che i bambini che muoiono durante una malattia da Rotavirus divengono viremici prima della morte, perché i Rotavirus sono stati ritrovati in molte sedi extraintestinali. Ma, anche in soggetti che non giungono a morte, i Rotavirus superano la barriera intestinale e sono responsabili di una viremia. Immunità Il ruolo dell immunità nelle infezioni da Rotavirus è stato compreso abbastanza tardi. La guarigione da una gastroenterite da Rotavirus dipende in gran parte dalle difese immunologiche dell ospite. In un ospite normale, gli antigeni del Rotavirus sono trasportati alle placche del Peyer, dove sono processati dalle cellule B, dai macrofagi o dalle cellule dendritiche e sono presentati alle cellule T helper. Questa cascata immunologica culmina nella stimolazione delle cellule B specifiche per i Rotavirus e con l espansione dei precursori dei linfociti T citotossici.
32 Le infezioni naturali da Rotavirus sono responsabili dell immunità umorale specifica, insieme all immunità cellulo-mediata. La concentrazione di IgA nelle feci raggiunge il massimo dopo giorni dall infezione e persiste, per quanto a livelli sempre più bassi, per tutto un anno. La protezione dalle forme gravi è mediata proprio dalla presenza di IgA virus-specifiche a livello della mucosa intestinale ed è dimostrata dalla presenza nel siero e nelle feci di IgA specifiche. Un anno dopo l infezione, nel siero si trovano ancora IgG specifiche, ma non IgA, che non si ritrovano più nemmeno a livello della mucosa intestinale. Quindi, la presenza in circolo di IgG è un ottimo indicatore di una precedente esposizione al Rotavirus nei bambini più grandi, mentre la presenza di IgA nel succo duodenale o nelle feci serve come indicazione di un infezione recente, proprio per la relativamente rapida scomparsa di questa classe di anticorpi dalle superfici mucose dell intestino e, quindi, dalle feci. L importanza dei fattori immunologici è dimostrata anche dalle difficoltà che i soggetti con immunocompromissione hanno nell allontanare i Rotavirus, per cui facilmente presentano diarree croniche. Ma, a parte le difese immunologiche, esistono altri fattori non immunologici che concorrono alla guarigione: gli enterociti dei villi sono rimpiazzati durante l infezione da cellule epiteliali più giovani, che salgono dalle cripte e che sono meno permissive nei confronti dell infezione e della crescita virale; l aumentata peristalsi del tenue, in corso di diarrea, probabilmente favorisce l allontanamento dell agente infettivo e riduce il tempo durante il quale il virus può venire in contatto con le cellule epiteliali suscettibili del villo intestinale; l interferone prodotto dalle cellule epiteliali del villo o dai linfociti intraepiteliali può interferire con il trasferimento delle proteine virali. Sebbene l infezione naturale con Rotavirus protegga contro la malattia da moderata a grave, causata da una reinfezione, come mai alcuni bambini hanno ripetuti episodi di diarrea con lo stesso sierotipo di Rotavirus durante la successiva stagione invernale? Come mai alcuni bambini hanno 2 episodi di diarrea da Rotavirus nella stessa stagione? Queste osservazioni sono in accordo con la constatazione che alcune funzioni immunitarie (come la produzione di IgA secretorie virus-specifiche) a livello delle mucose sono usualmente di breve durata, per cui non si ritrovano più di norma entro un anno dall infezione sintomatica, come d altra parte sono possibili infezioni a breve distanza di tempo da parte di sierotipi diversi. La presenza di IgA specifiche a livello dell intestino e nel siero è predittiva di protezione contro l infezione naturale; tuttavia questo non è vero dopo la vaccinazione, che non determina la presenza di IgA specifiche a livello dell intestino. Probabilmente, la protezione dopo la vaccinazione può essere mediata dai linfociti T citotossici virus-specifici, piuttosto che dalle IgA di superficie. I Rotavirus possono eludere le difese dell ospite e indurre una nuova infezione attraverso molti meccanismi: essi vengono suddivisi in molti gruppi, sottogruppi e sierotipi; la risposta iniziale all infezione è specifica di sierotipo, con una limitata produzione di anticorpi crossreattivi. Sono le successive infezioni da Rotavirus ad aumentare il tasso di anticorpi, che cross-reagiscono con molti sierotipi. Molti studi, sia dopo l infezione naturale sia dopo la vaccinazione con un solo sierotipo di Rotavirus, hanno dimostrato che è stata indotta protezione anche per un sierotipo differente (questo fenomeno si chiama protezione eterotipica). La protezione eterotipica può essere mediata da anticorpi diretti contro proteine del capside interno; d altra parte, i linfociti T citotossici cross-reagiscono largamente con le cellule infettate da differenti sierotipi di Rotavirus o entrano in gioco citochine antivirali, generate dalle cellule T della memoria. Diagnosi La diarrea da Rotavirus non ha niente di caratteristico per essere differenziabile dagli altri tipi di diarrea infettiva.
33 La diagnosi, quindi, richiede l identificazione dell agente eziologico, che si basa sulla ricerca dei Rotavirus nelle feci o in tamponi rettali. Quando, in una diarrea che si protrae, il pediatra ritiene utile ricercare l agente eziologico, manda un campione di feci al laboratorio per la coltura dei patogeni batterici e per la ricerca del Rotavirus. Inizialmente, il virus è stato identificato nelle feci con la microscopia elettronica, ma si tratta di un metodo indaginoso, ormai abbandonato. I metodi immuno-enzimatici (ELISA) e di agglutinazione al latex per la ricerca dei Rotavirus di gruppo A nelle feci, durante gli episodi di diarrea, sono di facile esecuzione e si trovano facilmente in commercio. Le prove di agglutinazione al latex sono molto specifiche, ma hanno meno sensibilità degli altri metodi. Nella fase tardiva della malattia, per documentare un infezione da Rotavirus, è più opportuno rivolgersi alla ricerca degli antigeni o degli anticorpi specifici nel siero. Il rilievo di false positività va comunque sempre tenuto presente, perché è relativamente frequente in soggetti con patologie intestinali. Per riconoscere queste reazioni aspecifiche è necessario eseguire un esame di conferma. Le moderne tecniche di amplificazione (PCR) degli acidi nucleici dei Rotavirus sono le più adatte. È possibile inoltre, con esami sofisticati, eseguire indagini epidemiologiche sulla base della caratterizzazione in sottogruppi e in sierotipi. Tuttavia, la determinazione dei sierotipi in causa non ha alcuna importanza clinica nella diagnosi, perché nessun tipo di virulenza si collega con il sierotipo. Trattamento Non esiste una terapia specifica. Vanno somministrate soluzioni di elettroliti, prevalentemente per via orale, per correggere la disidratazione. Per i pazienti con grave stato di disidratazione e vomito ripetuto, sono consigliati il ricovero e la somministrazione di liquidi e di sali per via venosa. Oggi, l alimentazione non viene mai completamente sospesa durante gli episodi di diarrea, meglio se è a disposizione il latte materno. È stato visto che la rialimentazione precoce durante gli episodi di diarrea facilita la rigenerazione degli enterociti e riduce la permeabilità intestinale. Non vengono consigliati gli antibiotici, né farmaci antisecretori, né farmaci contro la motilità, né assorbenti, né antiemetici. Misure generali e di profilassi È necessario mettere in pratica tutte le più comuni norme igieniche durante il ricovero dei lattanti con diarrea da Rotavirus. L allattamento al seno si è dimostrato importante per prevenire, in parte, la diarrea da Rotavirus. Nelle comunità infantili (asili nido, per esempio), i bambini con diarrea da Rotavirus che emettono feci così liquide da non poter essere contenute nel pannolino o che non usano autonomamente il gabinetto, vanno allontanati temporaneamente dall istituzione. Le superfici contaminate vanno lavate accuratamente con acqua e sapone; è utile anche l uso di disinfettanti per prevenire la trasmissione della malattia per contatti con oggetti o superfici. Una soluzione di alcol denaturato al 70% inattiva i Rotavirus e può aiutare a prevenire la trasmissione di malattie da contatto con superfici ambientali. Vaccino Lo scopo di un vaccino contro i Rotavirus è quello di moltiplicare il grado di protezione verso la malattia che segue l infezione naturale.
34 L obiettivo del programma di vaccinazione è proprio quello di impedire le malattie da moderate a gravi, e non quello di impedire le forme lievi di diarrea da Rotavirus. Quindi, fra gli scopi di un vaccino contro il Rotavirus, c è soprattutto quello di ridurre il numero di bambini che necessitano di un ricovero in ospedale per una grave disidratazione o in pronto soccorso per una diarrea profusa. Il vaccino contro il Rotavirus dovrebbe esercitare la propria funzione soprattutto nei paesi in via di sviluppo, dove la mortalità per Rotavirus è ancora molto alta. La ricerca di un vaccino adatto alla prevenzione delle enteriti da Rotavirus, da usare soprattutto nel Terzo Mondo, è stata intensa nell ultimo decennio. La constatazione di gravi complicanze a livello intestinale (invaginazione) ha arrestato per qualche anno l evolversi della ricerca. Ma, da qualche anno, la preparazione di nuovi vaccini contro il Rotavirus ha ripreso in pieno. Durante gli ultimi vent anni sono stati studiati soprattutto 3 tipi di vaccini anti-rotavirus: 1. vaccino monovalente con ceppi di origine umana, 2. vaccino multivalente con virus derivati dal riarrangiamento di ceppi di origine umanaanimale, 3. vaccino con un ceppo di Rotavirus umani, vivi e attenuati. Attualmente, in Italia sono disponibili 2 vaccini vivi attenuati contro il Rotavirus: 1. uno monovalente, derivato da un ceppo umano di Rotavirus, 2. uno pentavalente, derivato da una combinazione di ceppi umani e bovini di Rotavirus. Entrambi i vaccini si somministrano per bocca (vedi Tabella 8). Vaccino monovalente da Rotavirus umani Un secondo vaccino contro i Rotavirus (RV1) è stato approvato il 3 aprile 2008 per l uso negli Stati Uniti. Il vaccino contiene il ceppo RIX4414 del Rotavirus umano G1P. Il ceppo RIX4414 è stato sviluppato ulteriormente dal ceppo di Rotavirus 89-12, che originariamente era stato isolato in un piccolo bambino di Cincinnati, Ohio. Il RV1 viene somministrato a lattanti in 2 dosi per bocca. Vaccino pentavalente contro i Rotavirus, ottenuto per riassortimento umano-bovino Nel febbraio 2006, è stato approvato negli Stati Uniti un vaccino orale, ottenuto per riassortimento di virus umano-bovino (RV5). RV5 contiene 5 ceppi di Rotavirus. I ceppi originali di Rotavirus sono stati isolati da ospiti umani e bovini: 4 Rotavirus esprimono una delle proteine del capside esterno (G1, G2, G3 e G4) di ceppi umani di Rotavirus, riassortiti con una proteina (P7) di un ceppo bovino di Rotavirus; il quinto virus esprime la proteina (P1A) di un ceppo originario umano di Rotavirus e la proteina G6 del capside esterno di un ceppo originario bovino di Rotavirus. Il RV5 viene somministrato ai bambini in 3 dosi per bocca (vedi Tabella 9).
35 CARATTERISTICHE MONOVALENTE PENTAVALENTE Tipo di vaccino Vivo attenuato per bocca Vivo attenuato per bocca Ceppo Ceppo umano Ceppo bovino WC3 Composizione Singolo ceppo umano RIX ceppi riarrangiati umani-bovini Tipi G e P Indicazioni della scheda tecnica Età ufficiale di somministrazione, in settimane G1P[8] Immunizzazione contro la gastroenterite da Rotavirus, causata da G1, G3, G4 e G9 G1P[5] G2P[5] G3P[5] G4P[5] G6P[8] Immunizzazione contro la gastroenterite da Rotavirus, causata da G1, G2, G3 e G4 Da 6 a 24 Da 6 a 32* Dosi, età in mesi 2 e 4 mesi 2, 4 e 6 mesi Formulazione Modalità di somministrazione Fiale di vaccino liofilizzato con applicatore orale, ripieno di liquido diluente Sospensione orale in contenitore in latex naturale + adattatore di trasferimento + siringa preriempita, non in latex Liquida, senza che sia necessaria una ricostruzione Flaconcino in plastica comprimibile per una dose singola Volume per dose, ml 1 2 Preservanti Nessuno Nessuno Scadenza in mesi Conservazione Conservazione prima della ricostruzione: fiale di vaccino liofilizzato a 2-8 C, protette dalla luce; conservare il diluente a C Conservazione dopo la ricostruzione: somministrare entro 24 ore dalla ricostruzione; può essere mantenuto in frigorifero a 2-8 C o a temperatura ambiente fino a 25 C Da conservare in frigorifero a 2-8 C, protetto dalla luce e somministrato il prima possibile dopo essere stato tolto dal frigorifero * L Accademia Americana di Pediatria raccomanda 8 mesi, 0 giorni come età massima per la somministrazione dell ultima dose del vaccino pentavalente. Tabella 8. Caratteristiche dei vaccini contro i Rotavirus (Fonte: Bartolozzi G. Linee Guida per la prevenzione della malattia da Rotavirus. Un aggiornamento in confronto al La sicurezza e l efficacia di RV5 e RV1 per la prevenzione della gastroenterite da Rotavirus in lattanti sani sono state valutate in 11 studi randomizzati e controllati, con il reclutamento di più di bambini in tutto il mondo (vedi Tabella 9); 3 sono gli studi randomizzati e controllati su RV5 e 7 quelli su RV1.
36 PROFILO RV1 RV5 Caratteristiche di sicurezza Nessun aumento di febbre, irritabilità, diarrea e vomito Nessun aumento di febbre o irritabilità, leggero aumento di diarrea e di vomito di lieve entità Invaginazione Nessuna associazione Nessuna associazione Diffusibilità del virus in % Efficacia nei confronti di ogni gastroenterite da Rotavirus in % Efficacia nei confronti delle gastroenteriti gravi da Rotavirus in % Efficacia nei confronti di visite con addetti alla salute Efficacia a seconda del sierotipo nella grave gastroenterite da Rotavirus 25 (dopo la prima dose, con punte dopo 7 giorni) Significativamente ridotte. Nessuna ospedalizzazione e nessuna attenzione da parte del medico 9 (dopo una dose, di rado dopo le successive) Nell America Latina: G1 (91%), G2 (41%), G3, G4 e G9 (85%) Significativamente ridotte. Nessuna ospedalizzazione, nessuna visita all ambulatorio del medico o al dipartimento di emergenza G1 (95%), G2 (88%), G3 (93%), G4 (89%), G9 (100%) Tabella 9. Effetti dei vaccini contro i Rotavirus nelle prove cliniche (Fonte: Bartolozzi G. Linee Guida per la prevenzione della malattia da Rotavirus. Un aggiornamento in confronto al SICUREZZA Reattogenicità Ambedue i vaccini sono ben tollerati e hanno un profilo di bassa reattogenicità quando dati isolatamente. Essi non causano aumenti clinicamente significativi nella reattogenicità quando co-somministrati con altri vaccini. Per entrambi i vaccini, l incidenza della febbre, del vomito, della diarrea e dell irritabilità è stata valutata in prove cliniche: per RV5 non venne osservata nessuna differenza significativa nei confronti del placebo è stata osservata per l incidenza della febbre o della febbre elevata e dell irritabilità o della grave irritabilità. È stato osservato un aumento del 3% nell incidenza della diarrea e del vomito, ma questi sintomi sono stati leggeri e non hanno richiesto alcun trattamento; per RV1 non è stata osservata nessuna differenza verso il placebo nell incidenza della diarrea, della febbre o della febbre elevata, del vomito o del vomito grave, e dell irritabilità o della grave irritabilità, entro 14 giorni dall immunizzazione con una dose. Non è stato notato nessun aumento del rischio di eventi gravi per entrambi i sierotipi vaccinali. Invaginazione Con ambedue i vaccini, il rischio di invaginazione non è risultato maggiore di quello osservato con il placebo. Con RV5, durante i 42 giorni successivi a ciascuna dose, sono stati registrati 6 casi di invaginazione su soggetti riceventi il vaccino, e 5 casi su soggetti riceventi il placebo [rischio relativo (RR): 1,2]. 12 mesi dopo ogni dose, sono risultati 12 casi di invaginazione fra i vaccinati e 15 fra i soggetti riceventi il placebo (RR: 0,8).
37 Con RV1, durante i 31 giorni successivi a ciascuna dose di vaccino, sono stati registrati 6 casi di invaginazione su riceventi il vaccino, contro 7 casi su riceventi il placebo (RR: 0,9). Durante i 12 mesi successivi a ciascuna dose di RV1, sono risultati 4 casi di invaginazione fra i vaccinati, contro 14 di quelli che ricevettero il placebo (RR: 0,3). Con più di 14 milioni di dosi di RV5, distribuite negli Stati Uniti dal 2006, l Ufficio Sicurezza delle Vaccinazioni del CDC afferma che la vaccinazione con RV5 non si associa a un aumentato rischio di invaginazione. Eliminazione e trasmissione del virus L eliminazione dei Rotavirus con le feci avviene in circa il 9% dei riceventi la prima dose di RV5, ma di rado dopo le dosi successive. Non è stato documentato alcun caso di trasmissione dopo RV5. Comunque, la diffusione e la trasmissione sono considerate possibili, a causa della natura attenuata dei Rotavirus contenuti nei vaccini. Con RV1, il Rotavirus vivo viene eliminato nel 25% dei riceventi il vaccino, con punte di escrezione al 7 giorno dopo la prima dose. Non è stata valutata l incidenza della trasmissione del virus, ma sono documentati solo pochi casi di trasmissione ai contatti, senza che si siano sviluppati sintomi di gastroenterite da Rotavirus. EFFICACIA È stata valutata l efficacia dei due vaccini contro i Rotavirus in lattanti sani. Studi sull efficacia del vaccino hanno dimostrato una protezione dell 85-98% verso la malattia grave da Rotavirus e del 74% (RV5) - 87% (RV1) verso qualsiasi malattia da Rotavirus. Nei lattanti europei, l efficacia dell RV1 nei confronti di ogni gastroenterite da Rotavirus, di qualsiasi gravità, è stata dell 87%. Questo tipo di efficacia non è stata misurata in America Latina. Ma che cos è la gastroenterite severa? La severità è definita su una scala di sintomi, ciascuno pesato per la sua intensità. Ma le scale sono diverse nei due lavori: per il vaccino pentavalente è stata usata la scala di Clark per RV5 e quella di Ruuska-Vesikari per RV1. Entrambe prendono in considerazione diarrea (numero di scariche, durata), vomito e febbre, ma solo la prima considera quale elemento di gravità alcuni sintomi neurologici (irritabilità, letargia, convulsioni), mentre solo la seconda considera la percentuale di disidratazione o il fatto che sia stata necessaria una reidratazione per via endovenosa o un ricovero. Anche il cut-off per la definizione di severità è diverso: nello studio di Vesikari per RV1 sono stati così definiti i casi con un punteggio superiore a 16 (su un massimo di 24, quindi al 75% della scala), mentre nello studio di Clark per RV5 il cut-off è stato posto a 11 su 20 (55%). La gravità della gastroenterite da Rotavirus è stata, quindi, valutata usando differenti scale cliniche (scala Vesikari per RV1 e scala Clark per RV5). Un confronto fra le due scale ha trovato che esse differiscono principalmente nella definizione di gravità dei casi: gli autori di questo studio concludono che l uso di differenti scale di valutazione riduce la capacità di confrontare l efficacia dei due vaccini contro i Rotavirus (Givon-Lavi N et al. Vaccine. 2008; 26: ). L efficacia dell RV5 per le gastroenteriti gravi da Rotavirus è stata del 98%; quella di RV1 in Europa è stata del 96% e in America Latina dell 85%. L efficacia nei confronti dell ospedalizzazione è stata del 96% per RV5. Per le visite al dipartimento di emergenza, associate a gastroenterite da Rotavirus, è stata del 94% alla terza dose di RV5. L efficacia dell RV1 per l ospedalizzazione è stata in Europa del 96% e in America Latina dell 85%. La vaccinazione contro i Rotavirus riduce dell 86% la necessità di una visita medica in ambulatorio per RV5. Con RV1 questa valutazione in Europa è stata dell 84% dopo la seconda stagione di follow-up. L efficacia dell RV5, associata all ospedalizzazione o alla visita al dipartimento di emergenza, è stata del 95% per il sierotipo G1, dell 88% per G2, del 93% per G3, dell 89% per G4 e del 100% per G9.
38 In America Latina, l efficacia dell RV1 contro episodi gravi, causati dai ceppi, sierotipo G1, omologo al ceppo contenuto nel vaccino, è stata del 91%, e l efficacia contro ceppi che condividevano soltanto l antigene P (G3, G4 e G9) è stata dell 87%. Per il sierotipo G2P di Rotavirus, l efficacia di RV1 è stata del 41%. In Europa, l efficacia di RV1 contro episodi gravi, causati da ceppi G1 è stata del 96%, del 94% per il G3, del 95% per il G4 e dell 86% per il G9. Per il sierotipo G2 l efficacia è stata dell 86%. I dati sull efficacia di meno di 3 dosi per RV5 e per meno di 2 dosi per RV1 sono stati dell 86%. In particolare, l effetto protettivo di RV1 nei confronti della gastroenterite da Rotavirus di qualsiasi grado di gravità è stato del 90% dopo aver ricevuto una dose e subito prima di avere ricevuto la seconda. Intercambiabilità dei vaccini contro i Rotavirus Nessuno studio è stato rivolto all intercambiabilità dei due vaccini contro i Rotavirus. Tuttavia, non ci sono ragioni teoriche per aspettarsi che il rischio di eventi avversi sia aumentato se la serie delle dosi contiene più di un prodotto, in confronto a una serie che contenga un solo prodotto. Inoltre, sebbene sia possibile che l efficacia di una serie costituita da due prodotti possa essere ridotta in confronto a una serie costituita da un unico prodotto, va affermato che è facile che una serie che contenga ambedue i prodotti abbia un efficacia superiore a quella di una serie incompleta di un solo prodotto. Efficacia in popolazioni speciali Studi hanno dimostrato che ambedue i vaccini contro i Rotavirus in lattanti alimentati al seno presentano una ridotta efficacia. Ambedue i vaccini contro i Rotavirus sono stati somministrati insieme ai vaccini pediatrici comunemente usati, come l anatossina difterica e tetanica, il vaccino acellulare contro la pertosse, il vaccino contro l Haemophilus influenzae tipo b (Hib), il vaccino antipolio inattivato (IPV), il vaccino contro l epatite B (HBV) e il vaccino pneumococcico coniugato, senza mai osservare interferenze immuni. Sono in corso studi per osservare la possibilità di vaccinare contro i Rotavirus bambini HIV positivi. Vi sono prove che RV5 può essere usato in bambini pretermine oltre la 32 a settimana di gestazione, con la stessa schedula usata per i nati a termine. Sono in corso studi per RV1 nei nati pretermine. ANALISI COSTI/BENEFICI È stato dimostrato che un programma di vaccinazione universale nazionale (USA) contro i Rotavirus, con 3 dosi, somministrate a 2, 4 e 6 mesi di età a 4 milioni di lattanti, riduce: di le visite dal pediatra, di le visite al dipartimento di emergenza, di le ospedalizzazioni, di 13 morti per anno in bambini in età inferiore ai 5 anni. Al prezzo di $ 62,5 per dose, una serie di 3 dosi di RV5 costerebbe $ 138 per caso risparmiato, $ per caso grave risparmiato e $ per anno di vita salvato. Il CDC conclude che il costo/efficacia di un programma di vaccinazione con 3 dosi di RV5 sarebbe simile come spesa a uno con il vaccino RV1 a 2 dosi. Il vaccino contro i Rotavirus può essere più costo/efficace di quanto è stato calcolato, se l immunizzazione fornisce una protezione indiretta nei bambini non immunizzati e in quelli che non hanno avuto una risposta immune adeguata al vaccino. È stato condotto uno studio di impatto economico in Brasile, paese che nel marzo del 2006 ha introdotto la vaccinazione anti-rotavirus nel piano nazionale di immunizzazione, che si propone di valutare l effetto della nuova vaccinazione sul costo di gestione della diarrea in bambini entro i 2 anni di età (Centenari C, Maggiore G, Gurgel RQ, Cuevas LE. Vaccinazione
39 anti-rotavirus: intervento lodevole ma fa risparmiare il Sistema Sanitario Nazionale? L esperienza del Brasile. In tali contesti, la vaccinazione anti-rotavirus viene introdotta principalmente per ridurre l impatto economico della malattia, più che per contenere i pochi decessi da essa causati. Lo studio è stato condotto dall Università di Pisa, in collaborazione con la scuola di Medicina Tropicale di Liverpool (UK) e l Università di Sergipe (Brasile). Il risultato di tale analisi rappresenta un importante strumento di valutazione economica da integrare agli studi di costo/efficacia per supportare decisioni di politica sanitaria. Questo può risultare particolarmente importante in paesi a bassa mortalità e alta morbilità per diarrea infantile. La morbilità per diarrea e il relativo costo di gestione sono stati ottenuti tramite il sistema di assistenza territoriale primaria, il database sanitario pubblico nazionale e intervistando le famiglie dei pazienti. L analisi ha riguardato i 25 mesi precedenti e successivi all introduzione del vaccino. L incidenza di visite ambulatoriali e ricoveri ospedalieri ha mostrato una progressiva riduzione durante l intero periodo analizzato, con una flessione maggiore dopo l introduzione della vaccinazione. Il periodo post-vaccinale è stato caratterizzato da una riduzione delle spese per il sistema sanitario e per le famiglie dei pazienti. Nonostante questa riduzione di costi, la spesa complessiva del sistema sanitario nazionale è aumentata. L analisi dei primi dati successivi all introduzione del vaccino anti-rotavirus in un paese a reddito medio-elevato e bassa mortalità per diarrea come il Brasile, dimostra che gli effetti del programma di immunizzazione non sono stati per ora in grado di compensare il costo di gestione delle gastroenteriti in bambini entro i 2 anni di vita. Il costo del programma di immunizzazione da solo è stato maggiore del costo complessivo di gestione della diarrea a livello statale (US$ ,28 versus US$ ,54). Per quanto riguarda la spesa sociale, invece, si è verificata una riduzione di costi per le famiglie, specialmente le più povere. Ulteriori vantaggi economici per la società sono ipotizzabili prendendo in analisi contesti a reddito superiore e includendo i costi correlati a episodi di diarrea severa. L introduzione del vaccino anti-rotavirus nel programma di immunizzazione brasiliano dovrebbe perciò essere basato sulla premessa che tale vaccino, al prezzo attuale, è da considerare un investimento in salute piuttosto che una tecnologia che può portare a un reale risparmio economico per il sistema sanitario. Tra gli interventi sanitari per limitare la diarrea infantile, il miglioramento delle condizioni igienico-sanitarie, la promozione dell educazione materna, dell allattamento al seno e della terapia reidratante orale potrebbero presentare un miglior impatto economico e rapporto costo/efficacia. I vaccini anti-rotavirus sono stati raccomandati universalmente e considerati uno strumento per migliorare la salute della popolazione pediatrica e raggiungere i Millennium Development Goal. Nonostante questo, la sorveglianza della diarrea infantile deve continuare a rimanere elevata. Futuri studi post-vaccinali sono necessari per dimostrare il reale impatto economico nei paesi che decidono di introdurre la vaccinazione anti-rotavirus all interno del Piano di Immunizzazione Nazionale. CONTROINDICAZIONI E PRECAUZIONI Controindicazioni Il vaccino contro il Rotavirus non deve essere somministrato a lattanti che hanno presentato gravi reazioni allergiche (anafilassi) alla precedente dose del vaccino contro i Rotavirus o a un suo componente. Latex è contenuto nell applicatore orale di RV1, per cui un lattante con grave allergia al lattice non deve ricevere RV1. Può usare in alternativa RV5 che non contiene lattice. Precauzioni Alterazioni dell immunocompetenza: in questi casi va consultato un immunologo o uno specialista di malattie infettive. Bambini e adulti che hanno immunodeficienze congenite, sono
40 stati sottoposti a trapianto di cellule staminali o di organi solidi, qualche volta hanno gastroenteriti gravi e prolungate da Rotavirus. Non sono disponibili dati di sicurezza e di efficacia per la somministrazione del vaccino in questi lattanti immunocompromessi o potenzialmente immunocompromessi: con immunodeficienze primitive o acquisite, incluse quelle cellulari e gli stati di ipogammaglobulinemia e di disgammaglobulinemia; con discrasie ematiche, leucemia, linfoma o altri tumori maligni che colpiscano il midollo osseo o il sistema linfatico; in terapia immunosoppressiva, per esempio con alte dosi di corticosteroidi ( 2 mg/kg/die di prednisone o equivalenti); che siano HIV esposti o HIV infetti. Tuttavia, questa decisione deve essere fatta sulla base di queste considerazioni: l infezione da HIV può essere esclusa da 4 a 8 settimane di età, prima che venga somministrata la prima dose di vaccino in lattanti figli di madri HIV positive; lattanti HIV esposti, non allattati al seno, possono essere identificati come infettati da HIV da 4 a 8 settimane di età; dati preliminari con uno dei due vaccini approvati hanno mostrato che il vaccino è sicuro quando dato a lattanti HIV infettati in Africa. Gastroenterite da moderata a grave: il vaccino contro i Rotavirus non deve essere somministrato a lattanti con gastroenterite acuta, da moderata a grave, finché le condizioni non migliorino. Tuttavia, lattanti con gastroenterite acuta lieve possono essere immunizzati, particolarmente se il ritardo nella vaccinazione possa essere importante e possa renderere il bambino non idoneo a ricevere il vaccino (cioè 15 settimane e 0 giorni di età o maggiori quando si inizi la prima dose di vaccino, o più vecchio di 8 mesi di età e 0 giorni al momento dell ultima dose). Il vaccino contro i Rotavirus non è stato studiato in lattanti con gastroenterite acuta ricorrente. In questi lattanti l immunogenicità e l efficacia del vaccino possono essere compromesse in linea teorica. Malattie da moderate a gravi: l immunizzazione non deve essere ritardata per malattie lievi delle vie aeree o per altre malattie acute lievi, con o senza febbre. La presenza di una malattia da moderata a grave, con o senza febbre, rappresenta una precauzione per la somministrazione del vaccino contro i Rotavirus. Lattanti con malattie acute da moderate a gravi dovrebbero essere immunizzati non appena essi abbiano superato la fase acuta della malattia. Malattie gastrointestinali croniche preesistenti: lattanti con sindromi congenite del metabolismo, malattia di Hirschsprung, sindrome dell intestino corto, che non siano sottoposti a terapia, beneficiano della vaccinazione contro i Rotavirus: l American Academy of Pediatrics (AAP) pensa che i benefici superino i rischi teorici. Non ci sono dati disponibili sulla sicurezza e l efficacia del vaccino contro i Rotavirus in lattanti con malattie croniche preesistenti dell apparato gastrointestinale. Storia precedente di invaginazione: i medici devono considerare i rischi e i benefici potenziali di vaccinare un bambino con una storia precedente di invaginazione. Nel confronto fra lattanti che non hanno avuto invaginazione e lattanti che l hanno avuta, risulta evidente che questi ultimi hanno un rischio maggiore di avere di nuovo un episodio di invaginazione. Non esistono tuttavia dati in proposito. Lattanti con spina bifida o estrofia vescicale: latex è contenuto nell applicatore orale dell RV1, mentre RV5 ne è privo. Per minimizzare il rischio nei bambini con spina bifida o estrofia vescicale, ad alto rischio di allergia al latex, alcuni esperti preferiscono somministrare RV5 invece di RV1. Tuttavia, se RV1 fosse il solo vaccino disponibile, esso dovrebbe essere ugualmente somministrato, perché il beneficio della vaccinazione è maggiore del rischio della sensibilizzazione.
41 RACCOMANDAZIONI Somministrazione routinaria L Accademia Americana di Pediatria raccomanda la vaccinazione routinaria dei lattanti degli Stati Uniti con il vaccino contro i Rotavirus. L AAP non esprime una preferenza per l uno o per l altro dei due vaccini, RV5 e RV1, per l uso nei lattanti degli Stati Uniti. RV5 deve essere somministrato per bocca in una serie di 3 dosi a 2, 4 e 6 mesi di età; RV1 deve essere somministrato per bocca in una serie di 2 dosi a 2 e 4 mesi di età (vedi Tabella 10). La prima dose di vaccino contro i Rotavirus va somministrata da 6 settimane e 0 giorni di età fino a 14 settimane e 6 giorni di età. La vaccinazione non deve essere iniziata in bambini di 15 settimane e 0 giorni o più vecchi per la mancanza di dati sulla sicurezza della prima dose di vaccino in bambini più vecchi. L intervallo minimo fra le dosi è di 4 settimane. Tutte le dosi devono essere somministrate entro gli 8 mesi, 0 giorni di età. Per i lattanti nei quali la prima dose sia stata inavvertitamente somministrata a 15 settimane e 0 giorni di età o superiori, il rimanente della serie di vaccinazione contro i Rotavirus deve essere completata, secondo la schedula, perché il tempo di somministrazione della prima dose non riguarda la sicurezza e l efficacia delle dosi successive. I lattanti che hanno avuto una gastroenterite da Rotavirus, prima di ricevere la dose completa di vaccinazione, devono iniziare o completare la schedula secondo le raccomandazioni per l età e per l intervallo, perché l infezione iniziale da Rotavirus fornisce solo una protezione parziale nei confronti della malattia successiva da Rotavirus. L allattamento al seno, prima o dopo aver ricevuto il vaccino contro i Rotavirus, va incoraggiato. L allattato al seno può essere immunizzato seguendo la stessa schedula del lattanti non allattati al seno. Come tutti gli altri vaccini, il vaccino contro i Rotavirus può essere somministrato a lattanti con malattie acute minori (cioè gastroenterite lieve o infezioni lievi delle vie aeree superiori, con o senza febbre). RACCOMANDAZIONI RV1 RV5 Numero di dosi nella serie 2 3 Età raccomandata per le dosi 2 e 4 mesi 2, 4 e 6 mesi Età minima per la prima dose 6 settimane 6 settimane Età massima per la prima dose 14 settimane e 6 giorni 14 settimane e 6 giorni Intervallo minimo fra le dosi 4 settimane 4 settimane Età massima all ultima dose 8 mesi e 0 giorni 8 mesi e 0 giorni Tabella 10. Schedula raccomandata per la somministrazione del vaccino contro i Rotavirus (Fonte: Bartolozzi G. Linee Guida per la prevenzione della malattia da Rotavirus. Un aggiornamento in confronto al Somministrazione simultanea (co-somministrazione) Il vaccino contro i Rotavirus può essere somministrato insieme con l anatossina difterica e tetanica e con il vaccino acellulare contro la pertosse, l Haemophilus influenzae tipo b, il vaccino antipolio inattivato, l HBV e il vaccino antipneumococcico coniugato. Il vaccino contro i Rotavirus può essere somministrato insieme al vaccino trivalente inattivato contro l influenza per lattanti di oltre 6 mesi, anche se non esistono ancora
42 prove sull immunogenicità. Il vaccino vivo attenuato contro l influenza non è stato approvato per la vaccinazione di bambini con meno di 2 anni. Intercambiabilità dei vaccini contro i Rotavirus L AAP raccomanda che la serie del vaccino contro i Rotavirus sia completata, se possibile, con lo stesso prodotto. La vaccinazione contro i Rotavirus non deve essere differita quando il prodotto usato per le dosi precedenti non sia disponibile. In queste circostanze, l esecutore delle vaccinazioni deve continuare e completare la serie con il prodotto disponibile. Se una qualsiasi dose della serie con RV5, o quando il vaccino usato per la serie sia sconosciuto per una qualsiasi serie, deve essere somministrato un totale di 3 dosi. Tutte le dosi devono essere date entro gli 8 mesi e 0 giorni. Situazioni speciali Lattanti pretermine (cioè nati prima della 37a settimana): i pretermine devono essere immunizzati con la stessa schedula e con le stesse precauzioni dei nati a termine e secondo queste condizioni: l età postnatale del lattante (età cronologica) corrisponde all età richiesta per la somministrazione del vaccino (cioè da 6 a 14 settimane per la prima dose), quando il lattante sia clinicamente stabile. Le prove suggeriscono che i pretermine sono ad aumentato rischio di ospedalizzazione per Rotavirus e per altri patogeni associati alla gastroenterite nel primo anno di vita. In prove cliniche, il vaccino contro i Rotavirus sembra essere ben tollerato. Sebbene livelli più bassi di anticorpi materni contro i sierotipi prevalenti nei lattanti molto pretermine in via teorica aumentino il rischio di eventi avversi al vaccino contro i Rotavirus, l AAP pensa che il beneficio dei lattanti vaccinati, secondo l età cronologica e in presenza di stabilizzazione, superi il rischio teorico. Lattanti pretermine in terapia intensiva o nella nursery: il lattante pretermine, all età opportuna e clinicamente stabile, può essere vaccinato al momento di uscita dall ospedale. I ceppi vaccinali di Rotavirus sono diffusi con le feci dai bambini immunizzati, per cui un bambino che, dopo essere stato vaccinato, necessiti ancora di ricovero in ospedale, può presentare un rischio teorico di trasmettere il virus del vaccino a lattanti che siano ricoverati nella stessa unità per malattie moderate-gravi o che non abbiano ancora raggiunta l età per la vaccinazione. L AAP in queste circostanze pensa che il rischio di diffusione del virus oltrepassi il beneficio dell immunizzazione del lattante, che ha l età giusta e che sia stabile, ma che rimane nella stessa unità dopo la vaccinazione. Riammissione di un pretermine vaccinato nell unità di terapia intensiva neonatale o nella nursery: se un bambino immunizzato contro i Rotavirus necessita della riammissione entro 2 settimane dall aver ricevuto il vaccino, debbono essere istituite attente precauzioni, che vanno mantenute per 2-3 settimane dopo la somministrazione del vaccino. Esposizione di lattanti vaccinati a persone immunocompromesse: i lattanti che convivono con persone immunocompromesse o che siano sospettate di immunocompromissione possono essere vaccinati. Il virus del vaccino viene diffuso con le feci del lattante dopo la vaccinazione contro i Rotavirus. Tuttavia, non ci sono dati sul rischio di trasmissione in contatti domiciliari e, quindi, del rischio di successive malattie. Il virus del vaccino viene diffuso più comunemente più a lungo dopo aver ricevuto RV1 che RV5. La maggioranza degli esperti suggerisce di proteggere in famiglia il soggetto immunocompromesso e di vaccinare il lattante. Il virus del vaccino viene eliminato prevalentemente nella prima settimana dalla somministrazione. Viene raccomandato il lavaggio delle mani dopo aver cambiato il pannolino.
43 Esposizione di una donna in gravidanza a un lattante immunizzato: lattanti che convivono con una donna in gravidanza nella stessa famiglia devono essere immunizzati con la stessa schedula di un lattante che non viva con una donna in stato di gravidanza. La maggior parte delle donne in età feconda ha un immunità verso i Rotavirus; d altra parte il rischio di infezione è molto basso. Rigurgito del vaccino: il vaccinatore non deve somministrare una seconda dose di vaccino contro i Rotavirus in un bambino che abbia rigurgitato, sputato o vomitato durante o dopo la somministrazione del vaccino. Non esistono tuttavia dati sui benefici o sui rischi della somministrazione di una seconda dose. Il lattante deve ricevere le rimanenti dosi raccomandate di vaccino, secondo la solita schedula. Ospedalizzazione dopo vaccinazione: se un lattante, di recente immunizzato, viene ricoverato per una qualsiasi ragione, non va presa nessuna precauzione, al di là delle precauzioni standard che vengono prese per prevenire la diffusione del virus del vaccino in ospedale. Lattanti che hanno ricevuto di recente o che riceveranno una preparazione di sangue che contiene anticorpi: il vaccino contro i Rotavirus può essere somministrato in qualsiasi momento, prima, insieme o dopo l uso di prodotti contenenti anticorpi, secondo la schedula routinaria raccomandata per il vaccino contro i Rotavirus fra i lattanti che sono in attesa di essere vaccinati. In teoria, lattanti che abbiano di recente ricevuto prodotti del sangue contenenti anticorpi hanno una risposta immune attenuata dopo una dose di vaccino contro i Rotavirus. Tuttavia, una serie completa comprende 2 o 3 dosi di vaccino, in modo tale da assicurare una protezione adeguata, spesso anticipata, mentre non è aumentato il rischio di eventi avversi.
44 VALUTAZIONE ANAMNESTICA Il percorso anamnestico nel paziente con diarrea acuta dovrebbe includere una prima fase volta a escludere tutte le possibili patologie diverse dalla gastroenterite, potenzialmente alla base dell episodio. Una volta escluse le altre cause, l anamnesi dovrebbe aiutarci a comprendere eziologia e gravità. La diarrea acuta può rappresentare il sintomo di presentazione di numerose patologie non gastrointestinali, come anche di patologie gastrointestinali non di natura infettiva, spesso molto gravi quali invaginazione intestinale, addome acuto, sepsi e sindrome uremicoemolitica. I seguenti aspetti vanno considerati come sintomi di allarme di tali gravi patologie, anche se raramente alcuni di essi sono riscontrabili anche in corso di gastroenterite: dolore e tensione dell addome, con o senza resistenza (cause chirurgiche: appendicite, invaginazione, occlusione intestinale); pallore, ittero, oligo-anuria, diarrea ematica (sindrome uremico-emolitica); compromissione dello stato generale, sproporzionato al livello di disidratazione (sepsi, cause chirurgiche); shock (cause chirurgiche, sindrome uremico-emolitica, sepsi). Nella Tabella 11 vengono riportate le altre potenziali cause di diarrea acuta con i relativi elementi anamnestici più suggestivi. Una volta escluse tutte le altre cause, l approfondimento anamnestico successivo dovrà includere i quesiti che ci possono orientare nell inquadramento eziologico e clinico dell episodio di gastroenterite. L anamnesi dovrà valutare i seguenti aspetti: epoca di inizio, durata ed entità della diarrea e del vomito; presenza di muco e sangue evidente nelle feci; diuresi; tipo e quantità di liquidi somministrati; tipo di alimentazione; pesi precedenti disponibili; comportamento e aspetto generale del bambino; presenza di febbre; condizioni correlabili ad altre possibili cause di diarrea e vomito (otalgia, sintomatologia catarrale, modificazioni delle caratteristiche delle urine, assunzione di antibiotici e dolori addominali) e altre patologie croniche preesistenti; eventuali contatti con persone affette (casi precedenti in famiglia e a scuola); viaggi in zone a rischio; riferite intolleranze alimentari. Nella valutazione iniziale di un paziente con diarrea acuta, l anamnesi può essere utile per orientarsi sulla possibile eziologia, batterica o virale. Fattori suggestivi di eziologia batterica sono la presenza di febbre elevata, sangue nelle feci, addominalgia e coinvolgimento del sistema nervoso centrale, con sintomi quali irritabilità, apatia o convulsioni. Al contrario, sintomi respiratori associati, come la rinorrea e la tosse, oppure la presenza di vomito, sono più tipici delle infezioni di origine virale.
45 CATEGORIA Infezioni non enteriche Patologie endocrino-metaboliche Uso di antibiotici o altri farmaci Patologie correlate agli alimenti Malassorbimento Infiammazione intestinale Disturbi funzionali dell intestino Urinarie, polmoniti, otite media, sepsi DIAGNOSI Diabete, ipertiroidismo, iperplasia surrenalica, morbo di Addison, ipoparatiroidismo, assunzione di sostanze tossiche Assunzione di antibiotici e, raramente, colite pseudomembranosa Allergie/intolleranze alimentari (intolleranza al lattosio, allergia alle proteine del latte vaccino), feci da fame Fibrosi cistica, celiachia, immunodeficit Malattie infiammatorie croniche intestinali, enterocolite in corso di Hirschsprung Stipsi (diarrea paradossa), colon irritabile ELEMENTI ANAMNESTICI/CLINICI Vomito esclusivo, compromissione generale, dolore addominale, shock Vomito esclusivo Infezioni recenti con assunzione di antibiotici Durata > 14 giorni Durata > 14 giorni Durata > 14 giorni Durata > 14 giorni Tabella 11. Cause di diarrea acuta con i relativi elementi anamnestici più suggestivi.
46 SOSPETTO DIAGNOSTICO E MANIFESTAZIONI CLINICHE Sospettare una diarrea acuta non è certamente difficile. La conoscenza del pattern abituale di evacuazioni del proprio bambino consente generalmente anche ai genitori di riconoscere come anormale una frequenza aumentata di evacuazioni. Molto più difficile è, invece, avere un orientamento diagnostico differenziale sulla base di una sintomatologia così aspecifica. Le caratteristiche cliniche della sintomatologia e la conoscenza del pattern epidemiologico degli agenti di diarrea, anche se non permettono una distinzione eziologica, possono essere utili indicatori. La distribuzione stagionale degli agenti di diarrea mostra un evidente prevalenza del Rotavirus nei mesi invernali e primaverili. Al contrario, i principali agenti batterici circolano più frequentemente in tarda estate e in autunno. Il sospetto eziologico può derivare dalla valutazione di una serie di fattori: la storia del paziente; l età; i segni e sintomi possono indirizzare a una valutazione diagnostica. Con una storia di viaggi recenti in zone endemiche per diarrea, Escherichia coli, Salmonella, Shigella, Campylobacter, Vibrio, Entamoeba histolytica e Giardia lamblia dovrebbero essere considerati in una diagnosi differenziale. La comparsa di vomito dopo l ingestione di carne, molluschi, verdure non lavate, uova non cotte (spesso dolci preparati con uova) suggerisce la possibilità di infezione con agenti produttori di enterotossine come Escherichia coli, Staphylococcus aureus, Bacillus cereus, Salmonella o da parassiti, ma anche da virus come il virus di Norwalk o Norovirus. Una storia di assunzione di antibiotici e di antiacidi potrebbe indirizzare il sospetto diagnostico verso il Clostridium difficile o una sindrome da colonizzazione batterica del tenue prossimale. L età del paziente è cruciale per la diagnosi differenziale. Nei paesi occidentali, il più alto tasso di infezione da Rotavirus si riscontra in bambini di età inferiore ai 12 mesi, mentre dopo i 24 mesi prevalgono infezioni da Salmonella e Campylobacter. Uno studio olandese ha mostrato una prevalenza pari al 50% di infezioni virali in bambini con gastroenterite acuta di età inferiore a 4 anni. Ovviamente, il Rotavirus rappresentava la principale causa di gastroenterite in questa fascia di età, ma la prevalenza del virus di Norwalk era molto elevata. Nei bambini di età compresa tra i 5 e i 15 anni, Campylobacter e Giardia lamblia erano i patogeni batterici più comuni. Uno studio prospettico di sorveglianza sui ricoveri ospedalieri per diarrea acuta, effettuato in 8 ospedali italiani, ha evidenziato una prevalenza di infezioni da Rotavirus nei primi 24 mesi di vita, mentre nei bambini di età superiore ai 24 mesi la prevalenza di altre infezioni raggiungeva il livello di significatività statistica. Questo studio ha evidenziato anche che la gravità della diarrea non è correlata all età del paziente ma all eziologia e che il Rotavirus costituisce l agente eziologico più frequente e anche più temibile in età pediatrica. Come detto, i segni e i sintomi possono indirizzare a una valutazione diagnostica. La presenza di febbre indica un processo infiammatorio, ma può essere un segno della disidratazione. Il vomito è frequente nella diarrea non infiammatoria, quando la febbre è solitamente assente o di lieve entità; il dolore addominale, più spesso periombelicale, anche se c è, raramente è grave. La nausea e il vomito indicano generalmente la presenza di microrganismi che infettano l intestino tenue, in particolare virus (Rotavirus, Calicivirus-virus di Norwalk e virus di Sapporo ecc.), i già ricordati batteri produttori di enterotossine e, infine, Giardia e Cryptosporidium parvum. La febbre e i dolori addominali severi indicano prevalentemente un interessamento del colon, che è più spesso associato a un infezione di tipo batterico che virale.
47 L esame diretto delle feci per la presenza di muco, sangue o leucociti può essere di ulteriore aiuto per un orientamento diagnostico differenziale. Per esempio, grossi volumi di feci acquose senza muco, sangue e leucociti sono caratteristiche di un infezione da Vibrio, Salmonella, Escherichia coli enterotossigeni (ETEC), Cryptosporidium parvum, Giardia e della maggioranza degli agenti virali. La presenza di muco, sangue e leucociti nelle feci è più consistente con un infezione infiammatoria come quelle causate da Campylobacter, Escherichia coli enteroinvasivi (EIEC), Shigella, Clostridium difficile, Yersinia, Entamoeba e Citomegalovirus (CMV). L associazione di questi segni e sintomi può aiutare a distinguere una diarrea virale da una batterica (vedi Tabella 12). Quando il sospetto è di una diarrea virale (feci acquose, vomito e conseguente disidratazione), alcune caratteristiche sono più frequentemente associate con specifici enterovirus (vedi Tabella 13). Uno stato di immunodeficienza comporta un rischio elevato di infezioni serie e protratte anche da patogeni che, in bambini immunocompetenti, danno una diarrea autolimitata. In particolare, alcune parassitosi, quali le coccidiosi enteriche, si manifestano con una maggiore frequenza e con una sintomatologia più grave. Infatti, il Cryptosporidium parvum, responsabile del 5-10% delle diarree acute nei bambini immunocompetenti, rappresenta il più frequente patogeno opportunista responsabile di una diarrea secretiva di elevata gravità, in particolare in bambini con stadio avanzato di infezione da HIV. Tuttavia, sia l incidenza sia la gravità della criptosporidiosi sono state ridotte dopo l introduzione della terapia antiretrovirale di combinazione. Salmonella species Campylobacter species Shigella Rotavirus Virus di Norwalk Giardia lamblia Febbre ++++ * ++++ * ++++ * ++++ * + + Sangue nelle feci * ++++ * Dolori addominali ++++ * * + + Vomito * ++++ * + > 6 evacuazioni/die * ++++ * Durata dei sintomi 7 giorni 7 giorni 7 giorni < 4 giorni < 4 giorni > 7 giorni * p < 0,05 Tabella 12. Caratteristiche cliniche associate ai più frequenti microrganismi responsabili di diarrea acuta (Fonte: Guarino A, Albano F. La gastroenterite: fisiopatologia e correlati clinici diagnostici. Area Pediatrica, n. 2, anno 7, febbraio 2006).
48 Rotavirus (N = 189) Adenovirus (N = 35) Astrovirus (N = 34) NLV (N = 115) SLV (N = 44) Durata della diarrea (giorni) Massimo numero di episodi di diarrea in 24 ore Durata del vomito (giorni) Massimo numero di episodi di vomito in 24 ore Temperatura ( C) 38,8 38,4 37,9 37,9 37,8 Gravità dei sintomi Nota: i dati sono le mediane dei sintomi. Legenda: NLV = Virus di Norwalk; SLV = Virus di Sapporo Tabella 13. Sintomi e segni in corso di gastroenterite acuta associata a enterovirus in bambini di età inferiore ai 2 anni (Fonte: Guarino A, Albano F. La gastroenterite: fisiopatologia e correlati clinici diagnostici. Area Pediatrica, n. 2, anno 7, febbraio 2006).
49 IL RUOLO DELLA DIAGNOSTICA DI LABORATORIO In considerazione della breve durata della sintomatologia, si ritiene superfluo effettuare indagini di laboratorio, e questo permette un notevole risparmio di costi e tempo. Inoltre, l identificazione di un microrganismo nelle feci non comporta di per sé l attribuzione di un ruolo patogeno. È noto il problema dei portatori sani di patogeni enterici, in particolare della Salmonella. Per alcune specie batteriche, la patogenicità è legata alla capacità di esprimere fattori di virulenza. I fattori di virulenza sono in genere proteine o peptidi codificati da geni spesso presenti sui plasmidi. Uno o più fattori di virulenza determinano la capacità di un microrganismo di indurre diarrea. Il prototipo di microrganismo, la cui capacità patogena dipende dai fattori di virulenza e dalla possibilità di esprimerli è l Escherichia coli, microrganismo normalmente saprofita. Alcuni ceppi, però, possono indurre diarrea. Quindi, nella maggior parte dei casi, l esame microbiologico delle feci per l individuazione dell agente responsabile dell enterite (coprocoltura e ricerche virali) non è necessario, se non a fini epidemiologici, per le seguenti ragioni. L individuazione dell agente responsabile non modifica in genere l atteggiamento terapeutico, basato primariamente, come specificato in altro capitolo, sulla correzione e prevenzione della disidratazione e sulla rialimentazione. La frequente negatività dell esame è legata al ristretto numero di patogeni che possono essere isolati. La disponibilità del risultato giunge solo dopo 2-3 giorni, quando la sintomatologia tende spontaneamente al progressivo miglioramento. La possibilità che esistano portatori sani, il cui riscontro complica la decisione terapeutica. Si capisce, da quanto detto sopra, che un esame microbiologico iniziale delle feci deve essere riservato solo a casi selezionati. Le principali indicazioni all esame colturale delle feci sono rappresentate da: numero molto elevato di scariche giornaliere (> 10/die); presenza di sangue nelle feci; anamnesi positiva per viaggi in paesi ad alto tasso di infezioni e parassitosi intestinali e riscontro di persistenza della diarrea stessa e/o della febbre; diarrea persistente (oltre i 14 giorni). In questi casi, l esame microbiologico dovrebbe prevedere la ricerca dei seguenti patogeni: Campylobacter, Giardia lamblia, Rotavirus, Salmonella, Shigella. Per la ricerca di enterovirus che rappresentano, insieme con il Rotavirus, le cause principali di gastroenteriti, sono state messe a punto numerose tecniche (vedi Tabella 14), generalmente disponibili in centri di riferimento ed effettuate per studi epidemiologici.
50 VIRUS Identificazione dell antigene Microscopia elettronica PCR Tecnica preferita Adenovirus EIA +++ RT-PCR EIA Astrovirus EIA + RT-PCR EIA Calicivirus EIA + RT-PCR RT-PCR CMV EBV PCR PCR istologia, immunoistochimica istologia, immunoistochimica Picornavirus EIA RT-PCR EIA Rotavirus EIA ++++ RT-PCR EIA Legenda: + = identificabile da un microscopista esperto; ++++ = facilmente visibile. RT-PCR = Reverse transcriptase PCR analisi; EIA = enzyme immunoassay Tabella 14. Tecniche diagnostiche utilizzabili in caso di gastroenteriti virali (Fonte: Guarino A, Albano F. La gastroenterite: fisiopatologia e correlati clinici diagnostici. Area Pediatrica, n. 2, anno 7, febbraio 2006). Da tempo, è stata avanzata l ipotesi di utilizzare marcatori prognostici di infezione intestinale per stabilire l indicazione all esame microbiologico. I marcatori includono alcuni sintomi (febbre, vomito) e alcuni marker fecali (sangue, muco, leucociti, lattoferrina e calprotectina). Questi marker fecali sono tutti indirizzati verso l identificazione di una diarrea di tipo invasivo, cioè con lesione più o meno grave della mucosa intestinale, che spesso è causata da batteri. È stato proposto di eseguire la coprocoltura solo in presenza di marcatori prognostici per aumentare la percentuale di risposte positive e diminuire il costo per risultato positivo. Il significato del sangue nelle feci è ben conosciuto e le informazioni sulla ricerca dei leucociti fecali, sulla lattoferrina e sulla calprotectina fecale sono riportate di seguito. RICERCA DEI LEUCOCITI FECALI Un filamento di muco o di materiale fecale viene strisciato su un vetrino portaoggetti. Si aggiungono 2 gocce di blu di metilene e si attendono 2-3 minuti per una soddisfacente colorazione dei nuclei degli eventuali leucociti. Si lava delicatamente con acqua, si copre con un vetrino coprioggetto e si osserva al microscopio con obiettivo a immersione. Si osservano un alto numero di polimorfonucleati (oltre 25/campo ad alto ingrandimento) in caso di infezioni da Escherichia coli enteropatogeni ed enteroinvasivi, Shigella, Yersinia, Campylobacter, ma anche in caso di rettocolite ulcerosa. La Salmonella parathyphi si accompagna spesso a un modesto numero di polimorfonucleati. La ricerca è in genere negativa nelle diarrea da Rotavirus, Escherichia coli enterotossigeni, Vibrio. LATTOFERRINA FECALE La lattoferrina può essere identificata nelle feci con un test di agglutinazione. La lattoferrina è una glicoproteina legante il ferro di peso molecolare pari a u. Facilita la produzione di radicali idrossidi e, chelando il ferro, previene l accessibilità di quest ultimo ai microrganismi, inibendone la crescita. È presente nei granuli dei neutrofili polimorfonucleati e si riscontra in varie concentrazioni nel colostro, nel latte materno, nel muco vaginale, nel sangue e nella saliva. Enteropatogeni invasivi o citotossici possono favorire il rilascio di mediatori che stimolano la risposta dei polimorfonucleati e, quindi, il rilascio di lattoferrina. CALPROTECTINA FECALE È una proteina di 36 kda legante il calcio e lo zinco. Costituisce oltre il 60% delle proteine citosoliche dei neutrofili e il 5% delle proteine totali dell organismo. Si mantiene stabile a
51 temperatura ambiente sino a 7 giorni ed è facilmente dosabile nelle feci mediante un kit ELISA. È un marcatore di flogosi mucosale a carico di ogni segmento del tratto gastrointestinale. I livelli normali di calprotectina fecale sono, per i soggetti di età compresa tra i 2 e 17 anni, inferiori a 100 mg/g feci, senza significative variazioni a seconda dell età, del sesso e del tipo di dieta. Al contrario, nel neonato e nel piccolo lattante sono stati descritti livelli molto elevati di calprotectina fecale e mancano ancora dei valori normali di riferimento, e questo limita un uso routinario di questo marcatore in tale fascia di età. È possibile osservare valori elevati mg/g feci in diverse patologie a componente flogistica a carico del tratto gastrointestinale quali: esofagite, gastrite, gastroenteriti acute, celiachia, enterocoliti allergiche. Al contrario, in bambini con disordini gastrointestinali di tipo funzionale, i livelli di calprotectina fecale sono sempre normali. Nei bambini con malattia infiammatoria cronica intestinale (MICI) in fase attiva si osservano i valori più elevati di calprotectina (> mg/g). La calprotectina è attualmente da considerare uno dei marcatori più sensibili e di facile utilizzo (non invasivo, rapido, economico) per evidenziare uno stato infiammatorio a livello di qualsiasi tratto dell apparato gastrointestinale, utile per distinguere tra patologie funzionali e organiche, e nella diagnosi e follow-up di patologie a prevalente componente infiammatoria, in particolare delle MICI. Tenuto conto dei limiti di specificità di tali marcatori, della difficoltà di eseguire le indagini in ambulatorio e del limitato numero di patogeni identificabili, l ipotesi di utilizzare sistematicamente i marcatori di laboratorio per effettuare, nei casi positivi, l analisi microbiologica non appare giustificata. A questo va aggiunto che l indicazione alla terapia antibiotica, anche in corso di diarrea batterica, è limitatissima, e non tale da giustificare l esecuzione di coprocoltura solo in base alla presenza di marker di diarrea batterica. Per quanto riguarda la terapia antibiotica, è bene ricordare che il suo uso deve essere sempre deciso sulla base della valutazione: dell agente eziologico responsabile, della gravità della sintomatologia, delle condizioni legate all ospite, dei fattori socioambientali. Le indagini bioumorali (emocromo, PCR, determinazione della glicemia e degli elettroliti sierici, creatinina, emogasanalisi) dovrebbero essere limitate soltanto a condizioni particolari: disidratazione severa con compromissione dello stato circolatorio; disidratazione moderata, dove una consistenza pastosa della cute può indicare una ipernatriemia; disidratazione moderata in soggetti la cui storia clinica e il cui esame obiettivo non sono giustificati dal semplice episodio di diarrea. La presenza di chetoni nelle urine è un segno del tutto aspecifico e fuorviante, e non andrebbe ricercata come segno indicativo del grado di disidratazione. La si trova in tantissimi bambini febbrili non disidratati. I chetoni si formano in situazioni di aumentato metabolismo, non solo in ipoglicemia. Le linee guida della National Institute for Health and Clinical Excellence (NICE) riportano chiaramente che chetonuria e peso specifico urinario non sono correlati allo stato di idratazione. Lo stesso vale, per i pazienti in età pediatrica, per i valori di azoto ureico. Ricordiamoci che la diagnosi è guidata sempre dall anamnesi In molti casi di diarrea acuta non complicata, gli esami di laboratorio eseguiti per identificare l agente patogeno implicato risultano costosi e non necessari. Infatti, anche quando viene eseguito un pannello ampio di accertamenti, l agente patogeno responsabile della sintomatologia viene riscontrato solo nel 50-60% dei casi. Gli sforzi maggiori per identificare il patogeno devono essere riservati per i casi di diarrea ematica, spesso accompagnata da crampi addominali, febbre, tenesmo e feci mucose. La diarrea è spesso causata da batteri che
52 invadono la mucosa del colon, causando infiammazione e danneggiando la superficie intestinale. La scelta degli accertamenti diagnostici deve sempre essere guidata dall anamnesi e dalla sintomatologia clinica del soggetto in esame.
53 GESTIONE CLINICA La valutazione del grado di disidratazione rappresenta il punto cardine del management clinico iniziale del paziente pediatrico con diarrea acuta. Nell approccio al paziente con diarrea acuta, la valutazione di disidratazione e alterazioni idroelettrolitiche costituisce l aspetto più importante. Infatti, il primo scopo della terapia è rimpiazzare le perdite fecali e ripristinare l equilibrio idroelettrolitico. Ogni altro intervento diagnostico e terapeutico deve passare in secondo piano. Nella maggioranza dei casi, grazie a una terapia reidratante e a una corretta alimentazione, la diarrea dura poco tempo e la sintomatologia regredisce in 3-5 giorni. La terapia di approccio consiste nella reidratazione e nel mantenimento di un adeguato stato di idratazione; un errata valutazione dello stato di disidratazione può avere conseguenze gravi quali squilibri elettrolitici, acidosi, fino ad arrivare all insufficienza renale e allo shock ipovolemico. Nella pratica clinica, in realtà, il pediatra più spesso tende a sovrastimare il grado di disidratazione. Esistono poi dei fattori di rischio ulteriori che possono influenzare l outcome della gastroenterite acuta: l eziologia sottostante (infettiva, da malassorbimento, come effetto collaterale all assunzione di farmaci, deficit vitaminico, da ingestione di tossici, post-interventi chirurgici); le caratteristiche intrinseche del bambino (età, stato nutrizionale); le caratteristiche ambientali (scarse condizioni igieniche). Il bambino a rischio Il quadro clinico e il decorso della gastroenterite acuta sono influenzati principalmente dall eziologia sottostante e dalle caratteristiche intrinseche del paziente. Le infezioni gastrointestinali sono la causa più frequente di diarrea acuta, e i patogeni responsabili sono numerosi e diversi a seconda delle età: la gastroenterite da Rotavirus colpisce principalmente la fascia di età compresa tra i 6 e i 23 mesi, mentre sopra i 5 anni è più frequente l infezione da Campylobacter. La gastroenterite acuta riconosce anche altre eziologie, e le caratteristiche cliniche che ci devono far pensare a una diagnosi diversa da quella infettiva sono: dolore addominale con dolorabilità alla palpazione associato o meno alla presenza di addome poco trattabile; pallore, ittero, oligo-anuria, diarrea ematica; shock; compromissione generale non proporzionale allo stato di disidratazione. Tra i fattori di rischio legati all ospite, l età e lo stato nutrizionale sembrano essere quelli più rilevanti nel determinare la severità del quadro clinico e la durata della diarrea. In realtà, l importanza dell età come fattore di rischio è dibattuta. È noto che, nei bambini più piccoli, la funzionalità renale non è ancora del tutto matura, e questo potrebbe ostacolare il mantenimento di un adeguato equilibrio elettrolitico e dei liquidi corporei, e comportare quindi un quadro di disidratazione più grave e protratto. Un recente studio prospettico europeo di coorte ha dimostrato che la maggiore severità della gastroenterite acuta nel lattante è dovuta a una maggiore esposizione all infezione da Rotavirus, mentre non sono state dimostrate differenze rilevanti nel quadro clinico in relazione all età. Diversa è la situazione nei paesi in via di sviluppo, dove assumono particolare importanza nell aggravare il quadro clinico lo stato nutrizionale e le caratteristiche ambientali (scarse
54 condizioni igieniche, sovraffollamento, malnutrizione). A tal proposito, vari studi dimostrano che lattanti di età inferiore a 6 mesi presentano un rischio significativamente superiore di sviluppare un quadro clinico severo e diarrea protratta rispetto a quelli di età superiore. Come anticipato, lo stato nutrizionale riveste un ruolo importante nella gastroenterite acuta. Esistono forti evidenze in letteratura sull importanza dell allattamento al seno: i bambini allattati al seno hanno un rischio minore di sviluppare diarrea protratta. In uno studio condotto da Weinberg et al, l allattamento al seno sembra proteggere i lattanti dall infezione da RTV. Inoltre, Quigley et al hanno dimostrato che bimbi allattati al seno per almeno 3 mesi hanno un minor rischio di gastroenterite acuta e gli episodi di diarrea acuta hanno in genere durata più breve. Nel 2003, il Center for Disease Control (CDC) ha pubblicato le linee guida per la gestione della gastroenterite acuta nei pazienti in età pediatrica e ha stabilito che necessitano di una valutazione medica i bambini con almeno una delle seguenti caratteristiche: età < 3 mesi; peso corporeo < 8 kg; anamnesi con storia di prematurità, malattie croniche o patologie concomitanti; febbre 38 C per bambini di età < 3 mesi o 39 C per quelli di età compresa tra 3 e 36 mesi; presenza di sangue nelle feci; diarrea importante; vomito persistente; segni di disidratazione segnalati dal genitore: occhi alonati, pianto senza lacrime, mucose secche, contrazione della diuresi; alterazioni del sensorio; scarsa risposta alla somministrazione di soluzione reidratante orale o incapacità del genitore a gestire tale terapia. Nelle linee guida pubblicate, invece, nel 2008 da ESPGHAN/ESPID (European Society for Paediatric Gastroenterology, Hepatology, and Nutrition/European Society for Paediatric Infectious Diseases), i criteri che individuano i bambini con gastroenterite acuta che necessitano di una valutazione medica sono almeno uno dei seguenti: età < 2 mesi; patologie croniche concomitanti (diabete, insufficienza renale e altre); diarrea importante (> 8 scariche/die); vomito persistente; contrazione della diuresi. Valutazione della disidratazione Le linee guida dell Organizzazione Mondiale della Sanità (WHO), del CDC e dell ESPGHAN stabiliscono che il criterio più preciso per valutare il grado di disidratazione sia la percentuale di peso perso durante l episodio acuto. Risulta fondamentale la corretta definizione di un eventuale calo ponderale, che si rivela un buon indicatore della disidratazione, in quanto correlato con la perdita idrica. Si possono dunque distinguere 3 diversi livelli di disidratazione, a seconda della perdita di peso: 1. disidratazione lieve, quando il calo ponderale è inferiore al 3%; 2. disidratazione moderata, se il calo ponderale è tra il 3 e il 9%; 3. disidratazione grave, se il calo ponderale è superiore al 9%. I primi segni clinici, in genere, compaiono tardivamente, ovvero quando la disidratazione è di entità moderata con un calo ponderale compreso tra il 3 e il 9% del peso corporeo.
55 Qualora non sia disponibile un peso attendibile, il grado di disidratazione può essere stimato considerando l anamnesi, i segni clinici e i sintomi. I dati forniti dai genitori generalmente sono imprecisi e poco attendibili (una differenza del 10% tra peso riferito dai genitori e peso al momento della visita in un bambino senza o con segni modesti di disidratazione non sarà da considerare realistica). Dagli studi presenti in letteratura risulta che il riscontro all anamnesi di una diuresi contratta, pur essendo un dato oggettivo e facilmente quantificabile, non si associa a un aumento del rischio di disidratazione superiore al 5%. Tuttavia, in presenza di una diuresi riferita regolare, il rischio di disidratazione diminuisce. Esistono invece pochi dati sull entità della diarrea come fattore di rischio. Nei paesi in via di sviluppo, un elevato numero di scariche correla con un aumentato rischio di disidratazione severa, mentre tale dato non è disponibile per la popolazione europea. Nelle linee guida ESPGHAN/ESPID del 2008 per la gestione della gastroenterite acuta i segni clinici che correlano maggiormente con la presenza di disidratazione sono stati identificati con: il tempo di refill (il riempimento capillare o tempo del ricircolo capillare): se superiore a 2 secondi, indica uno stato di disidratazione moderata grave, l aumento della frequenza respiratoria, il turgore cutaneo (aumento del tempo di retrazione della plica cutanea). Tale dato risulta anche da una review pubblicata nel 2004 da Steiner et al.: in questo studio, gli autori valutano la precisione e l accuratezza di diversi segni e sintomi nell identificare una disidratazione del 5% o superiore, e anche qui i segni più specifici e sensibili risultano essere quelli sopra citati. Inoltre, gli autori definiscono utili per l inquadramento generale (anche se con specificità e sensibilità minori) il riscontro di estremità fredde, pianto senza lacrime e polsi flebili. Il tempo di riempimento capillare (Capillary Refill Time) è un rapido indicatore dello status circolatorio. È stato introdotto da Beecher nel 1947, ma solo nel 1980 Champion ha quantificato il normale tempo di riempimento capillare con un valore inferiore a 2 secondi. È uno strumento non invasivo e rapido per valutare la perfusione sistemica, molto usato in età pediatrica e inserito nelle linee guida europee e americane sul trattamento del bambino critico. La metodica si basa sull azione di comprimere il letto capillare e vedere il tempo per il ritorno del flusso facendo riferimento alla colorazione della cute: deve ritornare rosea in un tempo inferiore a 2 secondi. La compressione va effettuata sullo sterno nei bambini in età prescolare, oppure su un dito o su un braccio tenuto all altezza del cuore in quelli più grandicelli. La misurazione va eseguita in ambiente tiepido e non è influenzata dalla presenza di febbre. Un altro indicatore importante è il tempo di retrazione della plica cutanea, che si misura pizzicando la cute della parete addominale laterale a livello dell ombelico. Normalmente, la retrazione è istantanea e aumenta in modo direttamente proporzionale al grado di disidratazione. Negli anni, sono stati fatti vari tentativi al fine di creare uno score del grado di disidratazione attendibile e facilmente applicabile, ma senza successo. Tra quelli presenti in letteratura, ricordiamo lo score di Fortin et al. proposto per valutare il grado di disidratazione nei bambini dei paesi in via di sviluppo, e quello di Ruuska-Vesikari, utilizzato per stimare la gravità dell infezione da Rotavirus. In quest ultimo, viene attribuito un punteggio ai seguenti parametri: durata dell ospedalizzazione, numero massimo e durata delle scariche diarroiche e del vomito, temperatura corporea massima, grado di disidratazione. Il punteggio massimo è 20 e si definisce gastroenterite lieve quella con un punteggio tra 0-7, moderata tra 8-14, grave tra
56 Oltre al peso, nel valutare il grado di disidratazione, il pediatra deve considerare altri segni e sintomi, intuibili sulla base delle alterazioni fisiopatologiche dell organismo in corso di diarrea acuta. È importante osservare lo stato di idratazione delle mucose, il turgore cutaneo, la presenza di ipotensione e/o tachicardia, come meccanismo di compenso per mantenere la perfusione in caso di ipovolemia, e il tempo di riempimento capillare, che nel paziente disidratato tende ad allungarsi. Nel lattante disidratato, la fontanella può risultare depressa alla palpazione. Nel bambino disidratato e in acidosi, può essere riscontrata tachipnea. Nella Tabella 15 vengono sintetizzate le manifestazioni cliniche correlate ai diversi gradi di disidratazione. Condizioni generali, stato di coscienza Sete Disidratazione minima o assente (perdita di peso < 3%) Buone, paziente lucido Normale Disidratazione lieve-moderata (perdita di peso 3-8%) Agitato, irritabile o stanco Assetato, beve vigorosamente Frequenza cardiaca Normale Normale-elevata Disidratazione severa (perdita di peso > 9%) Apatico, letargico Beve poco o non riesce a bere Tachicardia; con ulteriore peggioramento, bradicardia Qualità del polso Normale Normale-ridotta Non palpabile Respiro Normale Normale o profondo Profondo, respiro acidotico Occhi Normali Incavati Molto incavati Lacrimazione Presente Ridotta Assente Mucose Umide Asciutte Secche Pliche cutanee (turgore) Scompaiono immediatamente Riempimento capillare Normale Lento Scompaiono dopo un ritardo < 2 secondi Rimangono per più di 2 secondi Marcatamente ritardato Estremità Calde Fredde Fredde, cianotiche Diuresi Normale Ridotta Minima Tabella 15. Manifestazioni cliniche correlate ai diversi gradi di disidratazione (Fonte: Giovannini M, Ghisleni D, Cavalleri V, Farina F. Diarrea acuta: i rimedi a disposizione del pediatra. Doctor Pediatria, 2012; 4: 8-17). Indicazioni al ricovero Non esistono in letteratura indicazioni precise sui criteri di ricovero del paziente con gastroenterite acuta e non sono possibili, per motivi etici, studi caso-controllo. La scelta di ricoverare o rimandare al domicilio un bambino con diarrea acuta non può basarsi su un singolo parametro, ma deve poggiare sulla valutazione globale delle condizioni del piccolo paziente. I criteri stabiliti dalle linee guida ESPGHAN/ESPID del 2008 per la gestione della gastroenterite acuta si basano su un consenso generale dei partecipanti alla stesura e prevedono il ricovero in presenza di uno dei seguenti criteri: shock,
57 disidratazione severa (> 9% del peso corporeo), alterazioni neurologiche (letargia, convulsioni), vomito incoercibile o vomito biliare, fallimento della terapia reidratante orale, genitori non affidabili (non in grado di garantire un adeguata assistenza domiciliare), sospetto di una patologia chirurgica.
58 TRATTAMENTO La terapia della diarrea acuta si basa principalmente su 3 punti: 1. reidratazione e correzione degli squilibri elettrolitici e dell acidosi, 2. alimentazione (rialimentazione) del soggetto, 3. terapia con i farmaci. La reidratazione In età pediatrica, la disidratazione in corso di diarrea acuta è la maggior causa di morbilità. In accordo con WHO (World Health Organization) e CDC (Center for Disease Control), i pazienti vengono classificati in 3 sottogruppi: 1. disidratazione lieve (< 3%); 2. disidratazione moderata (3%-9%); 3. disidratazione severa (> 9%), in base alla percentuale di calo ponderale e a parametri clinici quali perdita di elasticità cutanea, secchezza delle mucose, refilling capillare > 2 secondi, pianto senza lacrime. Il primo approccio terapeutico al bambino con la diarrea è rappresentato dalla reidratazione per via orale (ORT = Oral Rehydration Therapy) attraverso l assunzione di soluzioni reidratanti orali (ORS = Oral Rehydration Solution) che stimolano il riassorbimento di Na+ e ripristinano il normale equilibrio elettrolitico intestinale. Un appropriato management nutrizionale rappresenta il secondo step di una corretta gestione terapeutica della diarrea acuta. In corso di diarrea acuta, un attento esame delle condizioni cliniche consente la valutazione del grado di disidratazione (vedi Tabella 15: Manifestazioni cliniche correlate ai diversi gradi di disidratazione). La comprensione dei meccanismi patogenetici con cui enterotossine patogene causano diarrea secretoria ha chiarito come le capacità di assorbimento intestinali non vengano modificate. Per comprendere il ruolo delle soluzioni reidratanti orali (ORS) nel ripristino dei liquidi in corso di diarrea acuta, è fondamentale, quindi, soffermarsi sui meccanismi di trasporto intestinale e sul loro funzionamento nel soggetto sano e nel paziente affetto da diarrea. In condizioni fisiologiche, i processi di assorbimento di acqua ed elettroliti, dipendenti soprattutto dagli enterociti dei villi intestinali, prevalgono rispetto ai meccanismi di secrezione delle cripte. In corso di diarrea, l equilibrio elettrolitico a livello intestinale risulta alterato, e l unico meccanismo che sembra rimanere indenne, anche nelle forme caratterizzate da un danno epiteliale diretto, è il co-trasporto sodio-glucosio. È su questa base fisiopatologica che si fonda il razionale dell utilizzo della reidratazione per via orale. Le soluzioni reidratanti orali, infatti, stimolano il riassorbimento di sodio grazie all azione del co-trasportatore Na-glucosio, con conseguente riassorbimento di sodio e acqua e riespansione dei liquidi extracellulari. La sete è sempre presente nel bambino con una vera disidratazione; si può dunque approfittare della necessità manifestata dal bambino per proporre la soluzione reidratante, facendo però attenzione a reidratare in maniera lenta e graduale, per evitare di provocare il vomito e di stimolare il riflesso gastro-colico.
59 La reidratazione per via orale risulta quindi maggiormente efficace in qualunque forma di diarrea, e solo in caso di fallimento è preferibile la reidratazione attraverso l utilizzo di un sondino naso-gastrico (SNG). La reidratazione per via orale o tramite SNG viene effettuata attraverso la somministrazione di soluzioni reidratanti orali, contenenti acqua, elettroliti (Na, K, Cl) e glucosio. Negli anni, la composizione della soluzione reidratante è stata infatti più volte rimaneggiata (vedi Tabella 16). WHO 1975 ESPGHAN 1992 WHO 2002 Glucosio 111 mmol/l 90 mmol/l 75 mmol/l Sodio 90 mmol/l 60 mmol/l 75 mmol/l Potassio 20 mmol/l 20 mmol/l 20 mmol/l Cloro 80 mmol/l 60 mmol/l 65 mmol/l Basi (lattato, citrato o acetato) 30 mmol/l 30 mmol/l 30 mmol/l Osmolarità 311 mosm/l 225 mosm/l 245 mosm/l Rapporto Glucosio/Sodio Tabella 16. Composizione delle soluzioni reidratanti orali (ORS). Nel 1975, venne promossa da parte della WHO una composizione reidratante ad alto contenuto di glucosio e sodio, ritenuta particolarmente adatta alla diarrea causata da agenti infettivi molto aggressivi e utile, pertanto, per la correzione di importanti perdite elettrolitiche. Successivamente, divenne subito chiaro che tale composizione si adattava poco alla reidratazione delle gastroenteriti acute dei paesi più sviluppati, a causa del grande carico di sodio, potenzialmente in grado di indurre ipernatriemia. Venne pertanto promossa dall ESPGHAN nel 1992 una composizione contenente una minore quota di glucosio e sodio e, pertanto, ridotta osmolarità. La formula standard raccomandata inizialmente dalla WHO era costituita da 90 mmol/l di Na, 111 mmol/l di glucosio per una osmolarità totale pari a 311 mmol/l. Negli ultimi anni, l utilizzo di ORS a ridotta osmolarità ( mmol/l), con più basse concentrazioni di Glu e di Na, è stato raccomandato da ESPGHAN, WHO e UNICEF per la sua maggiore capacità di assorbimento dei soluti (vedi Tabella 17). La composizione ideale è risultata pertanto: Glu: mmol/l; Na+: 60 meq/l; K: 20 meq/l; Cl: meq/l; Osmolarità: mosm/l. L uso di soluzioni reidratanti contenenti substrati o sostanze aggiuntive (amylase-resistant, gomma di guar, carboidrati non digeriti, glutammina, probiotici, zinco), definite come super- ORS mancano di evidenze scientifiche che dimostrino la loro efficacia e, pertanto, non andrebbero utilizzate.
60 Glucosio (g/l) (mmol/l) SOLUZIONE CONCENTRAZIONI Na + (meq/l) 60 K + (meq/l) 20 Cl - (meq/l) Citrato (mmol/l) 10 Altri anioni (meq/l) (kcal/l) Osmolarità (mosm) Rapporto glucosio/na 1,2-1,8 Tabella 17. Composizione della soluzione reidratante orale (ORS). La terapia reidratante orale dovrebbe essere garantita per almeno 4-6 ore ad libitum, assicurando il seguente fabbisogno (vedi Tabella 18): disidratazione lieve: 50 ml/kg se < 10 kg e ml/kg se > 10 kg; disidratazione media: ml/kg; disidratazione grave: ml/kg. La soluzione reidratante orale va somministrata preferibilmente fredda e a piccoli sorsi per evitare l insorgenza del vomito. In particolare, nel corso della prima ora, andrebbe offerto ai bambini più piccoli (fino a 2 anni) mezzo cucchiaino da caffè di soluzione ogni 2 minuti, per un totale di circa 50 ml; ai bambini sopra i 3 anni un cucchiaino da caffè di soluzione ogni 2 minuti, per un totale di 100 ml. La quantità di liquidi offerti va aumentata progressivamente nel corso delle ore successive, in modo da raggiungere la quantità prevista nel corso di 4-6 ore. È importante rivalutare periodicamente le condizioni cliniche del paziente, fino a che non sia evidente un miglioramento delle condizioni generali e dello stato di idratazione. Dopo un episodio di vomito, è bene attendere 30 minuti prima di ricominciare a somministrare la soluzione reidratante orale. Se il bambino vomita, la reidratazione per os andrà effettuata a piccoli sorsi (5 ml ogni 2 minuti) e aumentata in quantità proporzionale al vomito. Per reintegrare le perdite, vanno somministrati 10 ml/kg per ogni scarica di diarrea e 2 ml/kg per ogni episodio di vomito. Il paziente che non assume adeguatamente la soluzione o ha segni di peggioramento deve essere rivalutato dopo 1-2 ore per vagliare l eventuale indicazione al ricovero. PESO CORPOREO Fino a 10 kg VOLUME 100 ml/kg kg ml + 50 ml per ogni kg oltre 10 > 20 kg ml + 20 ml per ogni kg oltre 20 Perdite pregresse: in 4-6 ore offrire 100 ml per ogni 100 g di perdita stimata Ripristino perdite subentranti: rivalutare ogni 6-12 ore, in base alla gravità della diarrea e aggiungere la perdita stimata in questo intervallo al volume programmato per l intervallo successivo. Tabella 18. Calcolo dei fabbisogni nella reidratazione.
61 Le formule per il calcolo dei liquidi di mantenimento, delle perdite e del fabbisogno di elettroliti sono riportate nella Tabella 19. Il fabbisogno idrico può essere calcolato in base alla superficie corporea o con la regola di Hollyday e Segar. Fabbisogno di acqua in base alla superficie corporea = 1800 ml/m 2 Fabbisogno di acqua in base alla regola di Hollyday e Segar: 100 ml/kg per i primi 10 kg di peso 50 ml/kg dai 10 ai 20 kg di peso 20 ml/kg per ogni kg sopra i 20 Esempio: per un bambino di 23 kg fabbisogno idrico/die (100 x 10) + (50 x 10) + (20 x 3) = 1560 ml Fabbisogno di elettroliti/die NaCl 40 meq/m 2 KCl 40 meq/m 2 Superficie corporea = [(peso x 4) + 7] / (peso + 90) Esempio: per un bambino di 23 kg Superficie corporea = [(23 x 4) + 7] / ( ) = 0,87 NaCl e KCl = 40 x 0,87 = 35 meq/die Perdite prevedibili Perdita di peso percentuale x peso reale (kg) x 10 Esempio: bambino che pesava 10 kg e ha perso il 10% del peso 10 x 10 x 10 = 1000 ml Aggiungere alle perdite idriche precedenti anche quelle subentranti Se diarrea per ogni scarica: 10 ml/kg Se febbre: 10 ml/kg per ogni C > 38 C Tabella 19. Calcolo dei liquidi di mantenimento, delle perdite e del fabbisogno di elettroliti (Fonte: Massaro M, Germani C, Calligaris L, Schreiber S, Bortoluzzi R, Ronfani L, Barbi E, Marchetti F. La gestione del bambino con gastroenterite acuta. Più efficacia con minor invasività. Medico e Bambino, 9/2012: ). L uso di bevande domestiche (per esempio, acqua o tè zuccherati), succhi di frutta, coca cola, preparati liquidi per atleti non è raccomandato a causa dell inadeguata concentrazione di sodio e della loro elevata osmolarità (correlata alla concentrazione dei carboidrati), quest ultima responsabile di eventuale peggioramento della diarrea. Un altro problema da tenere in considerazione è che le soluzioni reidratanti orali sono ipocaloriche e non contengono proteine o altri nutrienti, per i quali è dunque necessaria la supplementazione al fine di assicurare un adeguato intake nutrizionale (vedi Tabella 20).
62 LIQUID CHO, mmol/l Na, mmol/l K, mmol/l Base, mmol/l Osmolality Cola 700 (F, G) Apple juice 690 (F, G, S) Chicken broth Sports beverage 255 (S, G) * Adapted from Snyder J. The continuing evolution of oral therapy for diarrhea. Semin Pediatr Infect Dis. 1994; 5: CHO = carbohydrate; F = fructose; G = glucose; K = potassium; Na = sodium; S = sucrose. Tabella 20. (Fonte: AAP. Practice Parameter: The Management of Acute Gastroenteritis in Young Children. Provisional Committee on Quality Improvement, Subcommittee on Acute Gastroenteritis. Pediatrics, 1996; 97; ). Terapia reidratante parenterale La via endovenosa, un tempo la più utilizzata, è riservata alle disidratazioni di grado più severo o in caso di fallimento delle precedenti opzioni (circa 5% dei casi). La terapia reidratante per via endovenosa sarà somministrata: nella grave disidratazione, nella disidratazione modesta e moderata con vomito persistente, nello stato di shock, nello stato di incoscienza, quando la reidratazione orale non è in grado di rimpiazzare le perdite idriche. Qualora si renda necessaria la terapia reidratante parenterale, sarà richiesto un attento monitoraggio clinico del paziente associato a un bilancio idrico che tenga conto delle entrate e delle uscite. La disidratazione può essere classificata in: ipotonica o iponatriemica Na sierico < 130 meq/l; isotonica o isonatriemica Na sierico meq/l; ipertonica o ipernatriemica Na sierico > 150 meq/l. La terapia reidratante per via endovenosa va sempre iniziata con soluzione fisiologica (NaCl 0,9%): è isotonica, permette di iniziare la reidratazione rapida anche in assenza del valore degli elettroliti, in quanto è adeguata per la disidratazione ipo, iso e ipernatriemica. Di fronte a un bambino in shock o con shock incipiente, nella prima fase si deve ripristinare rapidamente un adeguato circolo periferico: va somministrata soluzione fisiologica, 20 ml/kg in 20 minuti, eventualmente ripetibili. In caso di disidratazione non grave, che necessita di reidratazione parenterale a causa del fallimento della reidratazione orale, il bolo di fisiologica verrà somministrato più lentamente (ad esempio 20 ml/kg in 1-2 ore). Al ripristino della volemia dovrebbe corrispondere un miglioramento delle condizioni cliniche e dei parametri vitali. A questo punto, è necessario pianificare la terapia per le successive 24 ore: il bambino dovrà ricevere il suo normale fabbisogno di acqua ed elettroliti (mantenimento) più le perdite verificatesi con il vomito e la diarrea, sottraendo a questo volume i liquidi già somministrati. Si dovrà poi tenere conto anche delle perdite intercorrenti a seguito di ulteriori scariche e reintegrarle adeguatamente. Anche in questa fase, non vanno utilizzate soluzioni povere di sodio, che potrebbero comportare lo sviluppo di iponatriemia, sia perché insufficienti a ripristinare la perdita di sodio, sia perché la gastroenterite acuta si può associare ad aumentata increzione di ADH. Quest ultima, è dovuta a stimoli emodinamici conseguenti alla disidratazione, ma anche a
63 stimoli non emodinamici come la nausea e il vomito. Comporta ritenzione di acqua libera (senza sodio) a livello renale, che, associata alla somministrazione di liquidi ipotonici, può portare a iponatriemia iatrogena. Ricordiamo che una correzione troppo rapida dell iponatriemia espone al rischio di mielinolisi centrale pontina, mentre una correzione troppo rapida dell ipernatriemia espone al rischio di edema cerebrale. È utile in questi casi ricordare la Regola del 12: l aumento/diminuzione della sodiemia non deve superare i 12 meq/l nelle 24 ore (0,5 meq/l/ora). Nella Tabella 21 è riportato un protocollo pratico per la terapia reidratante per via endovenosa. Sarebbe preferibile, una volta ripristinata la volemia, tentare di somministrare la soluzione reidratante orale e, se tollerata, completare la reidratazione per os. È importante istruire i genitori affinché continuino a somministrare la soluzione reidratante orale, approssimativamente 5-10 ml/kg per ogni scarica di diarrea o vomito, fino a risoluzione del quadro clinico, in modo da reintegrare le perdite e prevenire altri episodi di disidratazione. Per ridurre il tempo di permanenza in ospedale, sono stati recentemente proposti regimi di reidratazione rapida in cui si somministra una maggiore quantità di liquidi con il bolo iniziale (60 ml/kg). Il loro impiego è tuttavia controverso e un recente lavoro non ha rilevato alcun vantaggio per il gruppo trattato con lo schema di reidratazione rapida rispetto a quello standard (20 ml/kg).
64 Ricordare che: disidratazione vuol dire sempre deficit di H 2O e Na a prescindere dal valore della sodiemia la reidratazione rapida va iniziata subito, senza attendere il risultato degli elettroliti, con soluzione fisiologica che va bene per tutti i 3 tipi di disidratazione (iso/ipo/ipernatriemica) la presenza di acidosi metabolica non modifica l approccio Che fare? Accesso venoso prelievo per elettroliti, creatinina, glucosio (emogas) se shock, bolo di soluzione fisiologica 20 ml/kg in 20 minuti monitorare il circolo controllando tempo di ricircolo, frequenza cardiaca, pressione arteriosa se non c è miglioramento del circolo fare 2 bolo, se non c è miglioramento considerare altre cause di shock Terminata la fase di reidratazione rapida: calcolare il deficit residuo di H 2O e Na (deficit residuo = deficit iniziale - quantità somministrata nella fase di reidratazione rapida) e il mantenimento per 24 ore in questa fase bisogna fornire substrato energetico: le soluzioni usate dovranno essere al 5% di glucosio aggiungere K pari al mantenimento (se diuresi presente) avviare il prima possibile la reidratazione orale se in corso di reidratazione parenterale ci saranno scariche abbondanti, somministrare boli aggiuntivi di soluzione fisiologica (SF): 5-10 ml/kg per ogni scarica DISIDRATAZIONE ISONATRIEMICA (Na meq/l) bolo di soluzione fisiologica calcolare il deficit e il deficit residuo dopo il bolo di SF deficit: ml di H 2O pari alla perdita di peso con concentrazione di Na pari a quella plasmatica (ha perso 1 kg: avrà perso 1000 ml di H 2O e 135 meq di Na) correggere metà delle perdite residue con SF al 5% di glucosio nelle prime 4-6 ore somministrare l altra metà + mantenimento nelle successive ore DISIDRATAZIONE IPONATRIEMICA (Na < 130 meq/l) bolo di soluzione fisiologica calcolare il deficit e il deficit residuo dopo il bolo di SF deficit di H 2O pari alla perdita di peso deficit di Na: come per la disidratazione isonatriemica + il delta di Na delta Na = (135 - Na attuale) x peso in kg x 0,6 somministrare il deficit residuo + il mantenimento in 24 ore facendo attenzione alla velocità di risalita della sodiemia che dovrebbe essere 0,5-1 meq/ora (rischio di mielolisi pontina) se i sintomi neurologici (coma o convulsioni), o Na < 120 meq/l utilizzare boli di soluzione ipertonica (4-6 ml/kg di NaCl 3%) DISIDRATAZIONE IPERNATRIEMICA (Na > 150 meq/l) bolo di soluzione fisiologica calcolare il deficit e il deficit residuo dopo il bolo di SF deficit di H 2O pari alla perdita di peso in questo caso il deficit residuo di Na sarà molto basso ma non andranno mai usate soluzioni povere di Na per il rischio di edema cerebrale correggere lentamente per evitare il rischio di edema cerebrale (max 12 meq/l/die ovvero 0,5 meq/l/h) il deficit residuo di H 2O andrà ripristinato in ore: in pratica se il deficit residuo è di 900 ml e decidiamo di ripristinarlo in 48 ore daremo 450 ml/24 ore + il mantenimento giornaliero si utilizzerà una soluzione con NaCl 75 meq/l al 5% di glucosio, la velocità di infusione andrà regolata in base ai valori della sodiemia Tabella 21. Protocollo pratico per la terapia reidratante per via endovenosa (Fonte: Massaro M, Germani C, Calligaris L, Schreiber S, Bortoluzzi R, Ronfani L, Barbi E, Marchetti F. La gestione del bambino con gastroenterite acuta. Più efficacia con minor invasività. Medico e Bambino, 9/2012: ). L alimentazione (rialimentazione) Dopo aver quantificato l eventuale stato di disidratazione e iniziato le misure adatte a ripristinare i liquidi persi, è importante individuare il momento opportuno per reintrodurre l alimentazione enterale. Il working group dell ESPGHAN e numerosi lavori (vedi Tabella 22) hanno dimostrato che la ripresa della normale alimentazione dopo 4-6 ore di adeguata reidratazione orale è ben
65 tollerata e determina un più veloce recupero ponderale con miglioramento immediato dello stato nutrizionale. Una rapida rialimentazione dopo reidratazione orale si accompagnava infatti a un ripristino delle normali funzioni di permeabilità intestinale. Per prevenire la malnutrizione postenteritica, è quindi opportuno, concluse le 4-6 ore di terapia reidratante orale (ORT), riprendere l alimentazione adeguata per l età. Nei lattanti sopra i 6 mesi verranno reintrodotti gli alimenti solidi che il bambino riceveva precedentemente con alimentazione adeguata per l età. I bambini di età superiore a 12 mesi verranno rialimentati con gli alimenti solidi che ricevevano normalmente, incluso il latte vaccino. È opportuno cercare di assicurare il più possibile l adeguato apporto calorico durante l episodio di diarrea acuta, offrendo pasti piccoli e frequenti e aumentando l apporto calorico nei giorni successivi. La dieta deve essere libera e può contenere carboidrati, carne, latticini, frutta e verdura; gli unici cibi da evitare sono quelli ad alto contenuto di zuccheri semplici (dolci, bevande gassate, succhi di frutta ecc.), perché la loro carica osmotica può peggiorare la diarrea; possono determinare inoltre iponatriemia. Il lattante che prende il latte materno non deve mai sospenderlo, né durante la ORT né nel periodo successivo, perché è dimostrato che in questo modo si reidrata più velocemente il bambino e si riducono il volume e la frequenza delle scariche diarroiche. I bambini allattati artificialmente possono continuare ad assumere il loro latte di formula nelle quantità usuali e adeguate alle loro necessità nutrizionali; riducendo le razioni e aumentando la frequenza dei pasti si può avere beneficio sul numero e la quantità di scariche diarroiche. Di regola, non sono necessarie formule prive di lattosio, né è utile somministrare formule diluite, anzi è stato dimostrato che questa pratica è associata a prolungamento dei sintomi e a un ritardo del recupero del deficit nutrizionale. Le formule prive di lattosio vanno riservate a quei pazienti con intolleranza dimostrata al lattosio (persistenza della diarrea oltre i 10 giorni, recidiva diarroica dopo reintroduzione di una formula normale e presenza nelle feci di sostanze riducenti superiori a 0.5% e ph acido nelle feci). Un intolleranza secondaria al lattosio è possibile solo nel 3% dei casi.
66 Rees, Lancet 1979 Isolauri, JPGN 1985, 1986 Brown, J Pediatr 1988 Isolauri, JPGN 1989 Knudsen/Levine Gastroenterology 1968/1974 ESPGHAN 1994 Metanalisi Pediatrics 1994 Nanulescu, Acta pediat 1995 Metanalisi Pediatrics 1999 Arch Dis Child 1999 Arch Dis Child EBM 2003 Gregorio GV et al. Early versus Delayed Refeeding for Children with Acute Diarrhoea. Cochrane Database Syst Rev, 2011; (6): CD Nessun vantaggio della rialimentazione graduale (6-12 m) rispetto alla rialimentazione precoce Nessun vantaggio della rialimentazione graduale Più veloce recupero di peso (3 m-3 a) con la rialimentazione precoce Più pronta normalizzazione della permeabilità intestinale Più pronta correzione delle disaccaridasi La rialimentazione dopo 4 ore abbrevia la durata della diarrea e accelera il recupero del peso La rialimentazione precoce ha effetti positivi sulla durata della diarrea, sulla ripresa ponderale, sulla durata del ricovero (N.B.: mai sospendere il latte materno) Rialimentazione precoce, intesa in ore, con formula normale, in Romania Anche il latte formulato per la rialimentazione precoce Latte meglio della dieta in bianco per la rialimentazione Nessun vantaggio della rialimentazione tardiva La rialimentazione precoce non comporta un maggior rischio di complicanze rispetto al digiuno prolungato Tabella 22. Lavori sperimentali, teorici e pratici (sperimentazioni controllate) che dimostrano i vantaggi della rialimentazione precoce nella diarrea acuta. La terapia con farmaci Sebbene la terapia reidratante orale rappresenti il cardine della terapia della diarrea acuta, essa non è in grado di influenzare la durata della patologia o la frequenza dei movimenti intestinali. Per tale ragione, ogni farmaco in grado di interferire con questi aspetti può (potrebbe) rappresentare un utile ausilio da affiancare alla reidratazione orale. Per una completa terapia corretta della diarrea acuta, si dovrebbe cercare di correggere la causa, controllare rapidamente i sintomi e ripristinare la condizione fisiologica dell intestino, migliorando anche la funzione di protezione muco-epiteliale. MICRONUTRIENTI Il deficit di zinco è una condizione comune nei bambini dei paesi in via di sviluppo e si accentua in corso di diarrea acuta. Tale micronutriente può migliorare la risposta immune e i meccanismi di difesa dell ospite nei confronti degli agenti infettivi, la permeabilità intestinale, le funzioni enzimatiche ed epiteliali, e il trasporto degli elettroliti. Questo micronutriente, attraverso una diretta interazione con l epitelio intestinale, induce:
67 un effetto pro-assorbitivo e antisecretivo sul trasporto di fluidi, diventando efficace antagonista dei meccanismi secretivi indotti dai principali microrganismi responsabili di gastroenterite acuta nel bambino; la proliferazione e differenziazione degli enterociti; l inibizione della replicazione del principale patogeno, il Rotavirus, responsabile di gastroenterite acuta nei bambini di tutte le aree del mondo; uno stimolo di diverse funzioni del sistema immunitario. Una metanalisi (Patro B. 2008) condotta sulla base di 8 trial clinici randomizzati, che includevano pazienti, ha evidenziato che la supplementazione con zinco può essere utile nel trattamento della diarrea acuta, riducendone la severità e la durata, principalmente nei paesi in via di sviluppo. La revisione Cochrane pubblicata nello stesso anno concorda nel sostenere che lo zinco può comportare dei benefici nei bambini di età superiore a 6 mesi con diarrea, soprattutto in quelle aree dove tale patologia rappresenta un importante causa di mortalità infantile (Lazzerini M. 2008). Tra i vari micronutrienti proposti nel trattamento della gastroenterite acuta, da soli o addizionati all ORS, lo zinco è sicuramente la sostanza su cui esistono le maggiori prove di efficacia. Per tale motivo, l UNICEF e l OMS hanno emanato delle linee guida per la prevenzione e il trattamento della gastroenterite acuta in bambini di paesi in via di sviluppo, prevedendo per la prima volta l utilizzo di zinco: 20 mg di zinco al giorno per giorni (10 mg/die nei primi 6 mesi di vita) (Scrimgeour AG. 2008). Ulteriori studi sono invece necessari per definire il ruolo della supplementazione con zinco nel trattamento della diarrea nei bambini dei paesi industrializzati. PROBIOTICI L intestino del bambino è un ecosistema complesso, sede di un continuo interscambio tra le cellule dell ospite (le cellule epiteliali e quelle del sistema immunitario) e i circa microrganismi residenti (la microflora intestinale). Questo interscambio ha un influenza fondamentale, sia sulla funzione intestinale, sia sul benessere dell intero organismo. I microrganismi costituenti la microflora intestinale hanno un ruolo cruciale nella regolazione dell equilibrio dell ecosistema intestinale, ma questo equilibrio può essere alterato dall azione di agenti esterni, come, per esempio, dai patogeni responsabili di diarrea acuta nel bambino. In Europa, l assunzione volontaria di specie microbiche vive, non patogene, singole o multiple, sotto forma di prodotti diversi (alimenti, integratori o specialità farmaceutiche) è una pratica molto diffusa, che risale all inizio del secolo scorso. Una serie crescente di ricerche scientifiche rigorose e di evidenze sui loro effetti benefici e sulla loro efficacia nel prevenire e/o trattare alcune malattie ha incrementato l assunzione, spontanea o prescritta, di microrganismi vivi. I probiotici sono stati proposti per il trattamento e la prevenzione di diverse patologie gastrointestinali pediatriche: gastroenterite acuta infettiva, diarrea da antibiotici, colite da Clostridium difficile, disordini funzionali gastrointestinali, coliche gassose, enterocolite necrotizzante, malattie infiammatorie croniche intestinali, allergie alimentari, intolleranza al lattosio, patologie epatiche croniche (steatosi, cirrosi), pancreatite. Malgrado l ampio spettro potenziale di applicazioni, il numero di indicazioni basate su solide evidenze sperimentali e cliniche è ancora esiguo.
68 In Italia il mercato dei probiotici è in continua crescita e nel 2008 erano presenti 246 aziende produttrici, con circa 390 marchi. Solo nel 2007 sono stati immessi in commercio 46 nuovi marchi e sono stati venduti quasi 30 milioni di confezioni di probiotici, per un fatturato totale di circa 290 milioni di euro, con un incremento di oltre il 25% nell ultimo triennio. Nel panorama attuale, è difficile trovare altri esempi di un mercato così florido e in così rapida espansione. In questo mercato, i pediatri sono tra i maggiori prescrittori di probiotici, mentre si fa sempre più evidente una larga quota di autoprescrizione, alimentata in parte dalla pubblicità presente nei vari mezzi di comunicazione. In Italia, i probiotici sono commercializzati talora come farmaci, molto più spesso come integratori alimentari o altro. La qualità di molti dei prodotti contenenti probiotici in circolazione nel mercato nazionale è per alcuni aspetti problematica; per questo motivo si è sentita la necessità di stabilire: i requisiti di sicurezza minimi per le diverse forme commerciali e le relative metodologie di valutazione; la dose minima giornaliera consigliabile per ciascuna specie; le linee guida che consentano ai laboratori deputati al controllo ufficiale di valutare in maniera omogenea l accettabilità dei prodotti ed evitare interpretazioni divergenti nella valutazione di conformità; un protocollo di riferimento per l esecuzione delle prove di valutazione della sicurezza e dell efficacia. Definizione I probiotici sono organismi vivi che, se somministrati in quantità adeguate, come parte di un alimento o di un integratore alimentare, sono in grado di esercitare effetti benefici sull organismo umano. Per essere definito probiotico, un microrganismo deve soddisfare i seguenti requisiti (Thomas D. 2010): essere sicuro per l impiego nell uomo; non essere portatore di antibiotico-resistenze acquisite e/o trasmissibili; essere attivo e vitale a livello intestinale; essere in grado di persistere e moltiplicarsi nell intestino umano; mantenere intatte le proprie caratteristiche durante la conservazione. Quindi, le caratteristiche di un probiotico possono essere così sintetizzate: è un normale componente della microflora intestinale, colonizza temporaneamente l intestino, è resistente al succo gastrico, pancreatico e alla bile, aderisce alla mucosa gastrointestinale, è vitale e attivo nell intestino, sintetizza sostanze ad attività antimicrobica, compete con i patogeni per i nutrienti e i siti di adesione alla mucosa intestinale, ha un evidenza clinica di sicurezza documentata nell uomo. I microrganismi che possono essere impiegati negli alimenti e negli integratori alimentari [secondo la Revisione 2011 del Ministero della Salute: Indicazioni per l uso negli alimenti e negli integratori alimentari di microrganismi probiotici (batteri e/o lieviti), tradizionalmente utilizzati per l equilibrio della flora intestinale] devono soddisfare i seguenti requisiti: essere usati tradizionalmente per integrare la microflora (microbiota) intestinale dell uomo; essere considerati sicuri per l impiego nell essere umano; a questo scopo, un utile riferimento sono i criteri definiti dalla European Food Safety Authority (EFSA) relativi allo status di QPS ( Presunzione Qualificata di Sicurezza ). In ogni caso, oltre agli eventuali ulteriori parametri che l EFSA considererà opportuno introdurre, i microrganismi usati per la produzione di alimenti non devono essere portatori di antibiotico-resistenza acquisita e/o trasmissibile; essere attivi a livello intestinale in quantità tale da moltiplicarsi nell intestino.
69 L EFSA ha il compito di valutare la sicurezza degli agenti biologici notificati nel contesto delle richieste di autorizzazione. Numerosi microrganismi e virus sono stati o saranno sottoposti all esame dell EFSA. Il comitato scientifico dell EFSA ha raccomandato ai gruppi di esperti scientifici di adottare un approccio alla valutazione dei rischi comune, così da garantire un metodo uniforme: ovvero la presunzione qualificata di sicurezza (QPS). L EFSA gestisce un elenco di agenti biologici idonei alla valutazione QPS. Tale elenco viene riveduto annualmente dal gruppo di esperti scientifici sui pericoli biologici. Identificazione della specie e del ceppo Sempre secondo la Revisione 2011 del Ministero della Salute, è molto importante l identificazione della specie e del ceppo. L accertamento della posizione tassonomica è volta a garantire la sicurezza del microrganismo usato, perché consente di riconoscere la specie batterica con una lunga storia di consumo sicuro. L identificazione della specie può essere eseguita tramite: sequenziamento del DNA codificante per il 16S rrna, ibridazione degli acidi nucleici. La tipizzazione del ceppo batterico può essere fatta tramite: PFGE (Pulsed Field Gel Electrophoresis). Per denominare la specie, occorre utilizzare la nomenclatura tassonomica riconosciuta dalla International Union of Microbiological. È, inoltre, raccomandato il deposito dei ceppi nelle Collezioni Internazionali che posseggano lo status di IDA (collezioni internazionali di ceppi batterici). Quantità di microrganismi Sulla base delle evidenze scientifiche disponibili, la quantità minima sufficiente per ottenere una temporanea colonizzazione dell intestino da parte di un ceppo di fermento lattico è di almeno 109 cellule vive per ceppo e per giorno. La porzione di prodotto raccomandata per il consumo giornaliero deve, quindi, contenere una quantità pari a 109 cellule vive per almeno uno dei ceppi presenti nel prodotto. L uso di quantità diverse può essere consentito solo se il razionale per tale scelta è supportato da adeguati studi scientifici. La quantità di cellule vive presenti nel prodotto deve essere riportata in etichetta e deve essere garantita, alle modalità di conservazione suggerite, fino al termine della shelf life, con un incertezza di 0,5 log. Si precisa che i metodi di analisi più adatti per quantificare le cellule batteriche vive possono essere diversi per ogni specie. Sicurezza dei probiotici L uso di un nuovo ceppo microbico, sia pure appartenente a una specie già impiegata, richiede una nuova valutazione della sicurezza e dell efficacia. Ai fini dell accertamento della sicurezza, si ribadisce la necessità di un identificazione tassonomica a livello di specie e di ceppo, con le tecniche precedentemente indicate, così come la valutazione del profilo di antibiotico-resistenze antibatteriche o antimicotiche a seconda dei casi. Il profilo delle antibiotico-resistenze va determinato per ogni singolo ceppo microbico utilizzato, al fine di escludere la presenza di quelle acquisite e anche di quelle solo potenzialmente trasmissibili. Come eccezione, non si ritiene necessaria la valutazione della sicurezza per un ceppo che appartiene a specie sufficientemente caratterizzate, così come definito dai documenti EFSA per lo status di QPS per alcuni gruppi batterici. Anche in questo caso, comunque, va valutato il profilo di antibiotico-resistenza. Indicazione d uso: Favorisce l equilibrio della flora intestinale Come viene specificato nella Revisione 2011 del Ministero della Salute [Indicazioni per l uso negli alimenti e negli integratori alimentari di microrganismi probiotici (batteri e/o lieviti), tradizionalmente utilizzati per l equilibrio della flora intestinale], l indicazione d uso è quella di: Favorire l equilibrio della flora intestinale.
70 Il razionale dell indicazione d uso deriva dal parere riportato in EFSA Journal 2009; 7(9):1232, il Panel NDA (nutrizione, dietetica e allergie) dell EFSA (autorità europea per la sicurezza alimentare) sostiene: Increasing the number of any groups of bacteria is not in itself considered as beneficial. Meccanismo d azione Il campo delle conoscenze sui meccanismi d azione dei probiotici nella prevenzione e nel trattamento della diarrea acuta è in continua evoluzione. Molti studi sperimentali suggeriscono che i probiotici sono in grado di rafforzare i meccanismi di difesa non-immunitari a livello intestinale attraverso i seguenti effetti: competizione per i nutrienti e per i siti recettoriali utilizzati dai patogeni; idrolisi di tossine e recettori; produzione di sostanze ad azione antimicrobica (peptidi dell immunità innata); produzione di acidi organici e modulazione della sintesi di ossido nitrico; regolazione della permeabilità intestinale attraverso un azione sulle giunzioni serrate epiteliali (alcune proteine solubili prodotte da Lactobacillus GG denominate P40 e P75 prevengono il disarrangiamento delle principali proteine del citoscheletro coinvolte nella regolazione delle giunzioni serrate attraverso un meccanismo PKC e MAPKdipendente); stimolazione del trofismo della mucosa intestinale con un azione su specifici enzimi e sul trasporto di glucosio a livello del versante luminale dell enterocita, ed effetto antiapoptotico diretto sull enterocita; inibizione di alcuni meccanismi intracellulari coinvolti nella moltiplicazione virale (MEK, PKA, p38 MAPK). Dai dati della letteratura risulta sempre più evidente che i probiotici sono in grado di comunicare con gli altri componenti dell ecosistema intestinale (cellule epiteliali e immunitarie), stimolando lo sviluppo e il funzionamento dei meccanismi di difesa contro le infezioni. Un ruolo centrale nella comunicazione tra probiotici e cellule dell ospite è svolto dalle cellule dendritiche e dai toll-like receptor, molecole in grado di ricevere segnali da particolari componenti strutturali dei probiotici (lipopolisaccardi, peptidoglicani, CpG DNA ecc.) e di trasmetterli ad altre componenti cellulari dell ospite per regolare la produzione di componenti dell immunità innata (peptidi ad azione antimicrobica e immunoregolatoria) e adattativa di fondamentale importanza per la difesa dalle infezioni (vedi Figura 5). Figura 5. Ruolo dei toll-like receptor e delle cellule dendritiche nella relazione probiotici-epitelio intestinalesistema immunitario (Fonte: Berni Canani R. Il ruolo dei probiotici nella diarrea acuta. Area Pediatrica, 2008; 8: 13-19).
71 Alcuni probiotici sono in grado di promuovere una risposta anticorpale specifica contro determinati agenti patogeni. È questo il caso di Saccharomyces boulardii, che, oltre a elaborare una proteasi di 54 kda capace di idrolizzare le tossine A e B di Clostridium difficile e i rispettivi recettori a livello intestinale, è anche in grado di stimolare la produzione di IgG e IgA specifiche anti-tossina A prodotta dal patogeno. Lactobacillus GG è in grado di stimolare la produzione mucosale di IgA specifiche anti- Rotavirus e di modulare la risposta infiammatoria mucosale ai patogeni, stimolando la produzione di citochine ad azione antinfiammatoria (interleuchine 10 e 4) e inibendo la produzione di citochine ad azione proinfiammatoria (tumor necrosis factor-α, interleuchina 6, interferone-γ). Questa modulazione è potenzialmente di grande utilità nel regolare positivamente il flusso transepiteliale di fluidi, perché queste citochine pro-infiammatorie inducono un potente effetto secretivo a livello intestinale e una loro inibizione è di fatto in grado di ridurre le perdite di fluidi a livello del lume intestinale nel bambino con diarrea. Alcuni ceppi di Lactobacillus sono in grado di stimolare direttamente l azione dei geni che regolano la produzione di muco da parte delle cellule mucipare dell epitelio intestinale. Questa stimolazione determina un aumento dello strato di muco, ostacolando l adesione di Escherichia coli patogeni a livello intestinale. Lactobacillus GG è anche in grado di modulare negativamente la produzione della tossina Stx2A prodotta da Escherichia coli enteroemorragico (EHEC), attraverso un meccanismo che vede coinvolta una modificazione del ph mediata dalla produzione di acidi organici. Tutti questi effetti sono stati dimostrati in studi sperimentali e in alcuni studi clinici, ma è tuttora poco chiaro quale sia il principale meccanismo di azione in ogni singola condizione patologica; è probabile che diversi meccanismi contribuiscano all efficacia dei probiotici con un ruolo diverso nelle differenti situazioni cliniche, mentre è evidente che, anche nell ambito della stessa specie, ceppi differenti possono avere meccanismi di azione diversi nei riguardi dei vari patogeni (Figura 6). I meccanismi alla base dell azione dei probiotici possono essere riassunti in: normalizzazione della microflora intestinale, riduzione dell infiammazione e della secrezione di fluidi, inibizione dei meccanismi di attacco e invasione dei patogeni, stimolazione dell immunità innata e acquisita, inibizione della produzione di tossine batteriche, inibizione dell invasione e della sopravvivenza virale, effetto trofico sulla mucosa intestinale.
72 Figura 6. I vari meccanismi di azione dei probiotici nella diarrea (Fonte: Berni Canani R. Il ruolo dei probiotici nella diarrea acuta. Area Pediatrica, 2008; 8: 13-19). Indicazioni L efficacia nell utilizzo dei probiotici nel trattamento della diarrea acuta è stata dimostrata soprattutto per Lactobacillus GG e Saccharomyces boulardii (Guandalini S. 2011). Una Cochrane review del 2010 (Allen SJ. 2010) ha dimostrato il beneficio dei probiotici nel trattamento della diarrea acuta in età pediatrica, soprattutto nella diarrea da Rotavirus. Nel complesso, i probiotici hanno ridotto la durata della diarrea di circa 25 ore, diminuendo il rischio di diarrea della durata di 4 o più giorni del 59%, e hanno ridotto di circa 1 il numero delle scariche al giorno 2 dal trattamento. L effetto appare dose-dipendente e i risultati più soddisfacenti si ottengono nei bambini al di sotto dei 3 anni di età con diarrea di origine virale, se la terapia con probiotici viene iniziata nelle prime 24 ore di malattia. Attualmente, il trattamento e la prevenzione della diarrea acuta del bambino sono le applicazioni per le quali esiste il più alto livello di evidenza dell efficacia dei probiotici. L utilizzo dei cosiddetti fermenti lattici per la terapia della gastroenterite acuta è sempre stato molto diffuso in Europa, e in particolare in Italia. Nelle ultime decadi, l utilizzo dei probiotici per questa indicazione si è fatto ancora più ampio sino a superare, in termini di frequenza di utilizzo, la stessa soluzione reidratante orale che è e dovrebbe essere sempre il cardine del trattamento di ogni caso di diarrea acuta. Diversi probiotici sono stati proposti per la terapia della diarrea: la Tabella 23 riporta i ceppi e i dosaggi dei probiotici su cui vi è un più alto grado di evidenza di efficacia.
73 INDICAZIONE SPECIE E CEPPI DOSI Gastroenterite acuta infettiva Trattamento Trattamento Prevenzione Lactobacillus GG Lactobacillus rhamnosus (573 L/1, L/2, L/3) Lactobacillus acidophilus Lactobacillus delbrueckii var. bulgaricus Lactobacillus reuteri Saccharomyces boulardii Diarrea da antibiotici Saccharomyces boulardii Lactobacillus GG 1-2 x x CFU/die per 5 giorni 2 x x CFU/die per 5 giorni 1 x germi vivi (500 mg)/die per 5 giorni 1 x germi vivi (500 mg)/die per la durata del trattamento antibiotico 1-2 x CFU/die per la durata del trattamento antibiotico Colite da Clostridium difficile Trattamento o prevenzione Saccharomyces boulardii 1 x germi vivi (500 mg)/die per 7-14 giorni Tabella 23. Indicazioni e dosi nella prevenzione e nel trattamento della diarrea acuta (Fonte: Berni Canani R. Il ruolo dei probiotici nella diarrea acuta. Area Pediatrica, 2008; 8: 13-19). In questi ultimi anni, diverse metanalisi sono state pubblicate sull argomento e tutte hanno dimostrato un efficacia evidence-based dell uso di alcuni probiotici in questa particolare condizione. L efficacia è particolarmente evidente nelle diarree virali, e in particolare nella diarrea da Rotavirus. In queste condizioni, l intervento terapeutico deve essere quanto più possibile precoce, con una dose generalmente di almeno 10 miliardi CFU/die. Sebbene nella quasi totalità degli studi sia stata utilizzata la doppia somministrazione giornaliera, non è ancora chiaro se un eventuale somministrazione unica possa essere altrettanto efficace. Lactobacillus GG è il probiotico sul quale vi è un più alto grado di evidenza scientifica di efficacia nella terapia della gastroenterite acuta infettiva. Lactobacillus GG è in grado di limitare significativamente la durata della diarrea e dell escrezione del Rotavirus, riducendo il rischio di diarrea protratta e di trasmissione nosocomiale. Al contrario, la sua efficacia nelle diarree batteriche è meno evidente e i dati in letteratura sono ancora contrastanti, ma va sottolineato che in diversi studi Lactobacillus GG è risultato efficace a prescindere dall eziologia. Altri probiotici, quali Lactobacillus reuteri, Lactobacillus rhamnosus, Saccharomyces boulardii o l associazione Lactobacillus acidophilus e Lactobacillus delbrueckii var. bulgaricus, si sono dimostrati efficaci nel ridurre la durata della diarrea nel bambino, ma i dati disponibili possono essere considerati ancora preliminari. Per altri microrganismi, come Streptococcus thermophilus e Lactobacillus paracasei ceppo ST11, i dati sono ancora contrastanti. Diversi studi dimostrano che alcuni probiotici sono in grado di ridurre l incidenza e la gravità della diarrea acuta associata all uso di antibiotici. In particolare, la somministrazione di Lactobacillus GG o di Saccharomyces boulardii è risultata efficace nel ridurre significativamente l insorgenza e la gravità della diarrea indotta da antibiotici. Al contrario, la somministrazione di Lactobacillus acidophilus o di Lactobacillus bulgaricus non si è dimostrata utile. Almeno quattro metanalisi sono state pubblicate sull efficacia preventiva dei probiotici nei riguardi della diarrea da antibiotici. Tutte dimostrano l efficacia in particolare di
74 Lactobacillus GG o di Saccharomyces boulardii o dell associazione Bifidobacterium lactis e Streptococcus thermophilus, con dosi di almeno 10 miliardi CFU/die. Saccharomyces boulardii è il probiotico che si è dimostrato più utile nel trattamento della colite da Clostridium difficile (in associazione ad alte dosi di vancomicina). Sia Saccharomyces boulardii sia Lactobacillus GG sono risultati efficaci nel ridurre significativamente il numero delle ricadute dopo terapia eradicante specifica con metronidazolo o vancomicina in pazienti con colite da Clostridium difficile. Le indicazioni sull efficacia di alcuni ceppi di probiotici nel trattamento e/o prevenzione della diarrea acuta nel bambino devono essere considerate con molta attenzione dal pediatra, perché i dati ottenuti con un particolare ceppo, a una determinata dose, e in una particolare condizione clinica non sono necessariamente estendibili ad altri ceppi di probiotici, ad altre dosi o ad altre condizioni cliniche. Spesso, gli autori delle metanalisi concludono sulla necessità di interpretare i dati con cautela a causa dei limiti metodologici riscontrati nel corso della valutazione degli studi (differenze nelle condizioni cliniche, negli indici di outcome, nella durata del trattamento, nelle dosi ecc.). È quindi sempre molto importante saper scegliere, basandosi sui dati della letteratura disponibile, il ceppo e le dosi da utilizzare di un particolare probiotico risultato efficace per prevenire o trattare un certo tipo di diarrea acuta. Complicanze Numerose evidenze scientifiche suggeriscono l assoluta sicurezza dell utilizzo dei probiotici per il trattamento e la prevenzione della diarrea acuta nel bambino altrimenti sano, anche nei primissimi mesi di vita. L aderenza al trattamento riportata dai vari studi è generalmente ottima, e i rari e lievi eventi avversi riportati riguardano solo una lieve flatulenza transitoria e/o modificazioni del pattern delle evacuazioni. Complicanze gravi, di tipo settico, sono state riportate solo in pazienti in condizioni scadenti ricoverati nei reparti di terapia intensiva e negli immunodepressi. Queste segnalazioni sollevano il problema di possibili differenze tra ceppi diversi di probiotici e sottolineano la necessità di un utilizzo cauto dei probiotici in particolari condizioni a rischio, nelle quali è assolutamente necessaria un attenta valutazione del rapporto costo/beneficio per il paziente, che deve scaturire da una profonda conoscenza del ceppo utilizzato, delle dosi e della via di somministrazione raccomandata. Quindi, in sintesi, possiamo concludere che la sicurezza dei probiotici è dimostrata in numerosi studi, ma ricordiamoci dei pazienti a rischio sepsi, dei pazienti allergici alle proteine del latte vaccino e non va trascurata la resistenza agli antibiotici (rischio basso, ma non assente, di trasferimento genico ad altri batteri). Conclusioni Negli ultimi anni, in Italia come in altre nazioni europee, la popolarità e l utilizzo dei probiotici sono molto aumentati. Talvolta, campagne pubblicitarie accattivanti e larghi consumi hanno preceduto la disponibilità di chiare prove scientifiche di efficacia. Vi sono prove di una non sempre precisa concordanza tra quanto pubblicizzato (e dichiarato sulla confezione) e quanto (e cosa) realmente presente nel prodotto. La ricerca di base, volta allo studio dei meccanismi di azione, e la ricerca clinica, atta a esplorare l efficacia clinica dei vari ceppi, sono molto attive in questo campo, e nuovi approcci sono attualmente utilizzati per definire meglio le reali potenzialità dei diversi ceppi di probiotici. Il percorso storico dell utilizzo dei probiotici per la diarrea acuta del bambino è stato molto lungo, tanti progressi sono stati compiuti negli ultimi anni ed è possibile prevedere ulteriori sviluppi molto interessanti nel prossimo futuro. Dai dati disponibili in letteratura, appare chiaro che quanto dimostrato per uno specifico ceppo, a una determinata dose e per una particolare condizione non è necessariamente estendibile a specie, ceppi, dosi e condizioni differenti. Se in Italia sono presenti in commercio circa 390 marchi di probiotici, e le diverse formulazioni hanno indicazioni differenti, derivanti dalle evidenze scientifiche disponibili, appare chiaro che è compito del pediatra selezionare accuratamente, basandosi su un attenta
75 valutazione della letteratura disponibile, il probiotico utile per la terapia di una particolare condizione, utilizzando dosaggi appropriati. ANTIMICROBICI La terapia antibiotica in caso di gastroenterite acuta non è indicata dal momento che: i virus sono la causa più frequente di diarrea acuta nel nostro paese; la maggior parte delle gastroenteriti acute si risolve spontaneamente e la sua durata non è abbreviata dal trattamento antibiotico; è in aumento la resistenza alla terapia antibiotica dei batteri enteropatogeni, specie Salmonella, Shigella, Campylobacter jejuni; l uso indiscriminato degli antibiotici può prolungare lo stato di portatore. L uso di antibiotici deve essere sempre deciso sulla base della valutazione: dell agente eziologico responsabile, della gravità della sintomatologia, delle condizioni legate all ospite. La gravità della sintomatologia è un elemento di valutazione fondamentale per stabilire l opportunità di un trattamento antimicrobico. Per quanto riguarda le condizioni legate all ospite, l età neonatale è un indicazione al trattamento. Nelle diarree gravi del neonato, il trattamento deve essere iniziato con una terapia ad ampio spettro per via generale, come per le sepsi. Appena disponibile una diagnosi eziologica, è indicato un antibiotico specifico. Tra le condizioni legate all ospite che costituiscono indicazione al trattamento antimicrobico vi sono anche le immunodeficienze e lo stato di malnutrizione. Nella Tabella 24 è riportata la terapia antimicrobica in corso di diarrea infettiva in relazione all agente eziologico. AGENTE PATOGENO FARMACO INDICAZIONI Shigella Salmonella typhi Salmonella non tifoidea Escherichia coli Vibrio colera Yersinia enterocolitica Campylobacter jejuni Ampicillina Cotrimossazolo Ampicillina Cloramfenicolo Cotrimossazolo Ampicillina Cloramfenicolo Cotrimossazolo Cotrimossazolo Cotrimossazolo Tetracicline Cotrimossazolo Cloramfenicolo Eritromicina Sempre Sempre Età < 6 mesi Portatori di protesi cardiache Malattie infiammatorie croniche intestinali Anemie emolitiche Emoglobinopatie Viaggiatori in aree endemiche Neonato Diarrea protratta Sempre Diarrea grave o protratta Pazienti con diarrea ematica o grave o pazienti che frequentano comunità ad alto rischio di diffusione Clostridium difficile Metronidazolo Colite pseudomembranosa Entamoeba histolytica Metronidazolo Sempre Giardia lamblia Tinidazolo Metronidazolo Sempre Tabella 24. Terapia antimicrobica della diarrea acuta (Fonte: Giovannini M, Ghisleni D, Cavalleri V, Farina F. Diarrea acuta: i rimedi a disposizione del pediatra. Doctor Pediatria, 2012; 4: 8-17).
76 Il trattamento antibiotico nella gestione della gastroenterite acuta è quindi, in genere, di scarsa utilità e spesso gli svantaggi a esso correlato superano i vantaggi che ne potrebbero derivare, come nel caso della gastroenterite acuta indotta da Salmonella non tifoidea, dove la terapia antimicrobica induce spesso uno stato di portatore sano, senza modificare il decorso della malattia. L uso empirico degli antibiotici nel trattamento della diarrea acuta non è usualmente raccomandato in età pediatrica, ma viene riservato ai pazienti immunocompromessi o affetti da patologie croniche severe. Il trattamento antibiotico può essere appropriato quando il patogeno responsabile della sintomatologia viene identificato. È importante l utilizzo di nuovi agenti antimicrobici, a spettro più ristretto e selettivo, in grado di minimizzare i potenziali danni a carico della flora intestinale, i quali invece possono spesso derivare dall impiego indiscriminato di antibiotici a largo spettro. I trattamenti antibiotici prolungati in età pediatrica possono, inoltre, predisporre alla comparsa di condizioni caratterizzate da alterata permeabilità intestinale in età adulta. L uso degli antibiotici andrebbe quindi riservato solo in caso di positività della coprocoltura per specifici agenti eziologici la cui frequenza è peraltro rara in Italia: Vibrio cholerae, Shigella spp., Entamoeba histolytica, Salmonella typhi, Giardia lamblia. Altri fattori potenzialmente utilizzabili per individuare la necessità di un trattamento antimicrobico sono la sintomatologia grave e le condizioni legate all ospite (vedi Tabella 25). L uso della terapia antimicrobica deve essere sempre effettuato nelle infezioni da Shigella, Salmonella typhi, Vibrio cholerae, Amebiasi e Giardiasi. EZIOLOGIA GRAVITÀ DEI SINTOMI FATTORI DI RISCHIO DELL OSPITE Salmonella typhi Batteriemia Età neonatale Shigella spp. Sintomi neurologici Malnutrizione Vibrio cholerae Entamoeba histolytica Giardia lamblia Diarrea persistente (> 14 giorni) Shock settico Diarrea invasiva Infezione da HIV e altre immunodeficienze Tabella 25. Indicazioni alla terapia antibiotica nel bambino con gastroenterite acuta. ADSORBENTI La diosmectite è un argilla naturale (silicato di alluminio e magnesio) con una struttura lamellare e cristallina e un elevato potere adsorbente. Il suo meccanismo d azione non è completamente noto, e si ritiene che possa derivare da una combinazione di effetti. La diosmectite riduce infatti l infiammazione, modifica le proprietà reologiche del muco, inibisce la mucolisi e adsorbe i batteri, le enterotossine batteriche, i virus e le altre sostanze potenzialmente responsabili di diarrea. Una recente revisione (Dupont C. 2009) ha evidenziato che la diosmectite riduce la durata della diarrea e la frequenza dei movimenti intestinali dopo 2 giorni di trattamento in bambini con diarrea acuta di grado lieve-moderato. Per il suo profilo di sicurezza, la diosmectite è oggi frequentemente utilizzata, specialmente nei paesi europei, in aggiunta alla terapia reidratante orale. Gli agenti intraluminali come i silicati (per esempio, diosmectite) che hanno mostrato un efficacia hanno però un effetto unicamente sintomatico sulla durata della diarrea.
77 Il loro elevato potere adsorbente può, inoltre, interferire con l assorbimento gastrointestinale di alcuni farmaci somministrati per via orale. ANTIPERISTALTICI I farmaci che presentano un azione sulla motilità intestinale comprendono gli oppiacei e gli anticolinergici. A causa degli effetti collaterali sul sistema nervoso centrale, la maggior parte di questi farmaci sono controindicati in età pediatrica nonostante il loro evidente effetto sull attività peristaltica e sull attività secretiva intestinale. Una rallentata peristalsi indotta da tali agenti, tra cui gli oppiacei (loperamide) e gli anticolinergici, può, oltre a mascherare le perdite idriche, aumentare il tempo di contatto tra patogeni (e sostanze da questi prodotte) e l epitelio intestinale, andando a minare la fisiologica funzione della diarrea. L unico farmaco di questa categoria che potrebbe essere potenzialmente utilizzato per la gastroenterite acuta è la loperamide. Tuttavia, la segnalazione di gravi effetti collaterali (letargia, ileo paralitico, depressione respiratoria, coma sino al decesso) ne sconsigliano fortemente l uso in età pediatrica e, di fatto, attualmente l utilizzo della loperamide (al pari di altre sostanze a effetto antiperistaltico) è controindicato nei pazienti di età inferiore ai 16 anni. ANTIEMETICI Il vomito è molto spesso il sintomo di esordio della gastroenterite acuta ed è frequentemente responsabile di disidratazione, difficoltà all assunzione delle soluzioni reidratanti orali, necessità di reidratazione per via parenterale e, quindi, di ricovero. Tuttavia, l uso di antiemetici è generalmente sconsigliato nel bambino con gastroenterite acuta per i numerosi effetti collaterali (letargia, sintomi extrapiramidali, depressione respiratoria e aritmie cardiache) dovuti all antagonismo dopaminergico delle formulazioni di più vecchia generazione, come il metoclopramide. Gli antiemetici sono comunque frequentemente prescritti nella pratica clinica. Secondo una recente indagine, in Europa e nel Nord America tra il 2% e il 23% dei bambini con diarrea acuta riceve un antiemetico (Pfeil N, Uhlig U, Kostev K et al. Antiemetic Medications in Children with Presumed Infectious Gastroenteritis-Pharmacoepidemiology in Europe and Northern America. J Pediatr, 2008; 153: ); in Italia, il 79% dei pediatri dichiara di prescrivere antiemetici ai propri pazienti in corso di gastroenterite acuta (Albano F, Bruzzese E, Spagnuolo M et al. Antiemetics for Children With Gastroenteritis: Off-Label but Still On in Clinical Practice. J Pediatr Gastroenterol Nutr, 2006; 43: ). Il vomito è un esperienza molto spiacevole, sia per il bambino sia per i genitori e, oltre a essere causa della stessa disidratazione, può ostacolare il successo della soluzione reidratante orale e, pertanto, determinarne il fallimento. Molti medici ritengono che il vomito rappresenti una controindicazione alla soluzione reidratante orale. Inoltre, in un contesto assistenziale come quello del PS, gli operatori sanitari sono più propensi a utilizzare la terapia reidratante per via endovenosa nei casi in cui il vomito rappresenti il sintomo più rilevante. Per queste ragioni, un efficace trattamento del sintomo vomito potrebbe avere un ruolo importante per ridurre l utilizzo della terapia reidratante per via endovenosa, e favorire l impiego della terapia reidratante orale nel caso in cui ci sia stato un iniziale fallimento nel suo utilizzo. L ondansetron (antagonista 5-HT3 selettivo che, non agendo sui recettori centrali della dopamina, è scevro di particolari effetti collaterali) è l antiemetico che presenta più evidenze a favore dell impiego nella gastroenterite acuta (DeCamp LR, Byerley JS, Doshi N, Steiner MJ. Use of Antiemetic Agents in Acute Gastroenteritis: A Systematic Review and Meta-Analysis. Arch Pediatr Adolesc Med, 2008; 162: ) e la sua prescrizione è molto frequente nelle strutture di PS Nordamericane.
78 È dimostrata la sua efficacia nel ridurre il rischio di nuovi episodi di vomito, nel diminuire il numero di pazienti che necessitano di terapia reidratante per via endovenosa e di ricovero ospedaliero e un recente lavoro ne ha anche dimostrato i vantaggi in termini di riduzione della spesa sanitaria (Freedman SB, Steiner MJ, Chan KJ. Oral Ondansetron Administration in Emergency Departments to Children with Gastroenteritis: An Economic Analysis. PLoS Med, 2010; 7/10). Le dimensioni relativamente piccole dei campioni su cui sono stati condotti gli studi non consentono però di trarre conclusioni definitive riguardo agli effetti collaterali. In Italia gli antiemetici hanno indicazioni molto ristrette: l ondansetron è indicato in età pediatrica solo per la nausea e il vomito da chemioterapia o postoperatorio, mentre l antiemetico più prescritto per il vomito da gastroenterite acuta è il domperidone, seguito dalla metoclopramide. Le evidenze disponibili riguardo all utilizzo di questi due farmaci sono però molto limitate: sono stati condotti pochi studi, su campioni piccoli e con scarsa qualità metodologica, con risultati non conclusivi, in particolare per quanto riguarda il domperidone. La metoclopramide è controindicata in Italia sotto i 16 anni di età a causa del rischio di reazioni extrapiramidali. Una recente metanalisi Cochrane (Fedorowicz Z, Jagannath VA, Carter B. Antiemetics for reducing vomiting related to acute gastroenteritis in children and adolescents. Cochrane Database Syst Rev, 2011; (9): CD005506) ha messo in evidenza la necessità di ulteriori studi che mettano a confronto antiemetici diversi e a diversi dosaggi, che diano informazioni sul tempo che intercorre tra la somministrazione del farmaco e la cessazione del vomito, e che definiscano in modo chiaro se l impiego degli antiemetici può ridurre effettivamente la frequenza delle ospedalizzazioni. Al momento, nella pratica clinica, in regime osservazionale di PS, è consigliabile l utilizzo dell ondansetron per via orale (alla dose di 0,15-0,20 mg/kg) nei casi che hanno avuto un fallimento con il primo tentativo di soluzione reidratante orale. In conclusione, possiamo affermare che negli ultimi anni numerose evidenze in letteratura dimostrano l efficacia dell ondansetron, in monosomministrazione per os nella terapia sintomatica del vomito in bambini giunti in pronto soccorso per gastroenterite acuta lievemoderata. L ondansetron si è rivelato utile nel ridurre severità e durata del vomito, necessità di reidratazione parenterale e di ricovero, favorendo anche l assunzione della soluzione reidratante orale. L unico effetto collaterale segnalato è un possibile aumento del numero di evacuazioni nelle 48 ore successive al trattamento. Si tratta, quindi, di una potenziale nuova strategia terapeutica da utilizzare in pazienti con gastroenterite acuta affetti da severa iperemesi che ne condiziona negativamente la possibilità di assumere adeguate quantità di soluzione reidratante orale. Nuovi studi sono necessari prima di prevedere un uso esteso di questa strategia terapeutica anche in pazienti ambulatoriali. ANTISECRETORI La gestione del bambino con diarrea acuta non necessita generalmente di terapie specifiche, oltre alla reidratazione. Il trattamento della diarrea acuta considerato di prima scelta dall OMS si fonda quindi sulla reidratazione orale con soluzione glucosalina e sulla rialimentazione precoce che favorisce la ricostruzione dei villi grazie alla presenza di alimenti all interno del tubo digerente. Nonostante la sua comprovata efficacia, la soluzione reidratante orale è tuttavia una terapia sottoutilizzata, sia per la difficoltà di somministrazione in un bambino che spesso vomita o non ne gradisce la palatabilità, sia perché, pur essendo efficace sulla disidratazione, non modifica in modo clinicamente importante la durata della diarrea. L effetto sull output fecale (emissioni di feci) è ritenuto dall OMS il principale criterio per concludere che un farmaco sia efficace nella diarrea acuta. Vi è, quindi, la richiesta, e non solo da parte dei genitori, di un farmaco che riduca frequenza e quantità di emissioni di feci durante un episodio di diarrea acuta.
79 Negli ultimi anni, vi è una maggiore disponibilità di farmaci efficaci e sicuri in grado di ridurre il numero di evacuazioni e la durata complessiva della diarrea. Tra questi, gli antisecretivi, e, in particolar modo il racecadotril, stanno trovando una crescente applicazione nella gestione pratica del bambino affetto da gastroenterite acuta. Le linee guida della Società Europea di Gastroenterologia, Epatologia e Nutrizione Pediatrica (ESPGHAN), del maggio 2008, forniscono un evidenza di tipo II B sul possibile uso del racecadotril nella gestione della gastroenterite acuta. Il racecadotril è una molecola recentemente introdotta nella terapia della diarrea acuta. Si tratta di un potente e selettivo inibitore delle encefalinasi intestinali, enzima chiave nel catabolismo delle encefaline (oppioidi endogeni), importanti neurotrasmettitori con un attività antisecretiva nel tratto gastrointestinale. L inibizione enzimatica, che il racecadotril determina, comporta un potenziamento dell azione delle encefaline sul recettore intestinale per gli oppioidi. Il blocco dell encefalinasi determina un attività antidiarroica dovuta a un aumento dell attività antisecretoria pura propria delle encefaline, senza alterare il normale tono e la motilità intestinale. L effetto antidiarroico si espleta per una diminuzione della secrezione di acqua e degli elettroliti intestinali, che generalmente aumenta in risposta all infezione locale. Nel 1999 è stato pubblicato il primo contributo in letteratura che paragonava l efficacia di racecadotril rispetto alla loperamide in bambini con diarrea acuta. Si trattava di uno studio multicentrico, in doppio cieco, condotto in bambini di età compresa tra 2 e 10 anni con diarrea acuta. La durata della diarrea era simile nei due gruppi, tuttavia l incidenza di effetti collaterali era maggiore nei bambini trattati con loperamide (22% vs 11%) e un numero elevato di pazienti trattati con loperamide presentava costipazione dopo il trattamento (58% vs 36.5%; P 0.03). Sulla base di tali dati, veniva evidenziato il miglior profilo di sicurezza del racecadotril nei bambini affetti da gastroenterite acuta (oltre al possibile uso del racecadotril nella fascia di età inferiore ai 2 anni, in cui la loperamide è controindicata). Uno dei primi RCT (Salazar-Lindo E et al., in doppio cieco), in cui si valutava l efficacia di racecadotril rispetto al placebo nel bambino con diarrea acuta, è stato pubblicato nel 2000 su New England Journal of Medicine. Sono stati reclutati 135 bambini maschi peruviani, di età compresa tra 3 e 35 mesi, ricoverati in ospedale a Lima con diarrea nei precedenti 5 giorni ed emissione di feci liquide. Gli autori dichiarano di aver scelto di includere solo maschi nello studio per avere una minore contaminazione di feci e urina. I pazienti ricevono il trattamento o il placebo sotto forma di polvere con identico gusto e aspetto, in aggiunta alla SRO. Il racecadotril è somministrato alla dose di 1,5 mg/kg/die; 68 bambini ricevono il trattamento e 67 il placebo. Obiettivo primario dello studio era la riduzione dell output fecale (espresso in g/kg) a 48 ore. L analisi Intention To Treat (ITT) mostrava che i bambini trattati con racecadotril presentavano un ridotto output fecale nelle prime 48 ore rispetto al gruppo trattato con placebo (92+/-12 g per kg nel gruppo racecadotril vs 170+/-15 g per kg nel gruppo placebo; P < 0.001), con una differenza media del 46% (IC 95%: ). Si considera terminata la diarrea quando i bambini hanno 2 emissioni consecutive di feci formate o nessuna emissione di feci per 12 ore. La durata media della diarrea è stata di 28 ore nel gruppo trattato senza differenze rispetto alla positività per Rotavirus; nel gruppo di controllo è stata di 72 ore nei pazienti Rotavirus-positivi e 52 ore nei Rotavirus-negativi. In 7 pazienti in trattamento e in 5 in placebo sono stati riscontrati effetti collaterali, e in 4 dei pazienti in racecadotril gli effetti collaterali sono stati attribuiti al trattamento. I bambini che assumevano racecadotril necessitavano inoltre di quantità inferiori di ORS rispetto al gruppo placebo (P < 0.001). Nel 2001 è stato pubblicato su Gastroenterology un altro RCT (Cézard JP et al., in doppio cieco). Il trial di Cézard confronta efficacia e tollerabilità del racecadotril rispetto al placebo.
80 Vengono arruolati 172 pazienti di entrambi i sessi, di età compresa tra 3 mesi e 4 anni (media 12,8 mesi) con diarrea acuta severa (almeno 3 scariche di feci acquose da più di 72 ore), ricoverati in 13 ospedali francesi. È uno studio randomizzato in doppio cieco. L outcome primario è l output fecale nelle 48 ore, calcolato in grammi per ora (g/h). Il peso delle feci viene calcolato ogni 12 ore, le urine raccolte a parte con il sacchetto. Outcome secondari sono l output fecale nelle prime 24 ore, il rapporto Na+/K+ nelle urine e la durata della diarrea. Vengono registrati tutti gli effetti avversi. I pazienti vengono randomizzati a ricevere farmaco o placebo, in entrambi i casi somministrati sotto forma di polvere dello stesso aspetto e gusto, in aggiunta alla soluzione reidratante, somministrata, a seconda della disidratazione, per via orale o in vena. Il racecadotril è somministrato alla dose di 1,5 mg/kg/die in 3 somministrazioni. I dati sono analizzati sia per ITT (Intention To Treat) sia per protocollo (analisi per protocollo: solo i pazienti di cui erano disponibili tutti i dati per l intera durata dello studio). All inizio dello studio, 84 pazienti ricevono il farmaco e 82 il placebo; di questi 121 (58 con il racecadotril e 63 con placebo) completano la raccolta dei dati e costituiscono la popolazione analizzata per protocollo. Per quanto riguarda l outcome primario, l output fecale nelle 48 ore è significativamente più basso nel gruppo dei trattati (P = 0.009) rispetto ai controlli; la differenza stimata del trattamento mostra che l output fecale con racecadotril è del 60% rispetto al placebo (IC 95%: 43-88). La guarigione a 5 giorni non mostra differenze fra trattati e controlli. La durata della diarrea, analizzata utilizzando le curve di Kaplan Meier, in un sottogruppo di pazienti positivi al Rotavirus, mostra una diminuzione nei pazienti trattati. Un rapporto Na+/K+ urinario inferiore a 1 (indice di disidratazione) è presente in un numero significativamente minore di pazienti in trattamento rispetto al placebo. Per quanto riguarda gli effetti avversi, sono segnalate due reazioni ascrivibili al trattamento, di cui uno di vomito con racecadotril e uno di eczema facciale con placebo. Dati simili sono emersi da un RCT pubblicato da Cojocaru nel 2002: in questo caso si comparava la reidratazione per os o ev isolata rispetto a reidratazione per os o ev più racecadotril in 166 bambini con diarrea acuta di età compresa tra 3 mesi e 3 anni. I bambini trattati con racecadotril mostravano una riduzione del numero di evacuazioni rispetto ai non trattati (P < 0.001) e una riduzione del numero di visite ambulatoriali (P < 0.05). Questo studio è però un RCT non in cieco e senza gruppo di controllo. Nel 2007 è stata pubblicata una revisione sistematica sull uso del racecadotril nella gastroenterite acuta (Szajewska et al.), che si basava sui tre trial clinici già menzionati. Tre RCT ottemperano per gli autori ai criteri di inclusione. Si tratta di una popolazione di 471 pazienti: bambini di età compresa tra 3 e 48 mesi. L outcome primario è costituito dalla riduzione dell emissione di feci a 48 ore (output fecale a 48 h), essendo questo il tempo nel quale si ha una maggiore perdita di liquidi e un conseguente maggiore rischio di disidratazione. Vengono inoltre presi in considerazione i dati sulla durata della diarrea e sulla guarigione a 5 giorni. Gli studi analizzano i dati con la differenza tra le medie (MD). Per potere stimare la dimensione dell effetto nell intera popolazione dei tre trial e combinare i risultati degli studi che negli articoli sono espressi in modo non omogeneo, gli autori della metanalisi utilizzano la differenza standardizzata delle medie (pooled SMD). L utilizzo della differenza standardizzata delle medie (Standardized Difference Mean, SMD) è il metodo comunemente utilizzato nelle metanalisi per stimare la dimensione dell effetto nel caso di studi che utilizzano come misura di esito variabili numeriche continue. Questo consente di aggregare i dati di studi in cui lo stesso outcome viene espresso in modo differente e cioè output fecale in g/h nello studio di Cézard e in g/kg in quello di Salazar-Lindo. La pooled SMD per tutti i pazienti arruolati nei trial indica che l output fecale è significativamente minore nei pazienti trattati (-0,67; IC 95%: da - 0,9 a -0,44). La
81 guarigione a 5 giorni calcolata su 307 pazienti in cui questo outcome è stato valutato non ha però dato differenze statisticamente significative fra i trattati e i controlli. Per la durata della diarrea, Szajewska dichiara che tutti gli RCT mostrano dati sulla durata della diarrea, tuttavia gli outcome riportati sono inconsistenti e inoltre un formale pooling dei dati non è possibile. Gli autori di tale lavoro concludevano che: i pochi trial pubblicati sul racecadotril forniscono un supporto all uso del farmaco rispetto al placebo o a nessun intervento per ridurre l output fecale e la durata della diarrea nel bambino con DA. Tuttavia, veniva evidenziata la necessità di ulteriori studi con un maggior numero di pazienti e in setting vari per una definizione del rapporto costo/beneficio e della sicurezza del farmaco prima di poterne consigliare l uso nella gestione routinaria del bambino con gastroenterite. Nel 2008, un altra revisione degli studi su racecadotril pubblicata su Acta Paediatrica (Tormo R, Polanco I et al.) concludeva in modo simile alla precedente, evidenziando il potenziale ruolo emergente del racecadotril nella gestione del bambino con diarrea acuta, ribadendo al contempo la necessità di ulteriori indagini. Uno studio con risultati meno incoraggianti è stato pubblicato sul Journal of Pediatrics nel 2009 (Santos M et al.): si tratta di un RCT in cui si paragona l efficacia del racecadotril associato a reidratazione per os vs reidratazione per os isolata nel trattamento della gastroenterite acuta. Il reclutamento dei pazienti è stato fatto in un pronto soccorso pediatrico di un ospedale di terzo livello. Gli autori hanno arruolato 188 bambini di età compresa tra i 3 e i 36 mesi con gastroenterite acuta e condizioni cliniche sovrapponibili: 94 bambini hanno ricevuto una soluzione reidratante per bocca (ORS), 94 una soluzione reidratante per bocca + racecadotril (ORS+R). A 48 ore gli autori non hanno trovato differenze significative tra i due gruppi nel numero di evacuazioni (4.1 +/- 2.7 nel gruppo ORS vs 3.8 +/- 2.4 nel gruppo ORS+R) e nella durata media della gastroenterite (4.7 +/- 2.2 giorni nel gruppo ORS, 4.0 +/- 2.1 giorni nel gruppo ORS+R; P =.15). Alla luce dei dati presenti in letteratura, si ravvisa un possibile ruolo del racecadotril nella gestione del bambino affetto da gastroenterite acuta. Il farmaco sembra essere efficace nel ridurre la durata e la severità della diarrea. Sono necessari, tuttavia, ulteriori studi per analizzarne il profilo di sicurezza a lungo termine, nonché il rapporto costo/beneficio, prima di poterne consigliare l uso estensivo nel bambino con diarrea acuta (evidenza II A). TANNATO DI GELATINA Una corretta terapia, oltre al ripristino del microbiota, dovrebbe anche prevedere la protezione della barriera gastrointestinale (gut barrier), dove il microbiota intestinale, la barriera mucosale e il sistema immunitario locale sono tra di loro in un interazione dinamica. Il tannato di gelatina rappresenta un importante novità nel panorama dei trattamenti della diarrea acuta. Si tratta di un dispositivo medico costituito dall associazione di gelatina, proteina costituita da una catena di 18 amminoacidi essenziali, e acido tannico, un antiossidante naturale di origine vegetale. L azione del tannato di gelatina si basa su 2 meccanismi fondamentali: 1. da un lato, un azione meccanica che prevede, grazie soprattutto alla gelatina, la formazione di una sorta di pellicola adesiva sulla mucosa intestinale che riduce il passaggio di elettroliti e conferisce protezione dall effetto irritante delle secrezioni intestinali; 2. dall altro, il tannato di gelatina forma un complesso legandosi alle mucoproteine proinfiammatorie, favorendone così la precipitazione e l eliminazione con le feci.
82 Il potere astringente del tannato di gelatina sembra derivare, oltre che dall azione sull infiammazione locale, anche dalla diminuzione della permeabilità cellulare e dalla riduzione delle secrezioni intestinali. È stata, inoltre, dimostrata in vitro la ridotta produzione di 2 molecole coinvolte nel processo infiammatorio: l IL-8 e l IFN-α (Frasca G. 2011). Lo studio condotto da Carretero et al. (2009) ha evidenziato che il tannato di gelatina è in grado di ridurre la frequenza delle scariche, la durata degli episodi diarroici e i sintomi associati alla diarrea in un gruppo di soggetti di età compresa tra 3 mesi e 12 anni. Il tannato di gelatina si è dimostrato sicuro ed efficace, anche nei lattanti, con risultati visibili entro poche ore dall assunzione. È efficace entro 12 ore.
83 PREVENZIONE Le norme igieniche giocano un ruolo fondamentale nel prevenire la trasmissione delle infezioni che causano la diarrea acuta. Il lavaggio delle mani, eseguito in modo corretto con la dovuta accuratezza, è la prima norma raccomandata per ridurre il rischio di trasmissione dell infezione, e deve essere praticato non solo dal paziente, ma da chiunque venga in contatto con il malato e le superfici da lui eventualmente contaminate, in modo particolare dagli operatori sanitari che rischierebbero altrimenti di diventare veicolo di trasmissione dell agente microbico tra un paziente e l altro. L esempio dell infezione da Rotavirus è emblematico in tal senso, se consideriamo che nelle feci dei soggetti affetti è riscontrabile un elevata carica virale ancora prima delle manifestazioni cliniche e che tale carica può persistere fino a 20 giorni dall insorgenza dei sintomi. Il Rotavirus è responsabile di forme severe di gastroenterite nei lattanti e nei bambini di età inferiore ai 5 anni, determinando circa mezzo milione di morti ogni anno al mondo (Meloni 2012). L impatto della patologia sulle famiglie e sulla società, in termini sia di spesa sanitaria sia di mancata produttività, è estremamente elevato, e l incidenza della gastroenterite da Rotavirus appare simile nei paesi industrializzati e nei paesi in via di sviluppo. Si ritiene che tutti i bambini vengano infettati dal Rotavirus entro i primi 5 anni di vita, con maggior tasso di incidenza tra i 6 e i 24 mesi di età. Clinicamente, l infezione può essere asintomatica oppure presentare un decorso variabile tra la forma subclinica, più comune nei bambini più grandi e negli adulti, e la gastroenterite acuta con febbre, vomito e diarrea acquosa che persiste per 3-8 giorni. Le forme severe con diarrea profusa accompagnata da vomito e febbre possono determinare grave disidratazione, che può risultare fatale se non adeguatamente e rapidamente corretta, soprattutto nei paesi in via di sviluppo. Le misure igienico-sanitarie, come l accurato lavaggio delle mani, sono utili per limitare la diffusione dell infezione, ma non possono completamente eliminare il rischio di infezione. Al momento attuale, la vaccinazione rappresenta l unica arma efficace nel ridurre il peso di questa patologia. L elevata frequenza e le importanti conseguenze delle infezioni da Rotavirus, specie nei paesi in via di sviluppo, hanno rappresentato un importante impulso per lo sviluppo di vaccini preventivi. Altre ragioni che hanno favorito gli studi per lo sviluppo di vaccini per queste infezioni sono l assenza di una terapia causale e l osservazione che le norme igieniche standard non sono efficaci nella prevenzione dell infezione come in altre gastroenteriti di origine batterica.
84 BIBLIOGRAFIA Guandalini S, Kahn S. Acute Diarrhea. In Walker Textbook of Pediatric GI, Guarino A, Albano F. La gastroenterite: fisiopatologia e correlati clinici diagnostici. Area Pediatrica, n. 2, anno 7, febbraio Giovannini M, Ghisleni D, Cavalleri V, Farina F. Diarrea acuta: i rimedi a disposizione del pediatra. Doctor Pediatria, 2012; 4: Guarino A, Albano F, Ashkenazi S, Gendrel D, Hoekstra JH, Shamir R, Szajewska H. European Society for Paediatric Gastroenterology, Hepatology, and Nutrition/European Society for Paediatric Infectious Diseases Evidence-based Guidelines for the Management of Acute Gastroenteritis in Children in Europe. Journal of Pediatric Gastroenterology and Nutrition, 2008; 46: S Weinberg RJ, Tipton G, Klish WJ et al. Effect of Breast-Feeding on Morbidity in Rotavirus Gastroenteritis. Pediatrics, 1984; 74: Bartolozzi G. Linee Guida per la prevenzione della malattia da rotavirus. Un aggiornamento in confronto al Centenari C, Maggiore G, Gurgel RQ, Cuevas LE. Vaccinazione anti-rotavirus: intervento lodevole ma fa risparmiare il Sistema Sanitario Nazionale? L esperienza del Brasile. Fontana M. Vaccini anti-rotavirus. Quale? quando? perché? per chi? Medico e Bambino, 3/2007: Ruiz-Palacios GM, Pérez-Schael I, Velázquez FR et al. Safety and Efficacy of an Attenuated Vaccine against Severe Rotavirus Gastroenteritis. N Engl J Med, 2006; 354: Vesikari T, Matson DO, Dennehy P et al. Safety and Efficacy of a Pentavalent Human- Bovine (WC3) Reassortant Rotavirus Vaccine. N Engl J Med, 2006; 354: Quigley MA, Kelly YJ, Sacker A. Breastfeeding and Hospitalization for Diarrheal and Respiratory Infection in the United Kingdom Millennium Cohort Study. Pediatrics, 2007; 119(4): e King CK et al. Managing Acute Gastroenteritis Among Children: Oral Rehydration, Maintenance, and Nutritional Therapy. MMWR Recommendations and Reports, 2003; 52: The Treatment of diarrhoea - A manual for physicians and other senior health workers. Geneva, Switzerland: World Health Organization; Fourth revision.
85 Steiner MJ, DeWalt DA, Byerley JS. Is This Child Dehydrated? JAMA, 2004; 291(22): Fortin J, Parent MA. Dehydration scoring system for infants. J Trop Pediatr Environ Child Health, 1978; 24: Ruuska T, Vesikari T. Rotavirus Disease in Finnish Children: Use of Numerical scores for Clinical Severity of Diarrhoeal Episodes. Scand J Infect Dis, 1990; 22: Diarrhoea and vomiting caused by gastroenteritis: diagnosis, assessment and management in children younger than 5 years. Clinical guideline by the National Collaborating Centre for Women s and Children s Health, commissioned by the National Institute for Health and Clinical Excellence. April American Academy of Pediatrics. Practice Parameter: The Management of Acute Gastroenteritis in Young Children. Provisional Committee on Quality Improvement, Subcommittee on Acute Gastroenteritis. Pediatrics, 1996; 97: Hartling L, Bellemare S, Wiebe N et al. Oral versus intravenous rehydration for treating dehydration due to gastroenteritis in children. Cochrane Database Syst Rev, 2006; 19; 3: CD Massaro M, Germani C, Calligaris L, Schreiber S, Bortoluzzi R, Ronfani L, Barbi E, Marchetti F. La gestione del bambino con gastroenterite acuta. Più efficacia con minor invasività. Medico e Bambino, 9/2012: Brown KH, Peerson JM, Fontaine O. Use of Nonhuman Milks in the Dietary Management of Young Children With Acute Diarrhea: A Meta-Analysis of clinical trials. Pediatrics, 1994; 93: Gregorio GV, Dans LF, Silvestre MA. Early versus Delayed Refeeding for Children with Acute Diarrhoea. Cochrane Database Syst Rev, 2011; (6): CD Patro B, Golicki D, Szajewska H. Meta-analysis: zinc supplementation for acute gastroenteritis in children. Alimentary Pharmacology & Therapeutics, 2008; 28(6): Lazzerini M, Ronfani L. Oral zinc for treating diarrhoea in children. Cochrane Database Syst Rev, 2008; (3): CD Scrimgeour AG, Lukaski HC. Zinc and diarrheal disease: current status and future perspectives. Curr Opin Clin Nutr Metab Care, 2008; 11(6): Dupont C, Vernisse B. Anti-Diarrheal Effects of Diosmectite in the Treatment of Acute Diarrhea in Children: A Review. Pediatr Drugs, 2009; 11(2): Berni Canani R. Il ruolo dei probiotici nella diarrea acuta. Area Pediatrica, 2008; 8:
86 Ministero della Salute, Commissione unica per la dietetica e la nutrizione. Indicazioni per l uso negli alimenti e negli integratori alimentari di microrganismi probiotici (batteri e/o lieviti), tradizionalmente utilizzati per l equilibrio della flora intestinale. Revisione Thomas D, Greer FR et al. Probiotics and Prebiotics in Pediatrics. Pediatrics, 2010; 126: Guandalini S. Probiotics for Prevention and Treatment of Diarrhea. J Clin Gastroenterol, 2011; 45: S Allen SJ, Martinez EG, Gregorio GV et al. Probiotics for treating acute infectious diarrhoea. Cochrane Database Syst Rev, 2010; (11): CD Turck D, Berard H et al. Comparison of racecadotril and loperamide in children with acute diarrhoea. Aliment Pharmacol Ther, 1999; 13(6): Salazar-Lindo E, Santisteban-Ponce et al. Racecadotril in the Treatment of Acute Watery Diarrhea in Children. N Engl J Med, 2000; 343(7): Tormo R, Polanco I et al. Acute infectious diarrhoea in children: new insights in antisecretory treatment with racecadotril. Acta Paediatr, 2008; 97(8): Santos M et al. Use of Racecadotril as Outpatient Treatment for Acute Gastroenteritis: A Prospective, Randomized, Parallel Study. J Pediatr, 2009; 155(1): Ciambra R, Simeone G et al. Racecadotril e diarrea: un farmaco nuovo, efficace e utile? Quaderni acp, 2008; 15(4): Frasca G et al. Gelatine tannate reduces the proinflammatory effects of lipopolysaccharide in human intestinal cells. Presented at 5 th International Conference on Polyphenols and Health Sitges, Spain, October 17-20, Carretero JB et al. A comparative analysis of response to ORS vs ORS + gelatin tannate in two cohorts of pediatric patients with acute diarrhea. Revista Española de Enfermedades Digestivas, 2009: 101(1): Linea Guida Clinica sulla gestione della gastroenterite acuta (nel bambino di età superiore ad 1 mese). Ospedale Pediatrico Bambino Gesù.
DIARREA ACUTA: PERDITA DI ACQUA CON LE FECI, SUPERIORE A 10 ml/kg/die E DI DURATA INFERIORE A 2 SETTIMANE
 DIARREA ACUTA: PERDITA DI ACQUA CON LE FECI, SUPERIORE A 10 ml/kg/die E DI DURATA INFERIORE A 2 SETTIMANE DIARREA CRONICA: DIARREA CHE DURA DA 14 GIORNI O PIU DIARREA PROTRATTA: DIARREA CRONICA ASSOCIATA
DIARREA ACUTA: PERDITA DI ACQUA CON LE FECI, SUPERIORE A 10 ml/kg/die E DI DURATA INFERIORE A 2 SETTIMANE DIARREA CRONICA: DIARREA CHE DURA DA 14 GIORNI O PIU DIARREA PROTRATTA: DIARREA CRONICA ASSOCIATA
DIARREA D ORIGINE INFETTIVA PERCORSI
 DIARREA D ORIGINE INFETTIVA PERCORSI Modalità di attivazione di un percorso Definizione di quale percorso utilizzare Iter diagnostico e microrganismi da considerare Procedure da adottare Valutazione clinicoanamnestica
DIARREA D ORIGINE INFETTIVA PERCORSI Modalità di attivazione di un percorso Definizione di quale percorso utilizzare Iter diagnostico e microrganismi da considerare Procedure da adottare Valutazione clinicoanamnestica
LE MALATTIE ALIMENTARI di origine batterica. ERUCON - ERUditio et CONsultum
 LE MALATTIE ALIMENTARI di origine batterica INTOSSICAZIONI ALIMENTARI consumo di alimenti contenenti tossine prodotte da microrganismi che si sono moltiplicati nell alimento precedentemente al suo consumo
LE MALATTIE ALIMENTARI di origine batterica INTOSSICAZIONI ALIMENTARI consumo di alimenti contenenti tossine prodotte da microrganismi che si sono moltiplicati nell alimento precedentemente al suo consumo
DIARREA - definizione
 DIARREA - definizione Cosa si intende per DIARREA: - E un sintomo - Aumento Acqua e fluidità delle feci - Aumento quantità feci >200 g/dì - Aumento frequenza evacuazioni (>3 v./dì) Distinzione clinica:
DIARREA - definizione Cosa si intende per DIARREA: - E un sintomo - Aumento Acqua e fluidità delle feci - Aumento quantità feci >200 g/dì - Aumento frequenza evacuazioni (>3 v./dì) Distinzione clinica:
Il disturbo primario del morbo celiaco è l intolleranza al glutine, ad una componente proteica, gliadina, presente nel grano, orzo e segale.
 La malattia celiaca è una condizione infiammatoria della mucosa del piccolo intestino che regredisce in seguito all eliminazione dalla dieta di alimenti contenenti glutine. Il disturbo primario del morbo
La malattia celiaca è una condizione infiammatoria della mucosa del piccolo intestino che regredisce in seguito all eliminazione dalla dieta di alimenti contenenti glutine. Il disturbo primario del morbo
Il ruolo del Laboratorio di Microbiologia nella diagnostica delle MTA
 Il ruolo del Laboratorio di Microbiologia nella diagnostica delle MTA Edoardo Carretto Laboratorio di Microbiologia IRCCS Arcispedale Santa Maria Nuova, Reggio Emilia Malattie trasmesse da alimenti: strategie
Il ruolo del Laboratorio di Microbiologia nella diagnostica delle MTA Edoardo Carretto Laboratorio di Microbiologia IRCCS Arcispedale Santa Maria Nuova, Reggio Emilia Malattie trasmesse da alimenti: strategie
La microflora gastro-intestinale
 La microflora gastro-intestinale Stomaco e Duodeno (10 1-10 3 CFU/ml) Lactobacilli Helicobacter pylori Digiuno e Ileo (10 4-10 8 CFU/ml) Lactobacilli Enterobacter Bacteroides Bifidobacter Holzapfel et
La microflora gastro-intestinale Stomaco e Duodeno (10 1-10 3 CFU/ml) Lactobacilli Helicobacter pylori Digiuno e Ileo (10 4-10 8 CFU/ml) Lactobacilli Enterobacter Bacteroides Bifidobacter Holzapfel et
UN CASO DI DIARREA INTRATTABILE, MA TRATTABILE. Dott.ssa Enrica Strati PLS, Frosinone
 UN CASO DI DIARREA INTRATTABILE, MA TRATTABILE Dott.ssa Enrica Strati PLS, Frosinone Andrea, 2 mesi. Nato a termine, normali fenomeni neonatali. Peso nascita: kg 3,750 Storia familiare negativa per atopia
UN CASO DI DIARREA INTRATTABILE, MA TRATTABILE Dott.ssa Enrica Strati PLS, Frosinone Andrea, 2 mesi. Nato a termine, normali fenomeni neonatali. Peso nascita: kg 3,750 Storia familiare negativa per atopia
STIPSI. Epidemiologia: 2,5 milioni di visite annuali negli USA
 STIPSI La stipsi o stitichezza ( constipation ) non è una malattia, ma un sintomo di svariate alterazioni organiche o funzionali dell intestino o, talvolta, di malattie extraintestinali. Definizione:
STIPSI La stipsi o stitichezza ( constipation ) non è una malattia, ma un sintomo di svariate alterazioni organiche o funzionali dell intestino o, talvolta, di malattie extraintestinali. Definizione:
Genere Yersinia. dolore addominale oro-fecale gastroenterite. Y.pseudotuberculosis PATOLOGIA TRASMISSIONE
 Genere Yersinia i SPECIE PATOLOGIA TRASMISSIONE Y.pestis Peste zoonotica Y.enterocolitica Y.pseudotuberculosis adeno-mesenterite dolore addominale oro-fecale gastroenterite febbre Genere Yersinia Contaminazione
Genere Yersinia i SPECIE PATOLOGIA TRASMISSIONE Y.pestis Peste zoonotica Y.enterocolitica Y.pseudotuberculosis adeno-mesenterite dolore addominale oro-fecale gastroenterite febbre Genere Yersinia Contaminazione
VITAMINA D E DENSITÀ MINERALE OSSEA IN PAZIENTI PEDIATRICI CON MALATTIA INFIAMMATORIA CRONICA INTESTINALE (MICI)
 Università degli studi di Parma Dipartimento Materno-Infantile U.O.C di Gastroenterologia ed Endoscopia Digestiva Scuola di Specializzazione in Gastroenterologia ed Endoscopia digestiva Direttore: Prof
Università degli studi di Parma Dipartimento Materno-Infantile U.O.C di Gastroenterologia ed Endoscopia Digestiva Scuola di Specializzazione in Gastroenterologia ed Endoscopia digestiva Direttore: Prof
Eziologia e fisiopatologia della diarrea acuta
 Eziologia e fisiopatologia della diarrea acuta Enrico Valletta Clinica Pediatrica Università di Verona Cos è la diarrea? Non cominciamo con le domande sceme Franco Panizon Professore Emerito, Dipartimento
Eziologia e fisiopatologia della diarrea acuta Enrico Valletta Clinica Pediatrica Università di Verona Cos è la diarrea? Non cominciamo con le domande sceme Franco Panizon Professore Emerito, Dipartimento
Bordetellosi. Prof. Alessandro FIORETTI Facoltà di Medicina Veterinaria Università di Napoli Federico II
 Prof. Alessandro FIORETTI Facoltà di Medicina Veterinaria Università di Napoli Federico II Patologia infettiva altamente contagiosa che colpisce prevalentemente il tacchino EZIOLOGIA Inizialmente identificato
Prof. Alessandro FIORETTI Facoltà di Medicina Veterinaria Università di Napoli Federico II Patologia infettiva altamente contagiosa che colpisce prevalentemente il tacchino EZIOLOGIA Inizialmente identificato
Sindromi da malassorbimento
 Sindromi da malassorbimento Definizione Patologia causata da diversi fattori che riducono l assorbimento di grassi, carboidrati, proteine, lipidi Malassorbimenti primitivi : - difetto di assorbimento dovuto
Sindromi da malassorbimento Definizione Patologia causata da diversi fattori che riducono l assorbimento di grassi, carboidrati, proteine, lipidi Malassorbimenti primitivi : - difetto di assorbimento dovuto
Acqua: nutriente essenziale
 Acqua: nutriente essenziale Funzioni dell acqua 1. Solvente delle reazioni metaboliche; 2. Regola il volume cellulare; 3. Regola la temperatura corporea; 4. Permette il trasporto dei nutrienti; 5. Permette
Acqua: nutriente essenziale Funzioni dell acqua 1. Solvente delle reazioni metaboliche; 2. Regola il volume cellulare; 3. Regola la temperatura corporea; 4. Permette il trasporto dei nutrienti; 5. Permette
Le intossicazioni alimentari
 Le intossicazioni alimentari Porte Aperte 22 novembre 2014 DI COSA PARLIAMO OGGI EFSA Intossicazioni & tossinfezioni alimentari Esempi Prevenzione 2 AMBITI DI COMPETENZA DELL EFSA Salute delle piante Protezione
Le intossicazioni alimentari Porte Aperte 22 novembre 2014 DI COSA PARLIAMO OGGI EFSA Intossicazioni & tossinfezioni alimentari Esempi Prevenzione 2 AMBITI DI COMPETENZA DELL EFSA Salute delle piante Protezione
Il controllo microbiologico sugli alimenti di origine animale in Emilia Romagna. Anno 2003
 Il controllo microbiologico sugli alimenti di origine animale in Emilia Romagna. Anno 2003 Nelle tabelle seguenti sono riassunti gli esiti delle analisi effettuate sui campioni di alimenti di origine animale
Il controllo microbiologico sugli alimenti di origine animale in Emilia Romagna. Anno 2003 Nelle tabelle seguenti sono riassunti gli esiti delle analisi effettuate sui campioni di alimenti di origine animale
Listeria monocytogenes
 Listeria monocytogenes Coccobacilli Gram+ Asporigeno Aerobio, Anaerobio facoltativo Comprende 6 specie, di cui solo 2 sono patogene per l uomo la monocytogenes e la L.ivanovi. Diametro di 0,4-0,5-2 micron
Listeria monocytogenes Coccobacilli Gram+ Asporigeno Aerobio, Anaerobio facoltativo Comprende 6 specie, di cui solo 2 sono patogene per l uomo la monocytogenes e la L.ivanovi. Diametro di 0,4-0,5-2 micron
Informativa in base all art. 43, comma 1, Nr. 1 della Legge sulla protezione dalle infezioni (Abbr. ted. IfSG)
 Timbro dell Ufficio sanitario Informativa in base all art. 43, comma 1, Nr. 1 della Legge sulla protezione dalle infezioni (Abbr. ted. IfSG) Informazioni sanitarie per la manipolazione degli alimenti Le
Timbro dell Ufficio sanitario Informativa in base all art. 43, comma 1, Nr. 1 della Legge sulla protezione dalle infezioni (Abbr. ted. IfSG) Informazioni sanitarie per la manipolazione degli alimenti Le
SORVEGLIANZA E CONTROLLO DELLE MALATTIE INFETTIVE NELL ASL DI BRESCIA. - anno 2010 -
 SORVEGLIANZA E CONTROLLO DELLE MALATTIE INFETTIVE NELL ASL DI BRESCIA - anno 2010 - Malattie infettive nell ASL di Brescia anno 2010- Pag. 1 MALATTIE INFETTIVE NELL ASL DI BRESCIA - ANNO 2009 - L attività
SORVEGLIANZA E CONTROLLO DELLE MALATTIE INFETTIVE NELL ASL DI BRESCIA - anno 2010 - Malattie infettive nell ASL di Brescia anno 2010- Pag. 1 MALATTIE INFETTIVE NELL ASL DI BRESCIA - ANNO 2009 - L attività
La regolazione di una via metabolica può riguardare:
 A- E1 B- E2 C- E3 D- En Z La regolazione di una via metabolica può riguardare: - attività enzimatica modulazione allosterica o covalente (msec o sec) - livelli dell enzima alterazione del bilancio tra
A- E1 B- E2 C- E3 D- En Z La regolazione di una via metabolica può riguardare: - attività enzimatica modulazione allosterica o covalente (msec o sec) - livelli dell enzima alterazione del bilancio tra
Le infezioni delle vie gastrointestinali. Dott.ssa Saveria Dodaro
 Le infezioni delle vie gastrointestinali Dott.ssa Saveria Dodaro Cosenza 27.05.2013 Sistema Digestivo Tratto Gastro Enterico: Bocca Faringe Esofago Stomaco Piccolo intestino (Tenue) Grande intestino (Crasso)
Le infezioni delle vie gastrointestinali Dott.ssa Saveria Dodaro Cosenza 27.05.2013 Sistema Digestivo Tratto Gastro Enterico: Bocca Faringe Esofago Stomaco Piccolo intestino (Tenue) Grande intestino (Crasso)
Epidemiologia e sorveglianza delle gastroenteriti ed episodi di MTA. Luca Busani
 Epidemiologia e sorveglianza delle gastroenteriti ed episodi di MTA Luca Busani Gestione per il contenimento ed il controllo delle malattie trasmesse da alimenti Torino, 9-10 aprile 2013 Scopi dell Epidemiologia
Epidemiologia e sorveglianza delle gastroenteriti ed episodi di MTA Luca Busani Gestione per il contenimento ed il controllo delle malattie trasmesse da alimenti Torino, 9-10 aprile 2013 Scopi dell Epidemiologia
Gastroenterite & Enterocolite. www.slidetube.it. www.slidetube.it
 Gastroenterite & Enterocolite Gastroenterite: DEFINIZIONE Enterocolite: Infiammazione dello stomaco e dell intestino che si manifesta prevalentemente con sintomi del tratto gastrointestinale superiore.
Gastroenterite & Enterocolite Gastroenterite: DEFINIZIONE Enterocolite: Infiammazione dello stomaco e dell intestino che si manifesta prevalentemente con sintomi del tratto gastrointestinale superiore.
Flora batterica intestinale DISBIOSI
 Flora batterica intestinale DISBIOSI Ruolo fisiologico della flora batterica intestinale A livello intestinale, soprattutto nel colon ed in misura minore nella parte più distale del tenue è presente LA
Flora batterica intestinale DISBIOSI Ruolo fisiologico della flora batterica intestinale A livello intestinale, soprattutto nel colon ed in misura minore nella parte più distale del tenue è presente LA
V = vascolari * I = infiammatorie **** T = traumi * A = anomalie congenite ** M = malattie metaboliche *** I = idiopatiche ** N = neoplastiche * D =
 MALATTIE DEL PANCREAS ESOCRINO Prof. Carlo Guglielmini Funzioni del pancreas esocrino Secrezione enzimi digestivi (lipasi, proteasi, amilasi) in forma inattiva (zimogeni) Secrezione di bicarbonati Facilitazione
MALATTIE DEL PANCREAS ESOCRINO Prof. Carlo Guglielmini Funzioni del pancreas esocrino Secrezione enzimi digestivi (lipasi, proteasi, amilasi) in forma inattiva (zimogeni) Secrezione di bicarbonati Facilitazione
Gennaio-maggio 2008( fonte dati Epicentro)
 LE TOSSINFEZIONI ALIMENTARI 1 Epidemiologia Esistono oggi al mondo più di 250 tossinfezioni alimentari che si manifestano con differenti sintomi e sono causate da diversi agenti patogeni. Con il passare
LE TOSSINFEZIONI ALIMENTARI 1 Epidemiologia Esistono oggi al mondo più di 250 tossinfezioni alimentari che si manifestano con differenti sintomi e sono causate da diversi agenti patogeni. Con il passare
REPORT DI STAMPA. Utente: Referti: GUTSCAN. Functional Point Srl Via Paleocapa, Bergamo
 REPORT DI STAMPA Utente: 1100000045 Referti: ESAME MACROSCOPICO CONSISTENZA SEMIFORMATE Indicano un aumento della velocità del transito intestinale dovuto a possibili cause infettivologiche ( virus, batteri,
REPORT DI STAMPA Utente: 1100000045 Referti: ESAME MACROSCOPICO CONSISTENZA SEMIFORMATE Indicano un aumento della velocità del transito intestinale dovuto a possibili cause infettivologiche ( virus, batteri,
Dott.. Giuseppe Di Mauro. (Caserta)
 Problematiche e prospettive dell antibioticoterapia in età pediatrica Dott.. Giuseppe Di Mauro (Caserta) Obiettivo Migliorare la prescrizione di farmaci in termini di efficacia e di efficienza tenendo
Problematiche e prospettive dell antibioticoterapia in età pediatrica Dott.. Giuseppe Di Mauro (Caserta) Obiettivo Migliorare la prescrizione di farmaci in termini di efficacia e di efficienza tenendo
mucosa normale neoplasia
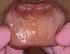 mucosa normale neoplasia emicolectomia destra anastomosi ileo-colica (fra ultima ansa ileale e colon trasverso) emicolectomia destra Polipo del colon, cancerizzato Neoplasia del cieco o del colon ascendente
mucosa normale neoplasia emicolectomia destra anastomosi ileo-colica (fra ultima ansa ileale e colon trasverso) emicolectomia destra Polipo del colon, cancerizzato Neoplasia del cieco o del colon ascendente
Modulo 4. Manifestazioni cliniche e possibili complicanze dell'asma allergico
 Modulo 4 Manifestazioni cliniche e possibili complicanze dell'asma allergico Classificazione di gravità prima dell inizio del trattamento STEP 4 Grave persistente STEP 3 Moderato persistente STEP 2 Lieve
Modulo 4 Manifestazioni cliniche e possibili complicanze dell'asma allergico Classificazione di gravità prima dell inizio del trattamento STEP 4 Grave persistente STEP 3 Moderato persistente STEP 2 Lieve
L igiene degli alimenti ha due scopi:
 IGIENE deglialimenti L igiene degli alimenti ha due scopi: Conservare le caratteristiche intrinseche di un alimento Assicurarne l innocuità Le alterazioni degli alimenti sono dovute allo sviluppo e alla
IGIENE deglialimenti L igiene degli alimenti ha due scopi: Conservare le caratteristiche intrinseche di un alimento Assicurarne l innocuità Le alterazioni degli alimenti sono dovute allo sviluppo e alla
RUOLO DEL MEDICO DI M.G. NELLA GESTIONE DELLE INTOLLERANZE ALIMENTARI. DOTT Pesola
 RUOLO DEL MEDICO DI M.G. NELLA GESTIONE DELLE INTOLLERANZE ALIMENTARI DOTT Pesola Ambito delle cure primarie Ospedale Specialistica Medicina di Famiglia Pazienti sintomatici esordio MALATTIA e MALATTIA
RUOLO DEL MEDICO DI M.G. NELLA GESTIONE DELLE INTOLLERANZE ALIMENTARI DOTT Pesola Ambito delle cure primarie Ospedale Specialistica Medicina di Famiglia Pazienti sintomatici esordio MALATTIA e MALATTIA
FOOD SAFETY : Rischio microbiologico dalla produzione al consumo dell alimento
 Corso di Educazione e Comunicazione ambientale per professionisti dell informazione FOOD SAFETY : Rischio microbiologico dalla produzione al consumo dell alimento Patrizia Romano Scuola di Scienze Agrarie,
Corso di Educazione e Comunicazione ambientale per professionisti dell informazione FOOD SAFETY : Rischio microbiologico dalla produzione al consumo dell alimento Patrizia Romano Scuola di Scienze Agrarie,
TABELLE RIASSUNTIVE DI BATTERIOLOGIA
 TABELLE RIASSUNTIVE DI BATTERIOLOGIA a cura di Paolo Di Francesco, Ersilia Castaldo e Alessandra Ricciardi Studenti del sesto anno del Corso di Laurea in Medicina e Chirurgia, Universita di Roma Tor Vergata
TABELLE RIASSUNTIVE DI BATTERIOLOGIA a cura di Paolo Di Francesco, Ersilia Castaldo e Alessandra Ricciardi Studenti del sesto anno del Corso di Laurea in Medicina e Chirurgia, Universita di Roma Tor Vergata
I rischi in piscina:dalle infezioni all incidente in vasca.
 I rischi in piscina:dalle infezioni all incidente in vasca. Seminari regionali per gestori di piscine 2007 Garda 13/04, Jesolo 03/05, Caorle 10/05, Chioggia 22/06 Giacomo Marchese Azienda Ulss 12 - Servizio
I rischi in piscina:dalle infezioni all incidente in vasca. Seminari regionali per gestori di piscine 2007 Garda 13/04, Jesolo 03/05, Caorle 10/05, Chioggia 22/06 Giacomo Marchese Azienda Ulss 12 - Servizio
Il gastrinoma è un raro tumore neuroendocrino che. insorge abitualmente nel duodeno o nel pancreas, anche se
 1. Aspetti generali Il gastrinoma è un raro tumore neuroendocrino che insorge abitualmente nel duodeno o nel pancreas, anche se è stato ritrovato anche in sedi atipiche come le ghiandole salivari, le ovaie
1. Aspetti generali Il gastrinoma è un raro tumore neuroendocrino che insorge abitualmente nel duodeno o nel pancreas, anche se è stato ritrovato anche in sedi atipiche come le ghiandole salivari, le ovaie
Malattia del Becco e delle Penne degli Psittacidi (PBFD) Dr. Ludovico Dipineto Facoltà di Medicina Veterinaria Università di Napoli Federico II
 Malattia del Becco e delle Penne degli Psittacidi (PBFD) Dr. Ludovico Dipineto Facoltà di Medicina Veterinaria Università di Napoli Federico II PBFD Una delle principali patologie infettive ad eziologia
Malattia del Becco e delle Penne degli Psittacidi (PBFD) Dr. Ludovico Dipineto Facoltà di Medicina Veterinaria Università di Napoli Federico II PBFD Una delle principali patologie infettive ad eziologia
Le Malattie alimentari
 Le Malattie alimentari Valerio Giaccone Dipartimento di Sanità pubblica, Patologia Comparata e Igiene veterinaria - Padova Sono quelle forme morbose che l uomo può contrarre per ingestione o manipolazione
Le Malattie alimentari Valerio Giaccone Dipartimento di Sanità pubblica, Patologia Comparata e Igiene veterinaria - Padova Sono quelle forme morbose che l uomo può contrarre per ingestione o manipolazione
Questa tabella riporta le principali classi di FANS e le rispettive molecole di riferimento.
 1 2 Questa tabella riporta le principali classi di FANS e le rispettive molecole di riferimento. 3 Per quanto la classe dei FANS sia molto ampia e articolata, come si evince da questa tabella, il loro
1 2 Questa tabella riporta le principali classi di FANS e le rispettive molecole di riferimento. 3 Per quanto la classe dei FANS sia molto ampia e articolata, come si evince da questa tabella, il loro
LE TOSSINFEZIONI ALIMENTARI
 LE TOSSINFEZIONI ALIMENTARI 1 OMS : 10 punti alla base della prevenzione delle malattie trasmesse dagli alimenti: 1. Scegliere i prodotti che abbiano subito trattamenti idonei ad assicurarne l innocuità
LE TOSSINFEZIONI ALIMENTARI 1 OMS : 10 punti alla base della prevenzione delle malattie trasmesse dagli alimenti: 1. Scegliere i prodotti che abbiano subito trattamenti idonei ad assicurarne l innocuità
FENILCHETONURIA. Adattarsi ad una nuova realtà
 FENILCHETONURIA Adattarsi ad una nuova realtà 9 Che cosa è la fenilchetonuria? Per capire la fenilchetonuria bisogna partire dal concetto che tutti gli alimenti, in quantità variabile, contengono una sostanza
FENILCHETONURIA Adattarsi ad una nuova realtà 9 Che cosa è la fenilchetonuria? Per capire la fenilchetonuria bisogna partire dal concetto che tutti gli alimenti, in quantità variabile, contengono una sostanza
I principali mediatori chimici dell infiammazione
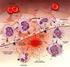 I principali mediatori chimici dell infiammazione Mediatori plasmatici Danno endoteliale! Il Fattore di Hageman ha un ruolo centrale nell attivazione dei mediatori plasmatici Mediatori plasmatici: IL SISTEMA
I principali mediatori chimici dell infiammazione Mediatori plasmatici Danno endoteliale! Il Fattore di Hageman ha un ruolo centrale nell attivazione dei mediatori plasmatici Mediatori plasmatici: IL SISTEMA
. L infezione può causare diarrea e vomito.
 La gastroenterite virale è l infiammazione dello stomaco e dell intestino causata da un viru s L infezione può causare e vomito CAUSE: La gastroenterite virale è la causa principale di grave in adulti
La gastroenterite virale è l infiammazione dello stomaco e dell intestino causata da un viru s L infezione può causare e vomito CAUSE: La gastroenterite virale è la causa principale di grave in adulti
Utilizzo del Synulox intrammamario con diversi tempi di somministrazione
 Utilizzo del Synulox intrammamario con diversi tempi di somministrazione Dr. Antonio Barberio 12 Dicembre 2013 Corte Benedettina- Legnaro in collaborazione con Hanno partecipato al Associazione G. Orus
Utilizzo del Synulox intrammamario con diversi tempi di somministrazione Dr. Antonio Barberio 12 Dicembre 2013 Corte Benedettina- Legnaro in collaborazione con Hanno partecipato al Associazione G. Orus
Diarrea da tossinfezione
 d origine infettiva: percorsi a b comunitaria del Viaggiatore acuta protratta c nosocomiale persistente d in immunocompromesso e da tossinfezione a d origine comunitaria Acuta Protratta Persistente Moderata/
d origine infettiva: percorsi a b comunitaria del Viaggiatore acuta protratta c nosocomiale persistente d in immunocompromesso e da tossinfezione a d origine comunitaria Acuta Protratta Persistente Moderata/
ENTEROBACTER SAKAZAKII (Cronobacter spp)
 ENTEROBACTER SAKAZAKII (Cronobacter spp) CRONOBACTER spp (già Enterobacter sakazakii) Nel 2008 Creazione del nuovo genere Cronobacter spp (prima genere Enterobacter) -bacillo Gram negativo appartenente
ENTEROBACTER SAKAZAKII (Cronobacter spp) CRONOBACTER spp (già Enterobacter sakazakii) Nel 2008 Creazione del nuovo genere Cronobacter spp (prima genere Enterobacter) -bacillo Gram negativo appartenente
Basso numero di pazienti affetti da MICI in carico a
 PREMESSA Basso numero di pazienti affetti da MICI in carico a ciascun MMG MA Le MICI sono patologie croniche recidivanti che colpiscono soggetti socialmente attivi con comorbidità e complicanze per cui
PREMESSA Basso numero di pazienti affetti da MICI in carico a ciascun MMG MA Le MICI sono patologie croniche recidivanti che colpiscono soggetti socialmente attivi con comorbidità e complicanze per cui
1. L INSUFFICIENZA RENALE CRONICA (IRC)
 1. L INSUFFICIENZA RENALE CRONICA (IRC) L insufficienza renale cronica (IRC) è caratterizzata dalla perdita progressiva ed irreversibile della funzione renale in conseguenza della riduzione di tessuto
1. L INSUFFICIENZA RENALE CRONICA (IRC) L insufficienza renale cronica (IRC) è caratterizzata dalla perdita progressiva ed irreversibile della funzione renale in conseguenza della riduzione di tessuto
Ispezione degli alimenti di origine animale
 Ispezione degli alimenti di origine animale Leonardo Alberghini DIPARTIMENTO DI SANITA PUBBLICA, PATOLOGIA COMPARATA E IGIENE VETERINARIA Facoltà di Medicina Veterinaria, Università degli Studi di Padova
Ispezione degli alimenti di origine animale Leonardo Alberghini DIPARTIMENTO DI SANITA PUBBLICA, PATOLOGIA COMPARATA E IGIENE VETERINARIA Facoltà di Medicina Veterinaria, Università degli Studi di Padova
La BPCO e le comorbilità. Federico Sciarra
 La BPCO e le comorbilità Federico Sciarra La BPCO, essendo una malattia cronica con caratteristiche di infiammazione sistemica, facilmente coesiste con altre patologie sia acute che croniche, che influenzano
La BPCO e le comorbilità Federico Sciarra La BPCO, essendo una malattia cronica con caratteristiche di infiammazione sistemica, facilmente coesiste con altre patologie sia acute che croniche, che influenzano
www.fisiokinesiterapia.biz
 INFEZIONI GASTROINTESTINALI: DIMENSIONI DEL PROBLEMA www.fisiokinesiterapia.biz Gastroenteriti diarroiche: seconda causa di morte su scala mondiale dopo le malattie cardiovascolari. 4.600.000-6.000.000
INFEZIONI GASTROINTESTINALI: DIMENSIONI DEL PROBLEMA www.fisiokinesiterapia.biz Gastroenteriti diarroiche: seconda causa di morte su scala mondiale dopo le malattie cardiovascolari. 4.600.000-6.000.000
Patogeni emergenti nel latte: il ruolo di Salmonella spp. Salmonellosi. Salmonellosi nei bovini
 5 Congresso annuale Mastitis Council Italia LODI 9 febbraio 2007 Patogeni emergenti nel latte: il ruolo di Salmonella spp Dott. Antonio Barberio Istituto Zooprofilattico Sperimentale delle Venezie Sezione
5 Congresso annuale Mastitis Council Italia LODI 9 febbraio 2007 Patogeni emergenti nel latte: il ruolo di Salmonella spp Dott. Antonio Barberio Istituto Zooprofilattico Sperimentale delle Venezie Sezione
regole d oro per la prevenzione della calcolosi renale
 10 regole d oro per la prevenzione della calcolosi renale La calcolosi renale è una patologia frequente, ricorrente e potenzialmente pericolosa se non adeguatamente inquadrata, prevenuta e trattata. Se
10 regole d oro per la prevenzione della calcolosi renale La calcolosi renale è una patologia frequente, ricorrente e potenzialmente pericolosa se non adeguatamente inquadrata, prevenuta e trattata. Se
Congresso SIAIP CAMPANIA
 Congresso SIAIP CAMPANIA PEDIATRIA & INNOVAZIONE Hotel Royal Continental Napoli, 24-25 ottobre 2014 1 SIAIP CAMPANIA TV REGIONALI Intervista al Prof. Michele Miraglia del Giudice del 24 ottobre 2014 ore
Congresso SIAIP CAMPANIA PEDIATRIA & INNOVAZIONE Hotel Royal Continental Napoli, 24-25 ottobre 2014 1 SIAIP CAMPANIA TV REGIONALI Intervista al Prof. Michele Miraglia del Giudice del 24 ottobre 2014 ore
INFORMATI VACCINATI PROTETTI VACCINO VARICELLA
 VARICELLA SEI SICURO DI USARE MISURE DI PREVENZIONE ADEGUATE PER PROTEGGERTI DALLA VARICELLA? INFORMATI VACCINATI PROTETTI VACCINO VARICELLA RICORDA CHE: La varicella contratta in età adulta può comportare
VARICELLA SEI SICURO DI USARE MISURE DI PREVENZIONE ADEGUATE PER PROTEGGERTI DALLA VARICELLA? INFORMATI VACCINATI PROTETTI VACCINO VARICELLA RICORDA CHE: La varicella contratta in età adulta può comportare
INFORMATI VACCINATI PROTETTI VACCINO EPATITE Β
 EPATITE B SEI SICURO DI USARE MISURE DI PREVENZIONE ADEGUATE PER PROTEGGERTI DALL EPATITE B? INFORMATI VACCINATI PROTETTI VACCINO EPATITE Β RICORDA CHE: L epatite B causa un infiammazione acuta del fegato,
EPATITE B SEI SICURO DI USARE MISURE DI PREVENZIONE ADEGUATE PER PROTEGGERTI DALL EPATITE B? INFORMATI VACCINATI PROTETTI VACCINO EPATITE Β RICORDA CHE: L epatite B causa un infiammazione acuta del fegato,
Deficit di lattosio: Malassorbimento o Intolleranza: Linee Guida
 Deficit di lattosio: Malassorbimento o Intolleranza: Linee Guida Latte Con la sola denominazione latte si deve indicare esclusivamente il latte di vacca. Il latte di altri animali deve essere indicato
Deficit di lattosio: Malassorbimento o Intolleranza: Linee Guida Latte Con la sola denominazione latte si deve indicare esclusivamente il latte di vacca. Il latte di altri animali deve essere indicato
La valutazione del rischio: zoonosi. Dr. Alessandro Broglia Unità Pericoli biologici (BIOHAZ)
 La valutazione del rischio: zoonosi Dr. Alessandro Broglia Unità Pericoli biologici (BIOHAZ) Workshop sulla Sicurezza degli Alimenti Parma, 5 maggio 2011 1 Zoonosi di origine alimentare Malattie causate
La valutazione del rischio: zoonosi Dr. Alessandro Broglia Unità Pericoli biologici (BIOHAZ) Workshop sulla Sicurezza degli Alimenti Parma, 5 maggio 2011 1 Zoonosi di origine alimentare Malattie causate
CONOSCERE LA CELIACHIA
 CONOSCERE LA CELIACHIA CORSO DI FORMAZIONE PER DIRIGENTI SCOLASTICI, DOCENTI, ATA, REFERENTI DEI COMUNI E DITTE DI RISTORAZIONE E ALTRO PERSONALE COINVOLTO NELLA DISTRIBUZIONE DEI PASTI Dr. Armando Franceschelli
CONOSCERE LA CELIACHIA CORSO DI FORMAZIONE PER DIRIGENTI SCOLASTICI, DOCENTI, ATA, REFERENTI DEI COMUNI E DITTE DI RISTORAZIONE E ALTRO PERSONALE COINVOLTO NELLA DISTRIBUZIONE DEI PASTI Dr. Armando Franceschelli
CONOSCERE LA CELIACHIA
 CONOSCERE LA CELIACHIA CORSO DI FORMAZIONE PER DIRIGENTI SCOLASTICI, DOCENTI, ATA, REFERENTI DEI COMUNI E DITTE DI RISTORAZIONE E ALTRO PERSONALE COINVOLTO NELLA DISTRIBUZIONE DEI PASTI Dr. Monica Selmi
CONOSCERE LA CELIACHIA CORSO DI FORMAZIONE PER DIRIGENTI SCOLASTICI, DOCENTI, ATA, REFERENTI DEI COMUNI E DITTE DI RISTORAZIONE E ALTRO PERSONALE COINVOLTO NELLA DISTRIBUZIONE DEI PASTI Dr. Monica Selmi
l'influenza e la vaccinazione antinfluenzale
 1 / 6 L'influenza e la vaccinazione antinfluenzale poche cose utili (...e risapute) da ricordare! L Influenza è una malattia molto contagiosa causata da virus che si trasmettono da persona a persona prevalentemente
1 / 6 L'influenza e la vaccinazione antinfluenzale poche cose utili (...e risapute) da ricordare! L Influenza è una malattia molto contagiosa causata da virus che si trasmettono da persona a persona prevalentemente
IPERTRIGLICERIDEMIA E PANCREATITE ACUTA
 SCUOLA REGIONALE DI FORMAZIONE SPECIFICA IN MEDICINA GENERALE, CORSO 2010/2013. PATOLOGIA DEL PANCREAS IPERTRIGLICERIDEMIA E PANCREATITE ACUTA Elisabetta Ascari Fabio Bassi Medicina III Gastroenterologia
SCUOLA REGIONALE DI FORMAZIONE SPECIFICA IN MEDICINA GENERALE, CORSO 2010/2013. PATOLOGIA DEL PANCREAS IPERTRIGLICERIDEMIA E PANCREATITE ACUTA Elisabetta Ascari Fabio Bassi Medicina III Gastroenterologia
La gestione clinica di un eventuale caso in Italia. Nicola Petrosillo INMI
 La gestione clinica di un eventuale caso in Italia Nicola Petrosillo INMI La gestione clinica di un eventuale caso in Italia Nicola Petrosillo INMI L. Spallanzani, Roma La malattia da virus Ebola (MVE)
La gestione clinica di un eventuale caso in Italia Nicola Petrosillo INMI La gestione clinica di un eventuale caso in Italia Nicola Petrosillo INMI L. Spallanzani, Roma La malattia da virus Ebola (MVE)
individuazione della causa di una patologia Diagnostica di laboratorio
 DIAGNOSI (διαγνωσισ = distinguere) individuazione della causa di una patologia Diagnosi su base clinica e/o anatomo-patologica sospetto o orientamento diagnostico Diagnosi di laboratorio (diagnosi eziologica)
DIAGNOSI (διαγνωσισ = distinguere) individuazione della causa di una patologia Diagnosi su base clinica e/o anatomo-patologica sospetto o orientamento diagnostico Diagnosi di laboratorio (diagnosi eziologica)
BACILLI GRAM NEGATIVI
 BACILLI GRAM NEGATIVI BACILLI GRAM NEGATIVI Fermentanti il glucosio Enterobacteriaceae NON fermentanti il glucosio (GNNF) Enterobatceriaceae " Bastoncini Gram negativi " Asporigeni " Aerobi-anaerobi facoltativi
BACILLI GRAM NEGATIVI BACILLI GRAM NEGATIVI Fermentanti il glucosio Enterobacteriaceae NON fermentanti il glucosio (GNNF) Enterobatceriaceae " Bastoncini Gram negativi " Asporigeni " Aerobi-anaerobi facoltativi
Le meningiti batteriche: aspetti microbiologici, immunologici ed epidemiologici Quadri clinici e fattori prognostici in corso di meningite batterica
 Le meningiti batteriche: aspetti microbiologici, immunologici ed epidemiologici Quadri clinici e fattori prognostici in corso di meningite batterica G. Bartolozzi ISS - Roma 4-5 luglio 2005 Agenti delle
Le meningiti batteriche: aspetti microbiologici, immunologici ed epidemiologici Quadri clinici e fattori prognostici in corso di meningite batterica G. Bartolozzi ISS - Roma 4-5 luglio 2005 Agenti delle
FONTE :
 FONTE : http://www.msd-italia.it/altre/manuale/sez01/0040059e.html MALATTIA DI WILSON Tossicosi da rame Il morbo di Wilson è una malattia progressiva e costantemente fatale del metabolismo del rame che
FONTE : http://www.msd-italia.it/altre/manuale/sez01/0040059e.html MALATTIA DI WILSON Tossicosi da rame Il morbo di Wilson è una malattia progressiva e costantemente fatale del metabolismo del rame che
IL CONCETTO DI ZOONOSI CLASSIFICAZIONE DELLE ZOONOSI. Zoonosi dirette. Ciclozoonosi. Metazoonosi. Saprozoonosi
 IL CONCETTO DI ZOONOSI Malattie ed infezioni che si trasmettono naturalmente dagli animali vertebrati all uomo e viceversa (O.M.S.) CLASSIFICAZIONE DELLE ZOONOSI Zoonosi dirette Trasmissione dall animale
IL CONCETTO DI ZOONOSI Malattie ed infezioni che si trasmettono naturalmente dagli animali vertebrati all uomo e viceversa (O.M.S.) CLASSIFICAZIONE DELLE ZOONOSI Zoonosi dirette Trasmissione dall animale
MORBILLO, IN CAMPANIA OLTRE 9 MILA BAMBINI NATI NEL 2012 NON VACCINATI
 MORBILLO, IN CAMPANIA OLTRE 9 MILA BAMBINI NATI NEL 2012 NON VACCINATI Nei primi tre mesi del 2016 sono stati segnalati 61 casi. Allerta dei medici campani: senza vaccinazione si rischia una epidemia simile
MORBILLO, IN CAMPANIA OLTRE 9 MILA BAMBINI NATI NEL 2012 NON VACCINATI Nei primi tre mesi del 2016 sono stati segnalati 61 casi. Allerta dei medici campani: senza vaccinazione si rischia una epidemia simile
Biodiversità e salute. Flavia Caretta
 Biodiversità e salute Flavia Caretta Biodiversità e salute salute degli ecosistemi salute umana Effetti della perdita di biodiversità sulla salute umana Ricerca epidemiologica Rivolta a fattori singoli
Biodiversità e salute Flavia Caretta Biodiversità e salute salute degli ecosistemi salute umana Effetti della perdita di biodiversità sulla salute umana Ricerca epidemiologica Rivolta a fattori singoli
STOMACO.
 STOMACO FONTE : RUGARLI Medicina Interna Lo stomaco è la parte più espansa di tutto il canale alimentare; la sua notevole capacità contenitiva (1000-1500 ml) e le peculiari modalità di svuotamento attribuiscono
STOMACO FONTE : RUGARLI Medicina Interna Lo stomaco è la parte più espansa di tutto il canale alimentare; la sua notevole capacità contenitiva (1000-1500 ml) e le peculiari modalità di svuotamento attribuiscono
APPARATO DIGERENTE. Digestione e assorbimento. A.Megighian Farmacia 2011
 APPARATO DIGERENTE Digestione e assorbimento A.Megighian Farmacia 2011 Composizione della dieta Contenuto energetico minimo per sopravvivere (metabolismo basale copertura consumo legato alla attivita 1700
APPARATO DIGERENTE Digestione e assorbimento A.Megighian Farmacia 2011 Composizione della dieta Contenuto energetico minimo per sopravvivere (metabolismo basale copertura consumo legato alla attivita 1700
TRASDUZIONE DEL SEGNALE CELLULARE
 TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
TRASDUZIONE DEL SEGNALE CELLULARE RECETTORI I recettori ormonali sono proteine (spesso glicoproteine) capaci di riconoscere e legare l ormone L interazione tra ormone e recettore è estremamente specifica
Sorveglianza di Laboratorio delle Tossinfezioni Alimentari con particolare attenzione a Escherichia coli O157
 Università degli Studi di Siena Facoltà di Scienza Matematiche Fisiche e Naturali Corso di Laurea Specialistica in Biologia Sanitaria Sorveglianza di Laboratorio delle Tossinfezioni Alimentari con particolare
Università degli Studi di Siena Facoltà di Scienza Matematiche Fisiche e Naturali Corso di Laurea Specialistica in Biologia Sanitaria Sorveglianza di Laboratorio delle Tossinfezioni Alimentari con particolare
RAZIONALE PER L IMPIEGO DELLA N.A. :INDICAZIONI E CRITERI DI SCELTA
 RAZIONALE PER L IMPIEGO DELLA N.A. :INDICAZIONI E CRITERI DI SCELTA SERVIZIO ANESTESIA RIANIMAZIONE MEDICINA IPERBARICA P.O. MARINO Dr. Paolo Castaldi NUTRIZIONE ARTIFICIALE procedura terapeutica per nutrire
RAZIONALE PER L IMPIEGO DELLA N.A. :INDICAZIONI E CRITERI DI SCELTA SERVIZIO ANESTESIA RIANIMAZIONE MEDICINA IPERBARICA P.O. MARINO Dr. Paolo Castaldi NUTRIZIONE ARTIFICIALE procedura terapeutica per nutrire
LPS. Enterobatteri. (antigene O) specifico
 Enterobatteri Habitat intestinale (uomo ed animali) Batteri gram negativi Asporigeni Mobili/immobili Provvisti di pili Aerobi/anaerobi facoltativi Ciclo di KREBS/ via fermentativa (mancano del citocromo
Enterobatteri Habitat intestinale (uomo ed animali) Batteri gram negativi Asporigeni Mobili/immobili Provvisti di pili Aerobi/anaerobi facoltativi Ciclo di KREBS/ via fermentativa (mancano del citocromo
Definizione ed obiettivi dell Igiene. Concetto di salute e malattia. Epidemiologia delle malattie infettive
 Obiettivi dell igiene CONTENUTI CORSO DI Definizione ed obiettivi dell Igiene. Concetto di salute e malattia Epidemiologia delle malattie infettive IGIENE Catena di contagio, sorgenti e serbatoi di infezione,
Obiettivi dell igiene CONTENUTI CORSO DI Definizione ed obiettivi dell Igiene. Concetto di salute e malattia Epidemiologia delle malattie infettive IGIENE Catena di contagio, sorgenti e serbatoi di infezione,
LO STREPTOCOCCO AGALACTIAE IN
 LO STREPTOCOCCO AGALACTIAE IN GRAVIDANZA: FATTORI DI RISCHIO E RESISTENZE AGLI ANTIBIOTICI. Chiara Matani Alice Matteini Marco Tanini Corrado Catalani I STUDIO Studio di prevalenza della resistenza di
LO STREPTOCOCCO AGALACTIAE IN GRAVIDANZA: FATTORI DI RISCHIO E RESISTENZE AGLI ANTIBIOTICI. Chiara Matani Alice Matteini Marco Tanini Corrado Catalani I STUDIO Studio di prevalenza della resistenza di
Dimensioni del tratto gastro-intestinale del suino adulto: Stomaco ph 2,0 capacità 7,5 litri. Intestino tenue lunghezza 18 metri capacità 9 litri
 Dimensioni del tratto gastro-intestinale del suino adulto: Stomaco ph 2,0 capacità 7,5 litri Intestino tenue lunghezza 18 metri capacità 9 litri Intestino crasso lunghezza 5 metri capacità 9 litri Regione
Dimensioni del tratto gastro-intestinale del suino adulto: Stomaco ph 2,0 capacità 7,5 litri Intestino tenue lunghezza 18 metri capacità 9 litri Intestino crasso lunghezza 5 metri capacità 9 litri Regione
I compartimenti liquidi corporei
 Bilancio idrico I compartimenti liquidi corporei E essenziale per l omeostasi mantenere costanti volume ed osmolalità dei liquidi corporei, attraverso il bilancio tra assunzione ed eliminazione di H 2
Bilancio idrico I compartimenti liquidi corporei E essenziale per l omeostasi mantenere costanti volume ed osmolalità dei liquidi corporei, attraverso il bilancio tra assunzione ed eliminazione di H 2
Entameba histolytica. Entameba histolytica
 AMEBIASI Entameba histolytica Protozoo Forma trofozoitica / cistica Trofozoite: 10-60 m, nucleo unico, mobile per pseudopodi, emazie nel citoplasma (forme invasive) Cisti: 9-16 m, fino a 4 nuclei, corpi
AMEBIASI Entameba histolytica Protozoo Forma trofozoitica / cistica Trofozoite: 10-60 m, nucleo unico, mobile per pseudopodi, emazie nel citoplasma (forme invasive) Cisti: 9-16 m, fino a 4 nuclei, corpi
La nuova biologia.blu
 David Sadava, David M. Hillis, H. Craig Heller, May R. Berenbaum La nuova biologia.blu Il corpo umano PLUS 2 Capitolo C6 Il sistema linfatico e l immunità 3 Il sistema linfatico /1 Il sistema linfatico
David Sadava, David M. Hillis, H. Craig Heller, May R. Berenbaum La nuova biologia.blu Il corpo umano PLUS 2 Capitolo C6 Il sistema linfatico e l immunità 3 Il sistema linfatico /1 Il sistema linfatico
Il paziente con problema renale: non solo Insufficienza Renale Cronica ma Malattia Renale Cronica
 Il paziente con problema renale: non solo Insufficienza Renale Cronica ma Malattia Renale Cronica I miei riferimenti per questa relazione: le linee-guida nazionali e internazionali Clinical Practice Guidelines
Il paziente con problema renale: non solo Insufficienza Renale Cronica ma Malattia Renale Cronica I miei riferimenti per questa relazione: le linee-guida nazionali e internazionali Clinical Practice Guidelines
Enterobatteri. Bacilli Gram- Oltre 40 specie e 150 specie. Asporigeni, sia mobili che immobili, anaerobi facoltativi.
 Enterobatteri Bacilli Gram- Oltre 40 specie e 150 specie. Asporigeni, sia mobili che immobili, anaerobi facoltativi. Batteri ubiquitari (acqua, suolo, vegetazione) fanno parte delle normale flora microbica
Enterobatteri Bacilli Gram- Oltre 40 specie e 150 specie. Asporigeni, sia mobili che immobili, anaerobi facoltativi. Batteri ubiquitari (acqua, suolo, vegetazione) fanno parte delle normale flora microbica
I termini e i concetti fondamentali
 unità Le malattie trasmesse da alimenti I termini e i concetti fondamentali lezione 1 Caratteristiche e classificazione delle malattie trasmesse da alimenti Per quanto riguarda gli alimenti e le industrie
unità Le malattie trasmesse da alimenti I termini e i concetti fondamentali lezione 1 Caratteristiche e classificazione delle malattie trasmesse da alimenti Per quanto riguarda gli alimenti e le industrie
Il pediatra di famiglia nell approccio alle infezioni respiratorie nella pratica quotidiana. Massimo Landi Pediatria di gruppo - Torino
 Il pediatra di famiglia nell approccio alle infezioni respiratorie nella pratica quotidiana Massimo Landi Pediatria di gruppo - Torino Rapporto pediatria 2003 Campione Arno Dei 645 principi attivi i primi
Il pediatra di famiglia nell approccio alle infezioni respiratorie nella pratica quotidiana Massimo Landi Pediatria di gruppo - Torino Rapporto pediatria 2003 Campione Arno Dei 645 principi attivi i primi
L intolleranza al lattosio lattasi lattosio zucchero del latte lattasi cellule della mucosa intestinale assorbente galattosio glucosio
 L intolleranza al lattosio si verifica in caso di deficienza dell enzima lattasi, si manifesta cioè quando viene a mancare parzialmente o totalmente l enzima in grado di scindere il lattosio (definita
L intolleranza al lattosio si verifica in caso di deficienza dell enzima lattasi, si manifesta cioè quando viene a mancare parzialmente o totalmente l enzima in grado di scindere il lattosio (definita
La sindrome dell intestino irritabile post-infettiva
 La sindrome dell intestino irritabile post-infettiva Dr.ssa Chiara Ricci Università di Brescia Spedali Civili, Brescia Definizione La sindrome dell intestino irritabile Disordine funzionale dell intestino
La sindrome dell intestino irritabile post-infettiva Dr.ssa Chiara Ricci Università di Brescia Spedali Civili, Brescia Definizione La sindrome dell intestino irritabile Disordine funzionale dell intestino
Training in Trombosi Società Italiana per lo Studio dell Emostasi e della Trombosi. Introduzione. Cremona settembre 2016
 Training in Trombosi Società Italiana per lo Studio dell Emostasi e della Trombosi Cremona 19-23 settembre 2016 Introduzione Anna Falanga Ospedale Papa Giovanni XXIII Bergamo www.siset.org Chi Siamo S
Training in Trombosi Società Italiana per lo Studio dell Emostasi e della Trombosi Cremona 19-23 settembre 2016 Introduzione Anna Falanga Ospedale Papa Giovanni XXIII Bergamo www.siset.org Chi Siamo S
Scelta dei farmaci antimicrobici
 Antibiotici Gram + Gram - Scelta dei farmaci antimicrobici Identita agente infettante Sensibilita ad un dato farmaco Sede dell infezione Fattori legati al paziente Sicurezza della terapia Costo della terapia
Antibiotici Gram + Gram - Scelta dei farmaci antimicrobici Identita agente infettante Sensibilita ad un dato farmaco Sede dell infezione Fattori legati al paziente Sicurezza della terapia Costo della terapia
Dr. Francesco MARUCCI
 1 Malattia infettiva che può aversi nei daini, cervi, in casi eccezionali nei caprioli provocata da micobatteri in particolare Mycobacterium bovis (bovino e ungulati selvatici) ma anche: Mycobacterium
1 Malattia infettiva che può aversi nei daini, cervi, in casi eccezionali nei caprioli provocata da micobatteri in particolare Mycobacterium bovis (bovino e ungulati selvatici) ma anche: Mycobacterium
Criteri di classificazione
 Cosa sono? Entità: non si ritengono organismi viventi infatti sono classificati in un impero diverso rispetto a quello cellulare impero virale Submicroscopiche: non sono visibili al M.O., ma solo a quello
Cosa sono? Entità: non si ritengono organismi viventi infatti sono classificati in un impero diverso rispetto a quello cellulare impero virale Submicroscopiche: non sono visibili al M.O., ma solo a quello
L APPARATO DIGERENTE E COSTITUITO DA UN LUNGO TUBO DI FORMA IRREGOLARE DETTO CANALE DIGERENTE CHE INIZIA CON L APERTURA DELLA BOCCA, PROSEGUE CON LA
 L APPARATO DIGERENTE E COSTITUITO DA UN LUNGO TUBO DI FORMA IRREGOLARE DETTO CANALE DIGERENTE CHE INIZIA CON L APERTURA DELLA BOCCA, PROSEGUE CON LA FARINGE, L ESOFAGO, LO STOMACO, L INTESTINO TENUE, L
L APPARATO DIGERENTE E COSTITUITO DA UN LUNGO TUBO DI FORMA IRREGOLARE DETTO CANALE DIGERENTE CHE INIZIA CON L APERTURA DELLA BOCCA, PROSEGUE CON LA FARINGE, L ESOFAGO, LO STOMACO, L INTESTINO TENUE, L
ELABORARE PROGRAMMA NUTRIZIONALE ENTERALE. Da dove comincio???
 ELABORARE PROGRAMMA NUTRIZIONALE ENTERALE Da dove comincio??? DOVE VOGLIO ANDARE??? Raccomandazioni pratiche L elaborazione di un piano terapeutico con la NA prevede: 1) L identificazione del soggetto
ELABORARE PROGRAMMA NUTRIZIONALE ENTERALE Da dove comincio??? DOVE VOGLIO ANDARE??? Raccomandazioni pratiche L elaborazione di un piano terapeutico con la NA prevede: 1) L identificazione del soggetto
La patologia epato- bilio-pancreatica
 La patologia epato- bilio-pancreatica Complicanze della colelitiasi Colecistite acuta Pancreatite acuta: Migrazione di calcoli e/o cristalli di colesterolo nella via biliare principale Colestasi extraepatica:
La patologia epato- bilio-pancreatica Complicanze della colelitiasi Colecistite acuta Pancreatite acuta: Migrazione di calcoli e/o cristalli di colesterolo nella via biliare principale Colestasi extraepatica:
