ENZIMI. Molecole proteiche globulari che consentono alle reazioni biochimiche di procedere ad una velocità adeguata alle
|
|
|
- Isidoro Giovannini
- 4 anni fa
- Visualizzazioni
Transcript
1 ENZIMI Molecole proteiche globulari che consentono alle reazioni biochimiche di procedere ad una velocità adeguata alle condizioni fisiologiche Aumentano la velocità delle reazioni senza alterarne l equilibrio Sono dotati di elevata specificità
2 Reazione di idratazione dell anidride carbonica CO 2 +H 2 O H 2 CO 3 Anche una reazione semplice come questa viene catalizzata da un enzima specifico: l anidrasi carbonica In assenza di questo enzima il trasferimento di CO 2 dai tessuti al sangue non sarebbe efficiente Una molecola di anidrasi carbonica catalizza reazioni di idratazione al secondo. La reazione catalizzata è 10 milioni di volte più veloce della reazione non catalizzata
3 Tutte le trasformazioni chimiche sono associate ad una variazione di energia. TERMODINAMICA studia i cambiamenti energetici relativi ad una reazione chimica (se e quanto una reazione avviene)
4 LE TRASFORMAZIONI BIOLOGICHE OBBEDISCONO ALLE LEGGI DELLA TERMODINAMICA I Legge della termodinamica (conservazione dell energia) La quantità totale di energia dell Universo (sistema isolato) rimane costante: l energia può essere trasformata in altre forme di energia ma non può essere né creata né distrutta. II Legge della termodinamica Tutti i processi naturali tendono ad un aumento del disordine, ossia ad un aumento dell entropia
5 Le variazioni di energia che accompagnano una reazione chimica sono definite dalle 3 grandezze termodinamiche. Entalpia (H) contenuto di calore di un sistema, riflette il numero e il tipo di legami chimici dei reagenti e dei prodotti Entropia (S) esprime quantitativamente il grado di disordine e la casualità di un sistema Energia libera di Gibbs (G) esprime la quantità di energia in grado di produrre un lavoro
6 Le variazioni di energia libera, di entalpia e di entropia sono tra loro correlate G = H -T S G < 0 reazione esoergonica, rilascia energia libera utilizzabile per compiere un lavoro. Il processo è spontaneo. Si verifica quando H< 0: la reazione rilascia calore (esotermica) S > 0: l entropia aumenta G > 0 reazione endoergonica, richiede energia. Il processo non è spontaneo. Si verifica quando H H > 0: la reazione richiede calore S < 0: l entropia diminuisce
7 Pertanto tutti i processi spontanei (che non richiedono energia) sono caratterizzati ti da un G G < 0 e da un aumento dell entropia ( S > 0)
8
9 Tutte le trasformazioni chimiche sono associate ad una variazione di energia. TERMODINAMICA studia i cambiamenti energetici relativi ad una reazione chimica (se e quanto una reazione avviene) CINETICA studia la velocità e il meccanismo di una reazione chimica i
10 VELOCITÀ DI REAZIONE quantità di reagenti che si trasformano nell unità di tempo Cosa determina la velocità di una reazione?
11 A + B C + D Affinchè A e B reagiscano è necessario 1) che A e B si avvicinino e si urtino 2) che l urto sia efficace, ossia che le molecole abbiano l energia cinetica sufficiente per far avvenire la reazione 3) che l orientamento sia vantaggioso (fattore sterico) E n e r g i a A + B Reagenti Complesso attivato Energia di attivazione Variazione di energia C + D prodotti Coordinata di reazione
12 Data la reazione A+B C+D la sua velocità dipenderà dal contenuto energetico delle molecole reagenti A + B C + D Reagiscono solo le molecole dotate di energia maggiore o uguale all energia richiesta per la formazione del complesso attivato (energia di attivazione E a ) Lo stato di transizione è un momento transitorio relativo alla formazione del complesso attivato
13 ENERGIA DI ATTIVAZIONE (E a ) E caratteristica di ogni reazione chimica A + B Complesso attivato E la quantità di energia necessaria a portare tutte le molecole contenute in una mole di sostanza al massimo della barriera di attivazione i È fornita principalmente dall energia cinetica delle molecole E n e r g i a Energia di attivazione i Reagenti Variazione di energia C+D prodotti Coordinata di reazione
14 Come può essere aumentata la velocità di una reazione?
15 VELOCITÀ DI REAZIONE quantità di reagenti che si trasformano nell unità di tempo La velocità di una reazione chimica aumenta all aumentare aumentare della concentrazione dei reagenti all aumentare della temperatura (aumento della velocità media dei reagenti e del numero degli urti) al diminuire della energia di attivazione
16
17 CATALISI Un catalizzatore è una sostanza che aumenta la velocità di una reazione chimica cambiando il percorso della reazione in un nuovo percorso con una più bassa energia di attivazione Ea non si consuma nel corso della reazione
18 GLI ENZIMI SONO CATALIZZATORI ORGANICI accelerano le reazioni abbassandone l energia di attivazione non sono consumati nella reazione che catalizzano e non vengono modificati in maniera permanente accelerano solo le reazioni che avvengono spontaneamente possono essere inattivati A+B A + B C + D C + D In una reazione reversibile accelerano sia la reazione inversa che quella diretta senza modificarne l equilibrio
19 E + S ES EP E + P G # = G X# -G S
20 CARATTERISTICHE DEGLI ENZIMI Sono molto specifici in quanto catalizzano solo alcuni tipi di reazioni chimiche La loro attività può essere regolata, cioè esaltata o repressa, in molti casi dalle stesse molecole su cui agiscono Ogni enzima ha un sito attivo in cui i substrati Ogni enzima ha un sito attivo in cui i substrati reagenti possono entrare
21 E + S ES EP E + P Le interazioni tra enzima (E) e substrato (S) si verificano in corrispondenza di una regione specifica: il sito catalitico o sito attivo
22 Come fa un enzima ad abbassare l energia di Gli enzimi sono dei catalizzatori proteici attivazione? Rimangono inalterati nel corso della reazione; rendono veloci reazioni termodinamicamente possibili; non alterano l equilibrio chimico della reazione Lo stato di transizione si trova ad un livello energetico superiore a quello del reagente e del prodotto Velocità Vantaggi Regolazione L enzima abbassa l energia libera dello stato di transizione Canalizzazione CH 2 OH O CH 2 OH O O Reazione non catalizzata libera, G G (A B) G (A B) G (B A) Energia G A Reazione catalizzata G (B A) k A B k11 K k k 1 k -1 G B Coordinata di reazione
23 Nel sito catalitico si verificano diversi tipi di reazioni chimiche tra substrato e i gruppi funzionali specifici dell enzima (catene laterali di alcuni amminoacidi) Alcuni enzimi per svolgere la loro attività funzionale hanno bisogno di componenti chimici addizionali: i cofattori Un cofattore può essere e costituito tu to da: ioni inorganici come Fe 2+, Mn 2+, Zn 2+ molecole organiche complesse, i coenzimi
24 Affinità di legame tra enzima e substrato h= residui idrofobici (interazioni idrofobiche) legami idrogeno Interazioni elettrostatiche (ponti salini) Forze non covalenti sono responsabili della complementarietà geometrica ti e fisica i tra enzima e substrato
25 Stereospecificità
26 Orientamento del substrato e specificità ità Il sito attivo rappresenta In genere meno del 5% della superficie di un enzima Glucosio
27 Interazione substrato-sito bt t attivo
28 L enzima è complementare allo stato di transizione
29 La specificità di un enzima e la sua capacità catalitica dipendono dall energia rilasciata in seguito alla formazione di legami ed interazioni i i deboli con il substrato Le interazioni deboli tra enzima e substrato sono ottimali nello stato di transizione L enzima è complementare allo stato di transizione L enzima può subire un cambiamento conformazionale reversibile in seguito all interazione con il substrato: adattamento indotto ESOCHINASI
30 Esochinasi e adattamento indotto Il legame del substrato (glucosio) induce una modificazione conformazionale reversibile dell enzima enzima esochinasi
31 Impossibile visualizzare l'immagine. La memoria del computer potrebbe essere insufficiente per aprire l'immagine oppure l'immagine potrebbe essere danneggiata. Riavviare il computer e aprire di nuovo il file. Se viene visualizzata di nuovo la x rossa, potrebbe essere necessario eliminare l'immagine e inserirla di nuovo. EVENTI AL SITO ATTIVO DI UN ENZIMA Reagenti (substrati) Enzima I reagenti si avvicinano all enzima I reagenti si legano al sito attivo Prodotti Cambiamento di coonformazione Rilascio dei prodotti
32 Come fa un enzima ad abbassare l energia di attivazione? Lo stato di transizione si trova ad un livello ll energetico superiore a quello del reagente e del prodotto L enzima abbassa l energia libera dello stato di transizione
33 L ATTIVITÀ ENZIMATICA DIPENDE DAL MANTENIMENTO DELLA CONFORMAZIONE NATIVA Effetto del ph ph ph Un cambiamento di ph può causare un cambiamento della carica della proteina
34 L attività enzimatica può essere modificata da ph Temperatura Concentrazione del substrato Modificazioni covalenti (es. fosforilazione)
35 L ATTIVITÀ ENZIMATICA HA UN ph OTTIMALE Ogni O i enzima è attivo in un ristretto ambito di ph. Il ph ottimale è quello al quale corrisponde la massima attività enzimatica. Cambiamenti di ph possono alterare i legami intra- e intermolecolari di un enzima cambiandone la conformazione nativa e quindi inducendo d una riduzione i dell efficienza catalitica
36 L ATTIVITÀ ENZIMATICA HA UNA TEMPERATURA OTTIMALE All aumentare della temperatura aumenta l energia cinetica delle molecole e quindi aumenta la possibilità degli urti UnU aumento di 10 C fa raddoppiare la velocità di una reazione LaL temperaturat ottimale è quella alla quale corrisponde la massima attività catalitica (circa 37 C per gli enzimi presenti nelle cellule umane). Al di sopra delle temperatura ottimale l enzima lenzima inizia a denaturare ovvero a perdere la sua conformazione nativa.
37 La velocità di una reazione cattalizzata da un enzima dipende dalla concentrazione dell enzima Velocità di reazione e Concentrazione enzimatica A ph e temperatura costanti la velocità è proporzionale alla concentrazione dell enzimaenzima
38 COME SI ESPRIME L ATTIVITÀ ENZIMATICA? 1 unità à enzimatica i (U) : quantità à di enzima che trasforma 1 micromole di substrato al minuto in condizioni i idefinite i di ph e temperatura.
39 PROPRIETÀ CINETICHE DEGLI ENZIMI v 0 = velocità iniziale numero di moli di prodotto che si formano, o di substrato che si consumano, nell unità di tempo V max = velocità massima, tutti i siti catalitici sono occupati Velocità iniziale v 0 ( M/ /min) Concentrazione di substrato, [S] (mm) K m = costante di Michaelis-Menten, esprime la concentrazione di substrato alla quale corrisponde una velocità di reazione pari alla metà della velocità massima
40 Ve elocità in niziale v 0 ( M/min) La velocità iniziale v 0 è direttamente proporzionale alla [S] (tratto lineare) Concentrazione di substrato, [S] (mm) Ad una concentrazione fissa di enzima, la velocità è proporzionale a [S], quando [S] è bassa. Ad elevate [S] invece la velocità è indipendente da [S]
41 La glucochinasi epatica è caratterizzata da un elevata K m per il glucosio e quindi può fosforilare il glucosio quando la sua concentrazione è elevata
42 Gli ENZIMI ALLOSTERICI non seguono la cinetica di Michaelis-Menten Presentano altre conformazioni Hanno più siti di legame Enzima meno attivo [S] Enzima più attivo Il grafico della velocità in funzione della [S] ha un andamento sigmoidale Spesso sono multimerici, formati da più subunità ciascuna contenente un sito attivo Presentano altre conformazioni indotte dal legame con modulatori o effettori L attività enzimatica può risultare esaltata o inibita in seguito al legame con un modulatore
43 EFFETTORI ALLOSTERICI EFFETTORI ETEROTROPICI Substrato Modulatore positivo i EFFETTORI OMOTROPICI Siti attivi Enzima meno attivo Enzima più attivo Complesso Enzima attivo - substrato Il legame con il modulatore induce un cambiamento conformazionale Siti attivi Il legame della prima molecola l di substrato favorisce il legame della seconda, ecc.
44 K 1 K 3 E + S ES E + P K 2 Cinetica di ordine zero Cinetica di primo ordine [S] >> K m V max = k 3 [E]. Se [S] è piu piccola della K m v=(v max /K m )[S] la [S] >> K m (circa 50 volte la K m ) E è saturo di S, la velocità La velocità iniziale è direttamente corrisponde quindi alla V dè proporzionale alla [S] (tratto lineare) max ed proporzionale alla [E].
45 EQUAZIONE DI MICHAELIS-MENTEN Velocità iniziale v 0 ( M/m min) rappresentazione grafica: iperbole [S] (mm) [S] v =V 0 MAX [S ] + K M
46 COME SI MISURANO K m E V max DI m max UNA REAZIONE ENZIMATICA?
47 Per determinare K M e V max si mantiene fissa la concentrazione di enzima e si misura la velocità di reazione v 0 in presenza di concentrazioni i crescenti di substrato La velocità di reazione v 0 può essere espressa come numero di moli di substrato che si consumano nell unità di tempo ( mol/l/min o M/min) oppure numero di moli di prodotto che si formano nell unità di tempo ( mol/l/min o M/min) Velocità di reazion ne v 0 ( M M/min) K M = [S] dove v 0 = ½ Vmax [S]
48 L equazione di Michaelis-Menten può essere trasformata algebricamente per analizzare più semplicemente i dati sperimentali
49 Pendenza = EQUAZIONE DI LINEWEAVER E BURK rappresentazione grafica: retta che non passa per l origine 1. + = K M 1 1 v 0 V max [S] V max corrispondente all equazione di una retta y = ax + b dove a rappresenta il coefficiente angolare (pendenza =K m /V max ) b rappresenta l intercetta sull asse delle ordinate (1/V max )
50 L ATTIVITÀ ENZIMATICA PUÒ ESSERE INIBITA Inibizione reversibile: legami deboli tra inibitore ed enzima 1) Inibizione i competitiva TIPI DI INIBIZIONE l inibitore ha una struttura simile al substrato e compete con il substrato per il sito attivo 2) Inibizione non competitiva l inibitore si lega a un sito diverso dal sito attivo Molti farmaci agiscono come inibitori enzimatici
51 1) INIBIZIONE COMPETITIVA Inibizione competitiva Gli inibitori competitivi (I) si legano al sito attivo degli enzimi. Un inibitore competivo diminuisce la velocità di catalisi riducendo il numero di molecole enzimatiche disponibili per il substrato
52 Stessa V MAX Diversa K M Un inibitore competivo diminuisce l efficienza catalitica riducendo il numero di molecole enzimatiche disponibili per il substrato In presenza di un p inibitore competitivo la K M aumenta
53 2) INIBIZIONE NON COMPETITIVA Inibizione incompetitiva Gli inibitori non competitivi (I) si legano a siti diversi dal sito attivo degli enzimi
54 INIBIZIONE NON COMPETITIVA In presenza di un inibitore non competitivo la V max diminuisce, la K M rimane invariata diversa V max 1/v 0 con inibitore stessa K M 1/V max 1/V max senza inibitore -1/K M 1/[S]
55 Classificazione degli enzimi 1. Ossidoreduttasi deidrogenasi, ossidasi, ossigenasi, transelettronasi 2. Transferasi amino-t, metil-t, fosfo-t, glicosil-t, ecc. 3. Idrolasi peptidasi, glicosidasi, esterasi, lipasi, fosfatasi 4. Liasi decarbossilasi, fumarasi, enolasi 5. Isomerasi fosfoesoso-i, fosfotrioso-i, ecc. 6. Ligasi sintetasi, sintasi, carbossilasi
56
57 Classificazione degli enzimi Ad ogni enzima è assegnato un numero a 4 cifre che identifica la sottoclasse ed il tipo di reazione catalizzata ATP + D- glucosio ADP + D-glucosio-6-fosfato Reazione catalizzata t dalla ATP glucosio fosfotransferasi f f Enzyme Commission number (2): transferasi (classe) (7): fosfotransferasi (sottoclasse) (1): gruppo OH come accettore (1): il D-glucosio come accettore del gruppo fosforico
58 REAZIONI CATALIZZATE DAGLI ENZIMI OSSIDOREDUTTASI Trasferimento di elettroni TRANSFERASI Trasferimento di gruppi funzionali IDROLASI Trasferimento di gruppi funzionali all acqua LIASI Addizione di gruppi funzionali a doppi legami o formazione di doppi legami mediante rimozione i di gruppi ISOMERASI Trasferimento di gruppi all interno di molecole per formare isomeri LIGASI Formazione di legami C-C, C-S, C-O e C-N mediante reazioni di condensazione
59 ISOENZIMI Enzimi che presentano forme molecolari diverse che catalizzano la stessa reazione Esempio: gli isoenzimi della lattico deidrogenasi, indicatori diagnostici di lesioni di organo
60
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
CLASSIFICAZIONE O.T.I.L.Is. Lig
 GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
3) La presenza di gruppi funzionali specifici che partecipano alla catalisi (quelli delle catene laterali dei suoi residui amminoacidici e/o quelli
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
2) La presenza di gruppi funzionali specifici che partecipano alla catalisi (quelli delle catene laterali dei suoi residui amminoacidici e/o quelli
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
Fondamenti di Chimica Farmaceutica. Inibizione enzimatica
 Fondamenti di Chimica Farmaceutica Inibizione enzimatica Cinetica enzimatica E + S k 1 k 1 ES k2 E + P La reazione catalizzata dall enzima avviene in due passaggi: la formazione del complesso enzima-substrato:
Fondamenti di Chimica Farmaceutica Inibizione enzimatica Cinetica enzimatica E + S k 1 k 1 ES k2 E + P La reazione catalizzata dall enzima avviene in due passaggi: la formazione del complesso enzima-substrato:
Enzimi e loro ruolo nel metabolismo
 Enzimi e loro ruolo nel metabolismo Definizioni e ruoli degli enzimi Cinetica enzimatica Localizzazione degli enzimi Enzimi come bersaglio di farmaci Enzimi come markers in Biochimica Clinica Errori congeniti
Enzimi e loro ruolo nel metabolismo Definizioni e ruoli degli enzimi Cinetica enzimatica Localizzazione degli enzimi Enzimi come bersaglio di farmaci Enzimi come markers in Biochimica Clinica Errori congeniti
BIOLOGIA GENERALE 19 dicembre 2006
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE 19 dicembre 2006 Facoltà di Psicologia Corso di Laurea in Scienze e Tecniche di Psicologia Generale e Sperimentale
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi
 1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
2. Quale delle seguenti affermazioni relative ad una reazione enzimatica è vera?
 1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
proteine enzimi RNA ribozimi substrati altamente specifici -asi
 I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
Casi più complicati. inibizione mista (competitiva e non competitiva)
 Casi più complicati inibizione mista (competitiva e non competitiva) reazioni reversibili reazioni a più substrati effetto del ph inibizione mista (competitiva e non competitiva) K I K I E + I EI ES +
Casi più complicati inibizione mista (competitiva e non competitiva) reazioni reversibili reazioni a più substrati effetto del ph inibizione mista (competitiva e non competitiva) K I K I E + I EI ES +
Esempi di funzioni svolte dalle proteine
 Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Enzimi come catalizzatori biologici
 Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
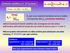 Costante catalitica o n di Turnover k 1 k 2 S + E ES E + P k -1 Vmax = k 2 [ES] = k 2 [E] TOT k Vmax 2 = [E] TOT k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
Costante catalitica o n di Turnover k 1 k 2 S + E ES E + P k -1 Vmax = k 2 [ES] = k 2 [E] TOT k Vmax 2 = [E] TOT k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Velocità di reazione. Consideriamo una generica reazione
 Velocità di reazione. Consideriamo una generica reazione Esprimiamo perciò la velocità di un processo chimico in un certo periodo di tempo tramite il rapporto tra la variazione di concentrazione di un
Velocità di reazione. Consideriamo una generica reazione Esprimiamo perciò la velocità di un processo chimico in un certo periodo di tempo tramite il rapporto tra la variazione di concentrazione di un
CINETICA ENZIMATICA - velocità di reazione
 [P] Velocità iniziale (V 0 ) CINETICA ENZIMATICA - velocità di reazione + + k 1 E + S ES ES E + P k 2 k 3 k 4 V = d[p]/dt = k 3 [ES] Velocità iniziale (V 0 ) quando [S] >> [P] V max t CINETICA ENZIMATICA:
[P] Velocità iniziale (V 0 ) CINETICA ENZIMATICA - velocità di reazione + + k 1 E + S ES ES E + P k 2 k 3 k 4 V = d[p]/dt = k 3 [ES] Velocità iniziale (V 0 ) quando [S] >> [P] V max t CINETICA ENZIMATICA:
Termodinamica ENTALPIA...6
 Termodinamica ORGANISMI PRIMO VIVENTI ED ENERGIA...2 PRINCIPIO DELLA TERMODINAMICA...5 ENTALPIA...6 SECONDO PRINCIPIO DELLA TERMODINAMICA... 7 energia libera di Gibbs (G)...9 Variazione di energia libera
Termodinamica ORGANISMI PRIMO VIVENTI ED ENERGIA...2 PRINCIPIO DELLA TERMODINAMICA...5 ENTALPIA...6 SECONDO PRINCIPIO DELLA TERMODINAMICA... 7 energia libera di Gibbs (G)...9 Variazione di energia libera
Gli enzimi e la catalisi
 Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori.
 Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione -
 Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione - esaminando il modo in cui il sito attivo favorisce la catalisi
Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione - esaminando il modo in cui il sito attivo favorisce la catalisi
ENZIMI : catalizzatori biologici
 ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
I catalizzatori della cellula: gli ENZIMI
 I catalizzatori della cellula: gli ENZIMI LA CATALISI ENZIMATICA E NECESSARIA PER PERMETTERE A MOLTE REAZIONI BIOCHIMICHE DI PROCEDERE AD UNA VELOCITA CONVENIENTE IN CONDIZIONI BIOLOGICHE UNA REAZIONE
I catalizzatori della cellula: gli ENZIMI LA CATALISI ENZIMATICA E NECESSARIA PER PERMETTERE A MOLTE REAZIONI BIOCHIMICHE DI PROCEDERE AD UNA VELOCITA CONVENIENTE IN CONDIZIONI BIOLOGICHE UNA REAZIONE
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
REGOLAZIONE DELL ATTIVITA ENZIMATICA 1) MODULAZIONE ALLOSTERICA NON-COVALENTE (REVERSIBILE)
 REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
Il laboratorio di Biochimica si svolgerà nei seguenti giorni;
 Il laboratorio di Biochimica si svolgerà nei seguenti giorni; Lunedì 7 marzo 2016 Lezione 9-11 aula 1 Martedì 8 marzo Mercoledì 9 marzo ESERCITAZ. Lab. PP1 Giovedì 10 marzo 14:00-18:00 La frequenza è obbligatoria
Il laboratorio di Biochimica si svolgerà nei seguenti giorni; Lunedì 7 marzo 2016 Lezione 9-11 aula 1 Martedì 8 marzo Mercoledì 9 marzo ESERCITAZ. Lab. PP1 Giovedì 10 marzo 14:00-18:00 La frequenza è obbligatoria
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
REAZIONI CHIMICHE. Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: I reagenti (substrati) devono entrare in collisione
 ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre
 Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Enzimi = catalizzatori di una reazione biochimica Caratteristiche: Specificità: ogni enzima riconosce specificamente il/i substrato/i e non altre molecole, anche chimicamente simili al substrato. Saturabilità:
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
Chimica Fisica Biologica
 Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
2015 /2016. scaricato da
 Enzimi Prof Spina Riabilitativa 2015 /2016 Gli enzimi i sono catalizzatori t i biologici i i molto efficienti: i caratterizzati da potere catalitico e specificità, possegono una porzione dedicata: il
Enzimi Prof Spina Riabilitativa 2015 /2016 Gli enzimi i sono catalizzatori t i biologici i i molto efficienti: i caratterizzati da potere catalitico e specificità, possegono una porzione dedicata: il
INIBIZIONE ENZIMATICA REVERSIBILE
 INIBIZIONE ENZIMATICA REVERSIBILE La reazione enzimatica in vitro o in vivo può essere INIBITA REVERSIBILMENTE. Un inibitore (I) legandosi all enzima interferisce con la sua attività modificando la Vmax,
INIBIZIONE ENZIMATICA REVERSIBILE La reazione enzimatica in vitro o in vivo può essere INIBITA REVERSIBILMENTE. Un inibitore (I) legandosi all enzima interferisce con la sua attività modificando la Vmax,
FUNZIONI delle PROTEINE
 FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
FUNZIONI delle PROTEINE Ha le dimensioni del reciproco di una concentrazione (M -1 ) Ha le dimensioni di una concentrazione (M) La frazione dei siti occupati rispetto ai siti totali è definita come θ FRAZIONE
REAZIONI CHIMICHE. Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: I reagenti (substrati) devono entrare in collisione
 ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
Spesso le reazioni chimiche sono accompagnate da. Le reazioni che sviluppano calore sono dette reazioni esotermiche
 Spesso le reazioni chimiche sono accompagnate da sviluppo o assorbimento di calore. Le reazioni che sviluppano calore sono dette reazioni esotermiche Le reazioni che assorbono calore sono dette reazioni
Spesso le reazioni chimiche sono accompagnate da sviluppo o assorbimento di calore. Le reazioni che sviluppano calore sono dette reazioni esotermiche Le reazioni che assorbono calore sono dette reazioni
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Tecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Tecnologie Biochimiche DISPENSA
Regolazione dell attività enzimatica. Allosteria Modificazioni covalenti Isoenzimi
 Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia. a.a
 Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia a.a. 2016-17 Cinetica Chimica studia i fenomeni connessi con la VELOCITA di una REAZIONE Reazioni
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia a.a. 2016-17 Cinetica Chimica studia i fenomeni connessi con la VELOCITA di una REAZIONE Reazioni
Cinetica chimica MECCANISMO <<Lo studio CINETICO fornisce invece queste informazioni>>
 Cinetica chimica La termodinamica studia gli aspetti energetici di una reazione nel senso che stabilisce se, da un punto di vista energetico, la reazione potrà avvenire o no. Niente, invece, dice sul tempo
Cinetica chimica La termodinamica studia gli aspetti energetici di una reazione nel senso che stabilisce se, da un punto di vista energetico, la reazione potrà avvenire o no. Niente, invece, dice sul tempo
ENZIMI. Catalizzatori delle reazioni biologiche
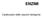 ENZIMI Catalizzatori delle reazioni biologiche I CATALIZZATORI ABBASSANO L ENERGIA DI ATTIVAZIONE FACILITANDO LA FORMAZIONE DELLO STATO DI TRANSIZIONE Il legame tra enzima e substrato genera un percorso
ENZIMI Catalizzatori delle reazioni biologiche I CATALIZZATORI ABBASSANO L ENERGIA DI ATTIVAZIONE FACILITANDO LA FORMAZIONE DELLO STATO DI TRANSIZIONE Il legame tra enzima e substrato genera un percorso
SISTEMI CHIMICI Si definiscono sistemi chimici le sostanze (reagenti e prodotti) che partecipano alle trasformazioni fisiche e chimiche della materia.
 TERMODINAMICA SISTEMI CHIMICI Si definiscono sistemi chimici le sostanze (reagenti e prodotti) che partecipano alle trasformazioni fisiche e chimiche della materia. Tutto ciò che circonda il sistema viene
TERMODINAMICA SISTEMI CHIMICI Si definiscono sistemi chimici le sostanze (reagenti e prodotti) che partecipano alle trasformazioni fisiche e chimiche della materia. Tutto ciò che circonda il sistema viene
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA
 Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
La velocità di reazione
 La velocità di reazione 1 Che cos è la velocità di reazione (I) Lo studio di tutti gli aspetti relativi alla velocità delle trasformazioni chimiche è affrontato dalla cinetica chimica. La velocità di reazione
La velocità di reazione 1 Che cos è la velocità di reazione (I) Lo studio di tutti gli aspetti relativi alla velocità delle trasformazioni chimiche è affrontato dalla cinetica chimica. La velocità di reazione
Gli enzimi. Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici
 Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA
 Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
Cap.15 BIOENERGETICA IL METABOLISMO RISULTA DALL INSIEME DELLE REAZIONI CHIMICHE CHE PERMETTONO AI SISTEMI VIVENTI DI UTILIZZARE ENERGIA E MATERIA I Legge della Termodinamica: Il contenuto energetico dell
Ioni inorganici (Mg 2+, Zn 2+ ), o molecole organiche o metallorganiche (coenzimi)
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
STRUTTURA E MECCANISMI D AZIONE DEGLI ENZIMI
 STRUTTURA E MECCANISMI D AZIONE DEGLI ENZIMI Confronto tra gli enzimi e i catalizzatori chimici Gli enzimi sono caratterizzati da: Velocità di reazione più elevate Condizioni di reazione più moderate
STRUTTURA E MECCANISMI D AZIONE DEGLI ENZIMI Confronto tra gli enzimi e i catalizzatori chimici Gli enzimi sono caratterizzati da: Velocità di reazione più elevate Condizioni di reazione più moderate
Enzimi: catalizzatori biologici
 Enzimi: catalizzatori biologici praticamente tutte le reazioni biochimiche della chimica della vita sono catalizzate da enzimi gli enzimi sono proteine la velocità di reazioni enzimatiche è aumentata di
Enzimi: catalizzatori biologici praticamente tutte le reazioni biochimiche della chimica della vita sono catalizzate da enzimi gli enzimi sono proteine la velocità di reazioni enzimatiche è aumentata di
Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari
 Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari Assunzione di principio: i sistemi si trovano in condizioni di controllo termodinamico e non cinetico (tutti
Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari Assunzione di principio: i sistemi si trovano in condizioni di controllo termodinamico e non cinetico (tutti
CLASSIFICAZIONE ENZIMI
 CLASSIFICAZIONE ENZIMI nome raccomandato nome sistematico reazione catalizzata Classe di enzima Reazione catalizzata 1. Ossidoreduttasi Ossido-riduzione 2. Transferasi Trasferimento di gruppi funzionali
CLASSIFICAZIONE ENZIMI nome raccomandato nome sistematico reazione catalizzata Classe di enzima Reazione catalizzata 1. Ossidoreduttasi Ossido-riduzione 2. Transferasi Trasferimento di gruppi funzionali
REGOLAZIONE ENZIMATICA
 REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
REGOLAZIONE ENZIMATICA Cambio conformazionale In molte molecole proteiche, cambiamenti strutturali possono determinare profondi cambiamenti nella funzione o nell attività. Il cambio conformazionale può
Cinetica Chimica. Cinetica chimica
 Cinetica Chimica CH 3 Cl + NaOH CH 3 OH + NaCl Le reazioni chimiche possono decorrere con cinetica molto veloce (come le reazioni di salificazione di un acido con una base) o lenta (come alcune reazioni
Cinetica Chimica CH 3 Cl + NaOH CH 3 OH + NaCl Le reazioni chimiche possono decorrere con cinetica molto veloce (come le reazioni di salificazione di un acido con una base) o lenta (come alcune reazioni
CATALISI COVALENTE. H 2 O Enz-R-OH + P. Enz-R-O S Enz-R-O-S
 CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
v = Δ[P] = _ Δ[S] S P
![v = Δ[P] = _ Δ[S] S P v = Δ[P] = _ Δ[S] S P](/thumbs/98/137173050.jpg) CINETICA ENZIMATICA Gli esperimenti di cinetica enzimatica si basano sulla determinazione della velocità di reazione, misurata come variazione della concentrazione del prodotto o del reagente in un dato
CINETICA ENZIMATICA Gli esperimenti di cinetica enzimatica si basano sulla determinazione della velocità di reazione, misurata come variazione della concentrazione del prodotto o del reagente in un dato
Lezione n. 11. Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione.
 Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
catabolismo anabolismo
 Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche
La velocità delle reazioni. Equilibrio chimico
 La velocità delle reazioni Equilibrio chimico Velocità di reazione È la velocità con cui i reagenti di una reazione si trasformano in prodotti nell unità di tempo Lo studio della velocità di reazione viene
La velocità delle reazioni Equilibrio chimico Velocità di reazione È la velocità con cui i reagenti di una reazione si trasformano in prodotti nell unità di tempo Lo studio della velocità di reazione viene
Scaricato da 1
 A AB B Scaricato da www.sunhope.it 1 1 1 1 2 2 2 3 45 5 5 4 20 20 5 40 40 6 40 20 23 7 5 12 8 35 2 6 9 1 1 Numero di mole ecole 30 25 20 15 10 5 0 0 2 4 6 8 10 Energia Scaricato da www.sunhope.it 2 Scaricato
A AB B Scaricato da www.sunhope.it 1 1 1 1 2 2 2 3 45 5 5 4 20 20 5 40 40 6 40 20 23 7 5 12 8 35 2 6 9 1 1 Numero di mole ecole 30 25 20 15 10 5 0 0 2 4 6 8 10 Energia Scaricato da www.sunhope.it 2 Scaricato
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Termochimica. La termochimica e la cinetica. Termochimica. Termochimica. Con il termine sistema s intende l oggetto di indagine.
 La termochimica e la cinetica Con il termine sistema s intende l oggetto di indagine. Tutto ciò che circonda il sistema costituisce l ambiente. I sistemi aperti scambiano energia e materia con l ambiente.
La termochimica e la cinetica Con il termine sistema s intende l oggetto di indagine. Tutto ciò che circonda il sistema costituisce l ambiente. I sistemi aperti scambiano energia e materia con l ambiente.
H = entalpia, contenuto termico di un sistema che sta reagendo; dipende dal numero e dal tipo di legami chimici dei reagenti e dei prodotti
 ΔG = ΔH - TΔS H = entalpia, contenuto termico di un sistema che sta reagendo; dipende dal numero e dal tipo di legami chimici dei reagenti e dei prodotti Reazione esotermica = rilascia colore, ΔH è negativo,
ΔG = ΔH - TΔS H = entalpia, contenuto termico di un sistema che sta reagendo; dipende dal numero e dal tipo di legami chimici dei reagenti e dei prodotti Reazione esotermica = rilascia colore, ΔH è negativo,
Determinazione dell attività enzimatica
 Determinazione dell attività enzimatica Gli enzimi sono una percentuale rilevante delle proteine cellulari anche se ciascun tipo di enzima è presente nella cellula in quantità molto bassa. Controllano
Determinazione dell attività enzimatica Gli enzimi sono una percentuale rilevante delle proteine cellulari anche se ciascun tipo di enzima è presente nella cellula in quantità molto bassa. Controllano
ENZIMI : catalizzatori biologici
 ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
Cinetica Chimica 1. esaminare quali condizioni debbono essere soddisfatte affinché una data reazione avvenga spontaneamente 2. esaminare quali sono i
 Cinetica Chimica 1. esaminare quali condizioni debbono essere soddisfatte affinché una data reazione avvenga spontaneamente 2. esaminare quali sono i fattori che influenzano il tempo richiesto affinché
Cinetica Chimica 1. esaminare quali condizioni debbono essere soddisfatte affinché una data reazione avvenga spontaneamente 2. esaminare quali sono i fattori che influenzano il tempo richiesto affinché
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
Metabolismo del glucosio
 Metabolismo del glucosio Metabolismo del glucosio La glicolisi avviene in tutte le cellule umane Percorsi metabolici del glucosio in varie cellule: è metabolizzato in modo diverso nelle varie cellule TABELLA
Metabolismo del glucosio Metabolismo del glucosio La glicolisi avviene in tutte le cellule umane Percorsi metabolici del glucosio in varie cellule: è metabolizzato in modo diverso nelle varie cellule TABELLA
TARGETS DEI FARMACI ATTUALMENTE IN USO
 TARGETS DEI FARMACI ATTUALMENTE IN USO INIBITORI ENZIMATICI INIBITORI ENZIMATICI Sintesi dell'uridine-5'-monophosphate (UMP) INIBITORI ENZIMATICI EFFICACIA DI INIBITORI COME AGENTI TERAPEUTICI Potenza
TARGETS DEI FARMACI ATTUALMENTE IN USO INIBITORI ENZIMATICI INIBITORI ENZIMATICI Sintesi dell'uridine-5'-monophosphate (UMP) INIBITORI ENZIMATICI EFFICACIA DI INIBITORI COME AGENTI TERAPEUTICI Potenza
Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe. Substrato
 Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe Substrato Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER, Zanichelli editore S.p.A. Copyright 2014 6 11
Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe Substrato Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER, Zanichelli editore S.p.A. Copyright 2014 6 11
PRINCIPALI CARATTERISTICHE DEGLI ENZIMI. 1) Aumentano la velocità di reazione. 2) Non modificano l equilibrio della reazione
 PRINCIPALI CARATTERISTICHE DEGLI ENZIMI 1) Aumentano la velocità di reazione 2) Non modificano l equilibrio della reazione S P 3) Presentano specificità di reazione 4) Richiedono condizioni di reazione
PRINCIPALI CARATTERISTICHE DEGLI ENZIMI 1) Aumentano la velocità di reazione 2) Non modificano l equilibrio della reazione S P 3) Presentano specificità di reazione 4) Richiedono condizioni di reazione
Velocità di reazione
 1 Velocità di reazione A B V = - d[a] dt = d[b] dt V= Velocità istantanea: coefficiente angolare della retta tangente alla curva in quel punto Quando t=0 la velocità istantanea sarà massima (V 0 ) 2 Energia
1 Velocità di reazione A B V = - d[a] dt = d[b] dt V= Velocità istantanea: coefficiente angolare della retta tangente alla curva in quel punto Quando t=0 la velocità istantanea sarà massima (V 0 ) 2 Energia
LE REAZIONI CHIMICHE
 LE REAZIONI CHIMICHE Una reazione chimica è una trasformazione che comporta una nuova distribuzione degli atomi in una o più determinate sostanze Una reazione chimica è un processo dinamico in cui alcune
LE REAZIONI CHIMICHE Una reazione chimica è una trasformazione che comporta una nuova distribuzione degli atomi in una o più determinate sostanze Una reazione chimica è un processo dinamico in cui alcune
03/03/19 L energia della vita
 METABOLISMO E BIOENERGIA FARMACIA L energia della vita L energia della vita 2 1 L energia della vita 3 L energia negli ecosistemi - Fotoautotrofi: 6CO 2 + 6H 2 O + luce = C 6 H 12 O 6 + 6O 2 - eterotrofi-autotrofi:
METABOLISMO E BIOENERGIA FARMACIA L energia della vita L energia della vita 2 1 L energia della vita 3 L energia negli ecosistemi - Fotoautotrofi: 6CO 2 + 6H 2 O + luce = C 6 H 12 O 6 + 6O 2 - eterotrofi-autotrofi:
catalizzatori biologici RUOLO DEGLI ENZIMI: 16/03/15
 I sistemi viventi sono caratterizzati da un enorme varietà reazioni chimiche la maggior parte delle quali è mediata da una serie di eccezionali CATALIZZATORI BIOLOGICI : GLI ENZIMI L ENZIMOLOGIA E UNA
I sistemi viventi sono caratterizzati da un enorme varietà reazioni chimiche la maggior parte delle quali è mediata da una serie di eccezionali CATALIZZATORI BIOLOGICI : GLI ENZIMI L ENZIMOLOGIA E UNA
L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO
 L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO ( L ATP e l energia L energia Energia e reazioni chimiche Una reazione chimica avviene quando gli atomi possiedono energia a sufficiente a combinarsi tra
L ATP E L ENERGIA LA CHIMICA DELLA VITA GSCATULLO ( L ATP e l energia L energia Energia e reazioni chimiche Una reazione chimica avviene quando gli atomi possiedono energia a sufficiente a combinarsi tra
Organismi viventi ed energia
 Termodinamica ORGANISMI VIVENTI ED ENERGIA...2 Primo principio della termodinamica...5 Secondo principio della termodinamica...6 energia libera di Gibbs (G)...9 Variazione di energia libera in una reazione
Termodinamica ORGANISMI VIVENTI ED ENERGIA...2 Primo principio della termodinamica...5 Secondo principio della termodinamica...6 energia libera di Gibbs (G)...9 Variazione di energia libera in una reazione
12/03/18 L energia della vita
 METABOLISMO E BIOENERGIA FARMACIA L energia della vita 12/03/18 L energia della vita 2 1 12/03/18 L energia della vita 3 L energia negli ecosistemi - Fotoautotrofi: 6CO 2 + 6H 2 O + luce = C 6 H 12 O 6
METABOLISMO E BIOENERGIA FARMACIA L energia della vita 12/03/18 L energia della vita 2 1 12/03/18 L energia della vita 3 L energia negli ecosistemi - Fotoautotrofi: 6CO 2 + 6H 2 O + luce = C 6 H 12 O 6
Laurea di I Livello in SCIENZE E TECNOLOGIE AGRARIE L 25
 Laurea di I Livello in SCIENZE E TECNOLOGIE AGRARIE L 25 Corso Integrato Chimica Agraria (12 CFU) Moduli didattici Biochimica e Fisiologia Vegetale (6 CFU) Chimica del Suolo (6 CFU) Prof. Maria Rosaria
Laurea di I Livello in SCIENZE E TECNOLOGIE AGRARIE L 25 Corso Integrato Chimica Agraria (12 CFU) Moduli didattici Biochimica e Fisiologia Vegetale (6 CFU) Chimica del Suolo (6 CFU) Prof. Maria Rosaria
Catalisi. Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A Modulo di Biologia Strutturale
 Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Biotecnologie applicate alla progettazione e sviluppo di molecole biologicamente attive A.A. 2010-2011 Modulo di Biologia Strutturale Catalisi Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie
Dalle soluzioni alla chimica del carbonio
 Dalle soluzioni alla chimica del carbonio Capitolo 9 Energia e velocità delle reazioni chimiche Unità 27 Energia di sistemi chimici 9.1 Energia di legame ed energia chimica 9.2 Primo principio della termodinamica
Dalle soluzioni alla chimica del carbonio Capitolo 9 Energia e velocità delle reazioni chimiche Unità 27 Energia di sistemi chimici 9.1 Energia di legame ed energia chimica 9.2 Primo principio della termodinamica
In questo caso parliamo di un processo entalpico. Si tratta di un processo entalpico.
 LEZIONE DEL 10/04/2017 ENZIMOLOGIA - APPLICAZIONI DELLA CINETICA ENZIMATICA Essa trova applicazioni nel processamento dei rifiuti, nelle materie organiche. Si tratta dell'ingegnerizzazione dei processi
LEZIONE DEL 10/04/2017 ENZIMOLOGIA - APPLICAZIONI DELLA CINETICA ENZIMATICA Essa trova applicazioni nel processamento dei rifiuti, nelle materie organiche. Si tratta dell'ingegnerizzazione dei processi
ENZIMI. A + B AB (100 Kcal= E. Attiv.) A + B AB (50 Kcal) SUBSTRATO ENZIMA E N E R G I A
 ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
09/10/18 L energia della vita
 METABOLISMO E BIOENERGIA BIOTECNOLOGIE L energia della vita 09/10/18 L energia della vita 2 1 09/10/18 L energia della vita 3 L energia negli ecosistemi - Fotoautotrofi: 6CO 2 + 6H 2 O + luce = C 6 H 12
METABOLISMO E BIOENERGIA BIOTECNOLOGIE L energia della vita 09/10/18 L energia della vita 2 1 09/10/18 L energia della vita 3 L energia negli ecosistemi - Fotoautotrofi: 6CO 2 + 6H 2 O + luce = C 6 H 12
costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più
 Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Simonetta Klein. Il racconto della chimica e della Terra
 Simonetta Klein Il racconto della chimica e della Terra Capitolo 23 Energia e velocità delle reazioni chimiche Sommario 1. Aspetti energetici delle reazioni chimiche 2. L energia nei sistemi viventi 3.
Simonetta Klein Il racconto della chimica e della Terra Capitolo 23 Energia e velocità delle reazioni chimiche Sommario 1. Aspetti energetici delle reazioni chimiche 2. L energia nei sistemi viventi 3.
Capitolo 5 L energia e il trasporto
 Capitolo 5 L energia e il trasporto La cellula e l energia 5.1 L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità
Capitolo 5 L energia e il trasporto La cellula e l energia 5.1 L energia è la capacità di produrre lavoro Tutti gli organismi hanno bisogno di energia per vivere. L energia è definita come la capacità
La cinetica chimica studia la velocità con cui avviene una reazione chimica. dc dt. dn dt. per reazioni che avvengono a V costante
 Cinetica chimica La cinetica chimica studia la velocità con cui avviene una reazione chimica. a A + b B + l L + m M +... Velocità di reazione rispetto al componente i-esimo: v 1 = ± V dn dt (+) velocità
Cinetica chimica La cinetica chimica studia la velocità con cui avviene una reazione chimica. a A + b B + l L + m M +... Velocità di reazione rispetto al componente i-esimo: v 1 = ± V dn dt (+) velocità
