v = Δ[P] = _ Δ[S] S P
|
|
|
- Chiara Contini
- 5 anni fa
- Visualizzazioni
Transcript
1 CINETICA ENZIMATICA Gli esperimenti di cinetica enzimatica si basano sulla determinazione della velocità di reazione, misurata come variazione della concentrazione del prodotto o del reagente in un dato intervallo di tempo. S P [P] = aumenta nel tempo [S]= diminuisce nel tempo v = Δ[P] = _ Δ[S] Δt Δt [S] [P] Col procedere della reazione le curve cinetiche si appiattiscono: la velocità non subisce variazioni. S è consumato perché trasformato in P e la reazione tenderà a raggiungere l equilibrio.
2 S P v = Δ[P] = _ Δ[S] Δt Δt [S] =5 mm [P] Problema: se miscelo un enzima con diverse concentrazioni di substrato (5, 10 o 20 mm, per es ), come varia la velocità della reazione alle diverse concentrazioni di substrato utilizzate? Tempo (min) [S] =20 mm [P] [S] =10 mm [P] Tempo (min) Tempo (min)
3 La velocità della reazione aumenta all aumentare della [S], ma per avere un valore preciso devo considerare la VELOCITA INIZIALE di reazione [S] [P] Devo misurare la velocità della reazione al MOMENTO INIZIALE (entro i primi sec), quando la quantità di prodotto formato è molto bassa e la concentrazione del substrato ha un valore preciso e noto (quello iniziale stabilito dallo sperimentatore). tempo In questo modo posso associare al valore di [S] utilizzata un dato valore di V 0 (velocità iniziale)
4 COME DETERMINO LA VELOCITA INIZIALE? Studio di una reazione enzimatica semplice (1 solo substrato e 1 solo stadio intermedio): 1) miscelo l enzima con il suo substrato, lavoro a temperatura e ph costanti, 2) Preparo un certo numero di miscele di reazione in cui la [E] è inalterata, ma la [S] è diversa: per ogni esperimento misuro come varia la concentrazione del prodotto, che si forma nel tempo. Substrato [S] = 1 mm Prodotto enzima v = Δ[P] = _ Δ[S] Δt Δt [S] = 5 mm [S] = 2 mm Substrato [S] = 2 mm [S] = 1 mm Substrato [S] = 5 mm
5 3) La velocità di reazione aumenta all aumentare della concentrazione del substrato utilizzata come in una reazione di 1 ordine. v = Δ[P] = _ Δ[S] Δt Δt v = k [S] -1/Δt = k (costante di velocità specifica per ogni reazione) -Reazione di 1 ordine- v = Δ[P] = _ Δ[S] Δt Δt
6 4) Calcolo il valore della velocità di reazione iniziale (v 0 ) alle diverse [S]. VELOCITA INIZIALE (v 0 ) è calcolata come pendenza della tangente alla curva cinetica. Per ognuna delle curve cinetiche ottenute a diverse [S] viene calcolata la v 0 (4) v 0 (3) v 0 (2) v 0 (1) Ogni punto rappresenta un diverso esperimento, ed è definito da due parametri: v 0 e [S] - La v 0 aumenta all aumentare della concentrazione di reagente [Substrato] usata per la reazione. - La dipendenza di v 0 dalla [S] è descritta da una curva iperbolica (Modello cinetico di Micaelis-Menten)
7 Leonor Micaelis Maud Menten
8 ENZIMI CHE SEGUONO IL MODELLO CINETICO DI MICHAELIS-MENTEN Mostrano una dipendenza della velocità iniziale (v 0 ) dalla concentrazione di substrato di tipo IPERBOLICO. Catalizzano una reazione enzimatica che nel caso più semplice prevede: 1 prima tappa veloce e reversibile (ΔG minore e k maggiore) S + E k 1 k -1 ES 1 seconda tappa lenta e irreversibile (ΔG maggiore e k minore) che determina la velocità globale di reazione ES k 2 k -2 E + P k 1 = cost cinetica reazione di formazione del complesso ES k -1 = cost cinetica reazione di decomposizione del complesso ES in E + S k 2 = cost cinetica reazione di decomposizione del complesso ES in E + P k -2 = talmente piccola da essere trascurabile
9 Velocità iniziale v 0 (μm/min) Inserendo in un grafico i valori di v 0 ottenuti per le diverse [S] utilizzate ottengo una curva iperbolica Alte [S] = la v 0 non varia molto al variare di [S], l enzima è quasi completamente saturato, viene raggiunta asintoticamente una velocità di reazione massima. La v 0 non dipende più da [S]. Basse [S] = la velocità di reazione v 0 dipende strettamente dalla [S], aumenta all aumentare della [S] Concentrazione substrato [S] (mm) Posso spiegare questo comportamento con un equazione che correla la v 0 alla [S], alla Vmax e ad una costante di affinità (Km)
10 v = k 1 [E] [S] v = k 2 [ES] 1a tappa: Passaggio rapido k 1 k 2 S + E ES E + P k -1 2a tappa: Passaggio lento v = k -1 [ES] La v 0 GLOBALE della reazione enzimatica dipende da [ES] Questa equazione non è sufficiente a spiegare la relazione iperbolica esistente tra v 0 e [S]. v 0 = k 2 [ES] [ES] = non è facilmente misurabile, e k 2 non è nota Bisogna ricavare un equazione alternativa partendo dalla considerazione che la [ES] rimane costante nel tempo della reazione, e che la 1a tappa della reazione enzimatica raggiunge rapidamente lo STATO STAZIONARIO k 1 S + E ES k -1
11 COMPLESSIVAMENTE [ES] RIMANE COSTANTE NEL TEMPO La concentrazione dell enzima libero [E] in soluzione diminuisce man mano che va a formare il complesso [ES]. Ma poiché il complesso ES è demolito continuamente (in E + S o in E + P), l ENZIMA è di nuovo reso libero. STATO STAZIONARIO
12 [ES] rimane costante: la velocità della sua formazione è uguale alla velocità della sua demolizione Velocità di Formazione di ES (E + S ES): V = k 1 [E] [S] = k 1 ([E] TOT [ES]) [S] k 1 k 2 S + E ES k E + P -1 k -1 k 2 Velocità di Demolizione di ES (ES S + E..ES P + E): V = k -1 [ES] + k 2 [ES] [E] = [E] TOT [ES] poiché la concentrazione TOTALE di Enzima è [E] TOT = [E] + [ES] Se è raggiunto lo stato stazionario posso dire che: V formazione ES = V demolizione ES k 1 ([E] TOT [ES]) [S] = k -1 [ES] + k 2 [ES] Riarrangiando l equazione tramite operazioni algebriche si ottiene che: ([E] TOT [ES]) [S] = ( k -1 + k 2 ) k -1 + k 2 [ES] k 1 K m = k 1 Costante di Michaelis-Menten
13 K m = k -1 + k 2 k 1 Costante di Michaelis-Menten Il rapporto fra le costanti cinetiche della dissociazione di ES e quella della sua formazione è uguale alla COSTANTE DI DISSOCIAZIONE DEL COMPLESSO ES Semplificando i termini dell equazione precedente si ottiene che: ([E] TOT [ES]) [S] = Km [ES] [E] TOT [S] [ES][S] = [ES] Km [ES] Km = [E] TOT [S] [ES][S] [ES] Km + [ES][S] = [E] TOT [S] [ES] (Km +[S]) = [E] TOT [S] [ES] = [E] TOT [S] [S] + K m
14 Poiché la v 0 globale di reazione è : v 0 = k 2 [ES] e quindi: [ES] = v 0 / k 2 [ES] = [E] TOT [S] [S] + K m k 2 [E] TOT = Vmax v 0 = k 2 [E] TOT [S] [S] + K m Introduciamo un altro parametro importante: la Velocità massima di reazione. Quando sono presenti nella miscela di reazione concentrazioni saturanti di substrato, allora, tutto l enzima è complessato col substrato e la [E] TOT = [ES] La velocità globale di reazione non dipende più dalla concentrazione di substrato, ma solo dalla concentrazione totale dell enzima: v 0 = k 2 [ES] diventa Vmax = k 2 [E] TOT
15 v 0 (μm/min) Equazione di Michaelis-Menten v 0 = Vmax [S] Km + [S] La velocità iniziale della reazione enzimatica dipende dalla [S] in modo iperbolico ed è correlata alla Vmax (= k 2 [E] tot ) e alla Km Il valore della Km si può determinare sperimentalmente = Corrisponde alla [S] alla quale raggiungo la metà della Vmax. Ha le unità di misura di una concentrazione k 1 k 2 S + E ES E + P k -1 [S] (mm) v 0 = ½ Vmax = Vmax [S] [S] + Km 1 [S] = 2 [S] + Km Km + [S] = 2 [S] Km = [S] Solo se v 0 = ½ Vmax
16 Km = k -1 + k 2 k 1 (k 2 << k -1 = trascurabile) La Km è uguale alla costante di dissociazione del complesso ES Km = La Km fornisce informazioni sull affinità che un enzima ha nei confronti del suo substrato ed è SPECIFICA per ogni diverso enzima nei confronti di un dato substrato. Più è grande, minore sarà l affinità dell enzima per il substrato (maggiore sarà la costante di dissociazione del complesso ES, k -1 > k 1 ) Più è piccola maggiore sarà l affinità (minore la costante di dissociazione di ES, k 1 > k -1 ) Considerazioni valide per reazioni enzimatiche semplici a due tappe e in cui k 2 << k -1, non per tutti gli enzimi, molte reazioni enzimatiche sono a più tappe e la Km diventa una funzione più complessa che dipende da varie costanti cinetiche. k -1 k 1
17 La Km fornisce informazioni sulla efficienza della catalisi e sul controllo della velocità se [S] >> 10 Km concentrazioni saturanti di substrato, la reazione è molto efficiente perché quasi a Vmax, ma non controllabile variando la [S] se [S] << 0.1 Km concentrazioni bassissime di substrato, la reazione non è efficiente ma la si può controllare variando [S], poiché la v 0 aumenta all aumentare della [S]. [S] >> 10 Km Nelle cellule [S] Km le reazione metaboliche sono regolabili variando [S] [S] << 0.1 Km Berg et al., BIOCHIMICA 6/E, Zanichelli editore S.p.A. Copyright 2007
18 v 0 (μm/min) 1 enzima 2 substrati simili A e B medesime condizioni di reazione Verso quale dei due l enzima è più affine? A A B ½ Vmax Km A Km B [S] mm
19 Costante catalitica o n di Turnover k 1 k 2 S + E ES E + P k -1 Vmax = k 2 [ES] = k 2 [E] TOT k Vmax 2 = [E] TOT k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica) Indica il numero di eventi catalitici che avvengono nel sito attivo dell enzima nell unità di tempo (le sue unità di misura sono s -1 o min -1 ). Misura quanto velocemente un dato enzima può catalizzare una data reazione. E SPECIFICA per ogni enzima. Problema: Esperimento 1. [S] = saturante [E] = mm Esperimento 2. [S] = saturante [E] = 0.05 mm Che differenza c è fra i due esperimenti in termini di Vmax e Km?
20 v 0 (μm/sec) A [S] saturante la v 0 raggiunge il suo valore massimo (Vmax), non può più variare in funzione della concentrazione di substrato, perché tutto l enzima presente è saturato. Se raddoppio la concentrazione dell enzima raddoppia la Vmax. Vmax = k 2 [E] tot Vmax B = k 2 [E] B [E] B = 0.05 mm LA Km RIMANE INVARIATA Vmax A = k 2 [E] A [E] = mm Km [S] mm
21 EFFICIENZA CATALITICA DI UN ENZIMA Parametro che utilizziamo per confrontare l efficienza catalitica e la specificità di enzimi diversi per uno stesso substrato o di uno stesso enzima per substrati diversi. Costante di specificità: k cat /Km (M -1 sec -1 ) Kcat più alta per la CO 2 = specificità maggiore ENZIMA SUBSTRATO kcat (sec -1 ) Km (M) kcat/km (M -1 sec -1 ) Acetilcolinesterasi Acetilcolina 1.4x10 4 9x x10 8 Anidrasi carbonica CO 2 1x x x10 7 Anidrasi carbonica HCO 3-4x x x10 7 Catalasi H 2 O 1.4x10 4 9x x10 8 Fumarasi Fumarato 8x10 2 5x x10 8 Fumarasi Malato 9x x x10 7 Km più bassa per il fumarato= specificità maggiore
Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe. Substrato
 Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe Substrato Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER, Zanichelli editore S.p.A. Copyright 2014 6 11
Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe Substrato Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER, Zanichelli editore S.p.A. Copyright 2014 6 11
k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
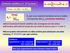 Costante catalitica o n di Turnover k 1 k 2 S + E ES E + P k -1 Vmax = k 2 [ES] = k 2 [E] TOT k Vmax 2 = [E] TOT k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
Costante catalitica o n di Turnover k 1 k 2 S + E ES E + P k -1 Vmax = k 2 [ES] = k 2 [E] TOT k Vmax 2 = [E] TOT k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Tecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Tecnologie Biochimiche DISPENSA
Ioni inorganici (Mg 2+, Zn 2+ ), o molecole organiche o metallorganiche (coenzimi)
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione -
 Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione - esaminando il modo in cui il sito attivo favorisce la catalisi
Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione - esaminando il modo in cui il sito attivo favorisce la catalisi
CINETICA ENZIMATICA - velocità di reazione
 [P] Velocità iniziale (V 0 ) CINETICA ENZIMATICA - velocità di reazione + + k 1 E + S ES ES E + P k 2 k 3 k 4 V = d[p]/dt = k 3 [ES] Velocità iniziale (V 0 ) quando [S] >> [P] V max t CINETICA ENZIMATICA:
[P] Velocità iniziale (V 0 ) CINETICA ENZIMATICA - velocità di reazione + + k 1 E + S ES ES E + P k 2 k 3 k 4 V = d[p]/dt = k 3 [ES] Velocità iniziale (V 0 ) quando [S] >> [P] V max t CINETICA ENZIMATICA:
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi
 1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
A = εlc c = A/εl c = 0.2/38000 M -1 cm -1 1 cm c = M = 5 μm
 COME PROCEDO? Ho una soluzione di una proteina purificata Preparo un bianco con lo stesso tampone utilizzato per dissolvere la proteina Effettuo l azzeramento dello spettrofotometro con il bianco e poi
COME PROCEDO? Ho una soluzione di una proteina purificata Preparo un bianco con lo stesso tampone utilizzato per dissolvere la proteina Effettuo l azzeramento dello spettrofotometro con il bianco e poi
CLASSIFICAZIONE O.T.I.L.Is. Lig
 GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio
 Cinetica enzimatica Cenni alla cinetica delle reazioni Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio OVVERO: CINETICA ENZIMATICA LO
Cinetica enzimatica Cenni alla cinetica delle reazioni Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio OVVERO: CINETICA ENZIMATICA LO
costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più
 Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Fondamenti di Chimica Farmaceutica. Inibizione enzimatica
 Fondamenti di Chimica Farmaceutica Inibizione enzimatica Cinetica enzimatica E + S k 1 k 1 ES k2 E + P La reazione catalizzata dall enzima avviene in due passaggi: la formazione del complesso enzima-substrato:
Fondamenti di Chimica Farmaceutica Inibizione enzimatica Cinetica enzimatica E + S k 1 k 1 ES k2 E + P La reazione catalizzata dall enzima avviene in due passaggi: la formazione del complesso enzima-substrato:
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Chimica Biologica A.A Cinetica Enzimatica. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari
 Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari Assunzione di principio: i sistemi si trovano in condizioni di controllo termodinamico e non cinetico (tutti
Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari Assunzione di principio: i sistemi si trovano in condizioni di controllo termodinamico e non cinetico (tutti
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
Cinetica Chimica. Cinetica chimica
 Cinetica Chimica CH 3 Cl + NaOH CH 3 OH + NaCl Le reazioni chimiche possono decorrere con cinetica molto veloce (come le reazioni di salificazione di un acido con una base) o lenta (come alcune reazioni
Cinetica Chimica CH 3 Cl + NaOH CH 3 OH + NaCl Le reazioni chimiche possono decorrere con cinetica molto veloce (come le reazioni di salificazione di un acido con una base) o lenta (come alcune reazioni
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
La cinetica enzimatica
 La cinetica enzimatica Cinetica chimica All equilibrio Ordine di reazione I ordine II ordine Ordine zero La cinetica di una reazione chimica Cinetica di una reazione enzimatica Ordine 1 (enzima costante)
La cinetica enzimatica Cinetica chimica All equilibrio Ordine di reazione I ordine II ordine Ordine zero La cinetica di una reazione chimica Cinetica di una reazione enzimatica Ordine 1 (enzima costante)
TARGETS DEI FARMACI ATTUALMENTE IN USO
 TARGETS DEI FARMACI ATTUALMENTE IN USO INIBITORI ENZIMATICI INIBITORI ENZIMATICI Sintesi dell'uridine-5'-monophosphate (UMP) INIBITORI ENZIMATICI EFFICACIA DI INIBITORI COME AGENTI TERAPEUTICI Potenza
TARGETS DEI FARMACI ATTUALMENTE IN USO INIBITORI ENZIMATICI INIBITORI ENZIMATICI Sintesi dell'uridine-5'-monophosphate (UMP) INIBITORI ENZIMATICI EFFICACIA DI INIBITORI COME AGENTI TERAPEUTICI Potenza
Velocità di reazione. Consideriamo una generica reazione
 Velocità di reazione. Consideriamo una generica reazione Esprimiamo perciò la velocità di un processo chimico in un certo periodo di tempo tramite il rapporto tra la variazione di concentrazione di un
Velocità di reazione. Consideriamo una generica reazione Esprimiamo perciò la velocità di un processo chimico in un certo periodo di tempo tramite il rapporto tra la variazione di concentrazione di un
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione.
 Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
Reazioni lente e reazioni veloci
 CINETICA CHIMICA Reazioni lente e reazioni veloci Cinetica Chimica Studio della velocità di reazione (v) Che cos è la velocità di reazione? è la diminuzione della concentrazione molare del reagente nell
CINETICA CHIMICA Reazioni lente e reazioni veloci Cinetica Chimica Studio della velocità di reazione (v) Che cos è la velocità di reazione? è la diminuzione della concentrazione molare del reagente nell
di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori.
 Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
REGOLAZIONE DELL ATTIVITA ENZIMATICA 1) MODULAZIONE ALLOSTERICA NON-COVALENTE (REVERSIBILE)
 REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
1/v
 1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
Cine%ca enzima%ca. Copyright 2013 Zanichelli editore S.p.A.
 Cine%ca enzima%ca Copyright 2013 Zanichelli editore S.p.A. La cinetica delle reazioni Conce, chiave Le semplici equazioni di velocità descrivono il progredire delle reazioni di primo e di secondo ordine.
Cine%ca enzima%ca Copyright 2013 Zanichelli editore S.p.A. La cinetica delle reazioni Conce, chiave Le semplici equazioni di velocità descrivono il progredire delle reazioni di primo e di secondo ordine.
2) La presenza di gruppi funzionali specifici che partecipano alla catalisi (quelli delle catene laterali dei suoi residui amminoacidici e/o quelli
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
Esistono reazioni energeticamente favorite (ΔH<0) che non avvengono.es. C(diamante) à C(grafite)
 CINETICA CHIMICA Esistono reazioni energeticamente favorite (ΔH
CINETICA CHIMICA Esistono reazioni energeticamente favorite (ΔH
Velocità di reazione
 1 Velocità di reazione A B V = - d[a] dt = d[b] dt V= Velocità istantanea: coefficiente angolare della retta tangente alla curva in quel punto Quando t=0 la velocità istantanea sarà massima (V 0 ) 2 Energia
1 Velocità di reazione A B V = - d[a] dt = d[b] dt V= Velocità istantanea: coefficiente angolare della retta tangente alla curva in quel punto Quando t=0 la velocità istantanea sarà massima (V 0 ) 2 Energia
La velocità di reazione
 La velocità di reazione 1 Che cos è la velocità di reazione (I) Lo studio di tutti gli aspetti relativi alla velocità delle trasformazioni chimiche è affrontato dalla cinetica chimica. La velocità di reazione
La velocità di reazione 1 Che cos è la velocità di reazione (I) Lo studio di tutti gli aspetti relativi alla velocità delle trasformazioni chimiche è affrontato dalla cinetica chimica. La velocità di reazione
ENZIMI. Catalizzatori delle reazioni biologiche
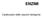 ENZIMI Catalizzatori delle reazioni biologiche I CATALIZZATORI ABBASSANO L ENERGIA DI ATTIVAZIONE FACILITANDO LA FORMAZIONE DELLO STATO DI TRANSIZIONE Il legame tra enzima e substrato genera un percorso
ENZIMI Catalizzatori delle reazioni biologiche I CATALIZZATORI ABBASSANO L ENERGIA DI ATTIVAZIONE FACILITANDO LA FORMAZIONE DELLO STATO DI TRANSIZIONE Il legame tra enzima e substrato genera un percorso
VELOCITA di REAZIONE. Quali sono le dimensioni di una velocità di reazione?? E una definizione che ha senso NON all equilibrio!!!
 VELOCITA di REAZIONE Quali sono le dimensioni di una velocità di reazione?? E una definizione che ha senso NON all equilibrio!!! Data la reazione: aa + bb cc + dd v = - 1 Δ[A] = - 1 Δ[B] = 1 Δ[C] = 1 Δ[D]
VELOCITA di REAZIONE Quali sono le dimensioni di una velocità di reazione?? E una definizione che ha senso NON all equilibrio!!! Data la reazione: aa + bb cc + dd v = - 1 Δ[A] = - 1 Δ[B] = 1 Δ[C] = 1 Δ[D]
2. Quale delle seguenti affermazioni relative ad una reazione enzimatica è vera?
 1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
In questo caso parliamo di un processo entalpico. Si tratta di un processo entalpico.
 LEZIONE DEL 10/04/2017 ENZIMOLOGIA - APPLICAZIONI DELLA CINETICA ENZIMATICA Essa trova applicazioni nel processamento dei rifiuti, nelle materie organiche. Si tratta dell'ingegnerizzazione dei processi
LEZIONE DEL 10/04/2017 ENZIMOLOGIA - APPLICAZIONI DELLA CINETICA ENZIMATICA Essa trova applicazioni nel processamento dei rifiuti, nelle materie organiche. Si tratta dell'ingegnerizzazione dei processi
Lezione n. 11. Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
La cinetica chimica. Si occupa dello studio dei meccanismi di reazione con i quali i reagenti si trasformano in prodotti (kinesis = movimento)
 La cinetica chimica Si occupa dello studio dei meccanismi di reazione con i quali i reagenti si trasformano in prodotti (kinesis = movimento) omogenee Reazioni eterogenee Termodinamica: permette di prevedere
La cinetica chimica Si occupa dello studio dei meccanismi di reazione con i quali i reagenti si trasformano in prodotti (kinesis = movimento) omogenee Reazioni eterogenee Termodinamica: permette di prevedere
Cinetica chimica MECCANISMO <<Lo studio CINETICO fornisce invece queste informazioni>>
 Cinetica chimica La termodinamica studia gli aspetti energetici di una reazione nel senso che stabilisce se, da un punto di vista energetico, la reazione potrà avvenire o no. Niente, invece, dice sul tempo
Cinetica chimica La termodinamica studia gli aspetti energetici di una reazione nel senso che stabilisce se, da un punto di vista energetico, la reazione potrà avvenire o no. Niente, invece, dice sul tempo
Cinetica di una reazione chimica. Studio della velocità con cui avviene una reazione e dei fattori che la influenzano.
 Cinetica di una reazione chimica Studio della velocità con cui avviene una reazione e dei fattori che la influenzano. RILEVANZA TEORICA: permette di ottenere informazioni sul meccanismo di reazione UTILITA
Cinetica di una reazione chimica Studio della velocità con cui avviene una reazione e dei fattori che la influenzano. RILEVANZA TEORICA: permette di ottenere informazioni sul meccanismo di reazione UTILITA
CINETICA CHIMICA E CATALISI
 CINETICA CHIMICA E CATALISI A (g) + B (g) AB (g) Reazione omogenea, irreversibile a T cost VELOCITA di REAZIONE : variazione, nell unità di tempo, della concentrazione delle sostanze reagenti A e B Tale
CINETICA CHIMICA E CATALISI A (g) + B (g) AB (g) Reazione omogenea, irreversibile a T cost VELOCITA di REAZIONE : variazione, nell unità di tempo, della concentrazione delle sostanze reagenti A e B Tale
Termochimica. La termochimica e la cinetica. Termochimica. Termochimica. Con il termine sistema s intende l oggetto di indagine.
 La termochimica e la cinetica Con il termine sistema s intende l oggetto di indagine. Tutto ciò che circonda il sistema costituisce l ambiente. I sistemi aperti scambiano energia e materia con l ambiente.
La termochimica e la cinetica Con il termine sistema s intende l oggetto di indagine. Tutto ciò che circonda il sistema costituisce l ambiente. I sistemi aperti scambiano energia e materia con l ambiente.
Cinetica chimica. Capitolo 13
 Cinetica chimica Capitolo 13 Cinetica chimica Termodinamica si verifica la reazione? Cinetica con che velocità si verifica la reazione? Velocità di reazione è la variazione di concentrazione di un reagente
Cinetica chimica Capitolo 13 Cinetica chimica Termodinamica si verifica la reazione? Cinetica con che velocità si verifica la reazione? Velocità di reazione è la variazione di concentrazione di un reagente
Analisi quantitativa dell interazione proteina-proteina
 Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
La via per accelerare i processi biologici
 La via per accelerare i processi biologici ENZIMI Sono delle proteine altamente specializzare con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa.
La via per accelerare i processi biologici ENZIMI Sono delle proteine altamente specializzare con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa.
Cinetica Chimica 07/01/2016
 Cinetica Chimica Rappresenta lo studio del modo in cui le reazioni vanno verso l equilibrio. Si misura la variazione nel tempo della concentrazione di prodotti e reagenti (velocità di reazione) e l effetto
Cinetica Chimica Rappresenta lo studio del modo in cui le reazioni vanno verso l equilibrio. Si misura la variazione nel tempo della concentrazione di prodotti e reagenti (velocità di reazione) e l effetto
INIBIZIONE ENZIMATICA REVERSIBILE
 INIBIZIONE ENZIMATICA REVERSIBILE La reazione enzimatica in vitro o in vivo può essere INIBITA REVERSIBILMENTE. Un inibitore (I) legandosi all enzima interferisce con la sua attività modificando la Vmax,
INIBIZIONE ENZIMATICA REVERSIBILE La reazione enzimatica in vitro o in vivo può essere INIBITA REVERSIBILMENTE. Un inibitore (I) legandosi all enzima interferisce con la sua attività modificando la Vmax,
TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA
 TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA Lo studio della cinetica enzimatica inizia nel 1909 con ADRIAN BROWN
TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA Lo studio della cinetica enzimatica inizia nel 1909 con ADRIAN BROWN
Cinetica chimica. Istantanea. Cinetica chimica : studio della velocita delle reazioni chimiche
 Cinetica chimica Cinetica chimica : studio della velocita delle reazioni chimiche La termodinamica ci dice se una reazione è possibile (termodinamicamente) ma non se è lenta o veloce. C diamante O g CO
Cinetica chimica Cinetica chimica : studio della velocita delle reazioni chimiche La termodinamica ci dice se una reazione è possibile (termodinamicamente) ma non se è lenta o veloce. C diamante O g CO
Appendice cap. 29: applicazioni
 2 Analisi chimica strumentale Appendice cap. 29: applicazioni Per una reazione del 1 ordine, l equazione differenziale, ovvero la forma differenziale della legge cinetica, assume la forma d[a]/dt = k [A]
2 Analisi chimica strumentale Appendice cap. 29: applicazioni Per una reazione del 1 ordine, l equazione differenziale, ovvero la forma differenziale della legge cinetica, assume la forma d[a]/dt = k [A]
ASPETTO TERMODINAMICO
 TUTTE LE REAZIONI CHE SCRIVIAMO SULLA CARTA, POSSONO AVVENIRE REALMENTE? ASPETTO TERMODINAMICO REAZIONI SPONTANEE E COMPLETE reazioni a favore dei prodotti es. 2 Na + 2 H 2 O 2 NaOH + H 2 REAZIONI CHE
TUTTE LE REAZIONI CHE SCRIVIAMO SULLA CARTA, POSSONO AVVENIRE REALMENTE? ASPETTO TERMODINAMICO REAZIONI SPONTANEE E COMPLETE reazioni a favore dei prodotti es. 2 Na + 2 H 2 O 2 NaOH + H 2 REAZIONI CHE
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
Cinetica chimica. studia l influenza di variabili quali T, concentrazione dei reattivi, natura solvente, pressione...
 Cinetica chimica la cinetica chimica studia la velocità delle reazioni chimiche e i meccanismi attraverso cui i reagenti si trasformano in prodotti studia l influenza di variabili quali T, concentrazione
Cinetica chimica la cinetica chimica studia la velocità delle reazioni chimiche e i meccanismi attraverso cui i reagenti si trasformano in prodotti studia l influenza di variabili quali T, concentrazione
PRINCIPALI CARATTERISTICHE DEGLI ENZIMI. 1) Aumentano la velocità di reazione. 2) Non modificano l equilibrio della reazione
 PRINCIPALI CARATTERISTICHE DEGLI ENZIMI 1) Aumentano la velocità di reazione 2) Non modificano l equilibrio della reazione S P 3) Presentano specificità di reazione 4) Richiedono condizioni di reazione
PRINCIPALI CARATTERISTICHE DEGLI ENZIMI 1) Aumentano la velocità di reazione 2) Non modificano l equilibrio della reazione S P 3) Presentano specificità di reazione 4) Richiedono condizioni di reazione
3) La presenza di gruppi funzionali specifici che partecipano alla catalisi (quelli delle catene laterali dei suoi residui amminoacidici e/o quelli
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
FUNZIONI BIOLOGICHE DELLE PROTEINE
 FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
FUNZIONI BIOLOGICHE DELLE PROTEINE ENZIMI PROTEINE DI TRASPORTO PROTEINE DI RISERVA PROTEINE CONTRATTILI PROTEINE DI DIFESA PROTEINE REGOLATRICI PROTEINE STRUTTURALI ENERGIA LIBERA (G) ΔG = ΔH - TΔS Variazioni
Cinetica Chimica 1. esaminare quali condizioni debbono essere soddisfatte affinché una data reazione avvenga spontaneamente 2. esaminare quali sono i
 Cinetica Chimica 1. esaminare quali condizioni debbono essere soddisfatte affinché una data reazione avvenga spontaneamente 2. esaminare quali sono i fattori che influenzano il tempo richiesto affinché
Cinetica Chimica 1. esaminare quali condizioni debbono essere soddisfatte affinché una data reazione avvenga spontaneamente 2. esaminare quali sono i fattori che influenzano il tempo richiesto affinché
CINETICA CHIMICA. Ogni reazione chimica però impiega un certo tempo per raggiungere le condizioni di equilibrio.
 Facendo reagire delle sostanze si arriva ad uno stato di equilibrio in cui le concentrazioni di reagenti e prodotto rispettano la legge di equilibrio chimico, definita da una costante di equilibrio. Ogni
Facendo reagire delle sostanze si arriva ad uno stato di equilibrio in cui le concentrazioni di reagenti e prodotto rispettano la legge di equilibrio chimico, definita da una costante di equilibrio. Ogni
Enzimi e loro ruolo nel metabolismo
 Enzimi e loro ruolo nel metabolismo Definizioni e ruoli degli enzimi Cinetica enzimatica Localizzazione degli enzimi Enzimi come bersaglio di farmaci Enzimi come markers in Biochimica Clinica Errori congeniti
Enzimi e loro ruolo nel metabolismo Definizioni e ruoli degli enzimi Cinetica enzimatica Localizzazione degli enzimi Enzimi come bersaglio di farmaci Enzimi come markers in Biochimica Clinica Errori congeniti
Regolazione dell attività enzimatica. Allosteria Modificazioni covalenti Isoenzimi
 Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Enzimi come catalizzatori biologici
 Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Limiti del criterio della variazione entropia
 Limiti del criterio della variazione entropia S universo = S sistema + S ambiente > 0 (nei processi irreversibili) S universo = S sistema + S ambiente = 0 (nei processi reversibili) Dalla valutazione di
Limiti del criterio della variazione entropia S universo = S sistema + S ambiente > 0 (nei processi irreversibili) S universo = S sistema + S ambiente = 0 (nei processi reversibili) Dalla valutazione di
Regolazione enzimatica Isoenzimi
 Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Regolazione enzimatica Isoenzimi Gli enzimi regolatori nel metabolismo gruppi di enzimi lavorano insieme per produrre una via metabolica in cui il prodotto del primo enzima diventa il substrato del secondo
Reazioni opposte. Reazioni opposte o reversibili A + B 2C (k 1 e k -1 )
 Reazioni complesse Reazioni opposte o reversibili A B ( e - ) Reazioni consecutive A B C ( e ) Reazioni competitive o parallele A B ( ) A C ( ) Reazioni opposte Reazioni opposte o reversibili A + B C (
Reazioni complesse Reazioni opposte o reversibili A B ( e - ) Reazioni consecutive A B C ( e ) Reazioni competitive o parallele A B ( ) A C ( ) Reazioni opposte Reazioni opposte o reversibili A + B C (
Casi più complicati. inibizione mista (competitiva e non competitiva)
 Casi più complicati inibizione mista (competitiva e non competitiva) reazioni reversibili reazioni a più substrati effetto del ph inibizione mista (competitiva e non competitiva) K I K I E + I EI ES +
Casi più complicati inibizione mista (competitiva e non competitiva) reazioni reversibili reazioni a più substrati effetto del ph inibizione mista (competitiva e non competitiva) K I K I E + I EI ES +
Per la stessa reazione possono essere utilizzati catalizzatori diversi. es. HCOOH H 2 + CO 2 viene catalizzata da Ni, Cd, Pt, Cu.
 CATALISI L'uso di un catalizzatore, sostanza capace di accelerare una reazione senza intervenire sulla T, è di enorme importanza in alcuni tipi di reazione. Ad esempio le proteine reagiscono velocemente
CATALISI L'uso di un catalizzatore, sostanza capace di accelerare una reazione senza intervenire sulla T, è di enorme importanza in alcuni tipi di reazione. Ad esempio le proteine reagiscono velocemente
IL METABOLISMO DEL GLICOGENO E FINEMENTE REGOLATO: Quando è attiva la sua sintesi non è attiva la sua demolizione e viceversa
 IL METABOLISMO DEL GLICOGENO E FINEMENTE REGOLATO: Quando è attiva la sua sintesi non è attiva la sua demolizione e viceversa Glucagone = innalza il livello ematico di glucosio Adrenalina = scatena una
IL METABOLISMO DEL GLICOGENO E FINEMENTE REGOLATO: Quando è attiva la sua sintesi non è attiva la sua demolizione e viceversa Glucagone = innalza il livello ematico di glucosio Adrenalina = scatena una
Chimica Fisica Biologica
 Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 20 La velocità di reazione 3 Sommario 1. Che cos è la velocità di reazione 2. L equazione cinetica 3. Gli altri fattori che influiscono
La velocità delle reazioni. Equilibrio chimico
 La velocità delle reazioni Equilibrio chimico Velocità di reazione È la velocità con cui i reagenti di una reazione si trasformano in prodotti nell unità di tempo Lo studio della velocità di reazione viene
La velocità delle reazioni Equilibrio chimico Velocità di reazione È la velocità con cui i reagenti di una reazione si trasformano in prodotti nell unità di tempo Lo studio della velocità di reazione viene
proteine enzimi RNA ribozimi substrati altamente specifici -asi
 I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
Studio della velocità delle reazioni ed interpretazione sulla base dei meccanismi di reazione
 Cinetica chimica Studio della velocità delle reazioni ed interpretazione sulla base dei meccanismi di reazione E anche importante conoscere il grado con cui la reazione favorisce i prodotti all equilibrio
Cinetica chimica Studio della velocità delle reazioni ed interpretazione sulla base dei meccanismi di reazione E anche importante conoscere il grado con cui la reazione favorisce i prodotti all equilibrio
INTRODUZIONE AI MODELLI MATEMATICI E NUMERICI PER LA CINETICA CHIMICA
 1 INTRODUZIONE AI MODELLI MATEMATICI E NUMERICI PER LA CINETICA CHIMICA a cura di P.Causin, M. Giaffredo, T. Motta Dipartimento di Matematica - Università degli Studi di Milano Immaginiamo un esperimento
1 INTRODUZIONE AI MODELLI MATEMATICI E NUMERICI PER LA CINETICA CHIMICA a cura di P.Causin, M. Giaffredo, T. Motta Dipartimento di Matematica - Università degli Studi di Milano Immaginiamo un esperimento
Cinetica chimica. 2 H 2 (g) + O 2 (g) 2 H 2 O (g)
 Cinetica chimica 2 H 2 (g) + O 2 (g) 2 H 2 O (g) Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione La cinetica chimica A differenza della termodinamica
Cinetica chimica 2 H 2 (g) + O 2 (g) 2 H 2 O (g) Alcune immagini sono state prese e modificate da Chimica di Kotz, Treichel & Weaver, Edises 2007, III edizione La cinetica chimica A differenza della termodinamica
12. CINETICA CHIMICA,
 . CINETICA CHIMICA, ovvero: un esempio di termodinamica di non equilibrio Semplificazione: reazione condotta in condizioni di ) equilibrio termico (temperatura costante) ) equilibrio meccanico (ad esempio
. CINETICA CHIMICA, ovvero: un esempio di termodinamica di non equilibrio Semplificazione: reazione condotta in condizioni di ) equilibrio termico (temperatura costante) ) equilibrio meccanico (ad esempio
Velocità di Reazione. H ICl I HCl
 Velocità di Reazione H 2 + 2 ICl I 2 + 2 HCl Cinetica Chimica ci dice se una reazione avviene spontaneamente. È indispensabile però sapere anche quanto impiega una reazione a raggiungere il proprio stato
Velocità di Reazione H 2 + 2 ICl I 2 + 2 HCl Cinetica Chimica ci dice se una reazione avviene spontaneamente. È indispensabile però sapere anche quanto impiega una reazione a raggiungere il proprio stato
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
LEZIONE 25: EMOGLOBINA L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 25_emoglobina 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata
Reazione di Briggs Rauscher
 Cinetica chimica 1 Reazione di Briggs Rauscher a) Come varia nel tempo la composizione chimica di un sistema? b) Qual è il meccanismo secondo cui avviene una reazione chimica? c) Come è possibile modificare
Cinetica chimica 1 Reazione di Briggs Rauscher a) Come varia nel tempo la composizione chimica di un sistema? b) Qual è il meccanismo secondo cui avviene una reazione chimica? c) Come è possibile modificare
CATALISI COVALENTE. H 2 O Enz-R-OH + P. Enz-R-O S Enz-R-O-S
 CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
CATALISI COVALENTE Comporta la formazione di intermedi in cui il substrato è legato covalentemente con un residuo amminoacidico del sito attivo dell enzima. La catena laterale re dell enzima può comportarsi
Esploriamo la chimica
 1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
1 Valitutti, Tifi, Gentile Esploriamo la chimica Seconda edizione di Chimica: molecole in movimento Capitolo 15 La termodinamica e la cinetica 1. Le reazioni producono energia 2. Il primo principio della
Laboratorio 29.1 CINETICA DI IDROLISI ALCALINA DELL ACETATO DI ETILE
 2 Analisi chimica strumentale Laboratorio 29.1 CINETICA DI IDROLISI ALCALINA DELL ACETATO DI ETILE SCOPO Determinazione della costante di velocità, dell energia di attivazione e del fattore di frequenza
2 Analisi chimica strumentale Laboratorio 29.1 CINETICA DI IDROLISI ALCALINA DELL ACETATO DI ETILE SCOPO Determinazione della costante di velocità, dell energia di attivazione e del fattore di frequenza
2 febbraio con 10 Pa, Pa, K, 1760 J mol e m mol. Con questi dati si ricava la temperatura finale. exp 422.
 febbraio 08. La temperatura di fusione dello zolfo monoclino alla pressione di un bar è 9.3 C. La variazione di volume molare durante la fusione è di.3 cm 3 mol -, mentre il calore latente di fusione è
febbraio 08. La temperatura di fusione dello zolfo monoclino alla pressione di un bar è 9.3 C. La variazione di volume molare durante la fusione è di.3 cm 3 mol -, mentre il calore latente di fusione è
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA
 Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
Corso di orientamento e preparazione ai Corsi di Laurea della Scuola di Medicina ad accesso programmato a.a. 2019/2020 CHIMICA «Nulla si crea, nulla si distrugge, ma tutto si trasforma.» (Antoine-Laurent
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Cinetica chimica. studia la velocità a cui decorrono le reazioni chimiche una velocità è la variazione di una proprietà per unità di tempo:
 Cinetica chimica Cosa è la velocità di reazione e fattori che la influenzano Effetto concentrazione e temperatura Equazione di Arrhenius Molecolarità reazione. Energia di attivazione e catalisi Cinetica
Cinetica chimica Cosa è la velocità di reazione e fattori che la influenzano Effetto concentrazione e temperatura Equazione di Arrhenius Molecolarità reazione. Energia di attivazione e catalisi Cinetica
ISIS A PONTI Gallarate
 4 A TCB 1 IL CROMATOGRAMMA: E il tracciato che descrive l andamento del segnale del rivelatore in funzione del tempo o del volume di eluente a partire dall istante in cui la miscela viene introdotta nella
4 A TCB 1 IL CROMATOGRAMMA: E il tracciato che descrive l andamento del segnale del rivelatore in funzione del tempo o del volume di eluente a partire dall istante in cui la miscela viene introdotta nella
ESERCIZI ESERCIZI. 3) Data la reazione chimica: H 2
 ESERCIZI 1) La velocità di una reazione chimica dipende: a. solo dalla temperatura b. solo dalla pressione c. dal fatto che la reazione sia eso- o endotermica d. dalla temperatura, dalle concentrazioni
ESERCIZI 1) La velocità di una reazione chimica dipende: a. solo dalla temperatura b. solo dalla pressione c. dal fatto che la reazione sia eso- o endotermica d. dalla temperatura, dalle concentrazioni
Cinetica chimica. Fattori che influenzano la velocità di reazione. Espressione della velocità di reazione. Legge cinetica e le sue componenti
 Cinetica chimica Fattori che influenzano la velocità di reazione Espressione della velocità di reazione Legge cinetica e le sue componenti Effetto della temperatura sulla velocità di reazione Velocità
Cinetica chimica Fattori che influenzano la velocità di reazione Espressione della velocità di reazione Legge cinetica e le sue componenti Effetto della temperatura sulla velocità di reazione Velocità
Biosensori.
 Biosensori nicola.carbonaro@centropiaggio.unipi.it Biosensori Definizione Un biosensore è un dispositivo di misura che utilizza un recettore biologico (o un suo derivato sintetico ) associato ad un trasduttore
Biosensori nicola.carbonaro@centropiaggio.unipi.it Biosensori Definizione Un biosensore è un dispositivo di misura che utilizza un recettore biologico (o un suo derivato sintetico ) associato ad un trasduttore
La cinetica enzimatica: Calcolo della K m e V max
 La cinetica enzimatica: Calcolo della K m e V max Parametri cinetici K m (numericamente uguale alla concentrazione di substrato alla quale la velocità iniziale è pari alla metà della velocità massima)
La cinetica enzimatica: Calcolo della K m e V max Parametri cinetici K m (numericamente uguale alla concentrazione di substrato alla quale la velocità iniziale è pari alla metà della velocità massima)
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO
 L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
L EMOGLOBINA ED IL TRASPORTO DI OSSIGENO Lezione 23 1 Concentrazione di O 2 nel plasma Il contenuto totale di O2 nel sangue è pari alla quantità disciolta più quella legata all emoglobina: L O 2 totale
ESERCITAZIONI CHIMICA-FISICA I a.a. 2012/2013. Metodo differenziale. Problema
 ESERCITAZIONI CHIMICA-FISICA I a.a. 0/03 Metodo differenziale Problema Per la reazione: A + B P sono stati condotti tre esperimenti cinetici a diverse concentrazioni iniziali dei reagenti. I valori iniziali
ESERCITAZIONI CHIMICA-FISICA I a.a. 0/03 Metodo differenziale Problema Per la reazione: A + B P sono stati condotti tre esperimenti cinetici a diverse concentrazioni iniziali dei reagenti. I valori iniziali
TERMODINAMICA I PRINCIPIO DELLA TERMODINAMICA DU = Q - W
 TERMODINAMICA Scambi di CALORE e LAVORO tra: SISTEMA AMBIENTE UNIVERSO APERTO SCAMBIA ENERGIA E MATERIA SISTEMA CHIUSO SCAMBIA ENERGIA, NON MATERIA ISOLATO NON SCAMBIA ENERGIA NE MATERIA ENERGIA INTERNA
TERMODINAMICA Scambi di CALORE e LAVORO tra: SISTEMA AMBIENTE UNIVERSO APERTO SCAMBIA ENERGIA E MATERIA SISTEMA CHIUSO SCAMBIA ENERGIA, NON MATERIA ISOLATO NON SCAMBIA ENERGIA NE MATERIA ENERGIA INTERNA
Attività sperimentale da laboratorio sul ciclo CaO-CaCO3 per la cattura della CO2 ad alta temperatura
 COPERTINA DEF2009-26.RdS:Layout 1 19-06-2009 12:25 Pagina 1 Attività sperimentale da laboratorio sul ciclo CaO-CaCO3 per la cattura della CO2 ad alta temperatura A. Calabrò, S. Stendardo Report RSE/2009/26
COPERTINA DEF2009-26.RdS:Layout 1 19-06-2009 12:25 Pagina 1 Attività sperimentale da laboratorio sul ciclo CaO-CaCO3 per la cattura della CO2 ad alta temperatura A. Calabrò, S. Stendardo Report RSE/2009/26
Energia di Gibbs. introduciamo una nuova funzione termodinamica così definita. energia di Gibbs ( energia libera)
 a, costanti Energia di Gibbs dh ds 0 dh ds 0 introduciamo una nuova funzione termodinamica così definita G = H S energia di Gibbs ( energia libera) Se lo stato del sistema cambia e è costante allora la
a, costanti Energia di Gibbs dh ds 0 dh ds 0 introduciamo una nuova funzione termodinamica così definita G = H S energia di Gibbs ( energia libera) Se lo stato del sistema cambia e è costante allora la
