ENZIMI. Catalizzatori delle reazioni biologiche
|
|
|
- Federigo Capone
- 5 anni fa
- Visualizzazioni
Transcript
1 ENZIMI Catalizzatori delle reazioni biologiche
2 I CATALIZZATORI ABBASSANO L ENERGIA DI ATTIVAZIONE FACILITANDO LA FORMAZIONE DELLO STATO DI TRANSIZIONE Il legame tra enzima e substrato genera un percorso di reazione caratterizzato da uno stato di transizione con una energia libera più bassa rispetto a quella priva di enzima
3 Ogni reazione è costituita da una serie di tappe in cui si ha la formazione e la scomparsa di varie specie chimiche transitorie specie che occupano livelli di minimi energetici E+S ES EP E+P
4 . L energia di legame ΔG B generata dalle interazioni deboli che l enzima stabilisce con il substrato nello stato di transizione è la fonte principale di energia libera usata dall enzima per abbassare l energia di attivazione
5 Le tre proprietà distintive degli enzimi sono A capacità catalitica B specificità C regolazione
6
7
8 Il citrato viene isomerizzato ad isocitrato dall ACONITASI che catalizza una reazione di deidratazione e di una successiva idratazione ΔG =5 kj mole -1
9 i Citrato molecola prochiralica: contiene due gruppi carbossimetilici che non risultano equivalenti se la molecola viene posta in uno stampo asimmetrico l aconitasi riesce a distinguere i due gruppi carbossimetilici poiché il substrato può legarsi con l enzima solo in un modo solo uno dei due gruppi CH 2 COO - può reagire e formare isocitrato.
10 NOMENCLATURA Gli enzimi sono classificati in base alle reazioni che catalizzano e sono divisi in 6 classi
11 numero classe Reazione catalizzata 1 ossidoreduttasi Reazioni di ossidoriduzone 2 Transferasi Reazione di trasferimento di gruppi funzionali 3 Idrolasi Reazione di idrolisi 4 Liasi Addizione rimozione di gruppichimici: possono agire sui legami del C-C (decarbossilasi, aldolasi), C-O (idratasi, deidratasi) o, C-S (desulfidrasi). 5 Isomerasi Trasferimento di gruppi all interno di molecole per formare isomeri 6 Ligasi Formazione di legami C-C, C-S, C-O, C-N accoppiate all idrolisi di ATP
12 Ogni enzima ha un numero di classificazione a quattro cifre e un nome sistematico ATP + D-glucosio ADP + D-glucosio 6P Nome sistematico glucoso fosfotransferasi Numero di classificazione E.C classe Transferasi 7 sottoclasse fosfotransferasi 1 Sotto sotto classe fosfotransferasi con un gruppo ossidrilico come accettore 1 numero dell enzima nella sotto-sotto classe
13 Cinetica enzimatica
14 1902 Adrian Brown dimostrò che quando la concentrazione del saccarosio è molto più alta di quella dell enzima, la velocità della reazione diventa indipendente da quella del substrato: la velocità è di ORDINE ZERO rispetto al saccarosio
15 MICHAELIS-MENTEN (1913) V 0 = k 2 [ES] Per semplicità matematica si assume k-2 trascurabile k 1 e k -1 >>k 2 (ipotesi dell equilibrio ES è in equilibrio rapido con E ed S)
16 MICHAELIS E MENTEN (1913) Assunzione di equilibrio Leonor Michaelis e Maude Menten, assunsero che k-1>>k2, cioè che la prima tappa della reazione potesse raggiungere l equilibrio K-1 = K S = [E] [S] [ES] k1 E+S ES E+P k-1 k2
17 Assunzione di stato stazionario d[es]/dt = 0 [S]>>[E]
18 EQUAZIONE DI MICHAELIS-MENTEN Ipotesi dell equilibrio Ipotesi dello stato stazionario k1 k2 E+S ES E+P V 0 = k 2 [ES] [S]>>[E] K-1 Velocità di formazione =Velocità di scissione Velocità di formazione di ES = k 1 [E] [S] Velocità di scissione di ES= k 2 [E S] +k -1 [ES]
19 Velocità di formazione di [ES] = velocità di scissione di [ES] k 1 [E] [S] = k 2 [E S] +k -1 [ES ] [S]>>[E] k1[e] [S]= [E S] (k2 +k-1) [E] [S]= [E S] (k2 +k-1) / k1 K M = (k2 +k-1)/ k1 costante di Michaelis Menten [E S] = [E] [S]/ K M [E] = [Et] - [E S] [E S] = ([Et] - [E S]) [S]/ K M K M [E S] = [Et] [S]] - [E S] [S] [E S] (K M + [S]) = [Et ][S] [E S] = [Et] [S ] K M + [S ]
20 [E S] = [Et] [S ] V 0 = k 2 [ES] K M + [S ] V 0 = k 2 [Et] [S ] K M + [S ] V max = k 2 [Et] V 0 = V max [S ] EQUAZIONE DI MICHAESIS MENTEN K M + [S ]
21 Questa equazione verifica i dati cinetici v max [S] V 0 = K M + [S] S >> K M v max [S] V 0 = K M + [S] Cioè V 0 è indipendente dalla [[S] S << K M v max [S] V 0 = K M + [S] V è proporzionale alla [S]
22 A Significato K M v max [S] V 0 = K M + [S] V 0 =1/2 V max K M = S Il valore di K M dipende dal substrato e dalle condizioni di reazione ph, T forza ionica. E variabile da 10-1 M a 10-7 M
23 B Significato della K M k1 k2 E+S ES E+P K M = (k 2 +k -1 )/ k 1 K-1 k 2 << k -1 k -1 /k 1 = Ks Ks = [E][S] = k -1 / k 1 [ES] K M = alla costante di dissociazione del complesso quindi è la misura della forza del complesso
24 Vmax = numero di molecole di substrato convertite in prodotto nell unità di tempo quando l enzima è completamente saturato Si esprime in concentrazione per unità di tempo (M s-1) E direttamente proporzionale alla concentrazione dell enzima usato V max = K cat [Et] numero di turnover o costante catalitica Kcat =numero di reazioni effettuati dall enzima nell unità di tempo Si esprime con il reciproco del tempo (s-1) E indipendente dalla concentrazione dell enzima Kcat = V max /[Et]
25
26 Costante di specificità K cat /K M È il rapporto tra la frequenza con cui l enzima catalizza la reazione e l affinità per il suo substrato Si esprime come il reciproco della concentrazione e il reciproco del tempo M-1 s-1 Non può essere superiore a k1 [S]<<K M Vo = k 2.Et.[S] K M Et = E Vo = k cat.e.[s] K M v max [S] V 0 = K M + [S] k1 E+S ES E+P K-1 k2 Vo = k cat /K M.[E].[S] K cat K M = costante di specificità misura dell efficienza catalitica dell interazione di S ed E In queste condizioni la costante di specificità è la costante di velocità usata per misurare l efficienza catalitica dell interazione S ed E
27 K cat K M È una misura dell efficienza catalitica dell enzima Qual è il limite superiore dell efficienza catalitica degli enzimi? K cat K 2 K 1 = K M K -1 +K 2 K 2 >> K -1 K cat K M = K 1 K 1 non può essere più grande della frequenza con cui le molecole di enzima e substrato arrivano a collisione in soluzione Questo limite controllato dalla diffusione varia da M -1 s -1
28 ENZIMI IL CUI VALORE K cat /k M È CONTROLLATO DALLA DIFFUSIONE ( M -1 s -1) Enzimi che hanno raggiunto la perfezione cinetica
29
30 Grafico dei doppi reciproci o di Lineweaver-Burk v max [S] V 0 = K M + [S] 1 K M = ( ) V 0 v max [S] v max
31 Inibizione reversibile: Competitiva Incompetitiva Mista o non competitiva
32
33 INIBIZIONE COMPETITIVA v max [S] V 0 = α K M + [S]
34
35
36
37 Inibizione incompetitiva
38 Inibizione incompetitiva L inibitore si lega al complesso enzima substrato ed influenza l attività catalitica ma non il legame con il substrato
39 Un esempio di inibizione incompetitiva è quella operata dal valproato sull acil CoA sintetasi
40 INIBIZIONE MISTA Gli inibitori interferiscono sia con il legame del substrato sia con l attività catalitica K I = [E] [I]/ [EI] K i K I = [ES] [I]/ [ESI] α=1+[i]/ Kì α'=1+[i]/ Kì
41 v max [S] V 0 = α K M + α [S] α α
42
43 Inibizione non competitiva
44
45 INIBIZIONE IRREVERSIBILE Reagenti gruppo specifici Analoghi del substrato Inibitori suicidi
46 Inibitori suicidi :sfruttano il meccanismo d azione dell enzima Sono analoghi del substrato che vengono inizialmente processati con il normale meccanismo catalitico Questo crea un intermedio chimicamente attivo che modifica covalentemente e inattiva l enzima
47
48
49
50 Come si ricavano sperimentalmente i parametri cinetici? v max [S] V 0 = K M + [S]
51 CONDIZIONI SPERIMENTALI DEL SAGGIO Controllo del ph con una soluzione tampone Controllo della temperatura Assenza di inibitori (agenti chelanti, metalli) In un saggio di attività enzimatica in genere si misura il prodotto della reazione, piuttosto che il consumo di substrato Saggi continui e discontinui
52 i Saggi continui Sono più accurati e meno laboriosi di quelli discontinui usano lo spettrofotometro Saggi diretti E + S E + P (prodotto colorato (fluorescente) cromoforo )
53 Saggi accoppiati Aspartico amminotrasferasi Malico Deidrogenasi OSSALACETATO + NADH NAD+ + MALATO
54 A NADH A340nm lunghezza d onda nm Tempo s vi (μm min-1) [S] (mm)
55 Saggi discontinui: 1)Durante la reazione non si formano o consumano cromofori o fluorofori e le condizioni per far sviluppare colore o fluorescenza sono diverse da quelle del saggio. 2) Non è possibile far sviluppare colore o fluorescenza. La misura del prodotto o del substrato (consumato) devono essere fatte con altri sistemi, ad esempio HPLC, saggi biologici o immunologici. 3) Presenza di un fondo ( background ) elevato; ad esempio di assorbanza dovuta alle proteine in un estratto crudo o di altre molecole che assorbono alla lunghezza d onda che a noi interessa. In questo caso dobbiamo condurre il saggio e poi eliminare la fonte di disturbo.
56
57
58
59 PPi pirofosfatasi 2Pì 2Pi pirofosfatasi
60 * 1 Hubei Key Laboratory of Genetic Regulation & Integrative Preparazione retta di taratura
61
62
63 Reazioni a due substrati A+B P+Q Reazioni sequenziali o a spostamento singolo (si forma un complesso ternario) meccanismo ordinato: il legame del primo substrato è necessario affinché l enzima possa formare il sito di legame per il secondo substrato meccanismo casuale: entrambi i siti di legame sono presenti nell enzima libero
64 Reazioni a ping-pong (non si forma un complesso ternario) Reazioni di trasferimento Si forma un complesso ES, l enzima viene modificato E a causa del trasferimento di un gruppo; viene allontanato dal complesso il primo prodotto P1, l enzima modificato genera un secondo complesso E S2 con il secondo substrato, viene rilasciato il secondo prodotto P2 e l enzima ritorna libero E
65 Meccanismo a ping pong 1 v 0 K M (A) = [Vmax [A] + K M (B) Vmax [B] + 1 V max [B] [A]
66 Reazioni sequenziali
67 Discriminazione tra meccanismi sequenziali casuali o ordinati Inibizione da prodotto Se alla miscela di reazione viene aggiunto solo uno dei prodotti la reazione non può tornare indietro ma legandosi all enzima questo inibirà la reazione Meccanismo molecolare ordinato L aggiunta del secondo prodotto Q compete con il primo substrato per il legame all enzima fungendo da inibitore competitivo mentre l aggiunta del prodotto P che si combina solo con EQ funziona da inibitore misto di A quando B è mantenuto costante e inibitore misto di B quando A è mantenuto costante Meccanismo casuale Poiché entrambi i substrati e i prodotti possono legarsi direttamente ad E sia P che Q sono inibitori competitivi
68
69
70
71
72
73 Metodi a mescolamento rapido Flusso continuo: le soluzioni dell enzima e del substrato sono introdotte mediante siringhe in una camera di mescolamento La miscela viene pompata ad una velocità prestabilita Il tempo di reazione viene calcolato dal punto di mescolamento al punto di osservazione variando il flusso si possono variare i tempi di reazione e calcolare direttamente le costanti cinetiche
74 Metodo a flusso interrotto Enzima e substrato inizialmente in siringhe separate vengono rilasciati attraverso una camera di miscelazione in una terza siringa detta di bloccaggio. Ciò permette ad un rivelatore di iniziare l analisi nel tubo che connette la camera di miscelazione con la siringa di bloccaggio Si possono facilmente raggiungere velocità di 1000 cm/sec cioè il sistema rivela una miscela vecchia di 1ms sorgente
75 Metodo a smorzamento In questa tecnica i reagenti provenienti dalla camera di mescolamento sono trattati con un agente di smorzamento che blocca la reazione che verrà poi analizzata per valutare la formazione degli intermedi Svantaggio è il tempo morto che è determinato dal tempo di mescolamento
76 Metodi di rilassamento Si allestisce prima una miscela all equilibrio, poi si altera la posizione dell equilibrio variando le condizioni della reazione( temperatura pressione) Il tempo di rilassamento (velocità con la quale il sistema raggiunge il nuovo equilibrio) è inversamente proporzionale alla costante di velocità della reazione
ENZIMI. Catalizzatori delle reazioni biologiche
 ENZIMI Catalizzatori delle reazioni biologiche Le tre proprietà distintive degli enzimi sono A capacità catalitica B specificità C regolazione NOMENCLATURA Gli enzimi sono classificati in base alle reazioni
ENZIMI Catalizzatori delle reazioni biologiche Le tre proprietà distintive degli enzimi sono A capacità catalitica B specificità C regolazione NOMENCLATURA Gli enzimi sono classificati in base alle reazioni
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30)
 TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
TEORIA DELLO STATO DI TRANSIZIONE (Henry Eyring anni 30) A + B-C A-B + C (A B C) Complesso attivato Stato di transizione Coordinata di reazione H A H B + H C H A + H B H C A+ K B X k' P + Q [ P] d dt =
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi
 1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
1. Ossidoreduttasi 2. Transferasi 3. Idrolasi 4. Liasi 5. Isomerasi 6. Ligasi ATP + glucosio glucochinasi ADP + glucosio-6-p E.C 2.7.1.2 glucochinasi E.C 2.7.1.1 esochinasi Energia libera,g S k 1 k 1 =
Prof. Maria Nicola GADALETA
 Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Tecnologie Biochimiche DISPENSA
Prof. Maria Nicola GADALETA E-mail: m.n.gadaleta@biologia.uniba.it Facoltà di Scienze Biotecnologiche Corso di Laurea in Biotecnologie Sanitarie e Farmaceutiche Biochimica e Tecnologie Biochimiche DISPENSA
Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi)
 ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
ENZIMI Gli enzimi sono i catalizzatori dei processi biologici. Possono essere proteine globulari oppure acidi nucleici (ribozimi) Sono in grado di aumentare la velocità dei processi catalizzati fino a
CINETICA ENZIMATICA - velocità di reazione
 [P] Velocità iniziale (V 0 ) CINETICA ENZIMATICA - velocità di reazione + + k 1 E + S ES ES E + P k 2 k 3 k 4 V = d[p]/dt = k 3 [ES] Velocità iniziale (V 0 ) quando [S] >> [P] V max t CINETICA ENZIMATICA:
[P] Velocità iniziale (V 0 ) CINETICA ENZIMATICA - velocità di reazione + + k 1 E + S ES ES E + P k 2 k 3 k 4 V = d[p]/dt = k 3 [ES] Velocità iniziale (V 0 ) quando [S] >> [P] V max t CINETICA ENZIMATICA:
ENZIMI. Un enzima è un catalizzatore (acceleratore) di reazioni biologiche.
 ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
ENZIMI ENZIMI Un enzima è un catalizzatore (acceleratore) di reazioni biologiche. Catalizzatore = sostanza in grado di accelerare lo svolgimento di una reazione chimica e quindi di aumentarne la sua velocità,
k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
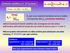 Costante catalitica o n di Turnover k 1 k 2 S + E ES E + P k -1 Vmax = k 2 [ES] = k 2 [E] TOT k Vmax 2 = [E] TOT k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
Costante catalitica o n di Turnover k 1 k 2 S + E ES E + P k -1 Vmax = k 2 [ES] = k 2 [E] TOT k Vmax 2 = [E] TOT k 2 per una reazione semplice ad uno stadio corrisponde alla k cat (costante catalitica)
GLI ENZIMI: proteine con attività CATALITICA
 Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Cap. 6 GLI ENZIMI: proteine con attività CATALITICA Catalizzatori biologici: permettono alle reazioni biochimiche di avvenire a temperature e pressioni fisiologiche e a velocità misurabile. Aumentano la
Fondamenti di Chimica Farmaceutica. Inibizione enzimatica
 Fondamenti di Chimica Farmaceutica Inibizione enzimatica Cinetica enzimatica E + S k 1 k 1 ES k2 E + P La reazione catalizzata dall enzima avviene in due passaggi: la formazione del complesso enzima-substrato:
Fondamenti di Chimica Farmaceutica Inibizione enzimatica Cinetica enzimatica E + S k 1 k 1 ES k2 E + P La reazione catalizzata dall enzima avviene in due passaggi: la formazione del complesso enzima-substrato:
Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione -
 Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione - esaminando il modo in cui il sito attivo favorisce la catalisi
Il meccanismo d azione degli enzimi può essere trattato: -analizzando i cambiamenti energetici che si verificano nel corso della reazione - esaminando il modo in cui il sito attivo favorisce la catalisi
v = Δ[P] = _ Δ[S] S P
![v = Δ[P] = _ Δ[S] S P v = Δ[P] = _ Δ[S] S P](/thumbs/98/137173050.jpg) CINETICA ENZIMATICA Gli esperimenti di cinetica enzimatica si basano sulla determinazione della velocità di reazione, misurata come variazione della concentrazione del prodotto o del reagente in un dato
CINETICA ENZIMATICA Gli esperimenti di cinetica enzimatica si basano sulla determinazione della velocità di reazione, misurata come variazione della concentrazione del prodotto o del reagente in un dato
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA
 TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA Lo studio della cinetica enzimatica inizia nel 1909 con ADRIAN BROWN
TUTTI GLI ENZIMI POSSONO ESSERE ANALIZZATI IN MODO DA POTER QUANTIFICARE SIA LA VELOCITA DI REAZIONE CHE LA LORO EFFICIENZA ENZIMATICA Lo studio della cinetica enzimatica inizia nel 1909 con ADRIAN BROWN
ENZIMI. Durante la reazione l enzima può essere temporaneamente modificato ma alla fine del processo ritorna nel suo stato originario, un enzima viene
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari, e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
CLASSIFICAZIONE O.T.I.L.Is. Lig
 GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
GLI ENZIMI CHE COSA SONO? Sono delle proteine altamente specializzate con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa. CLASSIFICAZIONE O.T.I.L.Is.
Chimica Biologica A.A Cinetica Enzimatica. Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano
 Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
Chimica Biologica A.A. 2010-2011 Cinetica Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Cinetica Chimica Termodinamica: fornisce
di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori.
 Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Enzimi Con l eccezione l di piccoli gruppi di molecole di RNA catalitico tutti gli enzimi sono proteine Molti enzimi per poter funzionare richiedono la presenza di cofattori. apoenzima + cofattore = oloenzima
Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio
 Cinetica enzimatica Cenni alla cinetica delle reazioni Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio OVVERO: CINETICA ENZIMATICA LO
Cinetica enzimatica Cenni alla cinetica delle reazioni Velocita di reazione Reazioni di I e II ordine Molecolarita di una reazione t 1/2 Velocita e costanti di equilibrio OVVERO: CINETICA ENZIMATICA LO
TARGETS DEI FARMACI ATTUALMENTE IN USO
 TARGETS DEI FARMACI ATTUALMENTE IN USO INIBITORI ENZIMATICI INIBITORI ENZIMATICI Sintesi dell'uridine-5'-monophosphate (UMP) INIBITORI ENZIMATICI EFFICACIA DI INIBITORI COME AGENTI TERAPEUTICI Potenza
TARGETS DEI FARMACI ATTUALMENTE IN USO INIBITORI ENZIMATICI INIBITORI ENZIMATICI Sintesi dell'uridine-5'-monophosphate (UMP) INIBITORI ENZIMATICI EFFICACIA DI INIBITORI COME AGENTI TERAPEUTICI Potenza
Gli enzimi e l inibizione enzimatica.
 Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi e l inibizione enzimatica. Catalisi enzimatica La velocità di una reazione è descritta dall equazione di Arrhenius: k = Ae -Ea/RT in cui A è il fattore pre-esponenziale R è la costante dei gas
Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi.
 ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
ENZIMI Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. Svolgono il loro ruolo con modalità differenti
Enzimi come catalizzatori biologici
 Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Enzimi come catalizzatori biologici Gli enzimi sono molecole proteiche aventi il compito di catalizzare praticamente tutte le reazioni chimiche che avvengono negli organismi viventi. La catalisi procede
Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe. Substrato
 Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe Substrato Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER, Zanichelli editore S.p.A. Copyright 2014 6 11
Se il sito attivo fosse perfettamente complementare al substrato la reazione non procederebbe Substrato Nelson Cox, I PRINCIPI DI BIOCHIMICA DI LEHNINGER, Zanichelli editore S.p.A. Copyright 2014 6 11
BIOCHIMICA APPLICATA e CLINICA
 BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
BIOCHIMICA APPLICATA e CLINICA Regolazione Enzimatica Biosegnalazione Regolazione Ormonale Specializzazioni metaboliche (Biochimica d Organo) Integrazione del metabolismo BIOCHIMICA APPLICATA e CLINICA
Determinazione dell attività enzimatica
 Determinazione dell attività enzimatica Gli enzimi sono una percentuale rilevante delle proteine cellulari anche se ciascun tipo di enzima è presente nella cellula in quantità molto bassa. Controllano
Determinazione dell attività enzimatica Gli enzimi sono una percentuale rilevante delle proteine cellulari anche se ciascun tipo di enzima è presente nella cellula in quantità molto bassa. Controllano
REAZIONI CHIMICHE. Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: I reagenti (substrati) devono entrare in collisione
 ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
ENZIMI : catalizzatori biologici
 ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
Ioni inorganici (Mg 2+, Zn 2+ ), o molecole organiche o metallorganiche (coenzimi)
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari e lavorano in condizioni blande di temperatura e ph (sono in grado di aumentare la velocità delle
2) La presenza di gruppi funzionali specifici che partecipano alla catalisi (quelli delle catene laterali dei suoi residui amminoacidici e/o quelli
 ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
ENZIMI Tutti gli enzimi sono PROTEINE che funzionano da catalizzatori biologici nelle reazioni cellulari (sono in grado di aumentare la velocità delle reazioni biologiche anche di 10 20 volte). Durante
Scaricato da 1
 A AB B Scaricato da www.sunhope.it 1 1 1 1 2 2 2 3 45 5 5 4 20 20 5 40 40 6 40 20 23 7 5 12 8 35 2 6 9 1 1 Numero di mole ecole 30 25 20 15 10 5 0 0 2 4 6 8 10 Energia Scaricato da www.sunhope.it 2 Scaricato
A AB B Scaricato da www.sunhope.it 1 1 1 1 2 2 2 3 45 5 5 4 20 20 5 40 40 6 40 20 23 7 5 12 8 35 2 6 9 1 1 Numero di mole ecole 30 25 20 15 10 5 0 0 2 4 6 8 10 Energia Scaricato da www.sunhope.it 2 Scaricato
REAZIONI CHIMICHE. Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: I reagenti (substrati) devono entrare in collisione
 ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
ENZIMI 1 REAZIONI CHIMICHE Perché una reazione chimica avvenga devono essere soddisfatte tre condizioni: 2 I reagenti (substrati) devono entrare in collisione Le collisione tra le molecole dei reagenti
costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più
 Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
Cinetica Enzimatica OBIETTIVO PRINCIPALE: costruire un equazione che potesse descrivere in generale il comportamento cinetico degli enzimi e quindi di determinare parametri cinetici più importanti (K M,
2. Quale delle seguenti affermazioni relative ad una reazione enzimatica è vera?
 1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
1. Gli enzimi agendo come catalizzatori: a) innalzano l'energia di attivazione b) innalzano il livello energetico dei prodotti c) abbassano il livello energetico dei reagenti d) diminuiscono l'energia
Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari
 Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari Assunzione di principio: i sistemi si trovano in condizioni di controllo termodinamico e non cinetico (tutti
Trattamento quantitativo della complessazione e della reattività nei sistemi supramolecolari Assunzione di principio: i sistemi si trovano in condizioni di controllo termodinamico e non cinetico (tutti
Funzioni dei nucleotidi
 Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Funzioni dei nucleotidi monomeri degli acidi nucleici esempi di altre funzioni ATP: moneta energetica GTP: fonte di energia nella sintesi proteica camp: secondo messaggero nella trasduzione del segnale
Enzimi e loro ruolo nel metabolismo
 Enzimi e loro ruolo nel metabolismo Definizioni e ruoli degli enzimi Cinetica enzimatica Localizzazione degli enzimi Enzimi come bersaglio di farmaci Enzimi come markers in Biochimica Clinica Errori congeniti
Enzimi e loro ruolo nel metabolismo Definizioni e ruoli degli enzimi Cinetica enzimatica Localizzazione degli enzimi Enzimi come bersaglio di farmaci Enzimi come markers in Biochimica Clinica Errori congeniti
Cine%ca enzima%ca. Copyright 2013 Zanichelli editore S.p.A.
 Cine%ca enzima%ca Copyright 2013 Zanichelli editore S.p.A. La cinetica delle reazioni Conce, chiave Le semplici equazioni di velocità descrivono il progredire delle reazioni di primo e di secondo ordine.
Cine%ca enzima%ca Copyright 2013 Zanichelli editore S.p.A. La cinetica delle reazioni Conce, chiave Le semplici equazioni di velocità descrivono il progredire delle reazioni di primo e di secondo ordine.
Chimica Fisica Biologica
 Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Chimica Fisica Biologica Università degli Studi di Padova Variazione della concentrazione [1] La variazione nel tempo della composizione di un sistema oggetto della cinetica chimica Le concentrazione delle
Gli enzimi e la catalisi
 Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Gli enzimi e la catalisi Distribuzione di energia in una popolazione di molecole Normalmente, le molecole stabili sono per lo più presenti ad un livello di energia relativamente basso Solo una piccola
Inibizione Enzimatica
 Chimica Biologica A.A. 2010-2011 Inibizione Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Inibizione enzimatica Inibitori: sostanze che riducono l
Chimica Biologica A.A. 2010-2011 Inibizione Enzimatica Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Inibizione enzimatica Inibitori: sostanze che riducono l
1/v
 1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
1. Nel seguente grafico sono descritti i risultati di cinetica enzimatica ottenuti in 3 esperimenti condotti in assenza di inibitori e in presenza di un inibitore a due diverse concentrazioni. a) Individuare
Lezione n. 11. Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T. Antonino Polimeno 1
 Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
Chimica Fisica Biotecnologie sanitarie Lezione n. 11 Reazioni enzimatiche Michaelis-Menten Dipendenza di k da T Antonino Polimeno 1 senza catalizzatore... con catalizzatore... Antonino Polimeno 2 Catalisi
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia.
 La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
La glicolisi non è l unica via catabolica in grado di produrre energia. Se il suo prodotto viene ulteriormente ossidato si ottiene molta più energia. Il ciclo dell acido citrico è una via metabolica centrale
La cinetica enzimatica
 La cinetica enzimatica Cinetica chimica All equilibrio Ordine di reazione I ordine II ordine Ordine zero La cinetica di una reazione chimica Cinetica di una reazione enzimatica Ordine 1 (enzima costante)
La cinetica enzimatica Cinetica chimica All equilibrio Ordine di reazione I ordine II ordine Ordine zero La cinetica di una reazione chimica Cinetica di una reazione enzimatica Ordine 1 (enzima costante)
Velocità di reazione. Consideriamo una generica reazione
 Velocità di reazione. Consideriamo una generica reazione Esprimiamo perciò la velocità di un processo chimico in un certo periodo di tempo tramite il rapporto tra la variazione di concentrazione di un
Velocità di reazione. Consideriamo una generica reazione Esprimiamo perciò la velocità di un processo chimico in un certo periodo di tempo tramite il rapporto tra la variazione di concentrazione di un
Cinetica chimica MECCANISMO <<Lo studio CINETICO fornisce invece queste informazioni>>
 Cinetica chimica La termodinamica studia gli aspetti energetici di una reazione nel senso che stabilisce se, da un punto di vista energetico, la reazione potrà avvenire o no. Niente, invece, dice sul tempo
Cinetica chimica La termodinamica studia gli aspetti energetici di una reazione nel senso che stabilisce se, da un punto di vista energetico, la reazione potrà avvenire o no. Niente, invece, dice sul tempo
REGOLAZIONE DELL ATTIVITA ENZIMATICA 1) MODULAZIONE ALLOSTERICA NON-COVALENTE (REVERSIBILE)
 REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
REGOLAZIONE DELL ATTIVITA ENZIMATICA - Regolazione a lungo termine: la quantità di enzima può essere controllata regolando la velocità della sua sintesi o degradazione (minuti o ore) - Regolazione a breve
Velocità di reazione
 1 Velocità di reazione A B V = - d[a] dt = d[b] dt V= Velocità istantanea: coefficiente angolare della retta tangente alla curva in quel punto Quando t=0 la velocità istantanea sarà massima (V 0 ) 2 Energia
1 Velocità di reazione A B V = - d[a] dt = d[b] dt V= Velocità istantanea: coefficiente angolare della retta tangente alla curva in quel punto Quando t=0 la velocità istantanea sarà massima (V 0 ) 2 Energia
Lo scopo della biochimica è la comprensione della vita in termini molecolari.
 Lo scopo della biochimica è la comprensione della vita in termini molecolari. Sebbene la biochimica venga spesso descritta come una scienza della vita e il suo sviluppo venga messo in relazione con la
Lo scopo della biochimica è la comprensione della vita in termini molecolari. Sebbene la biochimica venga spesso descritta come una scienza della vita e il suo sviluppo venga messo in relazione con la
Esempi di funzioni svolte dalle proteine
 Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
Esempi di funzioni svolte dalle proteine Trasporto di sostanze Esempi di funzioni svolte dalle proteine Trasporto di sostanze Funzioni strutturali Esempi di funzioni svolte dalle proteine Trasporto di
STRUTTURA E MECCANISMI D AZIONE DEGLI ENZIMI
 STRUTTURA E MECCANISMI D AZIONE DEGLI ENZIMI Confronto tra gli enzimi e i catalizzatori chimici Gli enzimi sono caratterizzati da: Velocità di reazione più elevate Condizioni di reazione più moderate
STRUTTURA E MECCANISMI D AZIONE DEGLI ENZIMI Confronto tra gli enzimi e i catalizzatori chimici Gli enzimi sono caratterizzati da: Velocità di reazione più elevate Condizioni di reazione più moderate
CLASSIFICAZIONE ENZIMI
 CLASSIFICAZIONE ENZIMI nome raccomandato nome sistematico reazione catalizzata Classe di enzima Reazione catalizzata 1. Ossidoreduttasi Ossido-riduzione 2. Transferasi Trasferimento di gruppi funzionali
CLASSIFICAZIONE ENZIMI nome raccomandato nome sistematico reazione catalizzata Classe di enzima Reazione catalizzata 1. Ossidoreduttasi Ossido-riduzione 2. Transferasi Trasferimento di gruppi funzionali
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione.
 Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
Cinetica chimica E lo studio della velocità delle reazioni chimiche, delle leggi di velocità e dei meccanismi di reazione. Es. 2H 2(g) + O 2(g) d 2H 2 O (l) K eq (25 C)=10 83 (ricavato da lnk=-δg /RT)
I catalizzatori della cellula: gli ENZIMI
 I catalizzatori della cellula: gli ENZIMI LA CATALISI ENZIMATICA E NECESSARIA PER PERMETTERE A MOLTE REAZIONI BIOCHIMICHE DI PROCEDERE AD UNA VELOCITA CONVENIENTE IN CONDIZIONI BIOLOGICHE UNA REAZIONE
I catalizzatori della cellula: gli ENZIMI LA CATALISI ENZIMATICA E NECESSARIA PER PERMETTERE A MOLTE REAZIONI BIOCHIMICHE DI PROCEDERE AD UNA VELOCITA CONVENIENTE IN CONDIZIONI BIOLOGICHE UNA REAZIONE
La cinetica enzimatica: Calcolo della K m e V max
 La cinetica enzimatica: Calcolo della K m e V max Parametri cinetici K m (numericamente uguale alla concentrazione di substrato alla quale la velocità iniziale è pari alla metà della velocità massima)
La cinetica enzimatica: Calcolo della K m e V max Parametri cinetici K m (numericamente uguale alla concentrazione di substrato alla quale la velocità iniziale è pari alla metà della velocità massima)
Cinetica chimica. studia la velocità a cui decorrono le reazioni chimiche una velocità è la variazione di una proprietà per unità di tempo:
 Cinetica chimica Cosa è la velocità di reazione e fattori che la influenzano Effetto concentrazione e temperatura Equazione di Arrhenius Molecolarità reazione. Energia di attivazione e catalisi Cinetica
Cinetica chimica Cosa è la velocità di reazione e fattori che la influenzano Effetto concentrazione e temperatura Equazione di Arrhenius Molecolarità reazione. Energia di attivazione e catalisi Cinetica
- utilizzano esclusivamente le reattività chimiche di alcuni residui AA
 Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Enzimi semplici Enzimi coniugati - utilizzano esclusivamente le reattività chimiche di alcuni residui AA - richiedono la reattività chimica aggiuntiva di COFATTORI o COENZIMI gruppi prostetici COENZIMI
Regolazione dell attività enzimatica. Allosteria Modificazioni covalenti Isoenzimi
 Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Regolazione dell attività enzimatica Allosteria Modificazioni covalenti Isoenzimi Regolazione della attività enzimatica L attività enzimatica deve potere essere regolata in base alle specifiche richieste
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
La velocità di reazione
 La velocità di reazione 1 Che cos è la velocità di reazione (I) Lo studio di tutti gli aspetti relativi alla velocità delle trasformazioni chimiche è affrontato dalla cinetica chimica. La velocità di reazione
La velocità di reazione 1 Che cos è la velocità di reazione (I) Lo studio di tutti gli aspetti relativi alla velocità delle trasformazioni chimiche è affrontato dalla cinetica chimica. La velocità di reazione
Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico
 Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico Dalla glicolisi alla fosforilazione ossidativa NAD + e NADP + Sono coinvolti nelle reazioni di trasferimento dell idruro H: -. Tutte le reazioni
Il ciclo degli acidi tricarbossilici o ciclo dell acido citrico Dalla glicolisi alla fosforilazione ossidativa NAD + e NADP + Sono coinvolti nelle reazioni di trasferimento dell idruro H: -. Tutte le reazioni
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio. GLUCONEOGENESI (sintesi da precursori non glucidici)
 DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
DEGRADAZIONE di polisaccaridi (glicogeno epatico, amido o glicogeno dalla dieta) Glucosio GLUCONEOGENESI (sintesi da precursori non glucidici) La gluconeogenesi utilizza il piruvato e altri composti a
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA
 Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
Via finale comune per l ossidazione di tutti i combustibili metabolici che entrano nella via come molecola di acetil CoA C 6 H 12 O 6 + 6O 2 6CO 2 + 6H 2 O Processi molecolari in cui è coinvolto il consumo
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Corso di Laurea in Scienze Biologiche. Insegnamento di. Anno Accademico
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Prof. Antimo Di Maro Anno Accademico 2016-17 Lezione 14 Ciclo di Krebs L ossidazione
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Cinetica Chimica. Cinetica chimica
 Cinetica Chimica CH 3 Cl + NaOH CH 3 OH + NaCl Le reazioni chimiche possono decorrere con cinetica molto veloce (come le reazioni di salificazione di un acido con una base) o lenta (come alcune reazioni
Cinetica Chimica CH 3 Cl + NaOH CH 3 OH + NaCl Le reazioni chimiche possono decorrere con cinetica molto veloce (come le reazioni di salificazione di un acido con una base) o lenta (come alcune reazioni
proteine enzimi RNA ribozimi substrati altamente specifici -asi
 I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
I catalizzatori sono sostanze che aumentano la velocità delle reazioni senza subire modificazioni. Un catalizzatore non induce una reazione che non può avvenire, fa solo in modo che avvenga più velocemente.
Cap.19. Ciclo di Krebs. o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico
 Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
Cap.19 Ciclo di Krebs o Ciclo degli acidi Tricarbossilici o Ciclo dell acido Citrico Acetil-CoA OSSIDAZIONE DEL GLUCOSIO C 6 H 12 O 6 (glucosio) + 6O 2.. 6CO 2 + 6H 2 O I tappa: GLICOLISI 2 + 2 H 2 O II
La via per accelerare i processi biologici
 La via per accelerare i processi biologici ENZIMI Sono delle proteine altamente specializzare con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa.
La via per accelerare i processi biologici ENZIMI Sono delle proteine altamente specializzare con attività catalitica, accelerano le reazioni chimiche rimanendo inalterati al termine della reazione stessa.
In questo caso parliamo di un processo entalpico. Si tratta di un processo entalpico.
 LEZIONE DEL 10/04/2017 ENZIMOLOGIA - APPLICAZIONI DELLA CINETICA ENZIMATICA Essa trova applicazioni nel processamento dei rifiuti, nelle materie organiche. Si tratta dell'ingegnerizzazione dei processi
LEZIONE DEL 10/04/2017 ENZIMOLOGIA - APPLICAZIONI DELLA CINETICA ENZIMATICA Essa trova applicazioni nel processamento dei rifiuti, nelle materie organiche. Si tratta dell'ingegnerizzazione dei processi
2015 /2016. scaricato da
 Enzimi Prof Spina Riabilitativa 2015 /2016 Gli enzimi i sono catalizzatori t i biologici i i molto efficienti: i caratterizzati da potere catalitico e specificità, possegono una porzione dedicata: il
Enzimi Prof Spina Riabilitativa 2015 /2016 Gli enzimi i sono catalizzatori t i biologici i i molto efficienti: i caratterizzati da potere catalitico e specificità, possegono una porzione dedicata: il
Modulo 14 Il ciclo di Krebs
 Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
Modulo 14 Il ciclo di Krebs Il destino ossidativo del piruvato In condizioni aerobie il piruvato viene decarbossilato ad acetato. L acetato è ossidato ulteriormente nel ciclo dell acido citrico. Una serie
ENZIMI : catalizzatori biologici
 ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
ENZIMI : catalizzatori biologici 1 Nell organismo sono indispensabili alla vita: per esempio le reazioni chimiche connesse con un singolo respiro, in assenza di enzimi, durerebbero ore. L enzima anidrasi
CINETICA CHIMICA E CATALISI
 CINETICA CHIMICA E CATALISI A (g) + B (g) AB (g) Reazione omogenea, irreversibile a T cost VELOCITA di REAZIONE : variazione, nell unità di tempo, della concentrazione delle sostanze reagenti A e B Tale
CINETICA CHIMICA E CATALISI A (g) + B (g) AB (g) Reazione omogenea, irreversibile a T cost VELOCITA di REAZIONE : variazione, nell unità di tempo, della concentrazione delle sostanze reagenti A e B Tale
Studio della velocità delle reazioni ed interpretazione sulla base dei meccanismi di reazione
 Cinetica chimica Studio della velocità delle reazioni ed interpretazione sulla base dei meccanismi di reazione E anche importante conoscere il grado con cui la reazione favorisce i prodotti all equilibrio
Cinetica chimica Studio della velocità delle reazioni ed interpretazione sulla base dei meccanismi di reazione E anche importante conoscere il grado con cui la reazione favorisce i prodotti all equilibrio
GLUCOSIO. Vena porta DIGESTIONE DEI DISACCARIDI. Enzimi parete intestinale
 DIGESTIONE DELL AMIDO AMIDO Amilasi salivare DESTRINE Amilasi pancreatica MALTOSIO Enzimi parete intestinale GLUCOSIO Vena porta DIGESTIONE DEI DISACCARIDI DISACCARIDI Enzimi parete intestinale MONOSACCARIDI
DIGESTIONE DELL AMIDO AMIDO Amilasi salivare DESTRINE Amilasi pancreatica MALTOSIO Enzimi parete intestinale GLUCOSIO Vena porta DIGESTIONE DEI DISACCARIDI DISACCARIDI Enzimi parete intestinale MONOSACCARIDI
Cap.16 GLICOLISI. Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP H 2 O 2 NAD + 2 NADH + 2H +
 Cap.16 GLICOLISI Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP 2 + 2 H 2 O 2 NAD + 2 NADH + 2H + Via metabolica in 10 tappe (reazioni) La glicolisi può
Cap.16 GLICOLISI Glucosio + 2 ADP + 2 Pi + 2 NAD + 2 Piruvato + 2 ATP + 2 H 2 O+ 2 NADH + 2H + 2 ADP + 2 Pi 2 ATP 2 + 2 H 2 O 2 NAD + 2 NADH + 2H + Via metabolica in 10 tappe (reazioni) La glicolisi può
ENZIMI Alcuni sono costituiti solo da a.a. Altri richiedono per la loro attività catalitica la presenza di COFATTORI
 ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
ENZIMI Tutti gli enzimi sono proteine Elevata specificità e senza la formazione di sottoprodotti Non vengono modificati o consumati durante la reazione alla fine si ritrovano inalterati Agiscono in condizioni
BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2016-17 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2016-17 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia. a.a
 Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia a.a. 2016-17 Cinetica Chimica studia i fenomeni connessi con la VELOCITA di una REAZIONE Reazioni
Precorsi Test AMMISSIONE Medicina e Chirurgia - Professioni Sanitarie Università degli Studi di Perugia a.a. 2016-17 Cinetica Chimica studia i fenomeni connessi con la VELOCITA di una REAZIONE Reazioni
ENZIMI. A + B AB (100 Kcal= E. Attiv.) A + B AB (50 Kcal) SUBSTRATO ENZIMA E N E R G I A
 ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
ENZIMI 1) sono catalizzatori di natura biologica e sono proteine 2) gli enzimi abbassano l energia di attivazione di un solo tipo di reazione senza intervenire nella reazione stessa cioè senza esserne
Una panoramica del ciclo dell acido ciclico
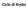 Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Ciclo di Krebs Una panoramica del ciclo dell acido ciclico Concetti chiave Il ciclo dell acido citrico, o ciclo di Krebs, o ciclo degli acidi tricarbossilici (TCA), è un processo catalitico a 8 tappe che
Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale
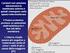 Ciclo di Krebs 1 Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale 2 Complesso della piruvato deidrogenasi (2) FAD Diidrolipoil deidrogenasi Piruvato decarbossilasi E 3 Diidrolipoil
Ciclo di Krebs 1 Complesso della piruvato deidrogenasi (1) Stechiometria della reazione finale 2 Complesso della piruvato deidrogenasi (2) FAD Diidrolipoil deidrogenasi Piruvato decarbossilasi E 3 Diidrolipoil
Gli enzimi. Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici
 Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
Gli enzimi Gli enzimi sono le proteine 1 che catalizzano 2 le reazioni chimiche che avvengono nei sistemi biologici 1 con l eccezione dei ribozimi (RNA catalitici) 2 un catalizzatore è una sostanza che
METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI
 METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI Nelle piante l ossidazione degli acidi grassi avviene nei perossisomi delle foglie e nei gliossisomi dei semi Nelle cellule animali il sito principale
METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI Nelle piante l ossidazione degli acidi grassi avviene nei perossisomi delle foglie e nei gliossisomi dei semi Nelle cellule animali il sito principale
VELOCITA di REAZIONE. Quali sono le dimensioni di una velocità di reazione?? E una definizione che ha senso NON all equilibrio!!!
 VELOCITA di REAZIONE Quali sono le dimensioni di una velocità di reazione?? E una definizione che ha senso NON all equilibrio!!! Data la reazione: aa + bb cc + dd v = - 1 Δ[A] = - 1 Δ[B] = 1 Δ[C] = 1 Δ[D]
VELOCITA di REAZIONE Quali sono le dimensioni di una velocità di reazione?? E una definizione che ha senso NON all equilibrio!!! Data la reazione: aa + bb cc + dd v = - 1 Δ[A] = - 1 Δ[B] = 1 Δ[C] = 1 Δ[D]
Cinetica Chimica 1. esaminare quali condizioni debbono essere soddisfatte affinché una data reazione avvenga spontaneamente 2. esaminare quali sono i
 Cinetica Chimica 1. esaminare quali condizioni debbono essere soddisfatte affinché una data reazione avvenga spontaneamente 2. esaminare quali sono i fattori che influenzano il tempo richiesto affinché
Cinetica Chimica 1. esaminare quali condizioni debbono essere soddisfatte affinché una data reazione avvenga spontaneamente 2. esaminare quali sono i fattori che influenzano il tempo richiesto affinché
Aerobiosi C A T A B O L I S M O. Lez 4A. Schema generale del metabolismo dei glucidi
 Schema generale del metabolismo dei glucidi -1- Aerobiosi In condizioni aerobiche il piruvato prodotto dalla glicolisi e dalla degradazione di alcuni aminoacidi è ossidato a H 2 O e CO 2 nella respirazione
Schema generale del metabolismo dei glucidi -1- Aerobiosi In condizioni aerobiche il piruvato prodotto dalla glicolisi e dalla degradazione di alcuni aminoacidi è ossidato a H 2 O e CO 2 nella respirazione
METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI
 METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI Nelle piante l ossidazione degli acidi grassi avviene nei perossisomi delle foglie e nei gliossisomi dei semi Nelle cellule animali il sito principale
METABOLISMO OSSIDATIVO VIE METABOLICHE CONVERGENTI Nelle piante l ossidazione degli acidi grassi avviene nei perossisomi delle foglie e nei gliossisomi dei semi Nelle cellule animali il sito principale
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
Il metabolismo: concetti di base
 Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
Corso di Laurea Magistrale in Ingegneria Biomedica Complementi di Chimica e Biochimica per le Tecnologie Biomediche Il metabolismo: concetti di base Caratteristiche generali Strategie Trofiche Il metabolismo:
