BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
|
|
|
- Silvano Antonini
- 9 anni fa
- Просмотров:
Транскрипт
1 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI Prof. Augusto Parente Lezione 32
2 DETERMINAZIONE DELLA CONCENTRAZIONE PROTEICA TOTALE Metodo Kjeldahl Per lunghi anni, la quantità di proteine (proteina grezza) di alimenti è stata determinata calcolando il contenuto di AZOTO totale. Il metodo Kjeldahl è il metodo di elezione per la determinazione del contenuto di AZOTO. Questo valore viene poi moltiplicato per un fattore per ottenere la quantità di proteine. Questo metodo si basa su due assunzioni: i) carboidrati e grassi alimentari non contengono azoto; ii) la quasi totalità dell azoto presente negli alimenti deriva dagli amminoacidi delle proteine. Sulla base delle prime determinazioni, il contenuto medio di N nelle proteine era di circa il 16% (160 g/1000 g), che ha portato all uso del calcolo Nx6,25 (1/0,16= 6,25). Tuttavia non tutto l azoto che si può titolare è presente nelle proteine, ma anche in amminoacidi liberi, nucleotidi, creatina e colina.
3 Inoltre, il contenuto di azoto di alcuni amminoacidi (come % in peso) varia in relazione al peso molecolare dell amminoacido ed al numero di atomi di azoto in essi contenuti [da uno a quattro a seconda degli amminoacidi: tutti uno ad eccezione di Lys e Gln/Asn (2), His (3), Arg (4)]. Sulla base di queste considerazione, in realtà il contenuto di N nelle proteine varia da 5,26 (1/0,19) a 7,69 (1/0,13).
4 Gli attuali fattori sono riportati nella seguente Tabella Origine Alimento Fattore Origine Alimento Fattore Animale Uova 6,25 Vegetale Grano Chicco intero 5,83 Carne 6,25 Crusca 6,31 Latte 6,38 Endosperma 5,70 Vegetale Orzo 5,83 Ricino 5,30 Mais 6,25 Fagioli (vari tipi) 6,25 Miglio 5,83 Soia 7,71 Avena 5,83 Noccioline 5,46 Riso 5,95 Segale 5,83 Sorgo 6,25
5 Metodo Kieldhal (1) Digestione + H 2 SO 4 concentrato + catalizzatore -> azoto convertito in ione ammonio. (2) Neutralizzare con NaOH per ottenere NH 3 (NH 4+ ) (3) distillare NH 3 (NH 4+ ) e intrappolare in acido borico. (4) Titolare con acido cloridrico.
6 Espressione dei risultati Calcolare il contenuto di sostanze azotate per 100 g di sostanza secca (s.s.) con la formula: V x N x F x Sostanze azotate % s.s. = E x (100 - U) dove: V = ml di acido 0,1 N (6.9); N = 0, (grammi di azoto corrispondenti a 1 ml di acido 0,1 N); E = peso del campione in grammi; U = umidità percentuale del campione; F = fattore di conversione dell'azoto in sostanze azotate, uguale a: 5,70 per grano e segale; 5,95 per riso; 6,25 per mais e orzo. Il fattore 6,25 viene anche usato nelle etichette nutrizionali e per i prodotti cerealicoli in miscela.
7 Metodo Kjeldhal SVANTAGGI: Non tutto l azoto viene dalle proteine: Purine Pirimidine DNA, RNA, ecc. Urea Altre sostanze aggiunte intenzionalmente (FRODI)
8 UREA MELAMMINA nel latte
9 Per la determinazione della concentrazione di proteine parzialmente purificate sono disponibili molti metodi. Parecchi di essi non forniscono un concentrazione assoluta ma relativa rispetto ad uno stock di proteina standard che viene usata per la preparazione di una retta di taratura (per il basso costo, la facile reperibilità, etc., si utilizza come standard l albumina da siero bovino, o BSA). Il Metodo Si costruisce innanzitutto una retta di taratura con quantità crescenti di albumina da siero bovino (BSA) utilizzata come riferimento. Vengono anche preparati un campione che non contiene BSA (detto bianco) e due aliquote (in L) del campione cx.
10 n. provetta BSA 2 mg/ml (1 L= 2 g) BSA presente Campione X ( L) H 2 O ( L) Reagente ( L) 0 (bianco) CX CX I campioni si incubano per un determinato tempo, poi...
11 595 nm 1- Lettura dei campioni, incluso il bianco; 2- costruzione della retta di taratura, con i campioni di BSA, utilizzando le letture a 595 nm, sottratte del valore del bianco; 3- interpolazione dei valori di assorbimento, anch essi sottratti del valore del bianco, dei campioni proteici a [X] (in doppio); 4- lettura sull ascissa della quantità di Lowry Assay Standard Curve Protein amount vs. Absorbance g proteine contenuta nel campione X (esprimendo la concentrazione in mg/ml ) A a Protein ( g) L intensità di colore aumenta all aumentare della quantità di proteine (osservazione qualitativa); La lettura dell assorbimento ed il ricorsi della retta di taratura ci fanno avere la QUANTITÀ di proteine (dato quantitativo).
12 Metodo del biureto Il reagente chiave è una soluzione fortemente alcalina di tartrato contenente solfato di rame(ii) diluito. Quando la soluzione è aggiunta alla proteina, il rame si può legare alle proteine, formando un complesso colorato (si ritiene che tale complesso includa la coordinazione contemporanea di 4 gruppi peptidici con un unico ione rame). Compare un colore viola-bruno ( max =540 nm) che ovviamente sarà proporzionale alla concentrazione totale dei legami peptidici e dunque di proteina. Biureto Si forma riscaldando l'urea a C. Reagisce con la soluzione fortemente alcalina di tartrato contenente solfato di rame(ii) diluito. Da ciò deriva il nome dato al metodo.
13 O H R O H N N Cu 2+ N N H O R H O Complesso formato dal rame, con colore viola-bruno Il metodo è generale (anche se i residui di prolina non reagiscono ) e molto riproducibile. Purtroppo, la sensibilità è bassa: non consente in genere di misurare concentrazioni proteiche <1 mg/ml.
14 METODO DI LOWRY (CON IL REATTIVO DI FOLIN-CIOCALTEAU) Molto usato, soprattutto nel passato. La miscela da saggiare viene dapprima portata in ambiente alcalino (ph ) e fatta reagire con citrato o tartrato di rame(ii). Dopo un certo tempo (necessario probabilmente per consentire la complessazione del rame da parte delle proteine) si aggiunge la miscela di Folin- Ciocalteau (sviluppato inizialmente per la determinazione della tirosina e quindi poi per fenoli e polifenoli), il cui componente attivo è rappresentato da una miscela di sodio molibdato, fosfato e tungstato. Con l andare del tempo si sviluppa un colore scuro, che tende al blu in presenza di proteina (in assenza, il colore tende al marrone). L intensità della colorazione blu (lettura a 660 nm), sarà proporzionale alla concentrazione di proteina.
15 Non è chiaro perché il colore blu si sviluppi, è possibile che gli acidi fosfomolibdotungstici formino dei complessi misti con rame e proteina. Poiché la presenza e quantità dei residui aromatici (in particolare, tirosinici) influenzano fortemente per lo sviluppo del colore, sembra più probabile che il meccanismo coinvolga una riduzione dello ione Cu 2+ a Cu + da parte di questi residui, seguita da una reazione dello ione rameoso con gli acidi fosfomolibdotungstici. Svantaggi: richiede tempi di incubazione precisi; inoltre alcuni tamponi (come il MES) ed altre sostanze possono interferire; infine, poiché il contenuto in tirosine può influenzare la colorazione, le risposte al saggio possono variare abbastanza a seconda del tipo di proteine presenti.
16 IL solo REATTIVO di Folin-Ciocalteau è molto utilizzato per la determinazione dei POLIFENOLI TOTALI nelle matrici alimentari: frutta e verdura (pomodoro), tè verde, tè nero, vino rosso, caffè, cioccolato, olive e olio extra vergine di oliva (per citare solo alcuni dei componenti della dieta mediterranea); etc; I POLIFENOLI sono delle particolari molecole che, in base alla loro struttura chimica, possono essere suddivisi in tre diverse classi principali: i) fenoli semplici; ii) flavonoidi; iii) tannini. I fenoli semplici comprendono gli acidi benzoici, le cumarine, gli acidi fenolici, e possono essere trovati in molti cibi e bevande, come per esempio nel caffè. I tannini si suddividono in due categorie: i condensati e gli idrolizzatili. I flavonoidi rappresentano la tipologia di fenoli più grande in natura. e, a seconda della loro composizione, si raggruppano essenzialmente in: flavoni, flavonoidi, antociani, e isoflavoni.
17 Il Reattivo è costituito da una miscela di acido fosfotungstico (H 3 PW 12 O40) e acido fosfomolibdico (H 3 PMo 12 O 40 ). Per reazione con i fenoli, questi acidi si riducono a ossidi di tungsteno e molibdeno (W 8 O 23 e Mo 8 O 23 ) dal tipico colore blu, con un massimo d'assorbimento a 750 nm. Contenuto di polifenoli totali in alcuni alimenti Succo d uva g polifenoli totali /ml di succo Varietà di mele Da 0,1 g polifenoli totali / kg peso fresco a 10 g / kg in alcune varietà di mele da sidro
18
19
20 Metodo dell acido bicinconinico BCA- un saggio molto simile a quello di Lowry, con la differenza che il rame(ii) anziché in associazione con il reagente di Folin-Ciocalteau si usa in associazione con l acido bicinconinico. Si ritiene che la riduzione dello ione Cu 2+ a Cu + sia qui seguita dall associazione dello ione rameoso con l acido, con formazione di un complesso che assorbe fortemente a 562 nm (colore viola-blu). Il saggio presenta la stessa variabilità da proteina a proteina già vista per il Lowry, ma è più riproducibile e un po più sensibile. N N O- O O- O Acido bicinconico
21 Metodo di Bradford Si basa sull interazione non-covalente di un colorante (il Coomassie Brilliant Blue R-250) con le proteine. Il saggio viene effettuato a ph acido. Il colorante si lega primariamente ai residui basici ed aromatici, e la formazione di questi complessi determina uno spostamento del massimo di assorbimento del colorante da 465 a 595 nm, che può essere misurato spettrofotometricamente. Anche se diverse proteine possono dare risposte alquanto diverse in questo saggio, la sua semplicità ed elevata sensibilità (<0.1 mg/ml) fa sì che sia largamente usato. Il Coomassie Blue si usa anche per evidenziare le bande proteiche nella gel elettroforesi. Coomassie Brilliant Blue R-250
22 Silver staining Questa tecnica è usata normalmente per colorare proteine nella gel elettroforesi, nel caso sia richiesta una elevata sensibilità. Assorbimento nel vicino UV La presenza degli anelli aromatici di tirosina e triptofano fa sì che le proteine presentino un assorbimento di luce nel vicino ultravioletto, con massimo a circa 280 nm. Il coefficiente di estinzione molare varia ovviamente da proteina a proteina (dipende dal numero e dalla posizione degli amminoacidi aromatici), ma in genere può essere calcolato con buona approssimazione partendo dalla sequenza amminoacidica. Va tenuto presente che molte altre sostanze possono assorbire nel vicino ultravioletto, e quindi condizionare i risultati della misura; fra queste gli acidi nucleici, che però hanno un massimo di assorbimento a 260 nm. A volte, nelle prime fasi di purificazione di una proteina, può essere utile verificare il rapporto tra gli assorbimenti a 280 e 260 nm, per verificare se e quanto una data frazione di proteina sia contaminata da acidi nucleici.
23 L assorbimento ultravioletto 280 nm: Può rappresentare un ottima tecnica quando non si ha alcuna idea della concentrazione di un campione che deve essere assolutamente recuperato. Si usa in genere prima di passare a metodi più precisi e sensibili; La determinazione si basa sull assorbimento specifico degli aminoacidi aromatici tirosina e triptofano; La misura è soggetta a interferenza da altri componenti cellulari e in particolare acidi nucleici; Il metodo non è molto sensibile e presuppone l uso di cuvette di quarzo; Il vantaggio reale è che il campione non viene distrutto e la misura è molto rapida.
24 1. Azzerare lo spettrofotometro con acqua o tampone 2. Misurare l assorbimento a 280 nm in cuvette di quarzo 3. Cambiare lunghezza d onda a 260 nm, fare lo zero con acqua o tampone 4. Misurare l assorbimento a 260 nm in cuvette di quarzo 5. Usare la seguente equazione per calcolare la concentrazione proteica [Proteina] (mg/ml) = 1.55*A *A260
25 DETERMINAZIONE DELLA COMPOSIZIONE AMMINOACIDICA DELLE PROTEINE ALIMENTARI Amminoacidi essenziali e Qualità proteica La determinazione della composizione amminoacidica* delle proteine alimentari prevede le seguenti fasi: 1- Idrolisi delle proteine 2- Separazione e identificazione degli amminoacidi 3- Quantizzazione degli amminoacidi *COMPOSIZIONE AMMINOACIDICA: quali dei venti amminoacidi sono presenti nelle proteine ed in che quantità.
26 1- IDROLISI DELLE PROTEINE 1- NELLE PROTEINE, COME È NOTO, gli amminoacidi sono uniti tra loro mediante il legame peptidico. Pertanto, per poterli separare e identificare, bisogna rompere il legame peptidico. Questo si può fare mediante una idrolisi CHIMICA oppure ENZIMATICA. IDROLISI CHIMICA: l idrolisi si effettua in presenza di HCl 6M, a 110 C per un tempo di ore In queste condizioni l idrolisi è completa. Tuttavia, alcuni amminoacidi possono subire delle modifiche o parziale idrolisi: - Thr, Ser e Tyr subiscono delle perdite parziali - Trp viene distrutto - Cys e Met possono in parte ossidarsi - Val e Ile richiedono una idrolisi a 72 ore, quando nella sequenza sono tra loro legati; - Le ammidi asparagina e glutammina vengono trasformate nei relativi amminoacidi.
27 Naturalmente, la determinazione del contenuto preciso riguarda gli amminoacidi essenziali (9): Thr, Val, Ile, Leu, Met, Lys, Phe, Trp, His (e Arg nei bambini) -Thr: Il suo contenuto viene corretto del 5% (in più) rispetto al contenuto calcolato a 24 h; - Val ed Ile vengono calcolate a 72 ore; -il Trp viene ottenuto dopo idrolisi basica con NaOH oppure con idrolisi acida con acido mercaptoetansolfonico; -Met subisce meno perdite se nella soluzione di idrolisi si aggiunge un agente protettore (tiodiglicole, fenolo); - Lys, Leu, His, Arg e Phe sono amminoacidi stabili e non richiedono particolari attenzioni.
28 IDROLISI ENZIMATICA L idrolisi enzimatica permette di evitare la distruzione degli amminoacidi, precedentemente riportati, ma rischia di essere incompleta. Tuttavia, essendo basata su enzimi dello stesso tipo di quelli utilizzati in vivo, questa tecnica libera solo gli amminoacidi effettivamente idrolizzabili durante la digestione. Per questo si ritiene che essa sia in grado di fornire la frazione di amminoacidi DISPONIBILI o UTILIZZABILI.
29 2- SEPARAZIONE E IDENTIFICAZIONE DEGLI AMMINOACIDI Dopo aver idrolizzato le proteine in modo opportuno, si passa alla separazione ed alla identificazione degli amminoacidi. -Il Trp si può determinare, senza separazione, utilizzando il metodo della triptofanasi, come in precedenza discusso. Per gli altri amminoacidi si possono applicare 1- Metodi di derivatizzazione pre-colonna seguiti dalla separazione; 2- Oppure metodi di derivatizzazione post-colonna, in cui si ha prima la separazione e poi la colorazione degli amminoacidi. Nel primo caso si utilizzato reagenti quali fenilisotiocianato, o- ftalaldeide, reattivo di Sanger (2,4 dinitrofluorobenzene), etc. I derivati degli amminoacidi ottenuti vengono separati mediante RP-HPLC, identificati utilizzando condizioni standard e separazioni di riferimento e quantizzati.
30 Nel secondo caso si utilizzano TECNICHE BASATE SULLE PROPRIETA DI CARICA: LA CROMATOGRAFIA A SCAMBIO IONICO Questa è la procedura che meglio si adatta alla separazione di amminoacidi proteici. Il principio su cui si basa è l instaurarsi di legami elettrostatici tra le molecole da separare e gruppi carichi presenti sul supporto cromatografico. Il supporto generalmente utilizzato per la separazione di amminoacidi è un polimero di stirene/divinilbenzene che, per essere utilizzato come scambiatore di ioni, viene modificato con l introduzione di gruppi solfonici, carichi negativamente (polivinilbenzene solfonato). SCAMBIATORI IONICI FORTI : Hanno gruppi ionizzabili che ritengono la loro carica ionica in quasi tutto l intervallo di ph (1-13). SCAMBIATORI IONICI DEBOLI Hanno gruppi ionizzabili solo in uno stretto intervallo di ph.
31 Polistirene/divinilbenzene CROMATOGRAFIA A SCAMBIO CATIONICO CH-CH 2 -CH-CH 2 -CH-CH 2 -CH-CH 2 SO 3 SO 3 SO 3 SO 3 POLIVINILBENZENE SOLFONATO
32 SCHEMA DELLA CROMATOGRAFIA A SCAMBIO IONICO
33 FASI DELLA CROMATOGRAFIA A SCAMBIO ANIONICO FASE 1: LEGAME ALLA RESINA: Una miscela di amminoacidi, disciolta in un tampone acido a ph 2,2, viene caricata su di una colonna cromatografica contenente la resina. In tali condizioni tutti gli amminoacidi possiedono una carica netta positiva e si legano con legame ionico alla resina Campione contenente diversi amminoacidi Colonna di eluizione contenente particelle di resina a scambio anionico
34 FASE 2: ELUIZIONE degli AMMINOACIDI: Il distacco selettivo degli amminoacidi viene effettuato facendo passare attraverso la colonna cromatografica una soluzione tampone a ph e forza ionica crescenti. Può anche essere aumentata la temperatura della colonna L incremento di forza ionica, ottenuto aumentando la concentrazione salina dell eluente, tenderà ad indebolire i ponti salini stabilitisi tra amminoacidi e resina; L aumento di ph porterà ad una graduale deprotonazione dei gruppi acido-basici presenti sulla catena laterale. Alcuni amminoacidi tenderanno ad assumere così carica netta zero interrompendo il legame ionico con la resina e passando nell eluente per poi emergere dalla colonna cromatografica. Quanto più basso è il punto isoelettrico di un amminoacido, tanto più facilmente l aumento di ph e forza ionica porterà alla sue eluizione. L aumento della temperatura della colonna ha un effetto simile.
35 FASI CROMATOGRAFIA A SCAMBIO IONICO
36 FASE 2: Il processo di separazione separa gli amminoacidi in bande discrete L eluato che esce dalla colonna viene raccolto Alcune frazioni non contengono amminoacidi
37 FASE 3: COLORAZIONE. L eluente, raccolto in differenti provette, è poi sottoposto alla reazione con ninidrina per rilevare la presenza di amminoacidi. Questa procedura può essere automatizzata in un apparecchio detto analizzatore di amminoacidi.
38 DIAGRAMMA DI FLUSSO DI UN ANALIZZATORE DI AMMINOACIDI
39 Assorbimento a 570 nm CROMATOGRAMMA DI IDROLIZZATO PROTEICO Tempo (minuti)
40 - ph dell eluente - Forza ionica dell eluente - Temperatura della colonna - Flusso dell eluente Se questi parametri sono fissi e controllati: -Il tempo di eluzione permette di identificare un certo amminoacido - L area del picco permette di determinare la quantità di amminoacido, in riferimento ad un cromatogramma ottenuto caricando quantità NOTE di ciascun amminoacido (CALIBRAZIONE) La calibrazione permette di calcolare per ciascun amminoacido una Costante di Colore (la reazione con ninidrina può dare una resa in colore violetto-letto a 570 nm- leggermente diverso per i singoli amminoacidi. La costante di colore si usa poi per trovare la quantità del determinato amminoacido. C = A nmoli (aa della calibrazione) nmoli (aa n ) = A C
41 OBIETTIVI DEL CORSO Il corso di Biochimica e Biotecnologie degli Alimenti fornirà conoscenza avanzate: i) sulla struttura e sulla funzione dei macronutrienti (carboidrati, lipidi e proteine); ii) sui relativi processi metabolici nell alimentazione e nelle biotecnologie alimentari; iii) sui principali enzimi coinvolti nella nutrizione e nelle biotecnologie (trasformazioni) del settore agroalimentare; iv) sulla qualità chimico-nutrizionale e autenticità degli alimenti e su metodologie per la loro determinazione. 41
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Cosa determina l assorbanza di un cromoforo?
 Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
Cosa determina l assorbanza di un cromoforo? I cromofori sono di solito caratterizzati da doppi legami e sistemi di risonanza Lo spettro di assorbimento di un cromoforo è solo parzialmente determinato
BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI Le proteine dovrebbero fornire circa il 12% delle calorie totali.
Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI Le proteine dovrebbero fornire circa il 12% delle calorie totali.
Analisi quantitative
 Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Analisi quantitative Diversi metodi per la quantificazione delle proteine totali (reazioni generali delle proteine): 1. Dosaggio spettrofotometrico diretto 2. Metodi colorimetrici 1. Dosaggio spettrofotometrico
Determinazioni quantitative in farmacologia
 Determinazioni quantitative in farmacologia 1 Dosaggio biologico determinazione quantitativa della concentrazione o della potenza di una sostanza per mezzo della valutazione della risposta biologica che
Determinazioni quantitative in farmacologia 1 Dosaggio biologico determinazione quantitativa della concentrazione o della potenza di una sostanza per mezzo della valutazione della risposta biologica che
DOSAGGIO ACIDI NUCLEICI
 DOSAGGIO ACIDI NUCLEICI l Cuvetta contenente il campione di proteina a concentrazione C Sorgente I 0 I 1 I 0 Rivelatore Quando si fa passare una luce di una particolare lunghezza d onda d
DOSAGGIO ACIDI NUCLEICI l Cuvetta contenente il campione di proteina a concentrazione C Sorgente I 0 I 1 I 0 Rivelatore Quando si fa passare una luce di una particolare lunghezza d onda d
Tra nm Nucleotidi mono-fosfato
 Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Un estratto proteico può contenere acidi nucleici, nucleotidi Posso verificare la loro presenza mediante la misura di uno spettro di assorbimento. Gli acidi nucleici e i nucleotidi assorbono nell UV, grazie
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
Purificazione e determinazione di proteine
 Corso di insegnamento Biochimica e Biotecnologie degli Alimenti Purificazione e determinazione di proteine O H N R O H N Cu 2+ N H O R N H O N N O- O O- O Acido bicinconico Lezione n.xxi-26.05.14 Estrazione
Corso di insegnamento Biochimica e Biotecnologie degli Alimenti Purificazione e determinazione di proteine O H N R O H N Cu 2+ N H O R N H O N N O- O O- O Acido bicinconico Lezione n.xxi-26.05.14 Estrazione
Dosaggio delle proteine
 Laboratorio Integrato 4 Lezione n.2 Dosaggio delle proteine Dott.ssa Francesca Zazzeroni METODI PER EFFETTUARE UN DOSAGGIO PROTEICO 1-Metodo del Biureto - il reattivo del biureto consiste in una soluzione
Laboratorio Integrato 4 Lezione n.2 Dosaggio delle proteine Dott.ssa Francesca Zazzeroni METODI PER EFFETTUARE UN DOSAGGIO PROTEICO 1-Metodo del Biureto - il reattivo del biureto consiste in una soluzione
Metodi di studio delle proteine :
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D determinazione del peso molecolare Spettrofotometro
Spettrofotometria e analisi di amminoacidi
 Spettrofotometria e analisi di amminoacidi Quantizzazione di proteine e di miscele di amminoacidi Antimo Di Maro Anno Accademico 2015-16 Assorbimento della luce ONDE ELETTROMAGNETICHE La radiazione elettromagnetica
Spettrofotometria e analisi di amminoacidi Quantizzazione di proteine e di miscele di amminoacidi Antimo Di Maro Anno Accademico 2015-16 Assorbimento della luce ONDE ELETTROMAGNETICHE La radiazione elettromagnetica
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. Metodologie 1. DiSTABiF. Corso di Laurea in SCIENZE BIOLOGICHE.
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2016-17 Metodologie 1 Spettrofotometria e analisi di amminoacidi
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in SCIENZE BIOLOGICHE Insegnamento di CHIMICA BIOLOGICA Anno Accademico 2016-17 Metodologie 1 Spettrofotometria e analisi di amminoacidi
La Spettroscopia in Biologia
 La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
La Spettroscopia in Biologia Linda Avesani Dip. Scientifico e Tecnologico Università di Verona Spettroscopia e Proprietà della luce La spettroscopia in biologia studia la struttura e la dinamica delle
1. Cromatografia per gel-filtrazione
 1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
1. Cromatografia per gel-filtrazione La gel filtrazione è un metodo cromatografico che separa le sostanze in base alle loro dimensioni molecolari. I materiali che costituiscono il supporto per la gel-filtrazione
ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M
![ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M ε 340 nm A 260 nm A 260nm = 1.36 A 340 nm = A 340nm A = c [NADH] = : 6.22 x 10 3 = x 10-6 M](/thumbs/59/43508258.jpg) ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2 Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione molare a 260 nm sono
ESERCIZI 2. Spiegare il principio di.
 ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
ESERCIZI 2 Spiegare il principio di. Esercizio n.1 Trovare la concentrazione di NAD e NADH in una soluzione miscelata basandosi sui seguenti dati ottenuti in una cuvetta da 1 cm : I coefficienti di estinzione
Le molecole della vita
 Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
La struttura covalente delle proteine (la sequenza amminoacidica)
 La struttura covalente delle proteine (la sequenza amminoacidica) Sequenza amminoacidica dell ormone insulina bovino (Frederick Sanger, 1953) Il primo passo per determinare la sequenza di un peptide è
La struttura covalente delle proteine (la sequenza amminoacidica) Sequenza amminoacidica dell ormone insulina bovino (Frederick Sanger, 1953) Il primo passo per determinare la sequenza di un peptide è
- determinazione colorimetrica della concentrazione di una miscela proteica. - Determinazione spettrofotometrica dell attività enzimatica
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2012/2013 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2012/2013 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Spettroscopia nell ultravioletto e nel visibile
 Spettroscopia nell ultravioletto e nel visibile Sono le regioni dello spettro elettromagnetico maggiormente utilizzate nelle ricerche in campo biomedico Le radiazioni elettromagnetiche e lo spettro Una
Spettroscopia nell ultravioletto e nel visibile Sono le regioni dello spettro elettromagnetico maggiormente utilizzate nelle ricerche in campo biomedico Le radiazioni elettromagnetiche e lo spettro Una
- determinazione colorimetrica della concentrazione di una miscela proteica
 CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2013/2014 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
CORSO DI LAUREA IN BIOLOGIA GENERALE E APPLICATA Anno Accademico 2013/2014 Laboratorio di Chimica Biologica - Cromatografia a scambio ionico - determinazione colorimetrica della concentrazione di una miscela
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE
 RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE 00049 Autori Vittorio Sirolli Contenuti Abstract raccolta e processamento dei campioni urinari Abstract release 1 pubblicata il 20 luglio 2012
RACCOLTA E PROCESSAMENTO CAMPIONE URINE PER ANALISI OMICHE 00049 Autori Vittorio Sirolli Contenuti Abstract raccolta e processamento dei campioni urinari Abstract release 1 pubblicata il 20 luglio 2012
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
α-amminoacidi O α O α R CH C O - NH 3 forma ionizzata sale interno (zwitterione) OH NH 2 forma non ionizzata (non esistente in realtà)
 Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
V R V t. Proteine ad alto peso molecolare. Proteine a peso molecolare intermedio. Proteine a basso peso molecolare. Kd + piccolo.
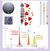 V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
V 0 Proteine ad alto peso molecolare Proteine a peso molecolare intermedio V R V t Proteine a basso peso molecolare Kd elevato Kd piccolo Esclusione molecolare o gelfiltrazione = Volume totale V T = V
IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO
 IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO SCARICATE DAI SITI WEB DI CUI SONO RIPORTATI I LINK METODOLOGIE BIOCHIMICHE
IL MATERIALE CONTENUTO IN QUESTE DIAPOSITIVE E AD ESCLUSIVO USO DIDATTICO PER L UNIVERSITA DI TERAMO LE IMMAGINE CONTENUTE SONO SCARICATE DAI SITI WEB DI CUI SONO RIPORTATI I LINK METODOLOGIE BIOCHIMICHE
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento
 TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
TECNICHE DI SEPARAZIONE DELLE PROTEINE Le proteine sono purificate con procedure di frazionamento Eliminazione selettiva di tutti gli altri componenti della miscela alla fine resta soltanto la sostanza
Soluzioni RAGIONAMENTO LOGICO E CULTURA GENERALE. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta. Risposta.
 Soluzioni 1 A 2 B 3 B 4 E 5 D 6 E 7 B 8 D 9 C 10 B 11 D 12 B 13 E 14 D 15 C 16 C 17 B 18 D 19 A 20 C 21 D 22 C 23 D 24 C 25 E 26 C 27 D 28 C 29 B 30 B 31 D 32 E 33 B 34 C 35 E 36 A 37 D 38 B 39 C 40 D
Soluzioni 1 A 2 B 3 B 4 E 5 D 6 E 7 B 8 D 9 C 10 B 11 D 12 B 13 E 14 D 15 C 16 C 17 B 18 D 19 A 20 C 21 D 22 C 23 D 24 C 25 E 26 C 27 D 28 C 29 B 30 B 31 D 32 E 33 B 34 C 35 E 36 A 37 D 38 B 39 C 40 D
Analisi e purificazione di proteine
 Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
Analisi e purificazione di proteine elettroforesi ultracentrifugazione cromatografia frammenti specifici sequenziamento struttura primaria livelli superiori contesto fisiologico funzione Condizioni denaturanti
TIPI di CROMATOGRAFIA
 Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
ESPERIENZE DI LABORATORIO CORSO CHIMICA ANALITICA II (A.A )
 ESPERIENZE DI LABORATORIO CORSO CHIMICA ANALITICA II (A.A. 2016-2017) Esp.1: DETERMINAZIONE DELLA CAFFEINA NELLE BEVANDE MEDIANTE ANALISI IN RP-HPLC-UV (metodo delle aggiunte multiple) Esp.2: DETERMINAZIONE
ESPERIENZE DI LABORATORIO CORSO CHIMICA ANALITICA II (A.A. 2016-2017) Esp.1: DETERMINAZIONE DELLA CAFFEINA NELLE BEVANDE MEDIANTE ANALISI IN RP-HPLC-UV (metodo delle aggiunte multiple) Esp.2: DETERMINAZIONE
Determinazione del contenuto di licopene
 Determinazione del contenuto di licopene (Corso di Fisiologia della produzione e della post-raccolta) Il colore arancione, giallo e rosso di foglie, fiori e frutti è dovuto principalmente alla presenza
Determinazione del contenuto di licopene (Corso di Fisiologia della produzione e della post-raccolta) Il colore arancione, giallo e rosso di foglie, fiori e frutti è dovuto principalmente alla presenza
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI
 METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
METODI DI BASE PER L ANALISI DEGLI ACIDI NUCLEICI SPETTRI UV E QUANTIZZAZIONE SPETTROFOTOMETRICA DEGLI ACIDI NUCLEICI FIGURA 7.6A METODOLOGIA BIOCHIMICA (WILSON) a a = a 1 Assorbimento = a b a 1 b FIGURA
Spettrofotometria e analisi di amminoacidi. Quantizzazione di proteine e di miscele di amminoacidi
 Spettrofotometria e analisi di amminoacidi Quantizzazione di proteine e di miscele di amminoacidi Assorbimento della luce ONDE ELETTROMAGNETICHE La radiazione elettromagnetica è, dal punto di vista dell'elettromagnetismo
Spettrofotometria e analisi di amminoacidi Quantizzazione di proteine e di miscele di amminoacidi Assorbimento della luce ONDE ELETTROMAGNETICHE La radiazione elettromagnetica è, dal punto di vista dell'elettromagnetismo
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
DNA, RNA E PROTEINE DA CAMPIONI BIOLOGICI
 DNA, RNA E PROTEINE DA CAMPIONI BIOLOGICI UNA VOLTA ESTRATTI VANNO QUANTIFICATI QUANTIFICAZIONE DEI CAMPIONI Vi sono numerosi metodi. Alcuni forniscono valori assoluti, altri relativi; in tal caso lo standard
DNA, RNA E PROTEINE DA CAMPIONI BIOLOGICI UNA VOLTA ESTRATTI VANNO QUANTIFICATI QUANTIFICAZIONE DEI CAMPIONI Vi sono numerosi metodi. Alcuni forniscono valori assoluti, altri relativi; in tal caso lo standard
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Cromatografia di scambio ionico su colonna
 S.A.G.T. Anno Accademico 2009/2010 Laboratorio Ambientale II A Dottoressa Valentina Gianotti Marco Soda Matricola num. 10015062 Cromatografia di scambio ionico su colonna La cromatografia è un metodo di
S.A.G.T. Anno Accademico 2009/2010 Laboratorio Ambientale II A Dottoressa Valentina Gianotti Marco Soda Matricola num. 10015062 Cromatografia di scambio ionico su colonna La cromatografia è un metodo di
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Principi di Biochimica
 Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
Principi di Biochimica Augusto Innocenti Biologo Nutrizionista Perfezionamento in Biochimica e Biologia Molecolare Phd in Neurobiologia e Neurofisiologia Materia: Atomi e Molecole La materie è costituita
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Antimo Di Maro. Lezione 3. Corso di Laurea in Scienze Biologiche
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
3.3.2. ALIMENTI DI ORIGINE VEGETALE. 3.3.2.1. Verdure
 3.3.2. ALIMENTI DI ORIGINE VEGETALE 3.3.2.1. Verdure Nella Tabella 9 sono riportati i valori degli aminoacidi liberi presenti in alcune fra le più diffuse verdure in commercio. In un passato recente era
3.3.2. ALIMENTI DI ORIGINE VEGETALE 3.3.2.1. Verdure Nella Tabella 9 sono riportati i valori degli aminoacidi liberi presenti in alcune fra le più diffuse verdure in commercio. In un passato recente era
moli OH - /mole amminoacido
 ) ) Di seguito è riportata la curva di titolazione di un amminoacido. Osservando il grafico: a) stabilire il valore dei pka dell aminoacido b) calcolare il valore del pi e individuarlo sul grafico. c)
) ) Di seguito è riportata la curva di titolazione di un amminoacido. Osservando il grafico: a) stabilire il valore dei pka dell aminoacido b) calcolare il valore del pi e individuarlo sul grafico. c)
I componenti chimici delle cellule
 I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D
 Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D Spettrofotometro cuvetta monocromatore rivelatore
Metodi di studio delle proteine : determinazione della quantità determinazione della struttura primaria (sequenza a.a.) determinazione della struttura 3D Spettrofotometro cuvetta monocromatore rivelatore
Jay Phelan, Maria Cristina Pignocchino. Scopriamo la biologia
 Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
1.2.5 Titolazioni acido-base
 1.2.5 Titolazioni acidobase Queste titolazioni si basano su reazioni di neutralizzazione in cui un acido cede un protone ad una base capace di accettarlo. Nel caso più semplice di un acido forte (es. HCl)
1.2.5 Titolazioni acidobase Queste titolazioni si basano su reazioni di neutralizzazione in cui un acido cede un protone ad una base capace di accettarlo. Nel caso più semplice di un acido forte (es. HCl)
La massa è la quantità di materia di cui è fatta una qualsiasi cosa
 Dall atomo all organizzazione cellulare Tutti gli organismi viventi sono costituiti da atomi Due o più atoni insieme formano le molecole La materia è tutto ciò che occupa uno spazio, ha un volume e una
Dall atomo all organizzazione cellulare Tutti gli organismi viventi sono costituiti da atomi Due o più atoni insieme formano le molecole La materia è tutto ciò che occupa uno spazio, ha un volume e una
BIOCHIMICA e BIOTECNOLOGIE degli ALIMENTI
 Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2016-17 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Seconda Università degli Studi di Napoli DiSTABiF Anno Accademico 2016-17 Corso di Laurea Magistrale in SCIENZE DEGLI ALIMENTI E DELLA NUTRIZIONE UMANA Insegnamento di BIOCHIMICA e BIOTECNOLOGIE degli
Analisi quantitativa dell interazione proteina-proteina
 Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Analisi quantitativa dell interazione proteina-proteina Legame recettore-ligando (proteina-proteina) Il legame per il ligando deve essere: reversibile ad alta affinità saturabile deve portare ad una risposta
Modulo 3. Lavorare con le proteine
 Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
Modulo 3 Lavorare con le proteine La purificazione delle proteine Il primo passaggio nello studio delle proprietà di una proteina è la sua purificazione: la sua estrazione dalla matrice biologica in cui
I componenti chimici delle cellule
 I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
I componenti chimici delle cellule Piccole molecole Macromolecole Piccole molecole C, H, N ed O costituiscono quasi il 99% del peso di una cellula Il 70 % della massa di una cellula è costituito da acqua
Soluzioni. Miscele: (gas in gas) Leghe: (solidi in solidi) Soluzioni p.d: (solventi liquidi)
 Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
Soluzioni Sono miscele omogenee in cui si riconoscono 2 componenti o fasi: il soluto, presente in quantità minore il solvente presente in quantità maggiore. Tipi di soluzioni: Miscele: (gas in gas) Leghe:
*Gli atomi sono tutti uguali tra loro?
 *Gli atomi sono tutti uguali tra loro? *Pur essendo tutti formati dalle stesse particelle, gli atomi non sono tutti uguali tra loro: alcuni sono più piccoli, altri più grandi. La piccolezza o la grandezza
*Gli atomi sono tutti uguali tra loro? *Pur essendo tutti formati dalle stesse particelle, gli atomi non sono tutti uguali tra loro: alcuni sono più piccoli, altri più grandi. La piccolezza o la grandezza
Analisi spettrofotometrica dell Albumina di siero bovino: applicazione della legge di Lambert-Beer:
 Analisi spettrofotometrica dell Albumina di siero bovino: applicazione della legge di Lambert-Beer: Introduzione: La spettrofotometria o fotometria è una tecnica analitica che sfrutta il fenomeno dell'assorbimento
Analisi spettrofotometrica dell Albumina di siero bovino: applicazione della legge di Lambert-Beer: Introduzione: La spettrofotometria o fotometria è una tecnica analitica che sfrutta il fenomeno dell'assorbimento
EQUILIBRI IN SOLUZIONE ACQUOSA
 EQUILIBRI IN SOLUZIONE ACQUOSA Costante di equilibrio Si consideri la seguente reazione di equilibrio: aa + bb cc + dd La costante di equilibrio della reazione ad una data temperatura è definita come il
EQUILIBRI IN SOLUZIONE ACQUOSA Costante di equilibrio Si consideri la seguente reazione di equilibrio: aa + bb cc + dd La costante di equilibrio della reazione ad una data temperatura è definita come il
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
TECNICHE CROMATOGRAFICHE ISOLAMENTO DI MOLECOLE BIOLOGICHE Distruzione delle cellule e dei tessuti che contengono le molecole biologiche di nostro interesse (proteine o acidi nucleici) -Tampone (ph) -Sali
Cromatografia ionica (IC)
 Cromatografia ionica (IC) Il principio di base della cromatografia ionica è lo scambio ionico su resine scambiatrici forti, che costituiscono la fase stazionaria con cui sono impaccate le colonne, in parziale
Cromatografia ionica (IC) Il principio di base della cromatografia ionica è lo scambio ionico su resine scambiatrici forti, che costituiscono la fase stazionaria con cui sono impaccate le colonne, in parziale
CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica
 Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
Laurea triennale in BIOLOGIA A. A. 2013-14 14 CHIMICA Ven 15 novembre 2013 Lezioni di Chimica Fisica Spettroscopia UltraVioletta-Visibile ibile (UV( UV-vis) 2^ parte Fluorescenza e Fosforescenza Prof.
FORMULARIO DI CHIMICA
 ARGOMENTO Grandezze chimiche fondamentali: 1. Numero di Avogadro 2. Mole 3. Massa Molare 4. Densità 5. Volume molare di un gas Modi di esprimere la concentrazione: 1. Molare M 2. Parti per milione ppm
ARGOMENTO Grandezze chimiche fondamentali: 1. Numero di Avogadro 2. Mole 3. Massa Molare 4. Densità 5. Volume molare di un gas Modi di esprimere la concentrazione: 1. Molare M 2. Parti per milione ppm
Argomenti 2 lezione. Bilanciamento delle reazioni chimiche. Resa teorica e resa effettiva. Esercitazioni di Chimica Generale ed Inorganica 2
 Un composto contenente sodio, cloro e ossigeno ha una percentuale in massa di sodio del 25.42. Se 3.25 g di tale composto forniscono 4.33 x 10 22 atomi di ossigeno, calcolare la formula minima. Na: 25.42
Un composto contenente sodio, cloro e ossigeno ha una percentuale in massa di sodio del 25.42. Se 3.25 g di tale composto forniscono 4.33 x 10 22 atomi di ossigeno, calcolare la formula minima. Na: 25.42
Estrazione con solventi. Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti
 Estrazione con solventi Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti Estrazione in Soxhlet Vantaggi: Estrazione in continuo Refrigerante Svantaggi: richiede molte ore (12/24)
Estrazione con solventi Dott.ssa Laura Casu Laurea in chimica e tecnologie farmaceutiche 9 crediti Estrazione in Soxhlet Vantaggi: Estrazione in continuo Refrigerante Svantaggi: richiede molte ore (12/24)
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
cromatografia Elettroforesi
 Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
Cromatografia ed Elettroforesi Prof.ssa Flavia Frabetti Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per potere
