2011 Reazione dell acido L-(+)-tartarico con etanolo per formare il dietil estere dell acido L-(+)-tartarico via catalisi acida
|
|
|
- Norberto Fumagalli
- 5 anni fa
- Visualizzazioni
Transcript
1 2011 Reazione dell acido L-(+)-tartarico con etanolo per formare il dietil estere dell acido L-(+)-tartarico via catalisi acida O H HO O C C OH OH H OH O O CH C 3 Amberlite 15 H OH + 2 H 3 C OH + 2 H HO H 2 O C O O CH 3 C 4 H 6 O 6 (150.1) C 2 H 6 O (46.1) C 8 H 14 O 6 (206.2) Classificazione Tipo di reazione e classi di sostanze Reazione del gruppo carbossile degli acidi carbossilici, esterificazione; Acido carbossilico, alcol, estere di acido carbossilico, scambiatore ionico, catalizzatore acido; Tecniche usate Riscaldamento sotto riflusso, filtrazione, concentrazione con evaporatore rotante, distillazione a pressione ridotta, agitazione con ancoretta magnetica, bagno di raffreddamento a ghiaccio, bagno riscaldante ad olio; Istruzioni (scala dell esperimento: 500 mmol) Attrezzatura Pallone da 1 L, condensatore a riflusso, valvola essiccante, agitatore magnetico riscaldante con ancoretta magnetica, regolatore elettronico della temperatura, evaporatore rotante, imbuto di vetro (grande), apparato per distillazione, pompa da vuoto, bagno ad olio, bagno di ghiaccio; Sostanze acido L-(+)-tartarico (pf 170 C) etanolo anidro (pe 78 C) Amberlite 15 (scambiatore acido forte) 75,0 g (500 mmol) 288 g (365 ml, 6,25 mol) 5,0 g Reazione Predisporre un pallone da 1 L asciutto e dotarlo di ancoretta magnetica e condensatore a riflusso con valvola essiccante; mettere nel recipiente 5,0 g di Amberlite 15, 288 g (365 ml, 6,25 mol) di etanolo anidro e 75,0 g (500 mmol) di acido L-(+)-tartarico. Mantenendo sotto costante agitazione, scaldare il tutto a riflusso per 48 ore. È molto importante mantenere bassa la velocità dell ancoretta magnetica, in maniera tale da evitare ritardi nell ebollizione; 1
2 un agitazione troppo vigorosa, inoltre, potrebbe frantumare l Amberlite (aspetto che ne renderebbe particolarmente difficile la successiva eliminazione tramite filtrazione). Work up Senza interrompere l agitazione, raffreddare la miscela di reazione in un bagno di ghiaccio; spegnere l agitatore magnetico solo verso la fine, in maniera tale che l Amberlite si possa depositare sul fondo del pallone. Ricorrendo ad un filtro a pieghe, filtrare la soluzione in un pallone pulito; eliminare quindi (molto rapidamente) quanto più etanolo possibile mediante evaporatore rotante (pressione: 20 hpa). Il prodotto grezzo si presenta come residuo liquido incolore, dalla consistenza leggermente oleosa. Resa di prodotto grezzo: 95,5 g; Trasferire il prodotto grezzo in un pallone da 250 ml e purificarlo mediante distillazione frazionata a pressione ridotta (circa 10-1 hpa) in un apparato per distillazione. Normalmente il prodotto distilla ad una temperatura che rimane costante lungo l intero processo e le singole frazioni presentano indici di rifrazione praticamente identici tra loro. Per evitare reazioni di decomposizione indesiderate (con formazione di sostanze volatili), è necessario lavorare ad una temperatura del bagno ad olio inferiore ai 165 C: questo inconveniente può essere superato senza difficoltà, a patto di mantenere una pressione sufficientemente bassa all interno dell apparecchiatura. Resa: 78,5 g (381 mmol, 76%); punto di ebollizione: C ( hpa); aspetto: liquido incolore; purezza secondo analisi GC: 98,4%; potere rotatorio specifico: [α] D 20 (sostanza pura); = Come residuo di distillazione si ottengono 16,5 g di materiale viscoso (leggermente colorato di giallo), che si indurisce durante il raffreddamento; il solido risultante (dall aspetto vetroso) può, tuttavia, essere sciolto in acqua tiepida. Commenti In presenza di acidi, è possibile che l acido tartarico liberi H 2 O e CO 2, fornendo in questo modo acido piruvico. Nelle condizioni sperimentali descritte, tuttavia, non è stato riscontrato alcuno sviluppo di CO 2 dall ambiente di reazione: collocando un contabolle riempito con una soluzione di idrossido di bario sull estremità del condensatore a riflusso, infatti, non è stato possibile individuare alcuna traccia di CO 2 (nessun intorbidamento della soluzione). Gestione dei rifiuti Riciclo L etanolo evaporato viene raccolto e distillato. 2
3 Suggerimenti per lo smaltimento dei rifiuti Rifiuto/i Residuo di distillazione (sciolto in poca acqua tiepida) Amberlite 15 Smaltimento Miscele acquose di solventi, non contenenti alogeni Rifiuti solidi, non contenenti mercurio Durata dell esperimento 4-5 ore, escluso il tempo necessario per scaldare a riflusso la miscela. A seconda dei casi, la filtrazione dell Amberlite 15 può richiedere molto tempo. Quando posso interrompere l esperimento? Dopo aver evaporato l etanolo. Grado di difficoltà Facile Istruzioni (scala dell esperimento: 100 mmol) Attrezzatura Pallone da 250 ml, condensatore a riflusso, valvola essiccante, agitatore magnetico riscaldante con ancoretta magnetica, regolatore elettronico della temperatura, evaporatore rotante, imbuto di vetro (grande), apparato per distillazione, pompa da vuoto, bagno ad olio, bagno di ghiaccio; Sostanze acido L-(+)-tartarico (pf 170 C) etanolo anidro (pe 78 C) Amberlite 15 (scambiatore acido forte) 15,0 g (100 mmol) 57,6 g (73,0 ml, 1,25 mol) 1,0 g Reazione Predisporre un pallone da 250 ml asciutto e dotarlo di ancoretta magnetica e condensatore a riflusso con valvola essiccante; mettere nel recipiente 1,0 g di Amberlite 15, 57,6 g (73,0 ml, 1,25 mol) di etanolo anidro e 15,0 g (100 mmol) di acido L-(+)-tartarico. Mantenendo sotto costante agitazione, scaldare il tutto a riflusso per 48 ore. È molto importante mantenere bassa la velocità dell ancoretta magnetica, in maniera tale da evitare ritardi nell ebollizione; un agitazione troppo vigorosa, inoltre, potrebbe frantumare l Amberlite (aspetto che ne renderebbe particolarmente difficile la successiva eliminazione tramite filtrazione). Work up Senza interrompere l agitazione, raffreddare la miscela di reazione in un bagno di ghiaccio; spegnere l agitatore magnetico solo verso la fine, in maniera tale che l Amberlite si possa depositare sul fondo del pallone. Ricorrendo ad un filtro a pieghe, filtrare la soluzione in un pallone pulito; eliminare quindi (molto rapidamente) quanto più etanolo possibile mediante evaporatore rotante (pressione: 20 hpa). 3
4 Il prodotto grezzo si presenta come residuo liquido incolore, dalla consistenza leggermente oleosa. Resa di prodotto grezzo: 19,1 g; Trasferire il prodotto grezzo in un pallone da 50 ml e purificarlo mediante distillazione frazionata a pressione ridotta (circa 10-1 hpa) in un apparato per distillazione. Normalmente il prodotto distilla ad una temperatura che rimane costante lungo l intero processo e le singole frazioni presentano indici di rifrazione praticamente identici tra loro. Per evitare reazioni di decomposizione indesiderate (con formazione di sostanze volatili), è necessario lavorare ad una temperatura del bagno ad olio inferiore ai 165 C: questo inconveniente può essere superato senza difficoltà, a patto di mantenere una pressione sufficientemente bassa all interno dell apparecchiatura. Resa: 15,7 g (76,1 mmol, 76%); punto di ebollizione: C ( hpa); aspetto: liquido incolore; purezza secondo analisi GC: 98,4%; potere rotatorio specifico: [α] D 20 (sostanza pura); = Come residuo di distillazione si ottengono 3,30 g di materiale viscoso (leggermente colorato di giallo), che si indurisce durante il raffreddamento; il solido risultante (dall aspetto vetroso) può, tuttavia, essere sciolto in acqua tiepida. Commenti In presenza di acidi, è possibile che l acido tartarico liberi H 2 O e CO 2, fornendo in questo modo acido piruvico. Nelle condizioni sperimentali descritte, tuttavia, non è stato riscontrato alcuno sviluppo di CO 2 dall ambiente di reazione: collocando un contabolle riempito con una soluzione di idrossido di bario sull estremità del condensatore a riflusso, infatti, non è stato possibile individuare alcuna traccia di CO 2 (nessun intorbidamento della soluzione). Gestione dei rifiuti Riciclo L etanolo evaporato viene raccolto e distillato. Suggerimenti per lo smaltimento dei rifiuti Rifiuto/i Residuo di distillazione (sciolto in poca acqua tiepida) Amberlite 15 Smaltimento Miscele acquose di solventi, non contenenti alogeni Rifiuti solidi, non contenenti mercurio 4
5 Durata dell esperimento 4-5 ore, escluso il tempo necessario per scaldare a riflusso la miscela. A seconda dei casi, la filtrazione dell Amberlite 15 può richiedere molto tempo. Quando posso interrompere l esperimento? Dopo aver evaporato l etanolo. Grado di difficoltà Facile Istruzioni (scala dell esperimento: 20 mmol) Attrezzatura Pallone da 50 ml, condensatore a riflusso, valvola essiccante, agitatore magnetico riscaldante con ancoretta magnetica, regolatore elettronico della temperatura, evaporatore rotante, imbuto di vetro, apparato per micro-distillazione, pompa da vuoto, bagno ad olio, bagno di ghiaccio; Sostanze acido L-(+)-tartarico (pf 170 C) etanolo anidro (pe 78 C) Amberlite 15 (scambiatore acido forte) 3,0 g (20,0 mmol) 11,5 g (14,6 ml, 250 mmol) 200 mg Reazione Predisporre un pallone da 50 ml asciutto e dotarlo di ancoretta magnetica e condensatore a riflusso con valvola essiccante; mettere nel recipiente 200 mg di Amberlite 15, 11,5 g (14,6 ml, 250 mmol) di etanolo anidro e 3,0 g (20,0 mmol) di acido L-(+)-tartarico. Mantenendo sotto costante agitazione, scaldare il tutto a riflusso per 48 ore. È molto importante mantenere bassa la velocità dell ancoretta magnetica, in maniera tale da evitare ritardi nell ebollizione; un agitazione troppo vigorosa, inoltre, potrebbe frantumare l Amberlite (aspetto che ne renderebbe particolarmente difficile la successiva eliminazione tramite filtrazione). Work up Senza interrompere l agitazione, raffreddare la miscela di reazione in un bagno di ghiaccio; spegnere l agitatore magnetico solo verso la fine, in maniera tale che l Amberlite si possa depositare sul fondo del pallone. Ricorrendo ad un filtro a pieghe, filtrare la soluzione in un pallone pulito; eliminare quindi (molto rapidamente) quanto più etanolo possibile mediante evaporatore rotante (pressione: 20 hpa). Il prodotto grezzo si presenta come residuo liquido incolore, dalla consistenza leggermente oleosa. Resa di prodotto grezzo: 3,82 g; Trasferire il prodotto grezzo in un pallone da 10 ml e purificarlo mediante distillazione frazionata a pressione ridotta (circa 10-1 hpa) in un apparato per micro-distillazione. 5
6 Normalmente il prodotto distilla ad una temperatura che rimane costante lungo l intero processo e le singole frazioni presentano indici di rifrazione praticamente identici tra loro. Per evitare reazioni di decomposizione indesiderate (con formazione di sostanze volatili), è necessario lavorare ad una temperatura del bagno ad olio inferiore ai 165 C: questo inconveniente può essere superato senza difficoltà, a patto di mantenere una pressione sufficientemente bassa all interno dell apparecchiatura. Resa: 2,85 g (13,8 mmol, 69%); punto di ebollizione: C ( hpa); aspetto: liquido incolore; purezza secondo analisi GC: 98,4%; potere rotatorio specifico: [α] D 20 (sostanza pura); = Come residuo di distillazione si ottengono 920 mg di materiale viscoso (leggermente colorato di giallo), che si indurisce durante il raffreddamento; il solido risultante (dall aspetto vetroso) può, tuttavia, essere sciolto in acqua tiepida. Commenti In presenza di acidi, è possibile che l acido tartarico liberi H 2 O e CO 2, fornendo in questo modo acido piruvico. Nelle condizioni sperimentali descritte, tuttavia, non è stato riscontrato alcuno sviluppo di CO 2 dall ambiente di reazione: collocando un contabolle riempito con una soluzione di idrossido di bario sull estremità del condensatore a riflusso, infatti, non è stato possibile individuare alcuna traccia di CO 2 (nessun intorbidamento della soluzione). Gestione dei rifiuti Riciclo L etanolo evaporato viene raccolto e distillato. Suggerimenti per lo smaltimento dei rifiuti Rifiuto/i Residuo di distillazione (sciolto in poca acqua tiepida) Amberlite 15 Smaltimento Miscele acquose di solventi, non contenenti alogeni Rifiuti solidi, non contenenti mercurio Durata dell esperimento 3 ore, escluso il tempo necessario per scaldare a riflusso la miscela. A seconda dei casi, la filtrazione dell Amberlite 15 può richiedere molto tempo. Quando posso interrompere l esperimento? Dopo aver evaporato l etanolo. Grado di difficoltà Facile 6
7 Caratterizzazione Monitoraggio della reazione tramite HPLC Le condizioni HPLC utilizzate non hanno permesso di analizzare con sicurezza l acido tartarico in presenza del dietil estere relativo. L analisi quantitativa del prodotto è stata quindi effettuata aggiungendo uno standard interno (acetanilide) ai diversi campioni. Preparazione del campione (per scala da 100 mmol): Utilizzare come recipiente di reazione un pallone a 2 o 3 colli da 250 ml (invece di quello a collo singolo), in maniera tale da rendere più agevole il prelievo dei campioni attraverso le aperture laterali. Abbassare il bagno ad olio e attendere che la miscela di reazione smetta di bollire; spegnere l agitatore magnetico ed aspettare che l Amberlite si depositi sul fondo del pallone (1 minuto circa). Prelevare 5 ml di soluzione tramite una pipetta Pasteur e trasferire il tutto in una provetta: chiudere immediatamente il contenitore e raffreddarlo in un bagno di ghiaccio. Conservare il campione in freezer fino al momento dell analisi. Utilizzare come standard interno una soluzione ottenuta sciogliendo 1,11 mg di acetanilide in 10 ml di etanolo anidro. Appena prima dell analisi, diluire il campione con etanolo anidro in un rapporto di 1 : 20 (rispettivamente); prelevare 1 ml della soluzione diluita e miscelarla con 1 ml di standard interno. Iniettare 15 µl della soluzione finale risultante. Condizioni HPLC: Colonna: Phenomenex Luna C18; dimensione delle particelle: 3 µm; lunghezza: 150 mm; diametro interno: 4;6 mm; Temperatura della colonna: 25 C; Volume iniettato: 15 µl; Eluizione in gradiente: 0 min 3% MeOH + 97% H 2 O; 30 min 98% MeOH + 2% H 2 O; 40 min 98% MeOH + 2% H 2 O; Flusso: 6 ml/min; Lunghezza d onda del rivelatore: 220 nm; 7
8 HPLC di un campione prelevato 6 ore dopo l inizio della reazione mau min HPLC di un campione prelevato 96 ore dopo l inizio della reazione mau min Tempo di ritenzione [min] Sostanza 16.2 dietil estere dell acido tartarico 18.0 acetanilide (standard interno) 8
9 Concentrazione del dietil estere dell acido tartarico in funzione del tempo di reazione nei campioni analizzati tramite HPLC Concentrazione dell estere [mg/ml] 250 ester concentration [mg/ml] Tempo time [ore] [h] Monitoraggio della reazione tramite work up preparativo dopo differenti tempi di reazione Tempo di reazione [ore] Scala dell esperimento [mmol] Resa [%] (prodotto isolato) Determinazione del dietil estere dell acido tartarico nel prodotto grezzo tramite HPLC (work up condotto dopo un tempo di reazione pari a 48 ore) La concentrazione del dietil estere dell acido tartarico è stata determinata quantitativamente ricorrendo all acetanilide come standard interno. Preparazione: Standard interno: sciogliere 1 mg di acetanilide in 10 ml di metanolo; Campione: sciogliere il prodotto grezzo in metanolo, rispettando la proporzione di 2 mg di sostanza per ml di solvente; Per la misura: miscelare 1 ml di soluzione standard e 1 ml di soluzione del campione. Iniettare 15 µl della soluzione risultante. Le condizioni HPLC utilizzate sono analoghe a quelle descritte nella sezione sul monitoraggio della reazione. 9
10 HPLC del prodotto grezzo isolato mau min Tempo di ritenzione [min] Sostanza 16.3 dietil estere dell acido tartarico 17.9 acetanilide (standard interno) Risultato dell analisi quantitativa delle diverse prove condotte (le ripetizioni differivano per le quantità di prodotto ottenibili): La massa di dietil estere dell acido tartarico riscontrata nel prodotto grezzo equivale mediamente ad una resa del 75% (con una variazione del 7%). Analisi GC Preparazione del campione: sciogliere 11,4 mg di sostanza in 0,5 ml di diclorometano. Condizioni GC: Colonna: Zebron ZB-1 (Phenomenex, Torrance, CA, USA); lunghezza: 15 m; diametro interno: 0,25 Iniezione: Gas carrier: Forno: Rivelatore: Integrazione: mm; film: 0,25 µm; Temperatura dell iniettore: 250 C; sistema split di iniezione; volume iniettato: 0,2 µl; He; pressione pre-colonna: 90 kpa; Temperatura iniziale: 30 C (4 min); 20 C/min fino a 240 C (7 min); FID, 230 C; H 2 30,8 ml/min; aria 361 ml/min; gas di supporto: N 2, flusso: 14,9 ml/min (59 kpa); Integrator 4290 (Thermo Separation Products); La concentrazione percentuale è stata calcolata tramite i valori delle aree dei picchi. 10
11 GC del prodotto puro 3,5 3,0 2,5 2,0 1,5 1,0 0,5 0, Tempo di ritenzione [min] Sostanza Area [%] del picco 19.8 dietil estere dell acido tartarico non identificata 1.6 Spettro 1 H NMR del prodotto grezzo (250 MHz, CDCl 3 ) (ppm) δ [ppm] Molteplicità Numero di H Assegnazione 1.33 t 6 CH q 4 CH s 2 CH OH 4.62 s OH 7.26 solvente 11
12 Spettro 1 H NMR del prodotto puro (250 MHz, CDCl 3 ) (ppm) δ [ppm] Molteplicità Numero di H Assegnazione 1.33 t 6 CH m 2 OH 4.32 q 4 CH s 2 CH OH 7.26 solvente Spettro 1 H NMR del prodotto puro (250 MHz, CDCl 3, scambio con D 2 O) (ppm) δ [ppm] Molteplicità Numero di H Assegnazione 1.33 t 6 CH q 4 CH s 2 CH OH 7.26 solvente 12
13 Spettro 1 H NMR del prodotto puro (250 MHz, DMSO-D 6 ) (ppm) δ [ppm] Molteplicità Numero di H Assegnazione 1.19 t 6 CH m DMSO 3.32 s H 2 O 4.31 q 4 CH d 2 CH OH 5.47 d 2 CH OH Spettro 13 C NMR del prodotto puro (62,5 MHz, CDCl 3 ) (ppm) δ [ppm] Assegnazione CH CH CH OH CO O solvente 13
14 Spettro IR del prodotto puro (film) Trasmissione [%] 80 Transmission [%] Numeri d onda [cm -1 ] Wellenzahl [cm -1 ] [cm -1 ] Assegnazione 3500 O H stretching 2985, 2940, 2910, C H stretching, alcano 1745 C=O stretching Lo spettro IR del prodotto grezzo non presenta differenze significative rispetto a quello sopra riportato. 14
2006 Reazione dell (R)-(-)-carvone con benzilammina in presenza di Montmorillonite K-10 per formare una base di Schiff
 6 Reazione dell (R)-(-)-carvone con benzilammina in presenza di Montmorillonite K-1 per formare una base di Schiff CH 3 O + CH 2 NH 2 Montmorillonite K-1 cicloesano CH 3 NCH 2 Ph + H 2 O H 3 C CH 2 C 1
6 Reazione dell (R)-(-)-carvone con benzilammina in presenza di Montmorillonite K-1 per formare una base di Schiff CH 3 O + CH 2 NH 2 Montmorillonite K-1 cicloesano CH 3 NCH 2 Ph + H 2 O H 3 C CH 2 C 1
4023 Sintesi dell estere etilico dell acido ciclopentanon-2-carbossilico. estere dietilico dell acido adipico (pe 245 C)
 NP 4023 Sintesi dell estere etilico dell acido ciclopentanon-2-carbossilico dall estere dietilico dell acido adipico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Classificazione
NP 4023 Sintesi dell estere etilico dell acido ciclopentanon-2-carbossilico dall estere dietilico dell acido adipico NaEt C 10 H 18 4 Na C 2 H 6 C 8 H 12 3 (202.2) (23.0) (46.1) (156.2) Classificazione
4010 Sintesi del p-metossiacetofenone dall anisolo
 4010 Sintesi del p-metossiacetofenone dall anisolo C 3 + 3 C C 3 Zeolite -BEA 25 C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Classificazione Tipo di reazione e classi
4010 Sintesi del p-metossiacetofenone dall anisolo C 3 + 3 C C 3 Zeolite -BEA 25 C 3 + C 3 C C 3 C 7 8 (108.1) C 4 6 3 (102.1) C 9 10 2 (150.2) C 2 4 2 (60.1) Classificazione Tipo di reazione e classi
4004 Sintesi del gamma-decalattone da 1-ottene ed estere etilico dell acido iodoacetico
 4004 Sintesi del gamma-decalattone da 1-ottene ed estere etilico dell acido iodoacetico + I CH 2 CH 3 Cu + CH 3 CH 2 I C 8 H 16 C 4 H 7 I 2 C 10 H 18 2 (112.2) (214.0) (63.6) (170.3) C 2 H 5 I (156.0)
4004 Sintesi del gamma-decalattone da 1-ottene ed estere etilico dell acido iodoacetico + I CH 2 CH 3 Cu + CH 3 CH 2 I C 8 H 16 C 4 H 7 I 2 C 10 H 18 2 (112.2) (214.0) (63.6) (170.3) C 2 H 5 I (156.0)
4013 Sintesi del benzalacetofenone da benzaldeide e acetofenone
 4013 Sintesi del benzalacetofenone da benzaldeide e acetofenone montmorillonite KSF/ + + H 2 C 8 H 8 C 7 H 6 C 15 H 12 (120.2) (106.1) (208.3) Classificazione Tipo di reazione e classi di sostanze Reazione
4013 Sintesi del benzalacetofenone da benzaldeide e acetofenone montmorillonite KSF/ + + H 2 C 8 H 8 C 7 H 6 C 15 H 12 (120.2) (106.1) (208.3) Classificazione Tipo di reazione e classi di sostanze Reazione
2008 Esterificazione dell acido propionico con 1-butanolo via catalisi acida per formare l estere butilico dell acido propionico
 28 Esterificazione dell acido propionico con 1-butanolo via catalisi acida per formare l estere butilico dell acido propionico H 3 C H acido 4-toluensolfonico + H C cicloesano 3 H CH 3 + CH 3 H 2 C 3 H
28 Esterificazione dell acido propionico con 1-butanolo via catalisi acida per formare l estere butilico dell acido propionico H 3 C H acido 4-toluensolfonico + H C cicloesano 3 H CH 3 + CH 3 H 2 C 3 H
4026 Sintesi del 2-cloro-2-metilpropano (tert-butil cloruro) dal tert-butanolo
 4026 Sintesi del 2-cloro-2-metilpropano (tert-butil cloruro) dal tert-butanolo OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Classificazione Tipo di reazione e classi di sostanze Sostituzione
4026 Sintesi del 2-cloro-2-metilpropano (tert-butil cloruro) dal tert-butanolo OH + HCl Cl + H 2 O C 4 H 10 O C 4 H 9 Cl (74.1) (36.5) (92.6) Classificazione Tipo di reazione e classi di sostanze Sostituzione
2029 Reazione della trifenilfosfina con l estere metilico dell acido bromoacetico per ottenere il bromuro di (carbometossimetil)trifenilfosfonio
 2029 Reazione della trifenilfosfina con l estere metilico dell acido bromoacetico per ottenere il bromuro di (carbometossimetil)trifenilfosfonio C H 3 Br + Br H 3 C C 3 H 5 Br 2 C 18 H 15 (153.0) (262.3)
2029 Reazione della trifenilfosfina con l estere metilico dell acido bromoacetico per ottenere il bromuro di (carbometossimetil)trifenilfosfonio C H 3 Br + Br H 3 C C 3 H 5 Br 2 C 18 H 15 (153.0) (262.3)
3012 Sintesi dell adamantilidenadamantano dall adamantanone
 Sintesi dell adamantilidenadamantano dall adamantanone O TiCl / Zn THF C H O (.) TiCl Zn (9.) (.) C H (.) Riferimento in letteratura: D. Lenoir, Synthesis, 99, -9; Classificazione Tipo di reazione e classi
Sintesi dell adamantilidenadamantano dall adamantanone O TiCl / Zn THF C H O (.) TiCl Zn (9.) (.) C H (.) Riferimento in letteratura: D. Lenoir, Synthesis, 99, -9; Classificazione Tipo di reazione e classi
1007 Sintesi della 2,4,6-tribromoanilina dalla 4-bromoacetanilide
 1007 Sintesi della 2,4,6-tribromoanilina dalla 4-bromoacetanilide O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Classificazione Tipo di reazione e classi
1007 Sintesi della 2,4,6-tribromoanilina dalla 4-bromoacetanilide O HN CH 3 NH 2 NH 2 KOH 2 C 8 H 8 NO C 6 H 6 N C 6 H 4 3 N (214.1) (56.1) (172.0) (159.8) (329.8) Classificazione Tipo di reazione e classi
4006 Sintesi dell estere etilico dell acido 2-(3-ossobutil)- ciclopentanon-2-carbossilico
 NP 4006 Sintesi dell estere etilico dell acido 2-(3-ossobutil)- ciclopentanon-2-carbossilico CEt + FeCl 3 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Classificazione Tipo di
NP 4006 Sintesi dell estere etilico dell acido 2-(3-ossobutil)- ciclopentanon-2-carbossilico CEt + FeCl 3 6 H 2 CEt C 8 H 12 3 C 4 H 6 C 12 H 18 4 (156.2) (70.2) (270.3) (226.3) Classificazione Tipo di
1024 Eliminazione di acqua dal 4-idrossi-4-metil-2-pentanone
 NP 0 Eliminazione di acqua dal -idrossi--metil--pentanone C H I CH CH H C CH - H H + H C CH H C CH C H I C H 0 (.) (.8) (98.) Classificazione Tipo di reazione e classi di sostanze Eliminazione; Alcol,
NP 0 Eliminazione di acqua dal -idrossi--metil--pentanone C H I CH CH H C CH - H H + H C CH H C CH C H I C H 0 (.) (.8) (98.) Classificazione Tipo di reazione e classi di sostanze Eliminazione; Alcol,
1006 Bromurazione della 4-etossiacetanilide (fenacetina) a 3-bromo-4-etossiacetanilide
 NP 1006 Bromurazione della 4-etossiacetanilide (fenacetina) a 3-bromo-4-etossiacetanilide KBr 3, HBr acido acetico Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Riferimento in letteratura:
NP 1006 Bromurazione della 4-etossiacetanilide (fenacetina) a 3-bromo-4-etossiacetanilide KBr 3, HBr acido acetico Br C 10 H 13 N 2 C 10 H 12 BrN 2 (179.2) (167.0) (80.9) (258.1) Riferimento in letteratura:
4005 Sintesi dell estere metilico dell acido 9-(5-ossotetraidrofuran-2-il)nonanoico
 NP 4005 Sintesi dell estere metilico dell acido 9-(5-ossotetraidrofuran-2-il)nonanoico H 3 C (CH 2 ) 8 I Cu + CH 2 CH 3 H 3 C (CH 2 ) 8 + CH 3 CH 2 I C 12 H 22 2 C 4 H 7 I 2 C 14 H 24 4 C 2 H 5 I (198.3)
NP 4005 Sintesi dell estere metilico dell acido 9-(5-ossotetraidrofuran-2-il)nonanoico H 3 C (CH 2 ) 8 I Cu + CH 2 CH 3 H 3 C (CH 2 ) 8 + CH 3 CH 2 I C 12 H 22 2 C 4 H 7 I 2 C 14 H 24 4 C 2 H 5 I (198.3)
3034 Sintesi del trans-1,2-cicloesandiolo dal cicloesene
 0 Sintesi del trans-,-cicloesandiolo dal cicloesene H O / HCO C H 0 (8.) Classificazione H O HCO H (.0) (.0) C H O (.) Tipo di reazione e classi di sostanze Addizione agli alcheni, addizione stereoselettiva,
0 Sintesi del trans-,-cicloesandiolo dal cicloesene H O / HCO C H 0 (8.) Classificazione H O HCO H (.0) (.0) C H O (.) Tipo di reazione e classi di sostanze Addizione agli alcheni, addizione stereoselettiva,
2017 Reazione del cinnamoil cloruro con ammoniaca per formare l ammide cinnamica
 217 Reazione del cinnamoil cloruro con ammoniaca per formare l ammide cinnamica O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) Classificazione (17.) C 9 H 9 NO (147.2) Tipo di reazione e classi di sostanze Reazione
217 Reazione del cinnamoil cloruro con ammoniaca per formare l ammide cinnamica O O Cl NH 3 NH 2 C 9 H 7 ClO (166.6) Classificazione (17.) C 9 H 9 NO (147.2) Tipo di reazione e classi di sostanze Reazione
3021 Ossidazione dell antracene ad antrachinone
 ssidazione dell antracene ad antrachinone Ce IV (NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Riferimento in letteratura: Tse-Lok Ho et al., Synthesis 97, 6; Classificazione Tipo di reazione e classi
ssidazione dell antracene ad antrachinone Ce IV (NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Riferimento in letteratura: Tse-Lok Ho et al., Synthesis 97, 6; Classificazione Tipo di reazione e classi
3010 Sintesi del dietil estere dell acido 9,10-diidro-9,10- etanoantracen-11,12-trans-dicarbossilico
 31 Sintesi del dietil estere dell acido 9,1-diidro-9,1- etanoantracen-11,12-trans-dicarbossilico + H CO 2 AlCl 3 O 2 C H CO 2 H O 2 C H C 14 H 1 C 8 H 12 O 4 2 H 22 O 4 (178.2) (172.2) (133.3) (35.4) Riferimento
31 Sintesi del dietil estere dell acido 9,1-diidro-9,1- etanoantracen-11,12-trans-dicarbossilico + H CO 2 AlCl 3 O 2 C H CO 2 H O 2 C H C 14 H 1 C 8 H 12 O 4 2 H 22 O 4 (178.2) (172.2) (133.3) (35.4) Riferimento
4016 Sintesi di (±)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo)
 4016 Sintesi di (±)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo) FeCl 3 6 H 2 O C 10 H 7 C 20 H 14 O 2 (144.2) (270.3) (286.3) Classificazione Tipo di reazione e classi di sostanze Accoppiamento
4016 Sintesi di (±)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo) FeCl 3 6 H 2 O C 10 H 7 C 20 H 14 O 2 (144.2) (270.3) (286.3) Classificazione Tipo di reazione e classi di sostanze Accoppiamento
2022 Riduzione di L-(-)-mentone con litio alluminio idruro per formare una miscela di isomeri di (-)-mentolo e (+)-neomentolo
 22 Riduzione di L-(-)-mentone con litio alluminio idruro per formare una miscela di isomeri di (-)-mentolo e (+)-neomentolo 3 O LiAl 4 tert-butil metil etere 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
22 Riduzione di L-(-)-mentone con litio alluminio idruro per formare una miscela di isomeri di (-)-mentolo e (+)-neomentolo 3 O LiAl 4 tert-butil metil etere 3 O + 3 O a b 10 18 O (154.3) LiAl 4 (38.0)
4019 Sintesi dell estere metilico dell acido acetammidostearico dall estere metilico dell acido oleico
 NP 4019 Sintesi dell estere metilico dell acido acetammidostearico dall estere metilico dell acido oleico C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me
NP 4019 Sintesi dell estere metilico dell acido acetammidostearico dall estere metilico dell acido oleico C 19 H 36 2 (296.5) 10 9 SnCl 4 H 2 Me (260.5) + H 3 C C N C 2 H 3 N (41.1) NH + 10 10 9 9 Me Me
3003 Sintesi del trans-2-clorocicloesanolo dal cicloesene
 3003 Sintesi del trans-2-clorocicloesanolo dal cicloesene _ SO 2 NCl + Na H 2 SO 4 OH + 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H 9
3003 Sintesi del trans-2-clorocicloesanolo dal cicloesene _ SO 2 NCl + Na H 2 SO 4 OH + 3 H 2 O + Cl CH 3 SO 2 NH 2 CH 3 C 6 H 10 (82.2) C 7 H 13 ClNNaO 5 S (281.7) (98.1) C 6 H 11 ClO (134.6) C 7 H 9
2013 Reazione dell acido cinnamico con cloruro di tionile per formare cinnamoil cloruro
 2013 Reazione dell acido cinnamico con cloruro di tionile per formare cinnamoil cloruro O O OH + SOCl 2 Cl + HCl + SO 2 C 9 H 8 O 2 (148.2) (119.0) C 9 H 7 ClO (166.6) Classificazione Tipo di reazione
2013 Reazione dell acido cinnamico con cloruro di tionile per formare cinnamoil cloruro O O OH + SOCl 2 Cl + HCl + SO 2 C 9 H 8 O 2 (148.2) (119.0) C 9 H 7 ClO (166.6) Classificazione Tipo di reazione
3035 Sintesi del cis-1,2-epossiciclottano dal ciclottene
 3035 Sintesi del cis-1,2-epossiciclottano dal ciclottene H 2 O 2 lipasi O C 8 H 14 (110.2) H 2 O 2 (34.0) C 8 H 14 O (126.2) Riferimento in letteratura: S. Warwel, M. Rüsch gen. Klaas, J. Mol. Catalysis
3035 Sintesi del cis-1,2-epossiciclottano dal ciclottene H 2 O 2 lipasi O C 8 H 14 (110.2) H 2 O 2 (34.0) C 8 H 14 O (126.2) Riferimento in letteratura: S. Warwel, M. Rüsch gen. Klaas, J. Mol. Catalysis
2005 Sintesi dell acetonide del meso-1,2-difenil-1,2-etandiolo (2,2-dimetil-4,5-difenil-1,3-diossolano)
 2005 Sintesi dell acetonide del meso-1,2-difenil-1,2-etandiolo (2,2-dimetil-4,5-difenil-1,3-diossolano) Ph H H H H Ph + H 3 C CH 3 - H 2 FeCl 3 H Ph H Ph H 3 C CH 3 C 14 H 14 2 (214.3) C 3 H 6 (58.1) (162.2)
2005 Sintesi dell acetonide del meso-1,2-difenil-1,2-etandiolo (2,2-dimetil-4,5-difenil-1,3-diossolano) Ph H H H H Ph + H 3 C CH 3 - H 2 FeCl 3 H Ph H Ph H 3 C CH 3 C 14 H 14 2 (214.3) C 3 H 6 (58.1) (162.2)
3009 Sintesi dell acido trans-5-norbornen-2,3-dicarbossilico da acido fumarico e ciclopentadiene
 3009 Sintesi dell acido trans-5-norbornen-2,3-dicarbossilico da acido fumarico e ciclopentadiene 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H
3009 Sintesi dell acido trans-5-norbornen-2,3-dicarbossilico da acido fumarico e ciclopentadiene 170 C 2 C 10 H 12 C 5 H 6 (132.2) (66.1) + COOH COOH HOOC COOH C 5 H 6 (66.1) C 4 H 4 O 4 (116.1) C 9 H
1010 Acilazione intramolecolare dell acido 3-fenilpropionico a 2,3-diidroinden-1-one (α-indanone)
 1010 Acilazione intramolecolare dell acido 3-fenilpropionico a 2,3-diidroinden-1-one (α-indanone) H acido polifosforico (PPA) C 9 H 10 2 (150.2) C 9 H 8 (132.2) Classificazione Tipo di reazione e classi
1010 Acilazione intramolecolare dell acido 3-fenilpropionico a 2,3-diidroinden-1-one (α-indanone) H acido polifosforico (PPA) C 9 H 10 2 (150.2) C 9 H 8 (132.2) Classificazione Tipo di reazione e classi
2023 Riduzione della D-(+)-canfora con litio alluminio idruro ad una miscela di isomeri di (+)-borneolo e (-)-isoborneolo
 2023 Riduzione della D-(+)-canfora con litio alluminio idruro ad una miscela di isomeri di (+)-borneolo e (-)-isoborneolo LiAlH 4 tert-butil metil etere H + OH O OH H C 10 H 16 O (152.2) LiAlH 4 (38.0)
2023 Riduzione della D-(+)-canfora con litio alluminio idruro ad una miscela di isomeri di (+)-borneolo e (-)-isoborneolo LiAlH 4 tert-butil metil etere H + OH O OH H C 10 H 16 O (152.2) LiAlH 4 (38.0)
1003 Nitrazione della benzaldeide a 3-nitrobenzaldeide
 1003 Nitrazione della benzaldeide a 3-nitrobenzaldeide H O H O HNO 3 /H 3 / 2 HSO 2 SO 4 4 + sotto-prodotti NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) lassificazione Tipo di reazione
1003 Nitrazione della benzaldeide a 3-nitrobenzaldeide H O H O HNO 3 /H 3 / 2 HSO 2 SO 4 4 + sotto-prodotti NO 2 7 H 6 O HNO 3 (63.0) 7 H 5 NO 3 (106.1) H 2 SO 4 (98.1) (151.1) lassificazione Tipo di reazione
AlCl 3 H 22 (92.6) (133.3) (190.3)
 1011 Sintesi dell 1,4-di-tert-butilbenzene da tert-butilbenzene e tert-butil cloruro + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Classificazione Tipo di reazione e classi di sostanze
1011 Sintesi dell 1,4-di-tert-butilbenzene da tert-butilbenzene e tert-butil cloruro + Cl AlCl 3 C 10 H 14 (134.) C 4 H 9 Cl C 14 H (9.6) (133.3) (190.3) Classificazione Tipo di reazione e classi di sostanze
4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo)
 4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O (286.3) (421.0) enantiomero R enantiomero S Classificazione
4014 Risoluzione enantiomerica di (R)- e (S)-BINOL (2,2 -diidrossi-1,1 -binaftile o 1,1 -bi-2-naftolo) NBCC CH 3 CN + C 20 H 14 O 2 C 26 H 29 ClN 2 O (286.3) (421.0) enantiomero R enantiomero S Classificazione
1023 Separazione dell esperidina dalla buccia d arancia
 NP 0 Separazione dell esperidina dalla buccia d arancia buccia d'arancia H H C H H H H H H H CH C 8 H 5 (60.5) Classificazione Tipo di reazione e classi di sostanze Separazione di composti da prodotti
NP 0 Separazione dell esperidina dalla buccia d arancia buccia d'arancia H H C H H H H H H H CH C 8 H 5 (60.5) Classificazione Tipo di reazione e classi di sostanze Separazione di composti da prodotti
4002 Sintesi del benzile dal benzoino
 4002 Sintesi del benzile dal benzoino H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Classificazione Tipo di reazione e classi di sostanze ssidazione; Alcol, chetone, metallo
4002 Sintesi del benzile dal benzoino H VCl 3 + 1 / 2 2 + 1 / 2 H 2 C 14 H 12 2 C 14 H 10 2 (212.3) 173.3 (210.2) Classificazione Tipo di reazione e classi di sostanze ssidazione; Alcol, chetone, metallo
3016 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico
 6 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.)
6 Ossidazione dell acido ricinoleico (dall olio di ricino) con permanganato di potassio per formare acido azelaico CH -(CH ) OH (CH ) -COOH KMnO 4 /KOH HOOC-(CH ) -COOH C H 4 O (.) KMnO 4 KOH (.) (6.)
5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica
 NP 5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Classificazione
NP 5012 Sintesi dell acido acetilsalicilico (aspirina) da acido salicilico e anidride acetica CH CH + H H 2 S 4 + CH 3 CH C 4 H 6 3 C 7 H 6 3 C 9 H 8 4 C 2 H 4 2 (120.1) (138.1) (98.1) (180.2) (60.1) Classificazione
4024 Sintesi enantioselettiva dell estere etilico dell acido (1R,2S)- cis-idrossiciclopentancarbossilico
 4024 Sintesi enantioselettiva dell estere etilico dell acido (1R,2S)- cis-idrossiciclopentancarbossilico H lievito C 8 H 12 3 C 8 H 14 3 (156.2) (158.2) Classificazione Tipo di reazione e classi di sostanze
4024 Sintesi enantioselettiva dell estere etilico dell acido (1R,2S)- cis-idrossiciclopentancarbossilico H lievito C 8 H 12 3 C 8 H 14 3 (156.2) (158.2) Classificazione Tipo di reazione e classi di sostanze
2004 Riduzione diastereoselettiva del benzoino con sodio boroidruro a 1,2-difenil-1,2-etandiolo
 24 Riduzione diastereoselettiva del benzoino con sodio boroidruro a 1,2-difenil-1,2-etandiolo OH O NaBH 4 H HO OH meso H + H OH H OH racemo C 14 H 12 O 2 (212.3) (37.8) C 14 H 14 O 2 (214.3) Riferimento
24 Riduzione diastereoselettiva del benzoino con sodio boroidruro a 1,2-difenil-1,2-etandiolo OH O NaBH 4 H HO OH meso H + H OH H OH racemo C 14 H 12 O 2 (212.3) (37.8) C 14 H 14 O 2 (214.3) Riferimento
bromuro di (carbometossimetil)trifenilfosfonio
 23 Reazione del bromuro di (carbometossimetil)trifenilfosfonio con la benzaldeide H O H O P O Br + O H 3 C C 2 H 2 BrO 2 P C 7 H 6 O (45.3) (6.) NaOH (4.) + H C H O 2 (62.2) H H O CH 3 O O CH 3 + POPh
23 Reazione del bromuro di (carbometossimetil)trifenilfosfonio con la benzaldeide H O H O P O Br + O H 3 C C 2 H 2 BrO 2 P C 7 H 6 O (45.3) (6.) NaOH (4.) + H C H O 2 (62.2) H H O CH 3 O O CH 3 + POPh
2003 Acetalizzazione della 3-nitrobenzaldeide al corrispondente 1,3-diossolano con etandiolo (glicol etilenico) via catalisi acida
 2003 Acetalizzazione della 3-nitrobenzaldeide al corrispondente 1,3-diossolano con etandiolo (glicol etilenico) via catalisi acida H O NO 2 HO + + HO acido 4-toluensolfonico cicloesano O O NO 2 H 2 O C
2003 Acetalizzazione della 3-nitrobenzaldeide al corrispondente 1,3-diossolano con etandiolo (glicol etilenico) via catalisi acida H O NO 2 HO + + HO acido 4-toluensolfonico cicloesano O O NO 2 H 2 O C
3011 Sintesi dell acido eritro-9,10-diidrossistearico dall acido oleico
 311 Sintesi dell acido eritro-9,1-diidrossistearico dall acido oleico COOH KMnO 4 HO COOH NaOH HO C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Riferimento in letteratura: Lapworth,
311 Sintesi dell acido eritro-9,1-diidrossistearico dall acido oleico COOH KMnO 4 HO COOH NaOH HO C 18 H 34 O 2 (282.5) KMnO 4 (158.) NaOH (4.) C 18 H 36 O 4 (316.5) Riferimento in letteratura: Lapworth,
3018 Sintesi dell acido 3-fenilbenzoico dall acido 3-iodobenzoico
 3018 Sintesi dell acido 3-fenilbenzoico dall acido 3-iodobenzoico COOH COOH + PhB(OH) 2 NaOH/PdCl 2 I Ph C 7 H 5 IO 2 (248.0) C 6 H 7 BO 2 (121.9) NaOH PdCl 2 (40.0) (177.3) C 13 H 10 O 2 (198.2) Riferimento
3018 Sintesi dell acido 3-fenilbenzoico dall acido 3-iodobenzoico COOH COOH + PhB(OH) 2 NaOH/PdCl 2 I Ph C 7 H 5 IO 2 (248.0) C 6 H 7 BO 2 (121.9) NaOH PdCl 2 (40.0) (177.3) C 13 H 10 O 2 (198.2) Riferimento
2028 Reazione del cicloesil magnesio bromuro con anidride carbonica per formare l acido cicloesancarbossilico
 28 Reazione del cicloesil magnesio bromuro con anidride carbonica per formare l acido cicloesancarbossilico Br + Mg dietil etere MgBr 1. CO 2 2. H 3 O + O OH C 6 H 11 Br CO 2 (163.1) (24.3) (44.) C 7 H
28 Reazione del cicloesil magnesio bromuro con anidride carbonica per formare l acido cicloesancarbossilico Br + Mg dietil etere MgBr 1. CO 2 2. H 3 O + O OH C 6 H 11 Br CO 2 (163.1) (24.3) (44.) C 7 H
2002 Acetalizzazione dell estere etilico dell acido acetacetico al corrispondente 1,3-diossolano con etandiolo (glicol etilenico) via catalisi acida
 22 Acetalizzazione dell estere etilico dell acido acetacetico al corrispondente 1,3-diossolano con etandiolo (glicol etilenico) via catalisi acida 2 H 5 + H H Montmorillonite K 1 icloesano 2 H 5 + H 2
22 Acetalizzazione dell estere etilico dell acido acetacetico al corrispondente 1,3-diossolano con etandiolo (glicol etilenico) via catalisi acida 2 H 5 + H H Montmorillonite K 1 icloesano 2 H 5 + H 2
1017 Azoaccoppiamento del cloruro di benzendiazonio con 2-naftolo per formare l 1-fenilazo-2-naftolo
 1017 Azoaccoppiamento del cloruro di benzendiazonio con 2-naftolo per formare l 1-fenilazo-2-naftolo H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5
1017 Azoaccoppiamento del cloruro di benzendiazonio con 2-naftolo per formare l 1-fenilazo-2-naftolo H 3 Cl Cl ao 2 C 6 H 8 Cl (129.6) (69.0) C 6 H 5 Cl 2 (140.6) OH + Cl OH C 10 H 8 O (144.2) C 6 H 5
5026 Ossidazione dell antracene ad antrachinone
 NP 506 ssidazione dell antracene ad antrachinone KMn / Al C H 0 KMn C H 8 (78.) (58.0) (08.) Riferimento in letteratura: Nüchter, M., ndruschka, B., Trotzki, R., J. Prakt. Chem. 000,, No. 7; Classificazione
NP 506 ssidazione dell antracene ad antrachinone KMn / Al C H 0 KMn C H 8 (78.) (58.0) (08.) Riferimento in letteratura: Nüchter, M., ndruschka, B., Trotzki, R., J. Prakt. Chem. 000,, No. 7; Classificazione
1001 Nitrazione del toluene a 4-nitrotoluene, 2-nitrotoluene e 2,4-dinitrotoluene
 1001 Nitrazione del toluene a 4-nitrotoluene, 2-nitrotoluene e 2,4-dinitrotoluene CH 3 CH 3 CH 3 N 2 CH 3 N 2 HN 3 /H 2 S 4 + + ; sotto-prodotti N 2 N 2 C 7 H 8 (92.1) HN 3 (63.0) H 2 S 4 (98.1) C 7 H
1001 Nitrazione del toluene a 4-nitrotoluene, 2-nitrotoluene e 2,4-dinitrotoluene CH 3 CH 3 CH 3 N 2 CH 3 N 2 HN 3 /H 2 S 4 + + ; sotto-prodotti N 2 N 2 C 7 H 8 (92.1) HN 3 (63.0) H 2 S 4 (98.1) C 7 H
5009 Sintesi della ftalocianina rameica
 P 59 Sintesi della ftalocianina rameica (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Riferimento
P 59 Sintesi della ftalocianina rameica (H H ) 6 Mo 7 2 2. H2 + 8 + CuCl H 2-8 H 3-8 C 2 - H 2 - HCl Cu C 8 H 3 CH 2 CuCl H 2 Mo 7 6 2. H 2 C 32 H 16 8 Cu (18.1) (6.1) (99.) (1235.9) (576.1) Riferimento
5001 Nitrazione del fenolo a 2-nitrofenolo e 4-nitrofenolo
 00 Nitrazione del fenolo a -nitrofenolo e -nitrofenolo KNO, H SO + C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Classificazione Tipo di reazione e classi di sostanze Sostituzione elettrofila nei composti
00 Nitrazione del fenolo a -nitrofenolo e -nitrofenolo KNO, H SO + C H O (9.) KNO (0.) H SO (98.) C H NO (9.) Classificazione Tipo di reazione e classi di sostanze Sostituzione elettrofila nei composti
5007 Reazione dell anidride ftalica con la resorcina per formare fluoresceina
 57 Reazione dell anidride ftalica con la resorcina per formare fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificazione Tipo di reazione e classi di sostanze
57 Reazione dell anidride ftalica con la resorcina per formare fluoresceina CH H H + 2 + 2 H 2 H C 8 H 4 3 C 6 H 6 2 C 2 H 12 5 (148.1) (11.1) (332.3) Classificazione Tipo di reazione e classi di sostanze
4029 Sintesi del dodecil fenil etere da bromododecano e fenolo
 4029 Sintesi del dodecil fenil etere da bromododecano e fenolo OH C 12 H 25 Br (249.2) Br + NaOH (40.0) Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 O (94.1) C 18 H 30 O (262.4) O + NaBr (102.9) Classificazione
4029 Sintesi del dodecil fenil etere da bromododecano e fenolo OH C 12 H 25 Br (249.2) Br + NaOH (40.0) Adogen 464 C 25 H 54 ClN (404.2) C 6 H 6 O (94.1) C 18 H 30 O (262.4) O + NaBr (102.9) Classificazione
4001 Trans-esterificazione dell olio di ricino a estere metilico dell acido ricinoleico
 4001 Trans-esterificazione dell olio di ricino a estere metilico dell acido ricinoleico lio di ricino + MeH NaMe H Me CH 4 (32.0) C 19 H 36 3 (312.5) Classificazione Tipo di reazione e classi di sostanze
4001 Trans-esterificazione dell olio di ricino a estere metilico dell acido ricinoleico lio di ricino + MeH NaMe H Me CH 4 (32.0) C 19 H 36 3 (312.5) Classificazione Tipo di reazione e classi di sostanze
4025 Sintesi del 2-iodopropano dal 2-propanolo
 4025 Sintesi del 2-iodopropano dal 2-propanolo OH I + 1/2 I 2 + 1/3 P x + 1/3 P(OH) 3 C 3 H 8 O (60.1) (253.8) (31.0) C 3 H 7 I (170.0) (82.0) Classificazione Tipo di reazione e classi di sostanze Sostituzione
4025 Sintesi del 2-iodopropano dal 2-propanolo OH I + 1/2 I 2 + 1/3 P x + 1/3 P(OH) 3 C 3 H 8 O (60.1) (253.8) (31.0) C 3 H 7 I (170.0) (82.0) Classificazione Tipo di reazione e classi di sostanze Sostituzione
4009 Sintesi dell acido adipico dal cicloesene
 NP 4009 Sintesi dell acido adipico dal cicloesene Na W 4 H + 4 H H H + 4 H Aliquat 336 C 6 H 10 Na W 4 H (39.9) C 6 H 10 4 (8.) (34.0) C 5 H 54 ClN (404.) (146.1) Classificazione Tipo di reazione e classi
NP 4009 Sintesi dell acido adipico dal cicloesene Na W 4 H + 4 H H H + 4 H Aliquat 336 C 6 H 10 Na W 4 H (39.9) C 6 H 10 4 (8.) (34.0) C 5 H 54 ClN (404.) (146.1) Classificazione Tipo di reazione e classi
Chimica Organica II - Laboratorio A.A. 2008/09 2. H 3 O+
 Chimica Organica II - Laboratorio A.A. 2008/09 Esperienza 4 Sintesi del trifenil carbinolo mediante reattivo di Br + Mg MgBr 1. 2. H 3 O+ O C OH C Materiali: Pallone a tre colli da 250 ml, imbuto gocciolatore
Chimica Organica II - Laboratorio A.A. 2008/09 Esperienza 4 Sintesi del trifenil carbinolo mediante reattivo di Br + Mg MgBr 1. 2. H 3 O+ O C OH C Materiali: Pallone a tre colli da 250 ml, imbuto gocciolatore
CROMATOGRAFIA IONICA (IC)
 CROMATOGRAFIA IONICA (IC) CROMATOGRAFIA CROMATOGRAFIA IONICA RESINE A SCAMBIO IONICO Struttura Meccanismo di scambio STRUMENTAZIONE IC SOPPRESSORE A MEMBRANA PROTOCOLLO DI ANALISI CROMATOGRAFIA Analisi
CROMATOGRAFIA IONICA (IC) CROMATOGRAFIA CROMATOGRAFIA IONICA RESINE A SCAMBIO IONICO Struttura Meccanismo di scambio STRUMENTAZIONE IC SOPPRESSORE A MEMBRANA PROTOCOLLO DI ANALISI CROMATOGRAFIA Analisi
INIETTORI PER COLONNE CAPILLARI
 INIETTORI PER COLONNE CAPILLARI Nessun tipo di iniettore è adatto per tutti i tipi di campioni gas, liquidi, solidi (% ppt.) Tutti gli iniettori hanno vantaggi e svantaggi Devono essere studiati e testati
INIETTORI PER COLONNE CAPILLARI Nessun tipo di iniettore è adatto per tutti i tipi di campioni gas, liquidi, solidi (% ppt.) Tutti gli iniettori hanno vantaggi e svantaggi Devono essere studiati e testati
Il riscaldamento può essere effettuato con un bagno ad acqua, ad olio, un mantello scaldante, tenendo in considerazione che deve essere effettuato
 DISTILLAZIONE La distillazione è una tecnica di purificazione che permette la separazione di liquidi o di solidi bassofondenti che fondono senza alterazione chimica. Si basa fondamentalmente sull equilibrio
DISTILLAZIONE La distillazione è una tecnica di purificazione che permette la separazione di liquidi o di solidi bassofondenti che fondono senza alterazione chimica. Si basa fondamentalmente sull equilibrio
BENZILPENICILLINA BENZATINICA PREPARAZIONE INIETTABILI. Benzilpenicillina Benzatinica polvere sterile per preparazioni iniettabili
 1 1 1 1 1 1 1 1 0 1 0 1 0 1 1 01/FU Maggio 00 Commenti entro il 0 Settembre 00 NOTA: Corretta in seguito ai commenti della Dott.ssa Mozzetti La monografia è stata revisionata per armonizzarla con le altre
1 1 1 1 1 1 1 1 0 1 0 1 0 1 1 01/FU Maggio 00 Commenti entro il 0 Settembre 00 NOTA: Corretta in seguito ai commenti della Dott.ssa Mozzetti La monografia è stata revisionata per armonizzarla con le altre
AMPICILLINA SODICA PREPARAZIONE INIETTABILE. Ampicillina sodica polvere sterile per preparazioni iniettabili
 1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
AMOXICILLINA CAPSULE
 0 0 0 0 0 00/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. Caratteri: è stato inserito granulato di colore bianco o paglierino su informazioni di
0 0 0 0 0 00/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. Caratteri: è stato inserito granulato di colore bianco o paglierino su informazioni di
Sintesi dell acetanilide
 Sintesi dell acetanilide N 2 Cl N + + C 3 benzenammina anidride etanoica N - fenilacetammide acido etanoico (anilina) (anidride acetica) (acetanilide) (acido acetico) d = 1,02 g/ml d = 1,08 g/ml PM = 135
Sintesi dell acetanilide N 2 Cl N + + C 3 benzenammina anidride etanoica N - fenilacetammide acido etanoico (anilina) (anidride acetica) (acetanilide) (acido acetico) d = 1,02 g/ml d = 1,08 g/ml PM = 135
Isolamento della caffeina dalle foglie di tè
 SOMMARIO Isolamento della caffeina dalle foglie di tè L esperienza consiste nell isolamento e determinazione della quantità di caffeina, solido bianco cristallino, dalle foglie di tè (Camellia sinensis).
SOMMARIO Isolamento della caffeina dalle foglie di tè L esperienza consiste nell isolamento e determinazione della quantità di caffeina, solido bianco cristallino, dalle foglie di tè (Camellia sinensis).
ACETATO DI METILE urinario in GC-FID Codice GC02510
 ACETATO DI METILE urinario in GC-FID Codice GC02510 BIOCHIMICA L acetato di metile, a temperatura ambiente si presenta come un liquido volatile e incolore; è un composto molto infiammabile ed irritante.
ACETATO DI METILE urinario in GC-FID Codice GC02510 BIOCHIMICA L acetato di metile, a temperatura ambiente si presenta come un liquido volatile e incolore; è un composto molto infiammabile ed irritante.
ANALISI QUALITATIVA E QUANTITATIVA
 ANALISI QUALITATIVA E QUANTITATIVA 1. QUALITATIVA - Cosa è presente Cromatografia- comparare i t R s Spettroscopia - MS, IR, UV 2. QUANTITATIVA - Quantità presente nel campione Altezza del picco Area del
ANALISI QUALITATIVA E QUANTITATIVA 1. QUALITATIVA - Cosa è presente Cromatografia- comparare i t R s Spettroscopia - MS, IR, UV 2. QUANTITATIVA - Quantità presente nel campione Altezza del picco Area del
RISOLUZIONE ENO 25/2004
 DICARBONATO DI DIMETILE (DMDC) L'ASSEMBLEA GENERALE, Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce l'organizzazione internazionale della vigna e del vino Su proposta della
DICARBONATO DI DIMETILE (DMDC) L'ASSEMBLEA GENERALE, Visto l'articolo 2 paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce l'organizzazione internazionale della vigna e del vino Su proposta della
ANALISI DEI COMPOSTI VOLATILI PRESENTI NEI VINI MEDIANTE GASCROMATOGRAFIA ANALISI DEI COMPOSTI VOLATILI PRESENTI NEI VINI MEDIANTE GASCROMATOGRAFIA
 RISOLUZIONE OIV-OENO 553-2016 ANALISI DEI COMPOSTI VOLATILI PRESENTI NEI VINI MEDIANTE GASCROMATOGRAFIA L ASSEMBLEA GENERALE Visto l'articolo 2, paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce
RISOLUZIONE OIV-OENO 553-2016 ANALISI DEI COMPOSTI VOLATILI PRESENTI NEI VINI MEDIANTE GASCROMATOGRAFIA L ASSEMBLEA GENERALE Visto l'articolo 2, paragrafo 2 iv dell'accordo del 3 aprile 2001 che istituisce
XVII ZOLFO. Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE. Metodo XVII.2 DETERMINAZIONE DELLO ZOLFO DA SOLFATI
 XVII ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE Metodo XVII.2 DETERMINAZIONE DELLO ZOLFO DA SOLFATI XVII - ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE 1. Principio Il campione viene
XVII ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE Metodo XVII.2 DETERMINAZIONE DELLO ZOLFO DA SOLFATI XVII - ZOLFO Metodo XVII.1 DETERMINAZIONE DELLO ZOLFO TOTALE 1. Principio Il campione viene
Laboratorio di Chimica Organica II
 Laboratorio di Chimica Organica II A.A. 2017-2018 Paolo Pengo ppengo@units.it, stanza 344 Valutazione delle attività di laboratorio Griglia di valutazione Comportamento in laboratorio Quaderno di Laboratorio
Laboratorio di Chimica Organica II A.A. 2017-2018 Paolo Pengo ppengo@units.it, stanza 344 Valutazione delle attività di laboratorio Griglia di valutazione Comportamento in laboratorio Quaderno di Laboratorio
CHIMICA ORGANICA I - laboratorio AA 2009/10
 Esperienza 3 ESTRAZIIONE DELL EUGENOLO DAII CHIIODII DII GAROFANO PER DIISTIILLAZIIONE IIN CORRENTE DII VAPORE Gli oli essenziali sono i componenti volatili associati all aroma di molte piante. Tra questi,
Esperienza 3 ESTRAZIIONE DELL EUGENOLO DAII CHIIODII DII GAROFANO PER DIISTIILLAZIIONE IIN CORRENTE DII VAPORE Gli oli essenziali sono i componenti volatili associati all aroma di molte piante. Tra questi,
19a.5.1 Flaconcini in vetro, tipo Vial, con tappo in gomma rivestito in politetrafluoroetilene da 1.8-3.5-15 - 20 ml.
 Giugno 1993 19a. Fenoli 19a.l Principio del metodo II metodo si basa sull'analisi tramite cromatografia liquida ad alta prestazione (HPLC) di un estratto organico, ottenuto da un campione di fango o di
Giugno 1993 19a. Fenoli 19a.l Principio del metodo II metodo si basa sull'analisi tramite cromatografia liquida ad alta prestazione (HPLC) di un estratto organico, ottenuto da un campione di fango o di
METILISOBUTILCHETONE (4 metil-2 pentanone) urinario in GC/MS spazio di testa Codice GC10510
 METILISOBUTILCHETONE (4 metil-2 pentanone) urinario in GC/MS spazio di testa Codice GC10510 BIOCHIMICA Il metilisobutilchetone è un liquido incolore ed infiammabile che viene utilizzato in laboratorio
METILISOBUTILCHETONE (4 metil-2 pentanone) urinario in GC/MS spazio di testa Codice GC10510 BIOCHIMICA Il metilisobutilchetone è un liquido incolore ed infiammabile che viene utilizzato in laboratorio
DIETILCHETONE (3-pentanone) Urinario in GC/MS spazio di testa Codice GC11010
 DIETILCHETONE (3-pentanone) Urinario in GC/MS spazio di testa Codice GC11010 BIOCHIMICA Il Dietilchetone è un liquido incolore ed infiammabile che viene utilizzato in laboratorio come solvente organico
DIETILCHETONE (3-pentanone) Urinario in GC/MS spazio di testa Codice GC11010 BIOCHIMICA Il Dietilchetone è un liquido incolore ed infiammabile che viene utilizzato in laboratorio come solvente organico
DETERMINAZIONE SIMULTANEA DI ACIDO L-ASCORBICO E D-ISOASCORBICO (ACIDO ERITORBICO) NEL VINO MEDIANTE HPLC E RIVELATORE UV
 RISOLUZIONE ENO 11/008 DETERMINAZIONE SIMULTANEA DI ACIDO L-ASCORBICO E D-ISOASCORBICO (ACIDO ERITORBICO) NEL VINO MEDIANTE HPLC E RIVELATORE UV L ASSEMBLEA GENERALE Visto l'articolo paragrafo iv dell'accordo
RISOLUZIONE ENO 11/008 DETERMINAZIONE SIMULTANEA DI ACIDO L-ASCORBICO E D-ISOASCORBICO (ACIDO ERITORBICO) NEL VINO MEDIANTE HPLC E RIVELATORE UV L ASSEMBLEA GENERALE Visto l'articolo paragrafo iv dell'accordo
Analisi Chimica Relazione
 Titolo Sbarbada Davide 5 /CH I.S.I.I. Marconi -PC- Pagina 1 di 6 05/04/2006 Gascromatografia Obiettivo Analisi Chimica Relazione Effettuare l analisi di una miscela di alcoli mediante gascromatografia
Titolo Sbarbada Davide 5 /CH I.S.I.I. Marconi -PC- Pagina 1 di 6 05/04/2006 Gascromatografia Obiettivo Analisi Chimica Relazione Effettuare l analisi di una miscela di alcoli mediante gascromatografia
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia. Corso di Analisi Chimico-Tossicologica.
 Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
2. SISTEMA DI PURIFICAZIONE CROMATOGRAFICA A MEDIA PRESSIONE (Biotage).
 1. APPARECCHIO PER REAZIONI A MICROONDE (Cem). Apparecchio per reazioni a microonde con sistema di sfiato automatico delle sovrappressioni, che consente di condurre reazioni che superano i 300 psi (20
1. APPARECCHIO PER REAZIONI A MICROONDE (Cem). Apparecchio per reazioni a microonde con sistema di sfiato automatico delle sovrappressioni, che consente di condurre reazioni che superano i 300 psi (20
Leggere attentamente il file sulla sicurezza prima di accedere al laboratorio
 Didattica della Chimica organica (2 CFU, 16h) PAS/TFA A012/A013 16 ore: 4 ore Lezioni frontali: Lunedì 9 febbraio 2015, ore 15.00-16.30 mercoledì 11 febbraio 2015, ore 15.00-16.30 Aula A1 III piano edificio
Didattica della Chimica organica (2 CFU, 16h) PAS/TFA A012/A013 16 ore: 4 ore Lezioni frontali: Lunedì 9 febbraio 2015, ore 15.00-16.30 mercoledì 11 febbraio 2015, ore 15.00-16.30 Aula A1 III piano edificio
Istruzioni tecniche Apparato di riflusso standard nei forni a micro-onde
 Istruzioni tecniche Apparato di riflusso standard nei forni a micro-onde Le condizioni sperimentali di un processo condotto con l uso delle micro-onde dipendono dalle caratteristiche tecniche del dispositivo
Istruzioni tecniche Apparato di riflusso standard nei forni a micro-onde Le condizioni sperimentali di un processo condotto con l uso delle micro-onde dipendono dalle caratteristiche tecniche del dispositivo
ASPETTI PRATICI PER EFFETTUARE UNA REAZIONE CHIMICA
 ASPETTI PRATICI PER EFFETTUARE UNA REAZIONE CHIMICA Per effettuare una reazione chimica correttamente, si deve eseguire un certo numero di operazioni: 1. Si purificano (se necessario) reagenti e solventi.
ASPETTI PRATICI PER EFFETTUARE UNA REAZIONE CHIMICA Per effettuare una reazione chimica correttamente, si deve eseguire un certo numero di operazioni: 1. Si purificano (se necessario) reagenti e solventi.
ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) H 2 SO 4. Quantità: Acido salicilico 5.0 g (PM = 138.
 ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) COOH COOH OH OAc + Ac 2 O H 2 SO 4 ac. 2-idrossibenzoico ac. 2-acetossibenzoico Quantità: Acido salicilico 5.0 g (PM =
ACETILAZIONE DELL ACIDO SALICILICO (Sintesi dell Aspirina acido acetilsalicilico) COOH COOH OH OAc + Ac 2 O H 2 SO 4 ac. 2-idrossibenzoico ac. 2-acetossibenzoico Quantità: Acido salicilico 5.0 g (PM =
Sintesi verde malachite
 Sintesi verde malachite Prima di eseguire qualsiasi esperimento proposto è opportuno verificare che tutte le buone abitudini di sicurezza vengano applicate e rispettate. Prestare attenzione ai pittogrammi
Sintesi verde malachite Prima di eseguire qualsiasi esperimento proposto è opportuno verificare che tutte le buone abitudini di sicurezza vengano applicate e rispettate. Prestare attenzione ai pittogrammi
Esercitazione 4: determinazione della concentrazione di sodio e potassio nelle urine mediante spettroscopia di emissione in fiamma
 Esercitazione 4: determinazione della concentrazione di sodio e potassio nelle urine mediante spettroscopia di emissione in fiamma Apparato strumentale Sodio e potassio vengono determinati in campioni
Esercitazione 4: determinazione della concentrazione di sodio e potassio nelle urine mediante spettroscopia di emissione in fiamma Apparato strumentale Sodio e potassio vengono determinati in campioni
Rapporto tra soluto e solvente o soluzione
 Rapporto tra soluto e solvente o soluzione Dissoluzione delle sostanze Concentrazione espressa in unità chimiche : Molarità Frazione molare Concentrazione espressa in unità fisiche : Percentuale in
Rapporto tra soluto e solvente o soluzione Dissoluzione delle sostanze Concentrazione espressa in unità chimiche : Molarità Frazione molare Concentrazione espressa in unità fisiche : Percentuale in
FILTRAZIONE. Pagina 1 CANDELE FILTRANTI CANDELE FILTRANTI AD IMMERSIONE CANDELE FILTRANTI MICRO. Porosità ø ø filtro tubo
 CANDELE FILTRANTI Porosità ø ø filtro tubo mm mm 05.0335.00 1 30 14 05.0337.00 2 30 14 05.0338.00 3 30 14 05.0339.00 4 30 14 05.0336.00 1 60 16 05.0341.00 2 60 16 05.0343.00 3 60 16 05.0345.00 4 60 16
CANDELE FILTRANTI Porosità ø ø filtro tubo mm mm 05.0335.00 1 30 14 05.0337.00 2 30 14 05.0338.00 3 30 14 05.0339.00 4 30 14 05.0336.00 1 60 16 05.0341.00 2 60 16 05.0343.00 3 60 16 05.0345.00 4 60 16
CARATTERISTICHE. In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee.
 In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee. Sistema eterogeneo miscela di due o più sostanze in cui la composizione varia localmente. CARATTERISTICHE 1. I componenti mantengono
In chimica, si possono distinguere sistemi o miscele eterogenee ed omogenee. Sistema eterogeneo miscela di due o più sostanze in cui la composizione varia localmente. CARATTERISTICHE 1. I componenti mantengono
Eperienza di Laboratorio Sintesi del biodiesel
 Eperienza di Laboratorio Sintesi del biodiesel Preparazione dell'olio Le macchine per la produzione di biodiesel richiedono che l'olio abbia delle proprietà specifiche. Meno dell'1% (in peso) di particelle
Eperienza di Laboratorio Sintesi del biodiesel Preparazione dell'olio Le macchine per la produzione di biodiesel richiedono che l'olio abbia delle proprietà specifiche. Meno dell'1% (in peso) di particelle
OSSIDAZIONI CON PERMANGANATO DI POTASSIO
 OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
OSSIDAZIONI CON PERMANGANATO DI POTASSIO Il permanganato di potassio è agente ossidante forte di colore viola intenso. In soluzioni fortemente acide (ph ~1) è ridotto a Mn 2+ incolore. MnO 4 + 8H + + 5e
COMMISSIONE TECNICA SSOG
 COMMISSIONE TECNICA SSOG SOTTOCOMMISSIONE OLI VEGETALI Metodo in inchiesta pubblica Determinazione dei Biofenoli degli oli di oliva mediante HPLC. Derivati naturali e ossidati dell oleuropeina e del ligstroside,
COMMISSIONE TECNICA SSOG SOTTOCOMMISSIONE OLI VEGETALI Metodo in inchiesta pubblica Determinazione dei Biofenoli degli oli di oliva mediante HPLC. Derivati naturali e ossidati dell oleuropeina e del ligstroside,
ISTRUZIONE OPERATIVA:
 Pagina 1 di 5 INDICE: 1) Scopo 2) Campo di applicazione 3) Norma di riferimento 4) Definizioni e simboli 5) Responsabilità 6) Apparecchiature 7) Modalità esecutive 8) Esposizione dei risultati DOCUMENTI
Pagina 1 di 5 INDICE: 1) Scopo 2) Campo di applicazione 3) Norma di riferimento 4) Definizioni e simboli 5) Responsabilità 6) Apparecchiature 7) Modalità esecutive 8) Esposizione dei risultati DOCUMENTI
ESPERIENZA 1: DISTILLAZIONE FRAZIONATA DI UNA MISCELA DI ESANO - TOLUENE
 ESPERIENZA 1: DISTILLAZIONE FRAZIONATA DI UNA MISCELA DI ESANO - TOLUENE Materiale: un pallone da 100 ml, una colonna di frazionamento, una testa di distillazione, un termometro, un refrigerante, un raccordo
ESPERIENZA 1: DISTILLAZIONE FRAZIONATA DI UNA MISCELA DI ESANO - TOLUENE Materiale: un pallone da 100 ml, una colonna di frazionamento, una testa di distillazione, un termometro, un refrigerante, un raccordo
TRATTAMENTO DELL ACQUA DI LABORATORIO. sostanza più frequentemente adoperata in laboratorio.
 TRATTAMENTO DELL ACQUA DI LABORATORIO 15.10.17 sostanza più frequentemente adoperata in laboratorio. serve a molte cose solvente per preparare soluzioni, diluire, cristallizzare, lavare, raffreddare,..
TRATTAMENTO DELL ACQUA DI LABORATORIO 15.10.17 sostanza più frequentemente adoperata in laboratorio. serve a molte cose solvente per preparare soluzioni, diluire, cristallizzare, lavare, raffreddare,..
Esperienza tipo B: Rimozione di inquinanti organici ed inorganici mediante assorbimento o adsorbimento
 Esperienza tipo B: Rimozione di inquinanti organici ed inorganici mediante assorbimento o adsorbimento 1. Preparare una soluzione di CuSO4 1.6x10-3 M pesando circa ma esatti 0.1 g di 2. Travasare 50 ml
Esperienza tipo B: Rimozione di inquinanti organici ed inorganici mediante assorbimento o adsorbimento 1. Preparare una soluzione di CuSO4 1.6x10-3 M pesando circa ma esatti 0.1 g di 2. Travasare 50 ml
Estrazione con solvente 18/01/2010. Laboratorio di chimica. Prof. Aurelio Trevisi
 Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
DICLOROMETANO (METILENE CLORURO) urinario in GC/MS spazio di testa Codice GC18010
 DICLOROMETANO (METILENE CLORURO) urinario in GC/MS spazio di testa Codice GC18010 BIOCHIMICA Il diclorometano (o cloruro di metilene) è un composto chimico appartenente alla categoria degli alogenuri alchilici.
DICLOROMETANO (METILENE CLORURO) urinario in GC/MS spazio di testa Codice GC18010 BIOCHIMICA Il diclorometano (o cloruro di metilene) è un composto chimico appartenente alla categoria degli alogenuri alchilici.
DETERMINAZIONE DELLA CAPACITÀ DI UN PREPARATO ENZIMATICO DI ROMPERE LE CATENE PECTICHE TRAMITE LA MISURAZIONE DELLA VISCOSITÀ
 RISOLUZIONE OIV/ENO 351/2009 DETERMINAZIONE DELLA CAPACITÀ DI UN PREPARATO ENZIMATICO DI ROMPERE LE CATENE PECTICHE TRAMITE LA MISURAZIONE DELLA VISCOSITÀ L'ASSEMBLEA GENERALE Visto l'articolo 2 paragrafo
RISOLUZIONE OIV/ENO 351/2009 DETERMINAZIONE DELLA CAPACITÀ DI UN PREPARATO ENZIMATICO DI ROMPERE LE CATENE PECTICHE TRAMITE LA MISURAZIONE DELLA VISCOSITÀ L'ASSEMBLEA GENERALE Visto l'articolo 2 paragrafo
PROGRAMMAZIONE DI LABORATORIO DI: TECNOLOGIE CHIMICHE INDUSTRIALI, PRINCIPI DI AUTOMAZIONE E ORGANIZZAZIONE INDUSTRIALE
 PROGRAMMAZIONE DI LABORATORIO DI: TECNOLOGIE CHIMICHE INDUSTRIALI, PRINCIPI DI AUTOMAZIONE E ORGANIZZAZIONE INDUSTRIALE allegato 1 Distillazione di una soluzione pag 14 Bagatti presso Lab. 6 Esperienza:
PROGRAMMAZIONE DI LABORATORIO DI: TECNOLOGIE CHIMICHE INDUSTRIALI, PRINCIPI DI AUTOMAZIONE E ORGANIZZAZIONE INDUSTRIALE allegato 1 Distillazione di una soluzione pag 14 Bagatti presso Lab. 6 Esperienza:
SCHEMA DI UN GASCROMATOGRAFO
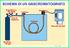 SCHEMA DI UN GASCROMATOGRAFO Regolatore a due Stadi Iniettore Rivelatore Gas di Trasporto Colonna Raccolta dei Dati Bombola del gas GC 2 14/15 1 REQUISITI DEL GAS DI TRASPORTO Filtro molecolare di 5 Angstrom
SCHEMA DI UN GASCROMATOGRAFO Regolatore a due Stadi Iniettore Rivelatore Gas di Trasporto Colonna Raccolta dei Dati Bombola del gas GC 2 14/15 1 REQUISITI DEL GAS DI TRASPORTO Filtro molecolare di 5 Angstrom
GASCROMATOGRAFIA (GC)
 GASCRMATGRAFIA (GC) Sostanze volatili possono essere analizzate (qualitativamente e quantitativamente) mediante cromatografia in fase vapore (vapour phase chromatography, VPC) detta anche cromatografia
GASCRMATGRAFIA (GC) Sostanze volatili possono essere analizzate (qualitativamente e quantitativamente) mediante cromatografia in fase vapore (vapour phase chromatography, VPC) detta anche cromatografia
Sintesi di cis e transbis(glicinato)rame(ii)
 Sintesi di cis e transbis(glicinato)rame(ii) Contenuti 1. Introduzione 2. Materiali 3. Condizioni operative Il metabolismo del rame Contribuisce al trasporto e metabolismo del ferro Necessario per la formazione
Sintesi di cis e transbis(glicinato)rame(ii) Contenuti 1. Introduzione 2. Materiali 3. Condizioni operative Il metabolismo del rame Contribuisce al trasporto e metabolismo del ferro Necessario per la formazione
 193 Per il cloramfenicolo il flusso della fase mobile (3.9) è di 1.0 mvmin. e la lunghezza d'onda impiegata per la rivelazione è di 280 nm. Per i nitrofurani il flusso della fase mobile (3.8) è di 1.2
193 Per il cloramfenicolo il flusso della fase mobile (3.9) è di 1.0 mvmin. e la lunghezza d'onda impiegata per la rivelazione è di 280 nm. Per i nitrofurani il flusso della fase mobile (3.8) è di 1.2
