ESERCIZI SUI SISTEMI CHIUSI UNIVERSITÀ DEGLI STUDI DI NAPOLI FEDERICO II POLO DELLE SCIENZE E DELLE TECNOLOGIE FACOLTÀ DI ARCHITETTURA A.A.
|
|
|
- Laura Manca
- 6 anni fa
- Visualizzazioni
Transcript
1 UNIVERSITÀ DEGLI STUDI DI NAPOLI FEDERICO II POLO DELLE SCIENZE E DELLE TECNOLOGIE FACOLTÀ DI ARCHITETTURA A.A CORSO DI LAUREA QUINQUENNALE, 1 ANNO INSEGNAMENTO DI FISICA TECNICA PROFF. L. BELLIA E F.CALISE APPUNTI DALLE LEZIONI ESERCIZI SUI SISTEMI CHIUSI NAPOLI, MARZO 2007
2 ESERCIZIO 1 Un recipiente chiuso a pareti rigide e fisse contiene 800 l di acqua liquida alla temperatura t A =35 C. Nel recipiente viene successivamente immerso un cilindro di metallo (D=0,200 m; H= 200 mm) alla t M = 93 C, avente densità di 4000 kg/m 3 e calore specifico di 500 J/kgK. Calcolare la tempertura dell'acqua e del metallo all'equilibrio, nell'ipotesi di ritenere trascurabile il calore disperso verso l'ambiente esterno V A 800 l t A 35 C r A 1000 kg/m 3 c A 4.2 kj/kgk r M 4000 kg/m 3 c M 500 J/kgK = 0.5 kj/kgk D 0.2 m H 200 mm = 0.2 m t M 93 C Il volume del cilindro di metallo è V M = p*d 2 H/4= 6.28E-03 m 3 la massa del cilindro quindi è m M =V M *r M = 2.51E+01 kg Il volume dell'acqua V A = 8.00E-01 m 3 la massa d'acqua m A =V A *r A = 8.00E+02 kg Scrivendo Il I primo principio relativamente al sistema acqua+ metallo si ha: DU=Q-L Ma Q=0 poiché l'energia termica scambiata con l'ambiente esterno è nulla; analogamente L=0 perché il sistema non scambia lavoro di variazione di volume Quindi il I principio diventa: DU=0 Sfruttando la proprità di additività dell'energia interna, si ha: DU=DU A +DU M =0 Esplicitando l'energia interna si ha: m A c A (t F -t A )+m M c M (t F -t M )=0 Dove t F è la temperatura all'equilibrio dell'acqua e del metallo. Risolvendo l'equazione precedente si ha: t F =(m A c A t A +m M c M t M )/(m A c A +m M c M )= C
3 ESERCIZIO 2 Un sistema cilindrico a pareti rigide e fisse, avente D= 0,200 m ed H 1 = 10 cm, contiene ossigeno inizialmente alla t 1 = 17,0 C e p 1 =1,00 bar. Il sistema cede all'ambiente 0,0200 kcal di energia termica. Calcolare la temperatura dell'ossigeno al termine della trasformazione D= 0.2 m H 1 = 10 cm = 0.1 m t 1 = 17 C = K p 1 = 1 bar = 1.00E+05 Pa Q= kcal = -8.37E-02 kj dalle tabelle per l'ossigeno R= J/kgK c v = kj/kgk Il volume occupato dall'ossigeno nello stato 1 è V 1 = p*d 2 H 1 /4= 3.14E-03 m 3 dall'equazione di stato dei gas si può calcolare la massa di ossigeno m=p 1 V 1 /(RT 1 )= 4.15E-03 kg Il primo principio si scrive (sistema a pareti rigide e fisse): DU=Q Quindi mc v (t 2 -t 1 )=Q ovvero t 2 =t 1 +(Q)/(mc v ) = C
4 ESERCIZIO 3 Un sistema chiuso evolve secondo una trasformazione ciclica costituita da 3 trasformazioni elementari (1-2, 2-3 e 3-1). Q 12 = -300 kcal; L 12 =0 kj; Q 23 =0 kj; L 23 = -100 kj; L 31 = kwh. Calcolare Q 31. Q 12 = -300 kcal = -1.26E+03 kj L 12 = 0 kj Q 23 = 0 kj L 23 = -100 kj L 31 = 2.00E-01 kwh = 7.20E+02 kj Il I principio relativo alla trasformazione 12: DU 12 =Q 12 -L 12 = -1.26E+03 kj Il I principio relativo alla trasformazione 23: DU 23 =Q 23 -L 23 = 1.00E+02 kj Il I principio relativo alla trasformazione 31: DU 31 =Q 31 -L 31 Ma DU 31 =U 1 -U 3 =-(U 2 -U 1 )-(U 3 -U 2 )=-(DU 12 +DU 23 )= 1.16E+03 kj Quindi Q 31 =DU 31 +L 31 = 1.88E+03 kj
5 ESERCIZIO 4 Un ambiente di dimensioni 3,0 m x 2,00 m x 3,50 m, schematizzabile come un sistema chiuso a pareti rigide e fisse, contiene aria alla pressione p 1 =1,00 bar ed alla temperatura t 1 = 15,0 C. L'aria contenuta nella stanza deve essere portata alla temperatura di 25,0 C in 1,0 ore. Calcolare l'energia termica e la potenza termica necessaria al riscaldamento. H= 3 m L= 2 m P= 3.5 m t 1 = 15 C = K p 1 = 1 bar = 1.00E+05 Pa t 2 = 25 C Dq= 1 h = 3600 s dalla tabella R= J/kgK c v = kj/kgk il volume dell'ambiente è V= 21 m 3 Dall'equazione di stato dei gas ideali è possibile calcolare la massa di aria: m=p 1 V 1 /(RT 1 )= kg Il I principio viene scritto nella forma: DU=Q-L=Q In quanto il lavoro di variazione di volume è nullo (sistema a pareti rigide e fisse) Quindi Q=mc v (t 2 -t 1 )= kj La potenza termica è P=Q/Dq 5.06E-02 kw = W
6 ESERCIZIO 5 Un recipiente cilindrico chiuso a pareti rigide e fisse contiene acqua liquida. Il diametro e l'altezza del recipiente sono rispettivamente pari a 1,00 m e 0,700 m. L'acqua si trova inizialmente alla temperatura di 25 C; successivamente riceve dall'ambiente un'energia termica specifica di m 2 /s 2. Calcolare: 1) la capacità termica dell'acqua; 2) la temperatura dell'acqua al termine del riscaldamento; 3) la potenza termica se il processo ha una durata di 0,30 h D= 1 m H= 0.7 m t 1 = 25 C = K q= 1.68E+05 m 2 /s 2 = 168 kj/kg Dq= 0.3 h = 1080 s c= 4.2 kj/kgk r= 1000 kg/m 3 Il volume dell'acqua è: V 1 = p*d 2 H/4= m 3 La massa dell'acqua m=v*r= kg La capacità termica è C=m*c= 2.31E+03 kj/k IL primo principio viene scritto nella forma DU=Q-L=Q Infatti il lavoro scambiato è nullo in quanto il sistema è a pareti rigide e fisse Quindi l'equazione può essere scritta anche in forma specifica Du=c(t 2 -t 1 )=q Da cui: t 2 =t 1 +q/c= 65 C La potenza termica è il raporto fra l'energia termica ed il tempo: P=Q/Dq=(qm)/Dq= kw
7 ESERCIZIO 6 Una parete di calcsestruzzo(200 mm x 3,7 m x 3,0 m), avente densità e calore specifico rispettivamente di 1800 kg/m 3 e 900 J/kgK, si trova inizialmente alla temperatura di 13,0 C. Successivamente riceve energia termica dall'ambiente fino a araggiungere la temperatura di 25 C. Calcolare l'energia termica s= 200 mm = 0.2 m L= 3 m H= 3.7 m t 1 = 13 C t 2 = 25 C c= 900 J/kgK r= 1800 kg/m 3 Il volume della parete è V=HLs= 2.22 m 3 La massa della parete è m=r*v= 4.00E+03 kg IL primo principio viene scritto nella forma DU=Q-L=Q Infatti, la parete è solida e non scambia lavoro di variazione di volume Esplicitando la funzione energia interna si ha Q=mc(t 2 -t 1 )= 4.32E+07 kj
8 ESERCIZIO 7 Un sistema chiuso evolve secondo una trasformazione ciclica in cui riceve 900 kcal di energia termica, cede alla'ambiente 0,700 kwh di energia termica e cede un lavoro specifico di 200 m 2 /s 2. Calcolare la massa del sistema Q 1 = 900 kcal = 3.77E+03 kj Q 2 = -0.7 kwh = -2.52E+03 kj l= 200 m 2 /s 2 = 0.2 kj/kg IL primo principio viene scritto nella forma DU=(Q 1 +Q 2 )-L=(Q 1 +Q 2 )-lm=0 La variazione di energia interna è nulla poiché la trasformazione è ciclica Quindi: m=(q 1 +Q 2 )/l= 6.24E+03 kg
9 ESERCIZIO 8 Un sistema pistone cilindro (D=100 mm; H 1 =20 cm) contiene aria alla p 1 =1,00 bar=costante. Inzialmente il sistema si triva alla t 1 =20,0 C; successivamente ad un riscaldamento si porta alla t 2 =90 C. Calcolare DU, Q ed L t 1 = 20 C = K p 1 = 1 bar = 1.00E+05 Pa D= 100 mm = 0.1 m H= 20 cm = 0.2 m t 2 = 90 C = K dalla tabella R= J/kgK cv= kj/kgk Il volume iniziale è: V 1 = p*d 2 H/4= 1.57E-03 m 3 La massa d'aria può essere cacolata utilizzando l'equazione di stato dei gas ideali m=pv 1 /(RT 1 )= 1.87E-03 kg Con la stessa equazione di stato è possibile calcolare il volume finale V 2 =mrt 2 /p 2 = 1.94E-03 m 3 Poiché la trasformazione è isobara il lavoro di variazione di volume è: L=p(V 2 -V 1 )= 3.75E+01 J = 3.75E-02 kj La variazione di energia interna è: DU=mc v (t 2 -t 1 )= 9.36E-02 kj Quindi, sulla base del primo principio Q=L+DU= 1.31E-01 kj
10 ESERCIZIO 9 Aria contenuta in un sistema pistone cilindro (D=0.300 m) subisce una trasformazione a pressione costante che la porta da t 1 =17 C fino a t 2 =54 C. Nello stato iniziale il pistone si trova ad un'altezza H 1 = 70 cm. Calcolare la variaizone di energia interna specifica, il volume finale e l'altezza finale. t 1 = 17 C = K t 2 = 54 C = K D= 0.3 m H 1 = 70 cm = 0.7 m dalla tabella R= J/kgK c v = kj/kgk Il volume iniziale è: V 1 = p*d 2 H 1 /4= 4.95E-02 m 3 Scrivendo le equazioni di stato relative agli stati 1 e 2, si ha: p 1 V 1 =mrt 1 p 2 V 2 =mrt 2 Facendone il rapporto membro a membro, utilizzando l'ipotesi di trasformazione isobara, si ha: V 2 =V 1 *T 2 /T 1 = 5.58E-02 m 3 L'altezza del pistone nello stato 2 è H 2 =4V 1 /(p*d 2 )= 7.89E-01 m Du=c v (t 2 -t 1 )= kj/kg
11 ESERCIZIO 10 Ossigeno si trova in un sistema chiuso a pareti rigide e fisse alla p 1 =1,00 bar e t 1 =10,0 C. Successivamente subisce una trasformazione dove riceve un lavoro specifico di 0,00300 kwh/kg (lavoro di elica) ed energia termica fino a portarsi alla t 2 =90,0 C. Calcolare la pressione finale e l'energia termica specifica scambiata. p 1 = 1 bar = 1.00E+05 Pa t 1 = 10 C = K t 2 = 90 C = K l= 3.00E-03 kwh/kg = 10.8 kj/kg dalle tabelle per l'ossigeno R= J/kgK c v = kj/kgk Scrivendo le equazioni di stato relative agli stati 1 e 2, si ha: p 1 V 1 =mrt 1 p 2 V 2 =mrt 2 Poiché il volume del sistema è costante, rapportando membro a membro le due equazioni precedenti, si ha: p 2 =p 1 *T 2 /T 1 = 1.28E+00 bar Il primo principio viene scritto nella forma specifica come segue: Du=q-l Quindi q=c v (t 2 -t 1 )+l= kj/kg
12 ESERCIZIO 11 Ad un sistema pistone cilindro è applicata una forza esterna di 100 N che esercita una pressione di 300 Pa. La forza esterna determina uno spostamento del pistone di 300 mm. Calcolare la variazione di volume del sistema F= 100 N p= 300 Pa s= 300 mm = 0.3 m Dalla definizione di pressione p=f/a Quindi l'area di base del cilindro è: A=F/p= 3.33E-01 m 2 Quindi la variazione di volume è data da: DV=As= 1.00E-01 m 3
6. Determinare il titolo del vapor d acqua che ad 8,00 bar ha un entalpia specifica di 2000 kj/kg.
 ESERCIZI DI FISICA TECNICA TERMODINAMICA APPLICATA Termodinamica degli stati 1. Utilizzando il piano pt e le tabelle A.3 del vapor d acqua saturo, si dica quali sono le fasi presenti nei sistemi costituiti
ESERCIZI DI FISICA TECNICA TERMODINAMICA APPLICATA Termodinamica degli stati 1. Utilizzando il piano pt e le tabelle A.3 del vapor d acqua saturo, si dica quali sono le fasi presenti nei sistemi costituiti
Corso di Termofluidodinamica
 Corso di Termofluidodinamica Modulo di Termodinamica Tecnica A.A. 2014-2015 - Esercizi di preparazione alla prima prova intermedia Problema N. 1 Un serbatoio deve essere dimensionato per contenere 200
Corso di Termofluidodinamica Modulo di Termodinamica Tecnica A.A. 2014-2015 - Esercizi di preparazione alla prima prova intermedia Problema N. 1 Un serbatoio deve essere dimensionato per contenere 200
Applicazioni del primo principio della termodinamica ed utilizzo delle tabelle del vapore: Esercizi svolti
 Applicazioni del primo principio della termodinamica ed utilizzo delle tabelle del vapore: Esercizi svolti 19 marzo 23 Esercizio 1 Un recipiente di volume ssato e con pareti adiabatiche è diviso in due
Applicazioni del primo principio della termodinamica ed utilizzo delle tabelle del vapore: Esercizi svolti 19 marzo 23 Esercizio 1 Un recipiente di volume ssato e con pareti adiabatiche è diviso in due
Esercitazione di Fisica Tecnica
 Anno Accademico 2016-2017 Prof. Ing. L. Maffei 1 Anno Accademico 2016-2017 - PARTE 1 Grandezze e unità di misura Consumi energetici 2 Grandezze e unità di misura 3 Convertire le seguenti misure usando
Anno Accademico 2016-2017 Prof. Ing. L. Maffei 1 Anno Accademico 2016-2017 - PARTE 1 Grandezze e unità di misura Consumi energetici 2 Grandezze e unità di misura 3 Convertire le seguenti misure usando
Corso di Laurea in Ing. Gestionale ESERCIZI DI TERMODINAMICA PER IL CORSO DI FISICA TECNICA
 Corso di laurea in Ingegneria Gestionale Aggiornato a ottobre 2016 Corso di Laurea in Ing. Gestionale ESERCIZI DI TERMODINAMICA PER IL CORSO DI FISICA TECNICA 1. TERMODINAMICA DEGLI STATI 2. SISTEMI CHIUSI
Corso di laurea in Ingegneria Gestionale Aggiornato a ottobre 2016 Corso di Laurea in Ing. Gestionale ESERCIZI DI TERMODINAMICA PER IL CORSO DI FISICA TECNICA 1. TERMODINAMICA DEGLI STATI 2. SISTEMI CHIUSI
2. SISTEMI CHIUSI ESERCIZI SUL SOLO BILANCIO DI ENERGIA
 2. SISTEMI CHIUSI Università degli Studi di Napoli Federico II - Facoltà di Ingegneria In tutte le applicazioni, si ipotizzino, se non diversamente specificato, condizioni di quiete o comunque di trascurabilità
2. SISTEMI CHIUSI Università degli Studi di Napoli Federico II - Facoltà di Ingegneria In tutte le applicazioni, si ipotizzino, se non diversamente specificato, condizioni di quiete o comunque di trascurabilità
Università degli Studi di Napoli Federico II - Facoltà di Ingegneria Esercizi di Fisica Tecnica per il Corso di laurea in Ingegneria Gestionale
 2. SISTEMI CHIUSI Università degli Studi di Napoli Federico II - Facoltà di Ingegneria In tutte le applicazioni, si ipotizzino, se non diversamente specificato, condizioni di quiete o comunque di trascurabilità
2. SISTEMI CHIUSI Università degli Studi di Napoli Federico II - Facoltà di Ingegneria In tutte le applicazioni, si ipotizzino, se non diversamente specificato, condizioni di quiete o comunque di trascurabilità
FISICA TECNICA - A.A. 99/00
 Termo-fluidodinamica applicata - 1 a Interprova del 30.3.2000 Cognome Nome Anno di Corso Matricola 1 T1=200 C p1=7,0 bar m1=40 kg/s 2 A2=25 cm 2 T2=40,0 C p2=7,0 bar 3 V3=0,060 m 3 /s p3=7,0 bar Q A) Due
Termo-fluidodinamica applicata - 1 a Interprova del 30.3.2000 Cognome Nome Anno di Corso Matricola 1 T1=200 C p1=7,0 bar m1=40 kg/s 2 A2=25 cm 2 T2=40,0 C p2=7,0 bar 3 V3=0,060 m 3 /s p3=7,0 bar Q A) Due
ENERGIA E CALORE energia Joule (J) KJ (Kilojoule). Kilowattora (KWh) calore Caloria (Cal o KCal) Caloria calore British Thermal Unit (Btu)
 ENERGIA E CALORE Unità di misura dell'energia: Joule (J), unità troppo piccola; comunemente si usa il suo multiplo, il KJ (Kilojoule). Importante è anche il Kilowattora (KWh), unità usata nella misura
ENERGIA E CALORE Unità di misura dell'energia: Joule (J), unità troppo piccola; comunemente si usa il suo multiplo, il KJ (Kilojoule). Importante è anche il Kilowattora (KWh), unità usata nella misura
Ingegneria Edile-Architettura Esercizi di Fisica Tecnica Ambientale Termodinamica
 Ingegneria Edile-Architettura Esercizi di Fisica Tecnica Ambientale 2012-2013 Termodinamica TD1 In un sistema pistone-cilindro, 1 kg di gas (! = 1,29 ed R * = 190 J/(kg"K)) si espande da 5 bar e 90 C ad
Ingegneria Edile-Architettura Esercizi di Fisica Tecnica Ambientale 2012-2013 Termodinamica TD1 In un sistema pistone-cilindro, 1 kg di gas (! = 1,29 ed R * = 190 J/(kg"K)) si espande da 5 bar e 90 C ad
1) Che cos é la pressione? Qual è la sua unità di misura nel S.I.?
 1) Che cos é la pressione? Qual è la sua unità di misura nel S.I.? 2) Da che cosa dipende la pressione esercitata da un oggetto di massa m poggiato su di una superficie? 3) Che cos è un fluido? 4) Come
1) Che cos é la pressione? Qual è la sua unità di misura nel S.I.? 2) Da che cosa dipende la pressione esercitata da un oggetto di massa m poggiato su di una superficie? 3) Che cos è un fluido? 4) Come
L ENERGIA CINETICA DELLE MOLECOLE DI UN GAS E LA TEMPERATURA Ogni molecola ha in media un'energia cinetica
 Primo principio- 1 - TERMODINAMICA ENERGIA INTERNA DI UN SISTEMA Ad ogni sistema fisico possiamo associare varie forme di energia, l energia cinetica delle molecole di cui è formato, energia potenziale,
Primo principio- 1 - TERMODINAMICA ENERGIA INTERNA DI UN SISTEMA Ad ogni sistema fisico possiamo associare varie forme di energia, l energia cinetica delle molecole di cui è formato, energia potenziale,
FISICA TECNICA (Ingegneria Medica)
 NOME N. MATRICOLA N. CREDITI E-MAIL Prova di esame del 11 Febbraio 2014 1. Sia dato un ciclo frigorifero, in cui il fluido evolvente è R134a, a cui in cascata è collegato un secondo ciclo il cui fluido
NOME N. MATRICOLA N. CREDITI E-MAIL Prova di esame del 11 Febbraio 2014 1. Sia dato un ciclo frigorifero, in cui il fluido evolvente è R134a, a cui in cascata è collegato un secondo ciclo il cui fluido
Termodinamica e trasmissione del calore 3/ed Yunus A. Çengel Copyright 2009 The McGraw-Hill Companies srl
 RISOLUZIONI cap.11 11.1 Si devono determinare le masse dell'aria secca e del vapore acqueo contenuti in una stanza in condizioni specificate e a un'umidità relativa specificata. Ipotesi L'aria e il vapore
RISOLUZIONI cap.11 11.1 Si devono determinare le masse dell'aria secca e del vapore acqueo contenuti in una stanza in condizioni specificate e a un'umidità relativa specificata. Ipotesi L'aria e il vapore
Kelvin K T [K] = T [ C] + 273,16. Fahrenheit F T [ F] = 1,8 T [ C] Atmosfera atm = Pa = 760 mm Hg
![Kelvin K T [K] = T [ C] + 273,16. Fahrenheit F T [ F] = 1,8 T [ C] Atmosfera atm = Pa = 760 mm Hg Kelvin K T [K] = T [ C] + 273,16. Fahrenheit F T [ F] = 1,8 T [ C] Atmosfera atm = Pa = 760 mm Hg](/thumbs/55/36027543.jpg) LE UNITA DI MISURA Temperatura Pressione Energia Potenza Costanti Celsius C Kelvin K T [K] = T [ C] + 273,16 Fahrenheit F T [ F] = 1,8 T [ C] + 32 Pascal Pa = Kg/(m s 2 ) Atmosfera atm = 101325 Pa = 760
LE UNITA DI MISURA Temperatura Pressione Energia Potenza Costanti Celsius C Kelvin K T [K] = T [ C] + 273,16 Fahrenheit F T [ F] = 1,8 T [ C] + 32 Pascal Pa = Kg/(m s 2 ) Atmosfera atm = 101325 Pa = 760
Dalla legge dei gas perfetti si ha il rapporto tra il numero di moli dei due gas R T 1 V 2 P V 1. =n 1. RT 2 =V 2 qundi: n 1 = T 2. =n 2.
 Compito intercorso Fisica II ICI 1 giugno 2006 1 Due recipienti uguali, isolati termicamente dall'ambiente esterno, sono connessi da un condotto con un rubinetto, inizialmente chiuso. Uno dei recipienti
Compito intercorso Fisica II ICI 1 giugno 2006 1 Due recipienti uguali, isolati termicamente dall'ambiente esterno, sono connessi da un condotto con un rubinetto, inizialmente chiuso. Uno dei recipienti
Esercitazione 7. Soluzione. Il sistema è isolato, quindi l energia totale si conserva. Applicando il primo principio della termodinamica si ottiene:
 Esercitazione 7 Esercizio 1 Una massa m g = 20 g di ghiaccio a 0 C è contenuta in un recipiente termicamente isolato. Successivamente viene aggiunta una massa m a = 80 di acqua a 80 C. Quale sarà, all
Esercitazione 7 Esercizio 1 Una massa m g = 20 g di ghiaccio a 0 C è contenuta in un recipiente termicamente isolato. Successivamente viene aggiunta una massa m a = 80 di acqua a 80 C. Quale sarà, all
temperatura ambientale massa totale d aria contenuta nella stanza temperatura raggiunta nella stanza dalla massa d aria pressione atmosferica
 Esercizio n.21 di pagina 26. L 1 = 6 m L 2 = 8 m L 3 = 10 m t 0F = 20 F M = 28.8 kg/kmol = 28.8 g/mol m =? t 1F = 75 F p a = 1.013 10 5 Pa temperatura ambientale massa molecolare media dell aria massa
Esercizio n.21 di pagina 26. L 1 = 6 m L 2 = 8 m L 3 = 10 m t 0F = 20 F M = 28.8 kg/kmol = 28.8 g/mol m =? t 1F = 75 F p a = 1.013 10 5 Pa temperatura ambientale massa molecolare media dell aria massa
Esercitazioni di Fisica Generale con elementi di Fisica Tecnica
 Esercitazioni di Fisica Generale con elementi di Fisica Tecnica Secondo Modulo A.A. 2014-2015 - 1/10 - 1 COSTANTI FONDAMENTALI Nome Simbolo Valore Unità di misura Costante gravitazionale G 6,670 10-11
Esercitazioni di Fisica Generale con elementi di Fisica Tecnica Secondo Modulo A.A. 2014-2015 - 1/10 - 1 COSTANTI FONDAMENTALI Nome Simbolo Valore Unità di misura Costante gravitazionale G 6,670 10-11
Compito di Fisica Generale I mod. B, Corsi di Laurea in Fisica e in Astronomia, AA 2010/11. Cognome... Nome... Matricola n...
 22.06.2011 Compito di Fisica Generale I mod. B, Corsi di Laurea in Fisica e in Astronomia, AA 2010/11 Cognome... Nome... Matricola n... Esercizio 1. Si abbia un recipiente a pareti adiabatiche contenente
22.06.2011 Compito di Fisica Generale I mod. B, Corsi di Laurea in Fisica e in Astronomia, AA 2010/11 Cognome... Nome... Matricola n... Esercizio 1. Si abbia un recipiente a pareti adiabatiche contenente
LEGGI DEI GAS / CALORI SPECIFICI. Introduzione 1
 LEGGI DEI GAS / CALORI SPECIFICI Introduzione 1 1 - TRASFORMAZIONE ISOBARA (p = costante) LA PRESSIONE RIMANE COSTANTE DURANTE TUTTA LA TRASFORMAZIONE V/T = costante (m, p costanti) Q = m c p (Tf - Ti)
LEGGI DEI GAS / CALORI SPECIFICI Introduzione 1 1 - TRASFORMAZIONE ISOBARA (p = costante) LA PRESSIONE RIMANE COSTANTE DURANTE TUTTA LA TRASFORMAZIONE V/T = costante (m, p costanti) Q = m c p (Tf - Ti)
 La costante (p 0 0 /273) la si riesprime come n R dove R è una costante universale il cui valore dipende solo dalle unità di misura usate: R8.31 Joule/(K mole) e n è il numero di moli L equazione di stato
La costante (p 0 0 /273) la si riesprime come n R dove R è una costante universale il cui valore dipende solo dalle unità di misura usate: R8.31 Joule/(K mole) e n è il numero di moli L equazione di stato
Temi di termodinamica
 Temi di termodinamica Prova scritta del 12/04/1995 Una mole di gas perfetto monoatomico alla temperatura T A =243 K e pressione p A = 2 atm, esegue un ciclo reversibile costituito dalle seguenti trasformazioni:
Temi di termodinamica Prova scritta del 12/04/1995 Una mole di gas perfetto monoatomico alla temperatura T A =243 K e pressione p A = 2 atm, esegue un ciclo reversibile costituito dalle seguenti trasformazioni:
Lezione 9. Statica dei fluidi
 Lezione 9 Statica dei fluidi Meccanica dei fluidi Un fluido e un corpo che non ha una forma definita, ma che, se e contenuto da un contenitore solido, tende a occupare (riempire) una parte o tutto il volume
Lezione 9 Statica dei fluidi Meccanica dei fluidi Un fluido e un corpo che non ha una forma definita, ma che, se e contenuto da un contenitore solido, tende a occupare (riempire) una parte o tutto il volume
Il primo principio della termodinamica
 1 Il primo principio della termodinamica Il primo principio della termodinamica Nelle lezioni precedenti abbiamo visto che per far innalzare la temperatura di un sistema vi sono due possibilità: fornendo
1 Il primo principio della termodinamica Il primo principio della termodinamica Nelle lezioni precedenti abbiamo visto che per far innalzare la temperatura di un sistema vi sono due possibilità: fornendo
Termodinamica e trasmissione del calore 3/ed Yunus A. Çengel Copyright 2009 The McGraw-Hill Companies srl
 SOLUZIONI CAPITOLO 5 5.1 L aria nelle condizioni specificate può essere assimilata a un gas perfetto. Quindi il lavoro di variazione di volume per questa trasformazione isotermica è dato da 5.2 (a) La
SOLUZIONI CAPITOLO 5 5.1 L aria nelle condizioni specificate può essere assimilata a un gas perfetto. Quindi il lavoro di variazione di volume per questa trasformazione isotermica è dato da 5.2 (a) La
LA CAPACITA TERMICA. Università Mediterranea degli Studi di Reggio Calabria Facoltà di Architettura FISICA TECNICA
 Università Mediterranea degli Studi di Reggio Calabria Facoltà di Architettura Dipartimento di Arte Scienza e Tecnica del Costruire Appunti delle lezioni di FISICA TECNICA Laboratorio di Conoscenza dell
Università Mediterranea degli Studi di Reggio Calabria Facoltà di Architettura Dipartimento di Arte Scienza e Tecnica del Costruire Appunti delle lezioni di FISICA TECNICA Laboratorio di Conoscenza dell
Tutorato di Fisica 1 - AA 2014/15
 Tutorato di Fisica 1-2014/15 Emanuele Fabbiani 21 febbraio 2015 1 Termodinamica 1.1 Esercizio 1 Una bolla di aria di volume V = 20 cm 3 si trova sul fondo di un lago di profondità h = 40 m dove la temperatura
Tutorato di Fisica 1-2014/15 Emanuele Fabbiani 21 febbraio 2015 1 Termodinamica 1.1 Esercizio 1 Una bolla di aria di volume V = 20 cm 3 si trova sul fondo di un lago di profondità h = 40 m dove la temperatura
STATICA DEI FLUIDI. 3 ) fino ad una distanza di 5 cm dall orlo. Nei due rami del
 SCHEDA PER IL RECUPERO DI FISICA DEL PRIMO PERIODO anno scolastico 2014-15 STATICA DEI FLUIDI Pressione Leggi il libro di testo (vol. 1) al cap. 11, prova a rispondere alle domande della scheda di verifica
SCHEDA PER IL RECUPERO DI FISICA DEL PRIMO PERIODO anno scolastico 2014-15 STATICA DEI FLUIDI Pressione Leggi il libro di testo (vol. 1) al cap. 11, prova a rispondere alle domande della scheda di verifica
COMPITO A. 4) Primo principio della termodinamica per sistemi chiusi ed aperti. 5)Teoremi di Carnot: enunciati ed esempi
 COMPITO A 1)In un vaso di alluminio, di massa m1, è contenuta la massa m2 di acqua di cui non si conosce la temperatura. Nell acqua si immerge un pezzo di rame di massa m3, riscaldato a t1 C e con ciò
COMPITO A 1)In un vaso di alluminio, di massa m1, è contenuta la massa m2 di acqua di cui non si conosce la temperatura. Nell acqua si immerge un pezzo di rame di massa m3, riscaldato a t1 C e con ciò
Statica dei fluidi & Termodinamica: I principio, gas perfetti e trasformazioni, calore
 Statica dei fluidi & Termodinamica: I principio, gas perfetti e trasformazioni, calore Legge di Stevino La pressione in un liquido a densità costante cresce linearmente con la profondità Il principio di
Statica dei fluidi & Termodinamica: I principio, gas perfetti e trasformazioni, calore Legge di Stevino La pressione in un liquido a densità costante cresce linearmente con la profondità Il principio di
PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI)
 1 PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI) Qui di seguito viene riportata la risoluzione dei problemi presentati nel file Unità omonimo (enunciati). Si raccomanda di prestare molta attenzione ai ragionamenti
1 PROBLEMI E QUESITI DI TERMOLOGIA (SOLUZIONI) Qui di seguito viene riportata la risoluzione dei problemi presentati nel file Unità omonimo (enunciati). Si raccomanda di prestare molta attenzione ai ragionamenti
Esercizi di Fisica Tecnica 2013-2014. Termodinamica
 Esercizi di Fisica Tecnica 2013-2014 Termodinamica TD1 In un sistema pistone-cilindro, 1 kg di gas ( = 1,29 ed R * = 190 J/(kg K)) si espande da 5 bar e 90 C ad 1 bar. Nell'ipotesi che la trasformazione
Esercizi di Fisica Tecnica 2013-2014 Termodinamica TD1 In un sistema pistone-cilindro, 1 kg di gas ( = 1,29 ed R * = 190 J/(kg K)) si espande da 5 bar e 90 C ad 1 bar. Nell'ipotesi che la trasformazione
Fisica Generale - Modulo Fisica I A.A Ingegneria Meccanica Edile Informatica Esercitazione 9 TERMOLOGIA E SCAMBI TERMICI
 Fisica Generale - Modulo Fisica I A.A. 6-7 TERMOLOGIA E SCAMBI TERMICI Ga. Un calorimetro contiene.5 kg di ghiaccio e.5 kg di acqua in equilibrio termico alla temperatura di C. Trascurando la capacità
Fisica Generale - Modulo Fisica I A.A. 6-7 TERMOLOGIA E SCAMBI TERMICI Ga. Un calorimetro contiene.5 kg di ghiaccio e.5 kg di acqua in equilibrio termico alla temperatura di C. Trascurando la capacità
2) Qual' e la massa di 10 litri di azoto alla pressione di 4 atmosfere ed alla temperatura di 30 C? (P.M.=28 g/mole). (R = J/moleK; ) Risp : 45g
 Aria : Miscuglio di gas costituito da azoto (75,45% in peso), e ossigeno (23,14% in peso), con una piccola percentuale di gas nobili, anidride carbonica e vapor acqueo. La composizione dell'aria non è
Aria : Miscuglio di gas costituito da azoto (75,45% in peso), e ossigeno (23,14% in peso), con una piccola percentuale di gas nobili, anidride carbonica e vapor acqueo. La composizione dell'aria non è
Fondamenti di Meteorologia e Climatologia
 Università degli studi di Trento Facoltà di Ingegneria Corso di Laurea in Ingegneria per l Ambiente e il Territorio Prof. Dino Zardi Dipartimento di Ingegneria Civile ed Ambientale Fondamenti di Meteorologia
Università degli studi di Trento Facoltà di Ingegneria Corso di Laurea in Ingegneria per l Ambiente e il Territorio Prof. Dino Zardi Dipartimento di Ingegneria Civile ed Ambientale Fondamenti di Meteorologia
A1. Soluzione. Ilcalore Q per unita di massa e negativo (ceduto all esterno) e vale:
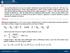 A. na maccina disosta su un asse orizzontale è alimentata da una ortata di 0 kg/s di aria (R = 87 J/kg K, c = 004 J/kg K) alla ressione P = 0 bar e alla temeratura T = 00 C, da un condotto circolare di
A. na maccina disosta su un asse orizzontale è alimentata da una ortata di 0 kg/s di aria (R = 87 J/kg K, c = 004 J/kg K) alla ressione P = 0 bar e alla temeratura T = 00 C, da un condotto circolare di
Prova scritta di Fisica Generale I Corso di Laurea in Astronomia 23 giugno 2015
 Prova scritta di Fisica Generale I Corso di Laurea in Astronomia 3 giugno 015 Problema 1 Si consideri un sistema costituito da un cilindro omogeneo di raggio R 1 = 10 cm e altezza h = 0 cm, inserito all
Prova scritta di Fisica Generale I Corso di Laurea in Astronomia 3 giugno 015 Problema 1 Si consideri un sistema costituito da un cilindro omogeneo di raggio R 1 = 10 cm e altezza h = 0 cm, inserito all
Prova Scritta Completa-Fisica 9 CFU Corso di Laurea in Tossicologia dell ambiente e degli alimenti Novembre 2013
 Prova Scritta Completa-Fisica 9 CFU Corso di Laurea in Tossicologia dell ambiente e degli alimenti Novembre 2013 Quesito 1 Due cubi A e B costruiti con lo stesso legno vengono trascinati sullo stesso pavimento.
Prova Scritta Completa-Fisica 9 CFU Corso di Laurea in Tossicologia dell ambiente e degli alimenti Novembre 2013 Quesito 1 Due cubi A e B costruiti con lo stesso legno vengono trascinati sullo stesso pavimento.
Termodinamica e termochimica
 Termodinamica e termochimica La termodinamica è una scienza che studia proprietà macroscopiche della materia e prevede quali processi chimici e fisici siano possibili, in quali condizioni e con quali energie
Termodinamica e termochimica La termodinamica è una scienza che studia proprietà macroscopiche della materia e prevede quali processi chimici e fisici siano possibili, in quali condizioni e con quali energie
Riepilogo di calorimetria
 Riepilogo di calorimetria Applicate la conservazione dell energia: Calore assorbito = Calore ceduto Se non ci sono trasformazioni di fase: 1. Calore assorbito = massa x calore specifico x (T fin T iniz
Riepilogo di calorimetria Applicate la conservazione dell energia: Calore assorbito = Calore ceduto Se non ci sono trasformazioni di fase: 1. Calore assorbito = massa x calore specifico x (T fin T iniz
IL PRIMO PRINCIPIO DELLA TERMODINAMICA
 IL PRIMO PRINCIPIO DELLA TERMODINAMICA T R AT TO DA: I P ro b l e m i D e l l a F i s i c a - C u t n e l l, J o h n s o n, Yo u n g, S t a d l e r Z a n i c h e l l i e d i t o r e Fo n d a m e n t i
IL PRIMO PRINCIPIO DELLA TERMODINAMICA T R AT TO DA: I P ro b l e m i D e l l a F i s i c a - C u t n e l l, J o h n s o n, Yo u n g, S t a d l e r Z a n i c h e l l i e d i t o r e Fo n d a m e n t i
Lezione 13: Calore e sua propagazione. Elementi di Fisica AA 2011/2012 Doc Claudia R. Calidonna
 Lezione 13: Calore e sua propagazione 1 Energia Interna L'energia interna di un sistema è la somma totale di tutta l'energia delle molecole presenti nel sistema. Include: Energia cinetica traslazionale
Lezione 13: Calore e sua propagazione 1 Energia Interna L'energia interna di un sistema è la somma totale di tutta l'energia delle molecole presenti nel sistema. Include: Energia cinetica traslazionale
Calore, lavoro e trasformazioni termodinamiche (1)
 Calore, lavoro e trasformazioni termodinamiche (1) Attraverso scambi di calore un sistema scambia energia con l ambiente. Tuttavia si scambia energia anche quando le forze (esterne e interne al sistema)
Calore, lavoro e trasformazioni termodinamiche (1) Attraverso scambi di calore un sistema scambia energia con l ambiente. Tuttavia si scambia energia anche quando le forze (esterne e interne al sistema)
Trasformazioni termodinamiche: Esercizi svolti
 Trasformazioni termodinamiche: Esercizi svolti 9 aprile 2013 Esercizio 1 Si consideri un sistema chiuso in cui si abbia inizialmente aria a 5 C, ad una pressione p 1 = 1 bar, che venga in un secondo momento
Trasformazioni termodinamiche: Esercizi svolti 9 aprile 2013 Esercizio 1 Si consideri un sistema chiuso in cui si abbia inizialmente aria a 5 C, ad una pressione p 1 = 1 bar, che venga in un secondo momento
FISICA. Un sistema formato da un gas ideale monoatomico(= sistema) alla pressione costante di 110kPa acquista 820J di energia nella modalità calore.
 Serie 5: Termodinamica V FISICA II liceo Esercizio 1 Primo principio Un cilindro contiene 4 mol di un gas(= sistema) monoatomico a temperatura iniziale di 27 C. Il gas viene compresso effettuano su di
Serie 5: Termodinamica V FISICA II liceo Esercizio 1 Primo principio Un cilindro contiene 4 mol di un gas(= sistema) monoatomico a temperatura iniziale di 27 C. Il gas viene compresso effettuano su di
Un problema di grande interesse è la possibilità di prevedere se due o più sostanze poste a contatto sono in grado di reagire.
 Un problema di grande interesse è la possibilità di prevedere se due o più sostanze poste a contatto sono in grado di reagire. Molte reazioni procedono in modo incompleto; è importante quindi determinare
Un problema di grande interesse è la possibilità di prevedere se due o più sostanze poste a contatto sono in grado di reagire. Molte reazioni procedono in modo incompleto; è importante quindi determinare
Termodinamica e trasmissione del calore 3/ed Yunus A. Çengel Copyright 2009 The McGraw-Hill Companies srl
 SOLUZIONI problemi cap.8 8.1 La pressione del vapore è mantenuta costante. Perciò, la temperatura del vapore rimane costante anche alla temperatura Se si suppone che la trasformazione non implichi irreversibilità
SOLUZIONI problemi cap.8 8.1 La pressione del vapore è mantenuta costante. Perciò, la temperatura del vapore rimane costante anche alla temperatura Se si suppone che la trasformazione non implichi irreversibilità
Il prodotto della pressione per il volume di una determinata massa gassosa è direttamente proporzionale alla temperatura assoluta: PV = KT
 ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
ESERCITAZIONE 5 LEGGI DEI GAS Le leggi che governano i rapporti che si stabiliscono tra massa, volume, temperatura e pressione di un gas, sono leggi limite, riferite cioè ad un comportamento ideale, cui
b) Essendo p A V A = p C V C ne risulta T C = T A = 300 K.
 2.00 moli di un gas perfetto di volume V 1 = 3.50 m 3 e T 1 = 300 K possono espandersi fino a V 2 = 7.00 m 3 e T 2 = 300 K. Il processo è compiuto isotermicamente. Determinare: a) Il lavoro fatto dal gas;
2.00 moli di un gas perfetto di volume V 1 = 3.50 m 3 e T 1 = 300 K possono espandersi fino a V 2 = 7.00 m 3 e T 2 = 300 K. Il processo è compiuto isotermicamente. Determinare: a) Il lavoro fatto dal gas;
Università degli Studi di Roma La Sapienza Corso di Laurea in Ingegneria Energetica. Esame di Fisica I Prova scritta del 9 giugno 2016.
 Università degli Studi di Roma La Sapienza Corso di Laurea in Ingegneria Energetica Esame di Fisica I Prova scritta del 9 giugno 2016 Compito A 1. Un trapezista di un circo (da assimilare a un punto materiale)
Università degli Studi di Roma La Sapienza Corso di Laurea in Ingegneria Energetica Esame di Fisica I Prova scritta del 9 giugno 2016 Compito A 1. Un trapezista di un circo (da assimilare a un punto materiale)
Prova scritta di Fisica Generale I Corso di studio in Astronomia 16 luglio 2013
 Prova scritta di Fisica Generale I Corso di studio in Astronomia 16 luglio 013 Problema 1 Un cubo di legno di densità ρ = 800 kg/m 3 e lato a = 50 cm è inizialmente in quiete, appoggiato su un piano orizzontale.
Prova scritta di Fisica Generale I Corso di studio in Astronomia 16 luglio 013 Problema 1 Un cubo di legno di densità ρ = 800 kg/m 3 e lato a = 50 cm è inizialmente in quiete, appoggiato su un piano orizzontale.
Esercizi di Fisica Tecnica Scambio termico
 Esercizi di Fisica Tecnica 013-014 Scambio termico ST1 Un serbatoio contenente azoto liquido saturo a pressione ambiente (temperatura di saturazione -196 C) ha forma sferica ed è realizzato con due gusci
Esercizi di Fisica Tecnica 013-014 Scambio termico ST1 Un serbatoio contenente azoto liquido saturo a pressione ambiente (temperatura di saturazione -196 C) ha forma sferica ed è realizzato con due gusci
Università degli Studi di Napoli Federico II - Facoltà di Ingegneria Esercizi di Fisica Tecnica per il Corso di laurea in Ingegneria Gestionale
 . SISTEMI APERTI Università degli Studi di Napoli Federico II - Facoltà di Ingegneria Si considerino sempre valide le seguenti ipotesi. ) Regime stazionario. ) Flusso monodimensionale ed equilibrio locale,
. SISTEMI APERTI Università degli Studi di Napoli Federico II - Facoltà di Ingegneria Si considerino sempre valide le seguenti ipotesi. ) Regime stazionario. ) Flusso monodimensionale ed equilibrio locale,
Esercizi di Meccanica
 Esercizi di Meccanica Esercizio N 1 Un calciatore lancia in verticale un pallone di massa 0.94 kg, il quale raggiunge la quota di 22.50 m. Calcolare : a) l'energia del pallone nel punto di quota massima;
Esercizi di Meccanica Esercizio N 1 Un calciatore lancia in verticale un pallone di massa 0.94 kg, il quale raggiunge la quota di 22.50 m. Calcolare : a) l'energia del pallone nel punto di quota massima;
Corso di Laurea in FARMACIA
 Corso di Laurea in FARMACIA 2015 simulazione 1 FISICA Cognome nome matricola a.a. immatric. firma N Evidenziare le risposte esatte Una sferetta è appesa con una cordicella al soffitto di un ascensore fermo.
Corso di Laurea in FARMACIA 2015 simulazione 1 FISICA Cognome nome matricola a.a. immatric. firma N Evidenziare le risposte esatte Una sferetta è appesa con una cordicella al soffitto di un ascensore fermo.
PROBLEMI SULLE MACCHINE TERMICHE A cura del Prof. T.Papa ; ) Q 2 = Q 1 Q 1. t = dm. dt H; = nrt A ln 4 < 0; R 1 = 3 2 R: C + ln 4 C p = 1
 PROBLEMI SULLE MACCHINE TERMICHE A cura del Prof. T.Papa. Il funzionamento di una macchina a vapore puo essere approssimato a quello di una macchina di Carnot, che assorbe calore alla temperatura 2 della
PROBLEMI SULLE MACCHINE TERMICHE A cura del Prof. T.Papa. Il funzionamento di una macchina a vapore puo essere approssimato a quello di una macchina di Carnot, che assorbe calore alla temperatura 2 della
4.1 La pressione sul fondo del recipiente profondo 5 cm è la pressione di saturazione corrispondente alla temperatura di ebollizione di 98 C:
 SOLUZIONI CAPITOLO 4 4.1 La pressione sul fondo del recipiente profondo 5 cm è la pressione di saturazione corrispondente alla temperatura di ebollizione di 98 C: La differenza di pressione tra i fondi
SOLUZIONI CAPITOLO 4 4.1 La pressione sul fondo del recipiente profondo 5 cm è la pressione di saturazione corrispondente alla temperatura di ebollizione di 98 C: La differenza di pressione tra i fondi
CALORE SPECIFICO E CAPACITÀ TERMICA
 1 CALORE SPECIFICO E CAPACITÀ TERMICA 1. (Da Veterinaria 2004) Una scatola di polistirolo (materiale sistemico bianco, leggero, a basso coefficiente di conducibilità termica) contiene 100 g di acqua a
1 CALORE SPECIFICO E CAPACITÀ TERMICA 1. (Da Veterinaria 2004) Una scatola di polistirolo (materiale sistemico bianco, leggero, a basso coefficiente di conducibilità termica) contiene 100 g di acqua a
Ottava esercitazione di Fisica I Termodinamica 1 PROBLEMI RISOLTI
 Ottava esercitazione di Fisica I ermodamica PROBLEMI RISOLI. Il rapporto tra il lavoro compiuto ed il calore assorbito da una mole di gas monoatomico che si espande isobaricamente alla pressione di una
Ottava esercitazione di Fisica I ermodamica PROBLEMI RISOLI. Il rapporto tra il lavoro compiuto ed il calore assorbito da una mole di gas monoatomico che si espande isobaricamente alla pressione di una
UNIVERSITÀ DI BERGAMO FACOLTÀ DI INGEGNERIA. Pneumatica. Roberto Strada
 Pneumatica Roberto Strada Calendario lezioni UNIVERSITÀ DI BERGAMO Programma UNIVERSITÀ DI BERGAMO Programma UNIVERSITÀ DI BERGAMO Programma http://mech.unibg.it/~strada/pne/pn.html L automazione pneumatica
Pneumatica Roberto Strada Calendario lezioni UNIVERSITÀ DI BERGAMO Programma UNIVERSITÀ DI BERGAMO Programma UNIVERSITÀ DI BERGAMO Programma http://mech.unibg.it/~strada/pne/pn.html L automazione pneumatica
CALCOLO DELL'ENERGIA INTERNA
 CALCOLO DELL'ENERGIA INTERNA Enrico Valenti Matricola 145442 29 novembre ore 10,30-12,30 ( trasformazione a temperatura costante ) U 0 = 0 J energia ( J ) p 0 = 1 bar pressione ( Pa ) T 0 = 273 K temperatura
CALCOLO DELL'ENERGIA INTERNA Enrico Valenti Matricola 145442 29 novembre ore 10,30-12,30 ( trasformazione a temperatura costante ) U 0 = 0 J energia ( J ) p 0 = 1 bar pressione ( Pa ) T 0 = 273 K temperatura
10.1 Sono date le frazioni molari dei costituenti dell'aria umida. Si devono determinare le frazioni di massa dei costituenti.
 1 RISOLUZIONI cap.10 10.1 Sono date le frazioni molari dei costituenti dell'aria umida. Si devono determinare le frazioni di massa dei costituenti. Ipotesi Si trascurano le piccole quantità di gas nell'aria
1 RISOLUZIONI cap.10 10.1 Sono date le frazioni molari dei costituenti dell'aria umida. Si devono determinare le frazioni di massa dei costituenti. Ipotesi Si trascurano le piccole quantità di gas nell'aria
Opera rilasciata sotto licenza CC BY-NC-SA 3.0 Italia da Studio Bells (www.studiobells.it)
 Esercizio Argomenti: gas perfetti, trasformazioni adiabatiche, primo principio. Livello: scuola superiore. Un gas perfetto monoatomico si trova in un contenitore chiuso da un pistone mobile. Inizialmente
Esercizio Argomenti: gas perfetti, trasformazioni adiabatiche, primo principio. Livello: scuola superiore. Un gas perfetto monoatomico si trova in un contenitore chiuso da un pistone mobile. Inizialmente
Lezione 5: Termodinamica. Seminario didattico
 Lezione 5: Termodinamica Seminario didattico Esercizio n 1 Ad una mole di gas monoatomico viene fatto percorrere il ciclo mostrato in figura il processo bc è una espansione adiabatica; p B =1.03 bar, V
Lezione 5: Termodinamica Seminario didattico Esercizio n 1 Ad una mole di gas monoatomico viene fatto percorrere il ciclo mostrato in figura il processo bc è una espansione adiabatica; p B =1.03 bar, V
Ultima verifica pentamestre. 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!
 Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Ultima verifica pentamestre 1)definizione di miscuglio, soluzione, composto, elemento, molecola ( definizione importantissima!!!!!!!!) 2) gruppi dal IV al VIII 3) differenza tra massa atomica e massa atomica
Dimensionamento rete aria compressa. Impianti Industriali
 Dimensionamento rete aria Impianti Industriali 2-2009 1 1 - Tratto di tubazione ogni tratto dell'impianto di distribuzione dell aria è individuato da lettere e numeri che ne definiscono gli estremi. Con
Dimensionamento rete aria Impianti Industriali 2-2009 1 1 - Tratto di tubazione ogni tratto dell'impianto di distribuzione dell aria è individuato da lettere e numeri che ne definiscono gli estremi. Con
Esercitazione 8: Aria Umida
 Esercitazione 8: Umida 8.1) Dell aria alla temperatura di 40 C e pressione atmosferica ha una temperatura di bulbo umido di 30 C. Calcolare l umidità assoluta, l umidità relativa e il punto di rugiada
Esercitazione 8: Umida 8.1) Dell aria alla temperatura di 40 C e pressione atmosferica ha una temperatura di bulbo umido di 30 C. Calcolare l umidità assoluta, l umidità relativa e il punto di rugiada
LEZIONE 5-6 ENERGIA TERMICA, TRASPORTO DEL CALORE (CONDUZIONE, CONVEZIONE) ESERCITAZIONI 2
 LEZIONE 5-6 ENERGIA TERMICA, TRASPORTO DEL CALORE (CONDUZIONE, CONVEZIONE) ESERCITAZIONI 2 Esercizio 11 Una pentola contiene 2 kg di acqua ad una temperatura iniziale di 17 C. Si vuole portare l'acqua
LEZIONE 5-6 ENERGIA TERMICA, TRASPORTO DEL CALORE (CONDUZIONE, CONVEZIONE) ESERCITAZIONI 2 Esercizio 11 Una pentola contiene 2 kg di acqua ad una temperatura iniziale di 17 C. Si vuole portare l'acqua
Università degli Studi di Genova DIPARTIMENTO DI TERMOENERGETICA E CONDIZIONAMENTO AMBIENTALE DIAGRAMMI E TABELLE INDICE
 Università degli Studi di Genova DIPARTIMENTO DI TERMOENERGETICA E CONDIZIONAMENTO AMBIENTALE DIAGRAMMI E TABELLE INDICE Diagr. Diagr. TAB. Diagr. Diagr. - 1 PROPRIETA TERMODINAMICHE DEI GAS PERFETTI -
Università degli Studi di Genova DIPARTIMENTO DI TERMOENERGETICA E CONDIZIONAMENTO AMBIENTALE DIAGRAMMI E TABELLE INDICE Diagr. Diagr. TAB. Diagr. Diagr. - 1 PROPRIETA TERMODINAMICHE DEI GAS PERFETTI -
Corso di Laurea in Scienze e Tecnologie Agrarie
 Corso di Laurea in Scienze e Tecnologie Agrarie Corso di Meccanica e Meccanizzazione Agricola Prof. S. Pascuzzi 1 Richiami di termodinamica Branca della fisica che si occupa del calore, del lavoro e di
Corso di Laurea in Scienze e Tecnologie Agrarie Corso di Meccanica e Meccanizzazione Agricola Prof. S. Pascuzzi 1 Richiami di termodinamica Branca della fisica che si occupa del calore, del lavoro e di
L equilibrio dei gas. Lo stato di equilibrio di una data massa di gas è caratterizzato da un volume, una pressione e una temperatura
 Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
Termodinamica 1. L equilibrio dei gas 2. L effetto della temperatura sui gas 3. La teoria cinetica dei gas 4. Lavoro e calore 5. Il rendimento delle macchine termiche 6. Il secondo principio della termodinamica
H - STATI DI AGGREGAZIONE DELLA MATERIA
 H - STATI DI AGGREGAZIONE DELLA MATERIA STATI DI AGGREGAZIONE DELLA MATERIA SOLIDO LIQUIDO AERIFORME STATO SOLIDO LA MATERIA E' COSTITUITA DA MOLECOLE MOLTO VICINE TRA LORO, DISPOSTE IN RETICOLI ORDINATI
H - STATI DI AGGREGAZIONE DELLA MATERIA STATI DI AGGREGAZIONE DELLA MATERIA SOLIDO LIQUIDO AERIFORME STATO SOLIDO LA MATERIA E' COSTITUITA DA MOLECOLE MOLTO VICINE TRA LORO, DISPOSTE IN RETICOLI ORDINATI
14 Gas reali. Potenziali termodinamici
 4 Gas reali. Potenziali termodinamici (9 problemi, difficoltà 62, soglia 43) Formulario Equazione di van der Waals per i gas reali per mol p + a v 2 (v b) RT, dove a e b sono due costanti diverse da gas
4 Gas reali. Potenziali termodinamici (9 problemi, difficoltà 62, soglia 43) Formulario Equazione di van der Waals per i gas reali per mol p + a v 2 (v b) RT, dove a e b sono due costanti diverse da gas
Scritti di Termodinamica dt + R dt T. = cp. = 1.4 = gas biatomico = 78.0 K
 Scritti di Termodinamica 2002 2016 (02/07/18) Una mole di gas ideale passa dallo stato A allo stato B con una trasformazione isobara in cui: H = 2269.72 J, U = 1621.23 J, S = 6.931 J/K Determinare i valori
Scritti di Termodinamica 2002 2016 (02/07/18) Una mole di gas ideale passa dallo stato A allo stato B con una trasformazione isobara in cui: H = 2269.72 J, U = 1621.23 J, S = 6.931 J/K Determinare i valori
Equilibrio dei corpi rigidi e dei fluidi 1
 Equilibrio dei corpi rigidi e dei fluidi 1 2 Modulo 4 Modulo 4 Equilibrio dei corpi rigidi e dei fluidi 4.1. Momento di una forza 4.2. Equilibrio dei corpi rigidi 4.3. La pressione 4.4. Equilibrio dei
Equilibrio dei corpi rigidi e dei fluidi 1 2 Modulo 4 Modulo 4 Equilibrio dei corpi rigidi e dei fluidi 4.1. Momento di una forza 4.2. Equilibrio dei corpi rigidi 4.3. La pressione 4.4. Equilibrio dei
Termodinamica dell atmosfera
 Fondamenti di Fisica dell Atmosfera e del Clima Trento, 3 Marzo 2016 Sistema termodinamico Sistema termodinamico: porzione di materia che occupa una determinata regione dello spazio e puó scambiare massa
Fondamenti di Fisica dell Atmosfera e del Clima Trento, 3 Marzo 2016 Sistema termodinamico Sistema termodinamico: porzione di materia che occupa una determinata regione dello spazio e puó scambiare massa
Gas, liquidi, solidi. Tutti i gas, tranne l'elio, solidificano a basse temperature (alcuni richiedono anche alte pressioni).
 Gas, liquidi, solidi Tutti i gas raffreddati liquefano Tutti i gas, tranne l'elio, solidificano a basse temperature (alcuni richiedono anche alte pressioni). Sostanza T L ( C) T E ( C) He - -269 H 2-263
Gas, liquidi, solidi Tutti i gas raffreddati liquefano Tutti i gas, tranne l'elio, solidificano a basse temperature (alcuni richiedono anche alte pressioni). Sostanza T L ( C) T E ( C) He - -269 H 2-263
PER ESERCITARSI Parte 2. Esercizi su Corpo rigido, variabili angolari, momenti, fluidi, termodinamica
 PER ESERCITARSI Parte 2 Esercizi su Corpo rigido, variabili angolari, momenti, fluidi, termodinamica ESERCIZIO n.1 Due forze uguali ed opposte sono applicate ad un oggetto lungo rette di azione tra loro
PER ESERCITARSI Parte 2 Esercizi su Corpo rigido, variabili angolari, momenti, fluidi, termodinamica ESERCIZIO n.1 Due forze uguali ed opposte sono applicate ad un oggetto lungo rette di azione tra loro
Bilanci macroscopici. Esercizi dal libro Fenomeni di Trsporto, Bird, Stewart, Lightfoot
 Bilanci macroscopici Esercizi dal libro Fenomeni di Trsporto, Bird, Stewart, Lightfoot 7A 7B 7C 7D 7E 7F Esercizio 1 Due recipienti, le cui basi si trovano su uno stesso piano, sono messi in comunicazione
Bilanci macroscopici Esercizi dal libro Fenomeni di Trsporto, Bird, Stewart, Lightfoot 7A 7B 7C 7D 7E 7F Esercizio 1 Due recipienti, le cui basi si trovano su uno stesso piano, sono messi in comunicazione
PRIMI ELEMENTI DI TERMODINAMICA. La termodinamica studia le leggi con cui i sistemi scambiano (cedono e ricevono) energia con l ambiente.
 PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
numero complessivo di variabili = c f + 2
 Regola delle fasi Definiamo sostanza pura quella che ha composizione chimica costante Diremo fase di una sostanza pura una sua regione omogenea dal punto di vista fisico. Lo stato di un sistema è individuato
Regola delle fasi Definiamo sostanza pura quella che ha composizione chimica costante Diremo fase di una sostanza pura una sua regione omogenea dal punto di vista fisico. Lo stato di un sistema è individuato
Corso di Laurea in Scienze Ambientali Corso di Fisica Generale II a.a. 2010/11. Prova di esame del 14/11/ NOME
 Corso di Laurea in Scienze Ambientali Corso di Fisica Generale II a.a. 2010/11 Prova di esame del 14/11/2011 - NOME 1) a) Quanto calore è necessario per aumentare la temperatura di una pentola di ferro
Corso di Laurea in Scienze Ambientali Corso di Fisica Generale II a.a. 2010/11 Prova di esame del 14/11/2011 - NOME 1) a) Quanto calore è necessario per aumentare la temperatura di una pentola di ferro
12/03/2013. Aria umida. Proprietà e trasformazioni
 Aria umida Proprietà e trasformazioni 1 Costituente Concentrazione volumetrica (%) Massa molecolare [kg/ kmol] Azoto (N 2 ) 78,084 28,0134 Ossigeno (O 2 ) 20,9476 31,9988 Argon (Ar) 0,934 39,948 Anidride
Aria umida Proprietà e trasformazioni 1 Costituente Concentrazione volumetrica (%) Massa molecolare [kg/ kmol] Azoto (N 2 ) 78,084 28,0134 Ossigeno (O 2 ) 20,9476 31,9988 Argon (Ar) 0,934 39,948 Anidride
( 160 mol) ( 8,31 J/(mol K) ) = 600 K
 6** T A nr Trasormazione isocora: ( 10 5 Pa) ( m ) ( 160 mol) ( 8,1 J/(mol K) ) 00 K P (10 5 Pa) 4 B A 1 1 4 5 V (m ) Trasormazione isobara: P (10 5 Pa) 4 A B 1 1 4 5 V (m ) Sì, poiché i due stati B e
6** T A nr Trasormazione isocora: ( 10 5 Pa) ( m ) ( 160 mol) ( 8,1 J/(mol K) ) 00 K P (10 5 Pa) 4 B A 1 1 4 5 V (m ) Trasormazione isobara: P (10 5 Pa) 4 A B 1 1 4 5 V (m ) Sì, poiché i due stati B e
REFRIGERAZIONE. Refrigerazione Riduzione e/o mantenimento della temperatura a valori più bassi della temperatura ambiente (<8 C)
 Refrigerazione Riduzione e/o mantenimento della temperatura a valori più bassi della temperatura ambiente (
Refrigerazione Riduzione e/o mantenimento della temperatura a valori più bassi della temperatura ambiente (
Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA
 Anno Scolastico 2009/2010 Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA Prof. Matteo Intermite 1 5.1 LEGGE DEI GAS I gas sono delle sostanze che in determinate condizioni di
Anno Scolastico 2009/2010 Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA Prof. Matteo Intermite 1 5.1 LEGGE DEI GAS I gas sono delle sostanze che in determinate condizioni di
è completamente immerso in acqua. La sua
 In un tubo scorre in regime stazionario un liquido ideale con densità 1.00 10 3 kg/m 3 ; in un punto A il tubo ha raggio R A = 2.00 cm, la velocità di scorrimento è v A = 5.00 m/se la pressione è P A =
In un tubo scorre in regime stazionario un liquido ideale con densità 1.00 10 3 kg/m 3 ; in un punto A il tubo ha raggio R A = 2.00 cm, la velocità di scorrimento è v A = 5.00 m/se la pressione è P A =
Esercizi sui Compressori e Ventilatori
 Esercizi sui Compressori e Ventilatori 27 COMPRESSORE VOLUMETRICO (Appello del 08.06.1998, esercizio N 2) Testo Un compressore alternativo monocilindrico di cilindrata V c = 100 cm 3 e volume nocivo V
Esercizi sui Compressori e Ventilatori 27 COMPRESSORE VOLUMETRICO (Appello del 08.06.1998, esercizio N 2) Testo Un compressore alternativo monocilindrico di cilindrata V c = 100 cm 3 e volume nocivo V
CALORIMETRIA E TERMODINAMICA. G. Roberti
 CALORIMETRIA E TERMODINAMICA G. Roberti 422. A due corpi, alla stessa temperatura, viene fornita la stessa quantità di calore. Al termine del riscaldamento i due corpi avranno ancora pari temperatura se:
CALORIMETRIA E TERMODINAMICA G. Roberti 422. A due corpi, alla stessa temperatura, viene fornita la stessa quantità di calore. Al termine del riscaldamento i due corpi avranno ancora pari temperatura se:
CONVENZIONE SUI SEGNI
 CONVENZIONE SUI SEGNI Si stabilisce una convenzione sui segni sia per gli scambi di calore che per il lavoro che il sistema compie o subisce L>0: LAVORO COMPIUTO DAL SISTEMA Q>0: CALORE ASSORBITO SISTEMA
CONVENZIONE SUI SEGNI Si stabilisce una convenzione sui segni sia per gli scambi di calore che per il lavoro che il sistema compie o subisce L>0: LAVORO COMPIUTO DAL SISTEMA Q>0: CALORE ASSORBITO SISTEMA
Corso Termodinamica. Esercitazione 3. II Principio
 Corso Termodinamica Esercitazione 3 II Principio 1. Una mole di metano fluisce in un condotto; la sua pressione passa da 1.5 a 0.5 atm a temperatura costante. Calcolare la variazione di entropia. 2. Calcolare
Corso Termodinamica Esercitazione 3 II Principio 1. Una mole di metano fluisce in un condotto; la sua pressione passa da 1.5 a 0.5 atm a temperatura costante. Calcolare la variazione di entropia. 2. Calcolare
Problemi di Fisica per l ammissione alla Scuola Galileiana Problema 1
 Problemi di Fisica per l ammissione alla Scuola Galileiana 2015-2016 Problema 1 Un secchio cilindrico di raggio R contiene un fluido di densità uniforme ρ, entrambi ruotanti intorno al loro comune asse
Problemi di Fisica per l ammissione alla Scuola Galileiana 2015-2016 Problema 1 Un secchio cilindrico di raggio R contiene un fluido di densità uniforme ρ, entrambi ruotanti intorno al loro comune asse
INTRODUZIONE ALLA TERMODINAMICA. Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta
 INTRODUZIONE ALLA TERMODINAMICA Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta in un recipiente, ad esempio 5g di ossigeno. Dato l elevato numero di molecole
INTRODUZIONE ALLA TERMODINAMICA Supponiamo di voler studiare il comportamento di una determinata quantità di gas contenuta in un recipiente, ad esempio 5g di ossigeno. Dato l elevato numero di molecole
Meccanica dei Fluidi. stati di aggregazione della materia: solidi liquidi gas. fluidi assumono la forma del contenitore
 Meccanica dei luidi stati di aggregazione della materia: solidi liquidi gas fluidi assumono la forma del contenitore Caratteristiche di un fluido LUIDO sostanza senza forma propria (assume la forma del
Meccanica dei luidi stati di aggregazione della materia: solidi liquidi gas fluidi assumono la forma del contenitore Caratteristiche di un fluido LUIDO sostanza senza forma propria (assume la forma del
La fisica al Mazzotti. Legge fondamentale della termologia
 La fisica al Mazzotti Legge fondamentale della termologia 17 1 3 L evoluzione del pensiero L evoluzione del pensiero per spiegare il riscaldamento di alcuni materiali dalla prima metà del Settecento gli
La fisica al Mazzotti Legge fondamentale della termologia 17 1 3 L evoluzione del pensiero L evoluzione del pensiero per spiegare il riscaldamento di alcuni materiali dalla prima metà del Settecento gli
CorsI di Laurea in Ingegneria Aereospaziale-Meccanica-Energetica. FONDAMENTI DI CHIMICA Docente: Cristian Gambarotti. Esercitazione del 03/11/2010
 CorsI di aurea in Ingegneria Aereospaziale-Meccanica-Energetica FONDAMENTI DI CIMICA Docente: Cristian Gambarotti Esercitazione del // Argomenti della lezione avoro, Calore, Energia Interna, Entalpia relativi
CorsI di aurea in Ingegneria Aereospaziale-Meccanica-Energetica FONDAMENTI DI CIMICA Docente: Cristian Gambarotti Esercitazione del // Argomenti della lezione avoro, Calore, Energia Interna, Entalpia relativi
PROBLEMI E QUESITI DI TERMOLOGIA (ENUNCIATI) INTRODUZIONE a cura di Nicola SANTORO
 1 PROBLEMI E QUESITI DI TERMOLOGIA (ENUNCIATI) INTRODUZIONE a cura di Nicola SANTORO I problemi ed i quesiti di Termologia che seguono sono il frutto di esperienze da me compiute principalmente nei licei
1 PROBLEMI E QUESITI DI TERMOLOGIA (ENUNCIATI) INTRODUZIONE a cura di Nicola SANTORO I problemi ed i quesiti di Termologia che seguono sono il frutto di esperienze da me compiute principalmente nei licei
Capacità termica e calore specifico
 Calori specifici Capacità termica e calore specifico Il calore si trasferisce da un corpo ad un altro fintanto che i corpi sono a temperature differenti. Potremo scrivere quindi: Q = C ΔT = C (T f T i
Calori specifici Capacità termica e calore specifico Il calore si trasferisce da un corpo ad un altro fintanto che i corpi sono a temperature differenti. Potremo scrivere quindi: Q = C ΔT = C (T f T i
= m 1c P b ln T e. + m 2 c acq ln T e. Essendo il sistema isolato tale variazione e anche la variazione d'entropia dell'universo.
 Problemi sul II Principio della Termodinamica e sull'entropia A cura del Prof. T.Papa 1. Un blocco di alluminio (M Al = 27) di massa m = 1 kg, alla temperatura di 500 C, viene rareddato ponendolo a contatto
Problemi sul II Principio della Termodinamica e sull'entropia A cura del Prof. T.Papa 1. Un blocco di alluminio (M Al = 27) di massa m = 1 kg, alla temperatura di 500 C, viene rareddato ponendolo a contatto
