LEZIONE 2 COMPOSTI DEL CARBONIO: MACROMOLECOLE:
|
|
|
- Isabella Corona
- 7 anni fa
- Visualizzazioni
Transcript
1 LEZIONE 2 COMPONENTI CHIMICI DELLA CELLULA ACQUA COMPOSTI DEL CARBONIO: MACROMOLECOLE: ZUCCHERI ACIDI GRASSI PROTEINE NUCLEOTIDI
2 percentuale di abbondanza relativa I componenti chimici di una cellula organismi crosta terrestre H C O N Ca e Mg Na e K P Si altri Una cellula vivente è composta da una serie ristretta di elementi, quattro dei quali (H, C, O e N) corrispondono al 99% del suo peso.
3 I componenti chimici di una cellula
4 I componenti chimici di una cellula La sostanza più abbondante nelle cellule viventi è l ACQUA; essa rappresenta il 70% del peso di una cellula e la maggior parte delle reazioni intracellulari avvengono in un ambiente acquoso. Se lasciamo da parte l H 2 O, quasi tutte le molecole di una cellula sono composti del carbonio, che costituiscono la materia della chimica organica. Composizione chimica approssimativa di una cellula batterica % del peso N di tipi di cellulare totale ciascuna molecola - Acqua Ioni inorganici Zuccheri e precursori Aminoacidi e precursori 0, Nucleotidi e precursori 0, Acidi grassi e precursori Altre piccole molecole 0, Macromolecole (proteine, acidi nucleici e polisaccaridi)
5 La molecola dell acqua O è più elettronegativo ed attrae maggiormente gli è O ha una parziale carica ; H ha una parziale carica + Quando la regione carica + di una molecola di H 2 O (H) viene a trovarsi in prossimità della regione carica (O) di un altra molecola di H 2 O, la reciproca attrazione elettrica può dar luogo a un legame debole: il LEGAME IDROGENO.
6 LEGAME IDROGENO A causa della loro polarizzazione, due molecole di H 2 O adiacenti possono formare un legame idrogeno (1/20 della forza di un legame covalente). d + d + d + 2d - d + 2d - legame idrogeno lunghezze di legame legame idrogeno 0,28 nm 0,104 nm, legame covalente ACQUA il legame covalente crea un legame dipolare d - regione elettronegativa H O d - d + H d + regione elettropositiva e- distribuiti in modo asimmetrico: molecola polare LA STRUTTURA DELL H 2 O Molecole di H 2 0 si uniscono transientemente in un reticolo di legami idrogeno Le molecole non polari interrompono i legami idrogeno MOLECOLE IDROFILICHE E IDROFOBICHE idrofobiche A causa della loro natura polare, le molecole d H 2 O si raccolgono intorno agli ioni e ad altre molecole polari. Perciò le molecole che possono trovare posto nelle strutture formate da legami idrogeno dell H 2 O sono idrofiliche e relativamente solubili in H 2 O
7 Le proprietà dell acqua Le proprietà dell acqua che scaturiscono dalla sua struttura sono quelle di seguito elencate: 1. Elevata coesione 2. Elevata tensione superficiale 3. Elevata capacità termica 4. Elevato calore di evaporazione 5. Elevato punto di ebollizione ed elevato punto di fusione Sostanze IDROFILICHE: si sciolgono in H 2 O perché sono composte da ioni o molecole polari che attraggono le molecole di H 2 O con interazioni elettriche. Le molecole di H 2 O circondano ogni ione o molecola polare che si trova sulla superficie del solido e lo portano in soluzione. Sostanze IDROFOBICHE: Contengono prevalentemente legami non polari perciò non sono solubili. L H 2 O non è attratta da tali molecole e perciò non tende ad avvolgerle e a portarle in soluzione
8 Il carbonio A parte l H 2 O quasi tutte le molecole cellulari si basano sul Carbonio, che si distingue tra tutti gli altri elementi per la sua eccezionale capacità di formare grandi molecole C Piccolo, con 4 elettroni e 4 posti vuoti nel suo guscio esterno, l atomo di C può dare 4 legami covalenti con altri atomi. Ogni atomo di C può unirsi ad altri C in catene ed anelli con legami covalenti stabilissimi e quindi dar luogo a molecole grandi e complesse di dimensioni praticamente illimitate: le molecole organiche
9 I componenti chimici di una cellula IV
10 I componenti chimici di una cellula Le cellule contengono 4 famiglie principali di piccole molecole organiche: subunità Macromolecole macromolecole
11 I componenti chimici di una cellula Le cellule contengono 4 famiglie principali di piccole molecole organiche: ZUCCHERI AMMINOACIDI ACIDI GRASSI - NUCLEOTIDI
12 Le macromolecole Le cellule contengono 4 famiglie principali di piccole molecole organiche Queste piccole molecole organiche si possono associare in lunghe catene formando le macromolecole Le macromolecole sono, in peso, i composti carboniosi + abbondanti della cellula vivente Le macromolecole cellulari sono polimeri formati semplicemente unendo con legami covalenti molecole organiche piccole (dette subunità o monomeri) in lunghe catene Benché differenti nei particolari, le reazioni chimiche con cui vengono aggiunte le subunità ai polimeri di proteine, acidi nucleici o polisaccaridi presentano importanti caratteristiche comuni Ogni polimero si allunga applicando un nuovo monomero all estremità di una catena polimerica in crescita mediante una reazione di condensazione, in cui una molecola di H 2 O viene eliminata per ogni subunità aggiunta In tutti i casi la reazione è catalizzata da enzimi che garantiscono l incorporazione esclusiva dei monomeri del tipo giusto
13 Le macromolecole La polimerizzazione, un monomero alla volta, in una catena lunga è un procedimento semplice per fabbricare una molecola grande e complessa, dato che ogni elemento viene ad aggiungersi grazie alla stessa reazione eseguita ripetutamente dalla stessa batteria enzimatica Quasi tutte le macromolecole vengono sintetizzate impiegando un gruppo di monomeri leggermente diversi tra loro (20 aa o 4 nt); inoltre nella catena polimerica le subunità non vengono montate a caso, ma in un ordine particolare o sequenza La funzione biologica di proteine, acidi nucleici e gran parte dei polisaccaridi dipende rigidamente dalla specifica sequenza delle subunità nella catena lineare. Per questo l apparato che polimerizza deve sottostare a un controllo molto fine e determinare con esattezza la subunità da collocare volta per volta nel polimero in crescita
14 I componenti chimici di una cellula Le macromolecole subunità Macromolecole macromolecole
15 MONOSACCARIDI L unità strutturale più semplice sono i monosaccaridi con formula generale: (CH 2 O) n e sono classificati in base a: 1.Presenza di un gruppo aldeidico o chetonico ALDOSI 2. Numero di atomi di carbonio (2,3,4,5 o 6) CHETOSI D-Glucosio: il più importante degli aldoesosi D-Fruttosio: il più importante dei chetoesosi
16 FORMAZIONE DEGLI ANELLI I gruppi aldeidici o chetonici di uno zucchero possono reagire con un gruppo ossidrilico della stessa molecola: D-Glucosio (aldoesoso, forma aperta) a-d-glucosio H C OH Forma piranosica b-d-glucosio Una conseguenza di questa reazione è la scomparsa del gruppo aldeidico (o chetonico) e la formazione di un nuovo atomo di C asimmetrico (definito glicosidico) che porta un nuovo OH, che potrà trovarsi: al di sotto (isoforma a) o la di sopra (isoforma b) del piano in cui giace la forma ciclica
17 ISOMERI I monosaccaridi hanno molti isomeri che differiscono soltanto nell orientamento dei loro gruppi ossidrilici. Es: glucosio mannosio FORME D E FORME L galattosio Due isomeri che sono immagini speculari l uno dell altro hanno la stessa chimica e perciò hanno lo stesso nome e si distinguono per il prefisso D o L. D-glucosio piano dello specchio L-glucosio
18 Carboidrati: monosaccaridi glucosio fruttosio galattosio Carboidrati: disaccaridi lattosio galattosio glucosio saccarosio glucosio fruttosio
19 IL LEGAME GLICOSIDICO E I DERIVATI DEI MONOSACCARIDI Il C che porta l aldeide o il chetone può reagire con qualunque gruppo ossidrilico di un secondo zucchero per formare un legame glicosidico. In questo modo si possono formare a-d-glucosio b-d-fruttosio DISACCARIDI saccarosio (glucosio a1,2 fruttosio) OLIGOSACCARIDI E POLISACCARIDI
20 Carboidrati: legami α- e β-glicosidici uniscono i monosaccaridi legame β-glicosidico legame α-glicosidico -
21 OLIGOSACCARIDI E POLISACCARIDI Glicogeno: le catene sono costituite da unità di glucosio unite da legami a, 1-4 glicosidici Le ramificazioni si inseriscono sulle catene principali mediante legami a, 1-6 glicosidici Amilosio e cellulosa differiscono solo per la conformazione a o b del legame glicosidico
22 Gli zuccheri sono importanti fonti di energia e costituiscono strutture di supporto Il glucosio è il monosaccaride cui spetta un ruolo centrale tra le fonti di energia della cellula. Esso viene demolito in molecole più piccole in una serie di reazioni, nelle quali si libera energia utilizzabile dalla cellula per compiere lavoro utile. Per immagazzinare energia e tenerla di riserva le cellule accantonano polisaccaridi contenenti solo glucosio sotto forma di glicogeno negli animali e amido nella piante Cellulosa: polisaccaride del glucosio che costituisce le pareti cellulari vegetali ed è la sostanza organica più abbondante sulla Terra cellulosa glicogeno legami b (1 4) Ramificazione: legami a1,6 legami a1,4
23 Carboidrati: polisaccaridi glicogeno
24 Le macromolecole - polisaccaridi Tra le 4 famiglie principali di piccole molecole organiche contenute nelle cellule, ora trattiamo i monosaccaridi. Unendo semplicemente i monosaccaridi con legami glicosidici (covalente) in lunghe catene si formano le macromolecole cellulari denominate polisaccaridi Le reazioni chimiche con cui vengono aggiunte le subunità di monosaccaridi ai polisaccaridi presentano importanti caratteristiche comuni alla polimerizzazione delle altre macrmolecole (proteine, acidi nucleici). Il polisaccaride si allunga applicando un nuovo monosaccaride all estremità di una catena polimerica in crescita mediante una reazione di condensazione, in cui una molecola di H 2 O viene eliminata per ogni subunità aggiunta. In tutti i casi la reazione è catalizzata da enzimi che garantiscono l incorporazione esclusiva dei monosaccaridi del tipo giusto
25 Le macromolecole - polisaccaridi La polimerizzazione, un monosaccaride alla volta, in una catena lunga è un procedimento semplice per fabbricare una molecola grande e complessa, dato che ogni elemento viene ad aggiungersi grazie alla stessa reazione eseguita ripetutamente dalla stessa batteria enzimatica I polisaccaridi vengono sintetizzati impiegando un gruppo di monosaccaridi leggermente diversi tra loro; inoltre nella catena polimerica le subunità non vengono montate a caso, ma in un ordine particolare detto sequenza La funzione biologica di gran parte dei polisaccaridi dipende rigidamente dalla specifica sequenza delle subunità nella catena lineare. Per questo l apparato che polimerizza deve sottostare a un controllo molto fine e determinare con esattezza il monosaccaride da collocare volta per volta nel polisaccaride in crescita
26 I componenti chimici di una cellula Le macromolecole subunità Macromolecole macromolecole
27 ACIDI GRASSI COMUNI La molecola di acido grasso presenta 2 regioni chimicamente distinte una lunga catena idrocarburica: idrofobica e chimicamente poco reattiva un gruppo COOH, che si comporta come un acido, ionizzato in soluzione (COO-) estremamente idrofilico e chimicamente reattivo Molecole anfipatiche: 1 regione idrofilica e 1 idrofobica Acido grasso saturo: contiene il massimo numero di H ed è privo di doppi legami Acido grasso insaturo: con uno o più doppi legami tra atomi di C I numerosi acidi grassi presenti nelle cellule differiscono solo per la lunghezza della catena idrocarburica e per il numero e la posizione dei doppi legami C-C
28 TRIGLICERIDI Gli acidi grassi sono immagazzinati come riserva di energia (grasso) come esteri del glicerolo a formare i trigliceridi. L esterificazione dei 3 gruppi alcolici del glicerolo con altrettanti acidi grassi porta alla formazione di un trigliceride
29 GRUPPO CARBOSSILICO Se libero, il gruppo carbossilico di un acido grasso si ionizza, ma più comunemente è legato ad altri gruppi a formare o esteri o amidi FOSFOLIPIDI testa polare Nei fosfolipidi: due dei gruppi OH del glicerolo sono legati ad acidi grassi il terzo gruppo OH è legato ad acido fosforico code idrofobiche di acidi grassi Il fosfato è ulteriormente legato ad un gruppo (un alcool) che forma una piccola testa polare
30 AGGREGATI LIPIDICI Gli acidi grassi e i fosfolipidi hanno: una testa idrofilica e una coda idrofobica In H 2 O possono formare piccole micelle un film superficiale un doppio strato fosfolipidico I fosfolipidi e i glicolipidi formano doppi strati lipidici autosigillanti che sono la base di tutte le membrane cellulari
31 Le macromolecole - lipidi Tra le 4 famiglie principali di piccole molecole organiche contenute nelle cellule, ora trattiamo gli acidi grassi. Gli acidi grassi si possono associare in lunghe catene formando le membrane, i lipidi, i grassi Le membrane, i lipidi e i grassi sono polimeri formati semplicemente unendo gli acidi grassi (in questo caso non con legami covalenti) in lunghe catene Gli acidi grassi differiscono dalle altre macromolecole, soprattutto perché le reazioni chimiche con cui vengono aggiunte le subunità di acidi grassi alle membrane non hanno le caratteristiche che accomunano gli altri 3 tipi di macromolecole: -catena polimerica in crescita -reazione di condensazione -eliminazione di una molecola di H 2 O -incorporazione esclusiva dei monomeri in una ben determinata sequenza -stessa reazione eseguita ripetutamente dalla stessa batteria enzimatica
32 I componenti chimici di una cellula Le cellule contengono 4 famiglie principali di piccole molecole organiche: subunità Macromolecole macromolecole
33 Struttura degli aminoacidi Gli amminoacidi sono una variegata classe di molecole che hanno alcune proprietà in comune e si distinguono solamente in base alla catena laterale: Gruppo amminico a Gruppo carbossilico + H 3 N- -COO - Catena laterale A ph fisiologico COOH ed NH 2 sono ionizzati
34 Stereochimica degli amminoacidi Il Ca è legato a 4 diversi sostituenti, pertanto è un atomo di C asimmetrico; ciò fa sì che ciascun amminoacido esista in 2 forme isomeriche (stereoisomeri) che possono essere orientate nello spazio secondo 2 conformazioni: L e D, l una immagine speculare dell altra (eccezione: la Gly) Gli aa presenti nelle proteine sono tutti della serie L
35 Polari ma privi di carica Serina Ser, S Treonina Thr, T Tirosina Tyr, Y Asparagina Asn, N Glutammina Gln, Q Gli amminoacidi costituenti le proteine vengono classificati in 3 gruppi sulla base delle proprietà chimico-fisiche del loro radicale: Apolari Glicina Gly, G Cisteina Cys, C Alanina Ala, A Metionina Met, M Valina Val, V Fenilalanina Phe, F Leucina Leu, L Triptofano Trp, W Isoleucina Ile, I Prolina Pro, P Ionizzabili: acidi o basici Acido Aspartico Asp, D Acido Glutammico Glu, E Lisina Lys, K Arginina Arg, R Istidina His, H
36 aminoacidi Le cellule umane e animali partendo da sostanze semplici possono sintetizzarne solo alcuni. Quelli che invece devono essere introdotti con la dieta si chiamano aminoacidi essenziali questi sono i 20 aminoacidi che si trovano nell organismo umano e che costituiscono le PROTEINE
37 Amminoacidi essenziali e non essenziali L organismo non è in grado di immagazzinare aa Le cellule traggono elementi necessari alla sintesi di nuove proteine attingendo ad un pool di amminoacidi liberi che provengono da: 1. sintesi (aa non essenziali) 2. processi di assorbimento (aa essenziali: devono essere introdotti con la dieta) 3. dalla demolizione di proteine (riciclaggio) Essenziali Non essenziali Istidina Isoleucina Leucina Lisina Metionina Fenilalanina Treonina Triptofano Valina Alanina Arginina a Asparagina Aspartato Cisteina Glutammato Glutammina Glicina Prolina Serina Tirosina a Arg: non essenziale, ma i bambini in crescita ne devono assumere anche con la dieta
38 Il legame peptidico La reazione di condensazione che si realizza tra gli aa per formare i peptidi avviene tra il gruppo COOH del primo aa ed il gruppo NH 2 di quello seguente con perdita di H 2 O Le proteine sono polimeri di aa che si uniscono con un legame peptidico in una lunga catena Il legame peptidico è una struttura planare e rigida: non è possibile effettuare rotazioni introno al legame C-N
39 Struttura delle proteine I polipeptidi hanno una precisa direzionalità, cioè una polarità strutturale: Catene laterali Ossatura polipeptidica Ammino o N-terminale Carbossi o C-terminale Legame peptidico Legami peptidici I polipeptidi sono sintetizzati dall N-term al C-term la seq degli aa viene scritta nello stesso ordine
40 Organizzazione tridimensionale delle proteine Le proteine sono polimeri di aa che si uniscono con un legame peptidico in una lunga catena che non rimane filamentosa, ma si ripiegano assumendo una struttura tridimensionale di tipo globulare che presenta una caratteristica conformazione per ognuna di esse. Le proteine si dispongono in modo da stabilire il maggior numero di interazioni con il mezzo circostante, con atomi o gruppi appartenenti alla molecola stessa (interazioni intramolecolari) o a molecole circostanti (interazioni intermolecolari). Legami deboli: legami H, interazioni elettrostatiche e forze di Van der Waals La struttura tridimensionale delle proteine è stata semplificata e scomposta in vari livelli di organizzazione: Struttura primaria Struttura secondaria Struttura terziaria Struttura quaternaria
41 La struttura primaria delle proteine è data dalla successione degli aminoacidi che compongono la proteina Legame disolfuro insulina La sequenza aa è unica per ogni tipo di proteina, e in ogni molecola di quella proteina la seq è rigorosamente la stessa Sono state identificate molte migliaia di proteine diverse: ognuna ha una sua propria seq aa Possono esistere infinite proteine con identica composizione aa, ma con diversa sequenza: sono pt diverse
42 La struttura secondaria delle proteine Interessa tratti più o meno lunghi di una catena polipeptidica, che assumono un ripiegamento regolare e ripetitivo Alfa elica Beta foglietto Entrambe queste strutture secondarie sono tenute insieme da legami idrogeno fra gruppi NH e CO dei legami peptidici
43 La struttura secondaria delle proteine: Struttura alfa-elica =O Un a-elica si forma quando una regione di una catena polipeptidica si avvolge su se stessa, con il gruppo CO di un legame peptidico che forma un legame idrogeno con il gruppo NH di un legame peptidico posto 4 residui più a valle nella catena polipeptidica lineare a4 a8 a1 H a5 a7 a3 a9 a2 =O a6 a10 a4 a1 a8 a7 a5 a3 a9 a2 a6 a10 a11 a11
44 La struttura secondaria delle proteine: Struttura beta-foglietto Si forma quando diversi filamenti di una catena polipeptidica si dispongono parallelamente gli uni agli altri. In ciascun filamento i gruppo NH e CO dei legami peptidici sono rivolti perpendicolarmente rispetto alla direzione della catena e formano legami-h con i gruppi NH e CO dei legami peptidici della catena affiancata. Ogni legame peptidico forma 2 legami-h Le catene laterali degli aa sporgono al di sopra o al di sotto delle catene affiancate NH 2 COOH Il b-foglietto si può formare fra parecchi filamenti polipeptidici, che possono essere: paralleli antiparalleli NH 2 NH 2 COOH COOH COOH NH 2
45 La struttura secondaria delle proteine: Struttura beta-foglietto Ca CO CO NH NH NH Ca Ca Ca Ca NH CO CO NH CO Ca Ca CO NH Ca CO NH Ca NH CO Ca CO NH Ca NH CO Ca
46 La struttura terziaria delle proteine: Legami deboli (o ponti disolfuro) fra catene laterali di aa che si trovano in regioni diverse della stessa seq primaria Domini: strutture globulari compatte: unità base della struttura terziaria: combinazioni di a-elica e b- foglietto, connesse da regioni ad ansa: unità funzionali e strutturali della pt. Pt con funzioni simili hanno domini simili Il ripiegamento della pt non è casuale, è dettato dalla struttura primaria e dall ambiente esterno: aa apolari nella parte interna (forze di van der Waals) aa polari esposti alla superficie (interazioni con H 2 O) Contrario per le proteine di membrana
47 La struttura quaternaria delle proteine La struttura quaternaria consiste nelle interazioni fra catene polipeptidiche diverse in proteine composte da più di un polipeptide. L associazione delle diverse catene è guidata dalla stessa logica che ha consentito il raggomitolamento nella struttura terziaria: legami deboli ponti disolfuro aa apolari e aa polari Emoglobina: Eterodimero costituito dall aggregazione di 4 subunità uguali a 2 a 2.
48 DOMINIO PROTEICO: è l unità strutturale base di una proteina. Il nucleo di ciascun dominio è composto in gran parte da una serie di foglietti b o a eliche o da un misto delle due a strutture. La struttura delle proteine I TRE LIVELLI DI ORGANIZZAZIONE DI UNA PROTEINA proteina CAP a-elica dominio foglietto b subunità proteica (monomero) molecola proteica (dimero) struttura secondaria struttura terziaria struttura quaternaria MOTIVI COMUNI NELLE PROTEINE motivo a forcina beta motivo beta-alfa-beta
49 Denaturazione e rinaturazione di una proteina Il riscaldamento e il trattamento con un riducente disgregano la conformazione nativa denaturando la proteina Agenti denaturanti: Fisici: calore, radiazioni Chimici: ph, urea, guanidina, ecc Rompono i legami che stabilizzano le strutture secondaria, terziaria e quaternaria: si modifica la struttura tridimensionale senza modificare la seq aa La denaturazione causa la scomparsa dell attività biologica della proteina, ciò evidenza chiaramente il legame tra attività biologica e struttura tridimensionale La rinaturazione si accompagna alla ricomparsa di tutte le proprietà della proteina nativa, compresa l attività biologica
50 Le proteine Rinaturazione e ripiegamento delle proteine Il riscaldamento e il trattamento con un riducente che rompe i legami disolfuro disgregano la conformazione nativa denaturando la proteina Se la Rnasi denaturata viene poi riportata in condizioni native si ripiega spontaneamente nella sua conformazione nativa Legami disolfuro RNasi nativa RNasi denaturata RNasi nativa La ribonucleasi (Rnasi)
51 FUNZIONI DELLE PROTEINE (proteios = di primaria importanza) Le cellule sono sostanzialmente formate da elementi proteici che costituiscono la maggior parte della loro massa, insieme all acqua Tuttavia le proteine non danno solo la forma e la struttura della cellula, ma eseguono anche quasi tutte le sue funzioni 1. Enzimi catalizzatori che accelerano la velocità delle reazioni chimiche 2. Proteine strutturali pt del citoscheletro, collagene, elastina, cheratina ecc. 3. Carriers proteine di trasporto inserite nella membrana citoplasmatica 4. Proteine contrattili assicurano la motilità delle cellule e degli organismi 5. Ormoni proteici es. ormoni ipotalamici, ipofisari, PTH, CT, insulina, glucagone 6. Proteine di trasporto es emoglobina del sangue 7. Anticorpi principale sistema di difesa degli organismi 8. Proteine di deposito deposito di materia o di energia (es, ovalbumina, caseina) o di particolari sostanze (la ferritina, deposito di ferro). 9. Tossine Le proteine costituiscono lo hardware delle cellule.
52 Le macromolecole - proteine Tra le 4 famiglie principali di piccole molecole organiche contenute nelle cellule, ora trattiamo gli amminoacidi. Unendo semplicemente gli amminoacidi con legami peptidici (covalente) in lunghe catene si formano le macromolecole cellulari denominate proteine Le reazioni chimiche con cui vengono aggiunti gli amminoacidi alle proteine presentano importanti caratteristiche comuni alla polimerizzazione delle altre macromolecole (polisaccaridi, acidi nucleici). La proteina si allunga applicando un nuovo amminoacido all estremità di una catena polimerica in crescita mediante una reazione di condensazione, in cui una molecola di H 2 O viene eliminata per ogni aminoacido aggiunto In tutti i casi la reazione è catalizzata da enzimi che garantiscono l incorporazione esclusiva dell amminoacido del tipo giusto
53 Le macromolecole - proteine La polimerizzazione, un amminoacido alla volta, in una catena lunga è un procedimento semplice per fabbricare una molecola grande e complessa, dato che ogni elemento viene ad aggiungersi grazie alla stessa reazione eseguita ripetutamente dalla stessa batteria enzimatica Le proteine vengono sintetizzate impiegando 20 amminoacidi leggermente diversi tra loro; inoltre nella catena polimerica le subunità non vengono montate a caso, ma in un ordine particolare: la sequenza amminoacidica La funzione biologica delle proteine dipende rigidamente dalla specifica sequenza delle subunità nella catena lineare. Per questo l apparato che polimerizza deve sottostare a un controllo molto fine e determinare con esattezza la subunità da collocare volta per volta nel polimero in crescita
54 I componenti chimici di una cellula Le cellule contengono 4 famiglie principali di piccole molecole organiche: subunità Macromolecole macromolecole
55 FINE
56 Regolazione dell attività biologica delle proteina Nella cellula l attività delle proteine deve essere finemente regolata attraverso diversi meccanismi. Vediamo 2 esempi: 1. Regolazione allosterica: Un effettore allosterico, composto chimico a basso PM si lega al sito allosterico della proteina e ne causa la transizione allosterica dalla conformazione attiva a quella inattiva 2. Regolazione per modificazione covalente: Una protein-chinasi fosforila la proteina, causando la transizione dalla conformazione attiva a quella inattiva
57 Il ruolo centrale degli enzimi come catalizzatori biologici Il compito fondamentale delle proteine è quello di agire da enzimi: catalizzatori che aumentano la velocità di quasi tutte le reazioni chimiche che avvengono all interno delle cellule. Substrato A Substrato B enzima Complesso enzima-substrato Gli enzimi accelerano la velocità di reazione di più di un milione di volte, così che reazioni che richiederebbero anni in assenza di catalisi possono avvenire in frazioni di secondo se catalizzate dall enzima appropriato. enzima Prodotto
LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche:
 LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
Le biomolecole si trovano negli organismi viventi
 Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
Le biomolecole si trovano negli organismi viventi I viventi sono formati per la maggior parte da acqua e molecole, chiamate biomolecole. Le biomolecole sono sostanze contenenti carbonio. I composti del
a) un movimento contro gradiente di concentrazione che utilizza fonti primarie di energia
 1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
1. Quale considerazione sulla struttura primaria di una proteina è vera? a) è caratteristica delle proteine insolubili b) i ponti S-S la stabilizzano c) i ponti H la stabilizzano d) la proteina assume
Jay Phelan, Maria Cristina Pignocchino. Scopriamo la biologia
 Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
Jay Phelan, Maria Cristina Pignocchino Scopriamo la biologia Capitolo 2 Le molecole della vita 3 1. Le classi delle biomolecole Le biomolecole sono composti organici formati da: catene di atomi di carbonio,
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Proteine strutturali Sostegno meccanico Cheratina: costituisce i capelli Collagene: costituisce le cartilagini Proteine di immagazzinamento
 Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Tipo Funzione Esempi Enzimi Accelerano le reazioni chimiche Saccarasi: posiziona il saccarosio in modo che possa essere scisso nelle due unità di glucosio e fruttosio che lo formano Ormoni Messaggeri chimici
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Il carbonio è l elemento di base delle biomolecole. Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici.
 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 1 Il carbonio deve acquistare quattro elettroni per essere stabile
Il carbonio è l elemento più abbondante nelle molecole biologiche
 Le biomolecole Il carbonio è l elemento più abbondante nelle molecole biologiche Le molecole contenenti carbonio sono chiamate biomolecole. Le biomolecole fanno parte di un gruppo molto ampio di composti
Le biomolecole Il carbonio è l elemento più abbondante nelle molecole biologiche Le molecole contenenti carbonio sono chiamate biomolecole. Le biomolecole fanno parte di un gruppo molto ampio di composti
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Schemi delle lezioni 1
 Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Schemi delle lezioni 1 Detti anche proteine sono i composti organici maggiormente presenti nelle cellule, dato che costituiscono circa il 50% del loro peso secco. Nell uomo adulto rappresentano circa
Le molecole biologiche. Sylvia S. Mader Immagini e concetti della biologia Zanichelli editore, 2012
 Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
Le molecole biologiche 1 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti organici. 2 Il carbonio deve acquistare quattro elettroni
COMPOSTI AZOTATI. derivanti dall ammoniaca AMMINE. desinenza -INA AMMIDE
 COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
COMPOSTI AZOTATI derivanti dall ammoniaca AMMINE desinenza -INA AMMIDE ANCORA AMMIDI RISONANZA A M M I D I Il legame ammidico ha parziale carattere di doppio legame per la seguente risonanza: Ammidi H
BIOMOLECOLE (PROTEINE)
 BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
BIOMOLECOLE (PROTEINE) Proteine: funzioni Strutturale (muscoli, scheletro, legamenti ) Contrattile (actina e miosina) Di riserva (ovoalbumina) Di difesa (anticorpi) Di trasporto (emoglobina, di membrana)
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Proteine: struttura e funzione
 Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
Proteine: struttura e funzione Prof.ssa Flavia Frabetti PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (C, H, O,
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Vittoria Patti MACROMOLECOLE BIOLOGICHE. 4. proteine
 Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Vittoria Patti MACROMOLECOLE BIOLOGICHE 4. proteine 1 Funzioni principali delle proteine funzione cosa significa esempi ENZIMATICA STRUTTURALE TRASPORTO MOVIMENTO DIFESA IMMUNITARIA ORMONALE catalizzare
Di cosa è fatta una cellula?
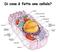 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O rappresentano il 96% della massa della cellula - Altri component frequenti
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare quattro legami covalenti. Questi
apitolo 3 Le biomolecole I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare quattro legami covalenti. Questi
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
LE PROTEINE: POLIMERI COSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOACIDI
 LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
LE PROTEINE: POLIMERI OSTITUITI DA 20 TIPI DI MONOMERI, I 20 AMINOAIDI OGNI PROTEINA PUO ESSERE FORMATA DA MOLTE DEINE O ENTINAIA DI AMINOAIDI E SI LEGANO A FORMARE UNA ATENA NON RAMIFIATA La catena di
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi. Possono assumere forme diverse a seconda della funzione
 Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Le proteine sono polimeri lineari costituiti da unità base formate da oltre 40 amminoacidi Hanno elevato PM Possono assumere forme diverse a seconda della funzione svolgono molteplici funzioni Tra le proteine
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
AMMINO ACIDI. L equilibrio è regolato dal ph
 AMMINO ACIDI AMMINO ACIDI Amminoacido: un composto difunzionale che contiene nell ambito della stessa molecola una funzione amminica -NH 2 e una funzione carbossilica -COOH α-ammino acido: I due gruppi
AMMINO ACIDI AMMINO ACIDI Amminoacido: un composto difunzionale che contiene nell ambito della stessa molecola una funzione amminica -NH 2 e una funzione carbossilica -COOH α-ammino acido: I due gruppi
04/10/17 I LEGAMI DEL CARBONIO. Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole
 04/10/17 I LEGAMI DEL CARBONIO TETRAEDRO se forma 4 legami semplici Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole SCHELETRO CARBONIOSO 1 04/10/17 Estrema
04/10/17 I LEGAMI DEL CARBONIO TETRAEDRO se forma 4 legami semplici Nei composti organici gli atomi di C sono uniti tra loro a formare lo scheletro delle molecole SCHELETRO CARBONIOSO 1 04/10/17 Estrema
Bagatti, Corradi, Desco, Ropa. Chimica. seconda edizione
 Bagatti, orradi, Desco, Ropa himica seconda edizione Bagatti, orradi, Desco, Ropa, himica seconda edizione apitolo 16. Molecole per la vita SEGUI LA MAPPA glicosidico distinguere tra peptidico Struttura
Bagatti, orradi, Desco, Ropa himica seconda edizione Bagatti, orradi, Desco, Ropa, himica seconda edizione apitolo 16. Molecole per la vita SEGUI LA MAPPA glicosidico distinguere tra peptidico Struttura
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
CARBOIDRATI SEMPLICI
 CARBOIDRATI Dal greco glucos =dolce Glucidi Zuccheri Sostanze formate acqua e carbonio Hanno forma molecolare (CH₂O)n 1 CARBOIDRATI SEMPLICI Monosaccaridi, una sola unità di poliidrossi aldeide o di poliidrossi
CARBOIDRATI Dal greco glucos =dolce Glucidi Zuccheri Sostanze formate acqua e carbonio Hanno forma molecolare (CH₂O)n 1 CARBOIDRATI SEMPLICI Monosaccaridi, una sola unità di poliidrossi aldeide o di poliidrossi
Di cosa è fatta una cellula?
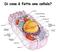 Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Di cosa è fatta una cellula? Composizione delle cellule - L acqua (H 2 O) rappresenta il 70% del massa della cellula - C,H,N,O,P,S rappresentano il 99% della massa della cellula - Altri elementi più rari
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
9) Scrivere un disaccaride formato dal β-d-galattosio e dall α-d-n-acetil-glucosammina legati da un legame glicosidico β(1-4).
 CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
Le molecole della vita
 Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
Le molecole della vita Introduzione: cose da sapere per capire. Gli atomi (es. carbonio, ossigeno, idrogeno) si uniscono a formare molecole Le molecole costituiscono tutta la materia che ci circonda Atomi
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
La chimica della vita
 La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
La chimica della vita La materia presente nell universo è formata da 92 elementi Gli elementi si legano tra loro per formare le molecole che costituiscono i composti Legame covalente O H H Molecola Composto
AMINOACIDI Struttura. Funzione. Classificazione. Proprietà
 AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
AMINOACIDI Struttura Funzione Classificazione Proprietà 1 STRUTTURA Composti caratterizzati dalla presenza di un gruppo aminico (NH 2 ) e di un gruppo acido (COOH) legati al medesimo carbonio (C). In soluzione
Percorsi di chimica organica - Soluzioni degli esercizi del testo
 ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
ercorsi di chimica organica - Soluzioni degli esercizi del testo AITL 14 1. Il prefisso α negli α-amminoacidi sta ad indicare che il gruppo amminico, - 2, si trova sul carbonio alfa (carbonio legato al
PROTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi
 POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
POTEINE dal greco al 1 posto costituiscono il 50% circa del peso secco della maggior parte degli organismi viventi composti quaternari (,, O, N) macromolecole organiche, molecole informazionali, polimeri
Formula generale di un amminoacido
 Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
Formula generale di un amminoacido Gruppo carbossilico Gruppo amminico Radicale variabile che caratterizza i singoli amminoacidi Le catene laterali R degli amminoacidi di distinguono in: Apolari o idrofobiche
 http://digilander.libero.it/glampis64 I composti organici di interesse biologico sono: Carboidrati Proteine Lipidi Acidi nucleici Le macromolecole sono composti di grandi dimensioni, unione di piccole
http://digilander.libero.it/glampis64 I composti organici di interesse biologico sono: Carboidrati Proteine Lipidi Acidi nucleici Le macromolecole sono composti di grandi dimensioni, unione di piccole
TUTORATO DI BIOLOGIA GENERALE PER BIOTECNOLOGIE ANNO 2018/2019
 TUTORATO DI BIOLOGIA GENERALE PER BIOTECNOLOGIE ANNO 2018/2019 TUTOR DEL CORSO: ALBERTO VICENZI E-mail: alberto.vicenzi@student.unife.it LE MACROMOLECOLE Le macromolecole biologiche più importanti sono:
TUTORATO DI BIOLOGIA GENERALE PER BIOTECNOLOGIE ANNO 2018/2019 TUTOR DEL CORSO: ALBERTO VICENZI E-mail: alberto.vicenzi@student.unife.it LE MACROMOLECOLE Le macromolecole biologiche più importanti sono:
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
α-amminoacidi O α O α R CH C O - NH 3 forma ionizzata sale interno (zwitterione) OH NH 2 forma non ionizzata (non esistente in realtà)
 Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Amminoacidi 2 forma non ionizzata (non esistente in realtà) 3 forma ionizzata sale interno (zwitterione) In soluzione acquosa c'è equilibrio tra tre forme 3 forma cationica p molto acidi 3 forma zwitterionica
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
CARBOIDRATI Sono aldeidi o chetoni con diversi gruppi ossidrilici (formula molecolare di base (CH2O)n, con n =>3) Funzioni riserva energetica
 CARBOIDRATI Sono aldeidi o chetoni con diversi gruppi ossidrilici (formula molecolare di base (CH2O)n, con n =>3) Funzioni riserva energetica combustibili intermedi metabolici Impalcatura del DNA e RNA
CARBOIDRATI Sono aldeidi o chetoni con diversi gruppi ossidrilici (formula molecolare di base (CH2O)n, con n =>3) Funzioni riserva energetica combustibili intermedi metabolici Impalcatura del DNA e RNA
H N H R N H R N R R N R H H H
 AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
Le proteine. Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico.
 Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Le proteine Sono polimeri di amminoacidi dispos$ in sequenza. Due amminoacidi si legano tra loro formando un legame pep-dico. Cur$s et al. Invito alla biologia.blu Zanichelli editore 2011 1 Struttura e
Università degli Studi di Ferrara Corso di laurea in Infermieristica Ostetricia A.A. 2016/17
 Università degli Studi di Ferrara Corso di laurea in Infermieristica Ostetricia A.A. 2016/17 Corso integrato di Basi molecolari e funzionali della vita Modulo di Biologia applicata (Prof. Paola Rizzo)
Università degli Studi di Ferrara Corso di laurea in Infermieristica Ostetricia A.A. 2016/17 Corso integrato di Basi molecolari e funzionali della vita Modulo di Biologia applicata (Prof. Paola Rizzo)
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
moli OH - /mole amminoacido
 ) ) Di seguito è riportata la curva di titolazione di un amminoacido. Osservando il grafico: a) stabilire il valore dei pka dell aminoacido b) calcolare il valore del pi e individuarlo sul grafico. c)
) ) Di seguito è riportata la curva di titolazione di un amminoacido. Osservando il grafico: a) stabilire il valore dei pka dell aminoacido b) calcolare il valore del pi e individuarlo sul grafico. c)
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Chimica generale e inorganica Studia gli elementi e i composti inorganici
 Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
BIOMOLECOLE. I mattoni delle cellule.
 BIMLECLE I mattoni delle cellule PRINCIPALI GRUPPI FUNZINALI I gruppi funzionali sono gruppi di atomi, uniti da legami covalenti, che conferiscono alla molecola di cui fanno parte un comportamento chimico
BIMLECLE I mattoni delle cellule PRINCIPALI GRUPPI FUNZINALI I gruppi funzionali sono gruppi di atomi, uniti da legami covalenti, che conferiscono alla molecola di cui fanno parte un comportamento chimico
Chimica generale e inorganica Studia gli elementi e i composti inorganici
 Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
Chimica generale e inorganica Studia gli elementi e i composti inorganici Chimica organica Studia i composti organici, cioè composti che contengono atomi di carbonio Biochimica È lo studio della chimica
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa.
 La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
La chimica della vita si basa sui composti del carbonio e dipende da reazioni chimiche che avvengono in soluzione acquosa. Le cellule contengono 4 famiglie principali di piccole molecole organiche: Amminoacidi
amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente
 Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Gli amminoacidi naturali sono α-amminoacidi : il gruppo amminico è legato all atomo di carbonio immediatamente adiacente al gruppo carbonilico e hanno la seguente formula generale: gruppo funzionale carbossilico
Indagine biologica: elevato livello di organizzazione delle strutture coinvolte.
 Indagine biologica: elevato livello di organizzazione delle strutture coinvolte. L organizzazione biologica si basa su una gerarchia di livelli strutturali Si parte dall atomo tessuti organi molecola organismo
Indagine biologica: elevato livello di organizzazione delle strutture coinvolte. L organizzazione biologica si basa su una gerarchia di livelli strutturali Si parte dall atomo tessuti organi molecola organismo
le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. STRUTTURA TERZIARIA
 STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( OO) nella stessa molecola 3 N 2 α * OO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-himica Organica 1 Amminoacidi
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
I PROTIDI ASPETTI GENERALI
 I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
I PROTIDI ASPETTI GENERALI I PROTIDI O PROTEINE SONO SOSTANZE ORGANICHE AZOTATE, DI STRUTTURA MOLTO COMPLESSA, PRESENTI IN OGNI FORMA DI VITA. LE PROTEINE SONO COMPOSTI QUATERNARI, OSSIA SONO FORMATE DA
Università degli Studi di Ferrara Corso di laurea in Infermieristica Ostetricia A.A. 2017/18
 Università degli Studi di Ferrara Corso di laurea in Infermieristica Ostetricia A.A. 2017/18 Corso integrato di Basi molecolari e funzionali della vita Modulo di Biologia applicata (Prof. Paola Rizzo)
Università degli Studi di Ferrara Corso di laurea in Infermieristica Ostetricia A.A. 2017/18 Corso integrato di Basi molecolari e funzionali della vita Modulo di Biologia applicata (Prof. Paola Rizzo)
Caratteristiche generali
 AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
AMMINOACIDI Gli amminoacidi sono le unità costruttive (building blocks) delle proteine. Come dice il termine, gli amminoacidi naturali sono costituiti da un gruppo amminico (-NH 2 ) e da un gruppo carbossilico
Esercitazione Esempi di domande del test intermedio
 Esercitazione Esempi di domande del test intermedio Materiale occorrente : Calcolatrice Penna Matita Righello Gomma Severamente vietato servirsi di libri, appunti, telefoni cellulari Quindi..!!!!! la legge
Esercitazione Esempi di domande del test intermedio Materiale occorrente : Calcolatrice Penna Matita Righello Gomma Severamente vietato servirsi di libri, appunti, telefoni cellulari Quindi..!!!!! la legge
Struttura degli Amminoacidi
 Amminoacidi Struttura degli Amminoacidi Amminoacido (o α-amminoacido): molecola che possiede un gruppo amminico primario (-NH 2 ) come sostituente dell atomo di carbonio α, e un gruppo carbossilico acido
Amminoacidi Struttura degli Amminoacidi Amminoacido (o α-amminoacido): molecola che possiede un gruppo amminico primario (-NH 2 ) come sostituente dell atomo di carbonio α, e un gruppo carbossilico acido
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
IN UN ATOMO SI DISTINGUE UN NUCLEO CARICO POSITIVAMENTE ATTORNO AL QUALE RUOTANO PARTICELLE CARICHE NEGATIVAMENTE: GLI ELETTRONI (e - ) (-)
 LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
LA VITA, LA CHIMICA E L ACQUA PER INIZIARE QUALCHE CENNO DI CHIMICA LA MATERIA E FATTA DI COMBINAZIONI DI ELEMENTI. GLI ELEMENTI SONO COMPOSTI DA SINGOLI ATOMI, LE PIU PICCOLE UNITA CHE MANTENGONO LE PROPRIETA
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente fondamenti di chimica indispensabili per lo studio della biologia Flavia Frabetti Tecnici di laboratorio 2010/2011 Cellula batterica PROTEINE (15%) 1 Composizione
Costituenti chimici della materia vivente fondamenti di chimica indispensabili per lo studio della biologia Flavia Frabetti Tecnici di laboratorio 2010/2011 Cellula batterica PROTEINE (15%) 1 Composizione
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH
 Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Nomenclatura AMIDI Alcol + alcol etere R-OH + R -OH R-O-R + H 2 O Aldeide + alcol emiacetale R-CHO + R -OH R-CHOH-O-R Acido + Acido anidride R-COOH + R -COOH R-CO-O-CO-R + H 2 O Alcol + Acido estere R-COOH
Proteine. Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana)
 Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
Proteine Enzimi Fattori di Trascrizione Proteine di Membrana (trasportatori, canale, recettori di membrana) Ormoni e Fattori di crescita Anticorpi Trasporto Trasporto (emoglobina, LDL, HDL.) Fenotipo Proteine
PROTIDI: LE PROTEINE E GLI AMMINOACIDI
 PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
PROTIDI: LE PROTEINE E GLI AMMINOACIDI GLI AMMINOACIDI Struttura generica di un amminoacido. R rappresenta un gruppo laterale specifico di ogni amminoacido. In chimica, gli amminoacidi (impropriamente
LE MACROMOLECOLE BIOLOGICHE
 LE MACROMOLECOLE BIOLOGICHE Proteine, lipidi, carboidrati ed acidi nucleici CORSO DI BIOLOGIA, PER OSTETRICIA LE MACROMOLECOLE BIOLOGICHE Poiché i fenomeni biologici sono il risultato delle specifiche
LE MACROMOLECOLE BIOLOGICHE Proteine, lipidi, carboidrati ed acidi nucleici CORSO DI BIOLOGIA, PER OSTETRICIA LE MACROMOLECOLE BIOLOGICHE Poiché i fenomeni biologici sono il risultato delle specifiche
CHIMICA BIOLOGICA. Seconda Università degli Studi di Napoli. DiSTABiF. Antimo Di Maro. Lezione 3. Corso di Laurea in Scienze Biologiche
 Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
Seconda Università degli Studi di Napoli DiSTABiF Corso di Laurea in Scienze Biologiche Insegnamento di CHIMICA BIOLOGICA Antimo Di Maro Anno Accademico 2016-2017 Lezione 3 GLI AMMINOACIDI PROTEICI Le
Lauree Triennali Professioni sanitarie: Corso comune di Biologia Applicata Dott.ssa Ilaria Bononi
 Lauree Triennali Professioni sanitarie: Corso comune di Biologia Applicata Dott.ssa Ilaria Bononi Corso Comune di Biologia Lauree Triennali Professioni Sanitarie 1 credito: 12 ore 1. Fisioterapia 2. Logopedia
Lauree Triennali Professioni sanitarie: Corso comune di Biologia Applicata Dott.ssa Ilaria Bononi Corso Comune di Biologia Lauree Triennali Professioni Sanitarie 1 credito: 12 ore 1. Fisioterapia 2. Logopedia
I composti organici e i loro polimeri
 I ARBIDRATI I composti organici e i loro polimeri La diversità molecolare della vita è basata sulle proprietà del ARBNI. Un atomo di carbonio può formare quattro legami covalenti. Questi legami gli permettono
I ARBIDRATI I composti organici e i loro polimeri La diversità molecolare della vita è basata sulle proprietà del ARBNI. Un atomo di carbonio può formare quattro legami covalenti. Questi legami gli permettono
Lauree Triennali Professioni sanitarie: Corso comune di Biologia Applicata Dott.ssa Ilaria Bononi
 Lauree Triennali Professioni sanitarie: Corso comune di Biologia Applicata Dott.ssa Ilaria Bononi Corso Comune di Biologia Lauree Triennali Professioni Sanitarie 1 credito: 12 ore 1. Fisioterapia 2. Logopedia
Lauree Triennali Professioni sanitarie: Corso comune di Biologia Applicata Dott.ssa Ilaria Bononi Corso Comune di Biologia Lauree Triennali Professioni Sanitarie 1 credito: 12 ore 1. Fisioterapia 2. Logopedia
10/12/2018. » I più importanti gruppi funzionali sono:
 » La maggior parte delle biomolecole organiche viene suddivisa in classi in base a specifici raggruppamenti atomici da esse posseduti e che conferiscono loro specifiche proprietà chimiche, sono i cosiddetti
» La maggior parte delle biomolecole organiche viene suddivisa in classi in base a specifici raggruppamenti atomici da esse posseduti e che conferiscono loro specifiche proprietà chimiche, sono i cosiddetti
I composti organici. Il carbonio e i composti organici
 I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
SOLUZIONI DEGLI ESERCIZI AGGIUNTIVI DI FINE CAPITOLO
 Phelan, Pignocchino Le scienze naturali Osservare i viventi SOLUZON DEGL ESERCZ AGGUNTV D FNE CAPTOLO Capitolo 2 L DENTTÀ DEGL ATOM 1. 2n 2 2. F = k Q 1 x Q 2 /d 2 3. F = forza in Newton k = costante di
Phelan, Pignocchino Le scienze naturali Osservare i viventi SOLUZON DEGL ESERCZ AGGUNTV D FNE CAPTOLO Capitolo 2 L DENTTÀ DEGL ATOM 1. 2n 2 2. F = k Q 1 x Q 2 /d 2 3. F = forza in Newton k = costante di
Biochimica. studio della vita a livello molecolare
 Biochimica studio della vita a livello molecolare studio della composizione molecolare dei sistemi viventi studio delle reazioni chimiche cui vanno incontro i sistemi viventi ALCUNI QUESITI DELLA BIOCHIMICA
Biochimica studio della vita a livello molecolare studio della composizione molecolare dei sistemi viventi studio delle reazioni chimiche cui vanno incontro i sistemi viventi ALCUNI QUESITI DELLA BIOCHIMICA
