VOLUME 2 - MODULO C UNITÀ DIDATTICA C1 SOLUZIONE DEL PROBLEMA INIZIALE
|
|
|
- Evangelina Nobile
- 7 anni fa
- Visualizzazioni
Transcript
1 Vol_C.doc VOLUME - MODULO C UNITÀ DIDATTICA C SOLUZIONI DELLE VERIFICHE DEI PREREQUISITI. Il eso volumico o eso secifico è ari al rodotto della massa volumica er l accelerazione di gravità. Pertanto si ha: γ ρ g 0 9,8 950 N/m. Ricordando che un litro è ari ad un decimetro cubo, risulta immediato calcolare la ortata massica; essa vale Q ρ V 0,640 /dm 0 l/s 6,4 /s.. b) d) 4. Vero 5. a) 4 Cl + Na S O + 0 NaOH Na SO NaCl + 5 H O b) Cu + 8 HNO Cu(NO ) + NO + 4 H O 6. b) 7. Sono combustibili fossili in quanto derivano da esseri viventi quali foreste e iccoli animali viventi nei bassofondali marini; entrambi srofondarono nel sottosuolo e furono sottoosti a lenta trasformazione er centinaia di milioni di anni. 8. a) CO; b) HNO ; c) SO ; d) NH 9. Le emissioni di CO in atmosfera dovute alle attività dell uomo causano un aumento dell effetto serra che consiste nel riscaldamento del ianeta in quanto gli strati di CO aumentano la riflessione delle onde termiche verso il suolo. SOLUZIONE DEL PROBLEMA INIZIALE Per il calcolo della quantità di calore Q che deve essere fornita alle barre occorre conoscere darima la massa totale m del lotto di barre. Si calcola l area e la massa di una singola barra, assumendo come unità di misura di riferimento il decimetro: π π A d 0,,46 0 dm 4 4 m ρ A l,7, , Consultando l aosita tabella si ricava la caacità termica massica dell alluminio c Al che vale 0,9 /( K). Alicando la formula che definisce la caacità termica si trova il calore necessario er riscaldare una singola barra: Q m c Al T 5, 0, Il calore necessario er scaldare il lotto di 50 barre vale: Q Prendendo in considerazione il rendimento del forno si ricava il calore totale Q tot: anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA DI 0
2 Vol_C.doc Q 5950 Q tot 7500 η 0,7 La seconda domanda chiede di valutare l allungamento subito dalla singola barra al termine del riscaldamento. Occorre ricavare dall aosita tabella il coefficiente di dilatazione lineare dell alluminio: esso vale λ / C. La formula dell allungamento lineare l dei cori sottoosti ad una variazione di temeratura t è la seguente: 6 l λ l t 4 0 0, , 44 mm Il otere calorifico inferiore del carbone in base alla sua comosizione viene valutato mediante la formula di Dulong. O P CI 8 C H S 5 U 8 Inserendo i dati relativi alla comosizione del carbone si ha: 0,078 P CI 8 0, , ,04 5 0, Per il calcolo della massa di carbone necessaria er il riscaldamento delle barre bisogna dividere il calore totale Q tot recedentemente trovato er il otere calorifico inferiore P CI del carbone: Q m P tot CI In alternativa al carbone, il testo roone l uso di un gas, del quale sono noti comosizione e otere calorifico. Per valutare la massa di gas necessaria si alica di nuovo la formula recedente: 7 m Q P tot CI 7500, Con la quinta domanda si calcolano le risettive quantità di aria necessarie er la combustione, servendosi delle aosite formule, quella er il carbone e quella er il gas. Per il carbone: 7,8 di aria A tm 0, ,44 4,4 + 0,04,4 0, 9 8 di carbne Per il gas: 4 6 A tv 0,08 ( 8 + ) + 0, ,0476 +, , , Si iotizza che il carbone sia bruciato allo stato finemente overizzato. In tal caso il valore di aria in eccesso er il carbone vale e 0,. Si calcolino le due quantità di aria effettivamente imiegata nelle risettive combustioni. Per il carbone: di aria di gas A e ( + 0,) 0,9, 08 Per il gas si assume e 0,. Mediante la medesima formula si trova che: A e ( + 0,) 4,855 5, 4 anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA DI 0
3 Vol_C.doc SOLUZIONI DEI PROBLEMI DI RIEPILOGO. La formula che ermette di convertire una temeratura in [ F] esrimendola in [ C] è la seguente:. Per risolvere il quesito si richiami il concetto di caacità termica massica esresso dalla formula seguente, nella quale si inserisce la costante del calcestruzzo, ricavata da tabella:. La caacità termica massica er l acqua è esressa in forma di tabella, in funzione della temeratura. Da essa si estraggono i valori necessari. Nel rimo caso: Nel secondo caso: I due valori risultano molto rossimi. 5 5 t F ( t ) ( 0 ) C C Q c m t 0, Q ,80 /( C) 860. Q ,08 /( C) La Btu (British termal unit) è l unità di misura dell energia termica utilizzata dalle norme anglosassoni. L equivalenza tra Btu e joule è la seguente: Btu, Nel nostro caso: , Btu, Il coefficiente di dilatazione termica er il mattone in argilla è riortato nell aosita tabella e vale λ / C. L allungamento l è dato dalla seguente formula: 6 l λ l t , 05 mm 6. La temeratura finale t viene calcolata attraverso l uguaglianza tra i calori Q e Q scambiati dalle due masse. I suddetti calori Q sono valutati con la seguente formula Q c m t. Si noti come, avendo imosto l uguaglianza tra i calori Q e Q scambiati dalle due masse, la caacità termica c è una costante che viene facilmente semlificata: ( m + m ) t c m t + c m t c m t + m t t 64 C m + m anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA DI 0
4 Vol_C.doc 7. Come rima cosa, occorre orre in evidenza il otere calorifico inferiore del GPL, esrimendolo in [/]. Esso vale /. Il calore liberato dalla combustione è ari al rodotto tra il otere calorifico e la massa bruciata che vale m 5, er il rendimento: Q (P CI m)/ η / 5 0, Per calcolare la massa comlessiva di antracite, occorre eseguire un bilancio di energia termica tra il calore assorbito dall acqua e il calore liberato dalla combustione; esso è esresso come segue, con a rimo membro il calore liberato dal carbone e a secondo quello assorbito dall acqua: m m P mh O c t 800 4,844 0,666 η P 0,6 500 CI CI η m H O c t Come valore er la caacità termica massica c dell acqua si è scelta la media fra i valori citati nella tabella resente sul testo, er le temerature di inizio e fine trasformazione. 9. La formula di Dulong ermette di calcolare il otere calorifico inferiore er il carbone la cui comosizione è descritta nel testo. La formula è la seguente: O P CI 8 C H S 5 U 8 Inseriamo i dati secifici del tio di carbone in oggetto: 0,08 P CI 8 0, , , 5 0, Il valore del otere calorifico sueriore uò essere ottenuto a artire dal otere calorifico inferiore esresso in [M], grazie alla seguente formula: ( U + 8,94H ),5( 0,08 + 8,94 0,04),5 PCS PCI +,6 +, M 0. La formula di Dulong è valida anche er i combustibili liquidi, quale aunto il kerosene. La formula è la seguente: O P CI 8 C H S 5 U 8 Inseriamo i dati secifici del kerosene: 0,06 P CI 8 0, , , Come controllo si uò eseguire il confronto tra il valore trovato e quello riortato nella tabella sul testo in cui comaiono le caratteristiche rinciali dei combustibili iù diffusi. Il valore trovato col calcolo è solo lievemente sueriore al valore del P CI del gasolio assunto come riferimento.. Si alica la formula che esrime il fabbisogno di aria er la combustione di un combustibile gassoso anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 4 DI 0
5 Vol_C.doc mi Atv 0,08( CO + H ) + 0,095 CH 4 + 0,0476 ni + Cni H mi 0, 0476 O i 4 Inseriamo i dati secifici del gas: 8 A tv 0, , , , ,57 + 5, ( ) + +,904 0, 7,95 m La formula ci dice che er la combustione di ogni m del gas in esame occorre un volume A tv 7,95 m di aria. SOLUZIONI AI QUESITI DI AUTOVERIFICA ALL APPRENDIMENTO Le risoste contengono i concetti chiave e sono fornite in forma di schema.. La temeratura misura lo stato di agitazione molecolare; non è un energia ma uò essere considerata come una misura indiretta dell energia. Il calore è una delle forme in cui si resenta l energia. La variazione di temeratura è roorzionale al raorto fra il calore fornito e la caacità termica.. zero assoluto; 7 K.. d) 4. Falso 5. l λ l t 6. La combustione è un insieme di reazioni chimiche di ossidazione tra una sostanza combustibile e l ossigeno contenuto nell aria avente funzione di comburente. 7. a) d) 8. Falso 9. roagazione assai veloce aumento.dei gas rodotti. 0. a) concentrazioni dei comonenti; b) temeratura dell ambiente; c) forma della camera di combustione.. a) azoto b) ossigeno. Vero. Una miscela di combustibile e comburente è detta stechiometrica se la comosizione in massa è tale da dar luogo alla combustione comleta, ovvero senza eccessi di una sostanza risetto all altra; un eccesso di combustibile risetto al comburente genera sostanze incombuste, un eccesso di comburente dà luogo alla resenza di comburente inutilizzato nei fumi. 4. a) 5. evaorazione; vaore acqueo. 6. Il Potere calorifico è definito come la quantità di calore emesso da un di combustibile, in seguito alla sua combustione comleta. Dimensionalmente è esresso come segue: [ ] P CI [ ] [ ] 7. a) 8. risetto all aria teorica.teorica. 9. a) b) 0. a) ovuli; b) mattonelle; c) granelle.. d). a) benzina; b) gasolio; c) kerosene.. Russia, Olanda, Algeria; gasdotti; bombole. 4. a) 5. Si definisce temeratura di ignizione la temeratura minima che un combustibile deve raggiungere, in resenza del comburente, affinché la reazione ossa comunicarsi a tutta la massa in modo sontaneo ed in breve temo. anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 5 DI 0
6 Vol_C.doc 6. Falso 7. minima; sontaneamente; scintille d innesco. 8. a) 9. Un elevato valore nel calore latente di evaorazione di un combustibile causa un forte raffreddamento interno della camera di combustione che, sorattutto nel caso di avviamento a freddo, uò inibire la combustione. 0. d). resistenza al moto.. er imedire usi fraudolenti essendo sottoosti a differenti regimi fiscali. UNITÀ DIDATTICA C SOLUZIONI DELLE VERIFICHE DEI PREREQUISITI. La formula che ermette di convertire una temeratura in [ C] esrimendola in [ F] è la seguente: Inserendo nella formula il valore di t C si trova t 9/5 + 89,6 F..,0 bar; 0 C.. La formula da usare è quella che lega il calore scambiato con la variazione di temeratura subita dal coro: 4. b) c) 5. Vero t 5 9 C F ( t ) Q m c t 600 4, La formula da usare è quella che lega il calore liberato in seguito alla combustione col otere calorifico inferiore del combustibile: Q η m P CI 0, / M 7. b) c) 8. Si definisce Potere Calorifico Inferiore P CI di un combustibile la quantità di calore rodotta dall unità di massa, o di volume se gassoso, in seguito alla sua combustione comleta; il P CI non comrende il calore di evaorazione contenuto dal vaore acqueo che è resente fra i rodotti della combustione. 9. a) gasolio; b) benzina; c) catrame; d) kerosene. 0. temeratura di ignizione. anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 6 DI 0
7 Vol_C.doc SOLUZIONE DEL PROBLEMA INIZIALE Il sistema resenta una massa di gas racchiusa in un contenitore tenuto taato da una massa m. Per conoscere la ressione relativa quindi manometrica - esercitata dal gas occorre er rima cosa calcolare la sezione A dello stantuffo su cui agisce la ressione del gas: π π A d 58 64mm 4 4 La ressione manometrica è dovuta esclusivamente all azione del eso gravante sulla sezione A, con l esclusione della ressione atmosferica. m g 8 9, Pa, 0967 bar 6 A 64 0 Per conoscere la massa ed il numero di moli di Ne conviene darima disorre dei seguenti dati: la ressione assoluta che vale ass,0 +,0967,0567 bar il volume del contenitore cilindrico nella configurazione iniziale (n ): V A h ,6 mm la costante universale R 84 /(kmole K) la massa molecolare µ del Ne, letto da tabella, ari a 0,8 /kmole Mediante l equazione di stato dei gas erfetti, nella formulazione in cui comaiono il volume occuato dal gas e la costante universale dei gas, si calcola direttamente il numero n di moli: V R T 5 9 ass, ,6 0 6 n 5, ( 7 + 9) La massa di gas è ricavabile moltilicando il numero di moli n er la massa molecolare µ del gas: 5 5 m n µ,56 0 0,8 0,95 0 0, g kmoli Nella seconda arte del roblema si è rovveduto a modificare sia la zavorra remente, sia la temeratura del gas. La nuova ressione calcolata come nel caso recedente ma con la nuova zavorra di massa m ora vale: m g 9, Pa 0, 854 bar 6 A 64 0 La ressione 0,854 bar così trovata è una ressione relativa, ovvero manometrica; la ressione assoluta è,ass,867 bar, avendo sommato il valore della ressione atmosferica, ari a circa,0 bar. Successivamente, mediante l equazione di stato dei gas nella formulazione recedentemente usata, si calcola il nuovo volume V, noto il numero n di moli, rimasto costante nel corso della trasformazione: 6 n R T 5, V 00, m Ricordando che il volume massico è ari al raorto tra volume e massa contenuta, si trova v : 6 V 00,8 0 v 0, 68 5 m 0,95 0 m anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 7 DI 0
8 Vol_C.doc La nuova altezza h raggiunta dallo stantuffo è ari al raorto tra volume V e sezione A: 6 V 00,8 0 h 0, 076 m 6 A 64 0 La nuova altezza h raggiunta dallo stantuffo vale dunque 76 mm. Vale la ena di soffermarsi brevemente sul fatto che la trasformazione resenta effetti contrastanti: da una arte la riduzione di ressione a causa dell alleggerimento della zavorra, il cui effetto è l esansione del volume occuato dal fluido; dall altra la riduzione della temeratura che induce nel gas il fenomeno oosto. Le formule della termodinamica da noi adottate hanno consentito di sovraorre entrambi gli effetti, anche se contrastanti: nel comlesso: osservando la quota finale h si nota che il livello del istone è otuto salire. SOLUZIONI DEI PROBLEMI DI RIEPILOGO. Calcolo della massa molecolare dell N O 5: µ 8 +,5 5,5 /kmole Si calcola il numero di moli di gas dividendo la massa er la massa molecolare: n m/µ 55/5,5 0 moli.. I risultati ottenuti saranno diversi, dato che il riscaldamento è iotizzato in due trasformazioni diverse. Si imiega la formula che lega calore, caacità termica massica e variazione di temeratura, riferita alla massa unitaria di gas. Si inserisce nella formula darima la caacità termica a ressione costante: Q c t 0, / Poi si riete la formula inserendo la caacità termica a volume costante: Q c v t 0,7 0 7,4 / Questo secondo caso ha evidenziato un fabbisogno di calore minore, dato che la trasformazione isovolumica non revede variazioni di volume er cui il gas è imossibilitato a svolgere lavoro di esansione.. Primo caso, comressione isoterma: T T 9 K; alicando l equazione di stato dei gas erfetti nella sua formulazione di base si trovano i volumi massici iniziale e finale v e v : R T 0 9 m v 0, R T 0 9 m v 0, Il secondo caso revede la comressione isovolumica, ovvero con volume costante. Dato che le condizioni di artenza sono le medesime del caso recedente, si conferma il valore del volume massico già calcolato. Pertanto si ha che v v 0,8 m /. Alicando nuovamente l equazione di stato dei gas erfetti, stavolta onendo in evidenza la temeratura finale T, si ha che: 5 v 0 0,8 T 879, K R 0 anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 8 DI 0
9 Vol_C.doc 4. Per trovare il volume del gas a zero gradi si alica la rima legge di Gay-Lussac, onendo in evidenza il volume V 0 alla temeratura di 0 C: 5 V 0 V, 94 m + α t Per trovare la ressione assoluta si alica l equazione di stato dei gas erfetti: ( 7+ 0) RT Pa 46, 64 kpa v,5 6. Dalla formula seguente, che one in relazione la costante del singolo gas con la costante universale dei gas, è ossibile risalire alla massa molecolare media µ della miscela. R 84 µ 84 R 98,95 kmole 7. Si richiama l equazione fondamentale dei gas, nella formulazione in cui comaiono la massa m e il volume V, onendo in evidenza la temeratura T: 6 T V K mr 0, La formula che descrive la trasformazione adiabatica fra i unti e è la seguente: Si onga in evidenza il volume massico finale v : k k v v k,0 0,5 0,769 v v,4,4 0,486 0, 70,5 m 9. Il Primo Princiio della Termodinamica afferma che Q U + L Inseriamo i valori numerici, con l avvertenza di far recedere il calore Q dal segno meno, dato che si tratta di un energia sottratta, osta a rimo membro. Anche il lavoro L deve essere receduto dal segno meno, dato che si tratta di un energia assorbita dall esterno, ma osta a secondo membro. -0 U -00 anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 9 DI 0
10 Vol_C.doc La variazione di energia interna vale U - 0. Da questo numero si deduce che il bilancio energetico della trasformazione è negativo, in quanto il gas deve attingere al rorio atrimonio energetico interno er realizzare la trasformazione in modo comleto. 0. Il lavoro unitario erogato da un gas nel corso di una trasformazione isobara è: L (v f v i); moltilicando il secondo membro er la massa m si ha il lavoro totale L tot. Inserendo i valori numerici si ha che: L tot m (v f v i), (0,8 0,56) ,46 Il risultato è esresso da un numero negativo: ciò è dovuto al fatto che, avendo realizzato una contrazione del volume, il gas subisce un azione roveniente dall ambiente, ad esemio, mediante una sottrazione di calore in uno scambiatore.. Il volume finale si calcola mediante la formula dell isoterma: V V cost Si metta in evidenza il volume finale V : V 6 8 dm Il lavoro unitario è dato dalla V 48 6 L RT ln ln , 7 SOLUZIONI AI QUESITI DI AUTOVERIFICA ALL APPRENDIMENTO Le risoste contengono i concetti chiave e sono fornite in forma di schema.. b). Una definita quantità di materia geometricamente determinata contenuta all interno di una suerficie chiusa.. una mole di gas normali. 4. a) 5. Falso 6. Clausius - coro freddo coro caldo lavoro esterno. 7. a) le molecole sono iotizzate di forma sferica; b) i loro movimenti sono casuali, gli urti elastici; c) le forze di interazione reciroca sono trascurabili. 8. b) c) 9. Vero 0. fisico finale rossimo fisico iniziale.. a) resta costante; b) vale zero; c) è raresentato dalla formula Q c v t.. Vero. Nel diagramma (,v) l isobara ha la forma di segmento orizzontale. L area sottesa che raresenta il lavoro unitario del gas ha rorio la forma di rettangolo avente er base la differenza dei volumi massici e er altezze la ressione. 4. d) 5. temeratura, esressa in [ C]; coefficiente termico di dilatazione volumetrica er i gas. anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 0 DI 0
11 Vol_C.doc 6. a) b) 7. Ponendo in evidenza la costante del gas R dall equazione di stato dei gas erfetti v RT, si ha: N m m [ ] [ Nm] [ ] R K K K [ ] [ ] [ ] [ ] 8. massa molare µ; la costante R. 9. b) c) 0. a) variazione di calore Q; b) lavoro scambiato L; c) variazione di energia interna U.. a). unti iniziale e finale; cammino.. il lavoro di un ciclo è la somma algebrica dei lavori arziali scambiati dal gas lungo le trasformazioni che formano il ciclo. 4. Vero anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA DI 0
12 Vol_C.doc UNITÀ DIDATTICA C SOLUZIONI DELLE VERIFICHE DEI PREREQUISITI. Si alica l equazione di stato dei gas erfetti onendo a rimo membro il volume massico: v RT ( 7 + 5) 58 0, 08 6,8 0 m. adiabatico; costante di Poisson.. Si calcola darima il volume massico iniziale v mediante la legge fondamentale dei gas: v RT ( 7 5) Ora si alica la formula della trasformazione isoterma: 87 m 0, ,8 0 v v cost 4. a) Si metta in evidenza la ressione assoluta finale : v 0,9645 0,8, 6 bar v 0,48 5. Vero 6. a) nel corso della trasformazione isoterma il gas non trattiene er sè nessuna quantità di calore, se non quanto basta er mantenere invariata la temeratura: allora c ; b) in una trasformazione isovolumica si ha che c c v; c) in una trasformazione isobara si ha che c c ; d) in una trasformazione adiabatica non si effettua nessuno scambio di calore er cui c 0 7. In un sistema termodinamico che scambia energia con l esterno, la somma algebrica dei calori, dei lavori e dell energia interna risulta ari a zero. 8. a) V V 0 ( + α t); b) 0 ( + α t). 9. Esiste una formula che esrime il lavoro unitario scambiato da un gas nel corso di una trasformazione adiabatica, di comressione come ure di esansione; er una corretta gestione della formula, si attribuisce al gas il edice nella condizione di inizio trasformazione, il edice alla conclusione: anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA DI 0
13 Vol_C.doc k R T k L 87 9,7 k, ,86,4,4 07 0,857 [ (,7) ] 07[ 0,455] 0. Vero. SOLUZIONE DEL PROBLEMA INIZIALE Del ciclo di Lenoir roosto sono note le ressioni dei tre unti e la temeratura iniziale. Dall aosita tabella resente sul testo si assumono i valori delle costanti caratteristiche del gas: c 5, /( K); c v,4 /( K); R,08 /( K); k,67. Utilizzando le leggi dei gas si calcolano i valori mancanti di v e T. Alicando l equazione di Claeyron si trova il valore del volume massico v v : R T v 5, Alicando la formula dell adiabatica ideale, con in evidenza il volume massico, si trova il valore del volume massico v : 0,5988 v v 5,678 8, 6 m k Alicando nuovamente l equazione fondamentale si trovano i valori delle temerature T e T : 5 v 0 5,678 T 546 R v 0 8,6 T 4, 5 R 080 Nella trasformazione - isovolumica il lavoro è nullo mentre il calore scambiato vale: m Q cv T 40 ( 546 7) , Nella trasformazione - adiabatica il calore scambiato è nullo mentre il lavoro unitario vale: L cv T 40 ( 4,5 546) , 05 Nella trasformazione - isobara il lavoro unitario ed il calore esulso valgono: 5 L v 0 ( 5,678 8,6) 900 9, Q c T 5 ( 7 4,5) , Per ottenere i valori dei lavori e dei calori totali è sufficiente moltilicare i valori unitari sin qui trovati, er la massa m,5. K K anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA DI 0
14 Vol_C.doc Il rendimento del ciclo è esresso dalla formula riferita agli scambi di calore: Q Q η Q 0 857, 75, 0,4 4, % 857, Il valore è decisamente basso a causa della iccola escursione fra le temeratura iniziale e quella massima a fine introduzione del calore Q. Infatti, dall analisi del ciclo di Carnot si è areso che il rendimento in generale cresce quanto iù è alta la temeratura T relativa all introduzione di calore, ovvero, nelle alicazioni reali, alla temeratura della combustione. Si comila la seguente tabella riassuntiva er ressioni, volumi massici e temerature, riferiti ai unti che definiscono il ciclo: Punto [bar] Grandezza fisica v [m /] T [K] 5, , ,6 4,5 Segue una seconda tabella riassuntiva er lavori e calori, riferiti alle tre trasformazioni: Trasformazione Grandezza fisica L [/] L [] Q [/] Q [], , 000, 46,05 456, 0 0, -9, -0,7-75, -57,8 Le variazioni di entroia delle tre trasformazioni si calcolano nell ordine mediante le aosite formule, ricordando in articolare come la variazione di entroia nel corso dell esansione adiabatica risulti evidentemente nulla: S, cv ln 40 ln 76 v 5,678 S, c ln 5 ln 7 v 8,6 K K La somma algebrica dei due valori così ottenuti dà zero, con ottima arossimazione di calcolo, come deve essere er ogni ciclo chiuso in ottemeranza a quanto revisto er via teorica. Nella figura di seguito riortata si è tracciato il diagramma (T,S) riortando i valori dei unti e e onendo il unto iniziale, assunto come riferimento, sull asse delle ordinate er ragioni di comodità. Per disegnare l isovolumica - con sufficiente arossimazione ci si serve di due unti intermedi, scelti a sentimento a ressioni grosso modo intermedie fra e ; essi sono:,4 bar e,7 bar. Per questi unti ausiliari si calcolano le risettive temerature e le variazioni di entroia mediante le formule consuete. Per calcolare le due temerature ci si riferisce alla legge fondamentale dei gas, comilata er i unti,, : anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 4 DI 0
15 Vol_C.doc v RT v RT v RT Ponendo la seconda delle tre leggi fondamentali a raorto con la rima si ha:,4 T T 7 8 K Ponendo ora la terza delle tre leggi fondamentali a raorto con la rima si ha:,7 T T K Ora si assa al calcolo delle variazioni di entroia, avendo reso il unto come riferimento. La formula è la stessa recedentemente utilizzata er la trasformazione isovolumica:,4 S, cv ln 40 ln 056,7 S, cv ln 40 ln 666 K K Anche er disegnare l isobara nel iano (T,S) ci si serve di due unti intermedi scelti a volumi massici circa intermedi, v 7,5 m / e v 6,5 m /. Anche er questi unti ausiliari si calcolano le risettive temerature e le variazioni di entroia mediante le formule consuete. Per calcolare le due temerature ci si riferisce alla legge fondamentale dei gas, comilata er i unti,, : v RT v RT v RT Ponendo la seconda delle tre leggi fondamentali a raorto con la rima si ha: v 6,5 T T 7, 5 K v 5,678 Ponendo ora la terza delle tre leggi fondamentali a raorto con la rima si ha: v 7,5 T T 7 60, 6 K v 5,678 Ora si assa al calcolo delle variazioni di entroia, avendo reso il unto come riferimento. La formula è la stessa recedentemente utilizzata er la trasformazione isobara: v 7,5 S, c ln 5 ln 456 v 5,678 v 6,5 S, c ln 5 ln 707, 4 v 5,678 K K anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 5 DI 0
16 Vol_C.doc Le due differenze di entroia er la comressione isobara risultano ositive in quanto valutate come variazioni orientate da sinistra a destra. In alternativa, è ossibile calcolare le due variazioni di entroia rendendo come riferimento il unto. In tal caso le due variazioni di entroia, stavolta valutate da destra a sinistra, quindi col segno negativo, valgono S, - 76 /( K) e S, /( K). Come verifica, si ossono sommare due variazioni consecutive, ad esemio la variazione di entroia da a con quella da a, er controllare che la somma aritmetica (non algebrica, erché su grafico esse corrisondono a distanze quotate) sia ari alla variazione comlessiva S, 7 /( K) recedentemente calcolata. Si ottengono i seguenti risultati: La verifica ha dato esito amiamente ositivo. S, S, + S, 707, , 4 K Diagramma del ciclo di Lenoir sul iano (T,S). SOLUZIONI DEI PROBLEMI DI RIEPILOGO. Note le temerature T e T 0 è immediato ricavare il rendimento del ciclo di Carnot: η C L Q Q Q 0 T T , Si risale al calore Q 0 scaricato nel corso della comressione isoterma inserendo nella formula del rendimento, recedentemente usata, il valore del rendimento aena trovato: Q Q ηc; Q0 Q ( ηc ) 770 ( 0,678) 48 0 Per il Primo Princiio della Termodinamica alicato al ciclo di Carnot, si ha che: L Q Q Si noti come nella formula non comaia la variazione U dell energia interna, essendo il ciclo di tio chiuso.. Noti il rendimento del ciclo di Carnot e la temeratura iniziale T, si ricava immediatamente la temeratura T 0: ( ) 600( 0,58) K T T ηc 5 0 Noti il rendimento ed il lavoro erogato, si ricava il calore unitario introdotto Q : L Q η 500 0,58 c 86 Per il Primo Princiio della Termodinamica alicato al ciclo chiuso di Carnot, si ha che: anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 6 DI 0
17 Vol_C.doc Q Q L Si alica la formula che consente di ottenere l efficienza ε note le temerature dell ambiente esterno e quella generata all interno della macchina frigorifera: T ε T T ( 7 + 0) ( 7 4) 5,89 4. Occorre darima calcolare i volumi massici e la temeratura finale; grazie all equazione di stato dei gas erfetti si calcola il volume massico v : RT m v 0, ,96 0 Alicando tra i unti e la formula dell adiabatica v k cost si ottiene il volume massico v : k,40 0,96 0,748 m v v 0,08 0,08 0,6 0, 075,6 Con l equazione di stato dei gas erfetti si calcola la temeratura T : 6 v,6 0 0,075 T 46, 8K R 60 Con questi valori si uò alicare la formula dell entroia er una generica trasformazione; si noterà che il risultato è rorio zero, come affermato teoricamente: S c v T v ln + R ln T v 5. L equazione di stato dei gas erfetti ermette di calcolare con ochi assaggi la temeratura finale T. Scrivendo l equazione er i unti e si ha che v v RT RT Ricordando che v v essendo la trasformazione di tio isovolumico, doo aver osto in evidenza i volumi massici è ossibile scrivere la seguente uguaglianza: Infine: RT RT 6 0 T T 00 6K 6,8 0 Poi er la formula secifica er il calcolo della variazione di entroia nel caso di una trasformazione isocora, si ha: T 6 S cv ln 0,670 ln 0, 94 T 00 K anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 7 DI 0
18 Vol_C.doc 6. La formula secifica er il calcolo della variazione di entroia nel caso di una trasformazione isoterma afferma che: S Rln 0,50 ln, 0,5 K 7. La formula secifica er il calcolo della variazione di entroia nel caso di una trasformazione isobara afferma che: T 440 S c ln 0,50 ln 0, 86 T 7 K 8. Occorre darima calcolare i volumi massici iniziale e finale e la temeratura finale. Grazie all equazione di stato dei gas erfetti si calcola il volume massico v : RT v 0, ,85 0 Alicando tra i unti e la formula della olitroica v m cost si ottiene il volume massico v : m m,9,85 0,56 m v v 0,4454 0,4454 0,5 0, 49 4,8 Con l equazione di stato dei gas erfetti si calcola la temeratura finale T : 6 v,48 0 0,49 T 07, K R 06 Ora si uò alicare la formula dell entroia er una generica trasformazione: T v S cv ln + R ln 0,09 0,544 8,87 0 /( K) 8,87 /( T v K ) 9. Dalla formula del rendimento del ciclo di Carnot T η 0 T si uò risalire alla temeratura T di ingresso del calore nel corso dell isoterma sueriore. Infatti, inserendo i valori numerici del rendimento e della temeratura T 0 in [K] del calore Q 0 scaricato, rimane come unica incognita la temeratura T : 58 0,68 T 50 T 9 K 0,68 La variazione di temeratura T è ari alla differenza fra le due temerature: T T T K anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 8 DI 0
19 Vol_C.doc Il ciclo di Carnot si resenta nel diagramma (T,S) in forma di rettangolo, avente er base la variazione di entroia S e er altezza la variazione di temeratura T. Dividendo l area del rettangolo (Q - Q 0) er l altezza (T) si trova la base: In altri termini, si è alicata la definizione di entroia. Q Q Q0 805 S 5 T T 76 K 0. Si alica la formula generale che lega l entalia con la caacità termica a ressione costante e con la variazione di temeratura: h c T 00 ( 90 8) 686 6, 86. Occorre darima calcolare i volumi massici iniziale v e finale v. RT v 0, 04 6,7 0 Alicando tra i unti e la formula dell adiabatica v k cost si ottiene il volume massico v : m k,9 7 0,775 m v v 0,04 0,04 7 0, 54 Con l equazione di stato dei gas erfetti si calcola la temeratura finale T : Quindi la variazione di entalia viene esressa come 5 v 0 0,54 T 85, 7 K R 89 ( ,7) h c T , 6 SOLUZIONI AI QUESITI DI AUTOVERIFICA ALL APPRENDIMENTO Le risoste contengono i concetti chiave e sono fornite in forma di schema.. Le trasformazioni irreversibili sono rocessi in base ai quali il sistema non uò tornare allo stato iniziale senza rodurre modificazioni nell ambiente esterno. Arendo il rubinetto della bombola il gas esande e si diffonde nell aria in modo sontaneo: l oerazione inversa non uò avvenire sontaneamente. Infatti, l oerazione inversa uò avvenire solo in seguito ad un rocesso industriale di filtraggio, comressione e omaggio che richiede un aorto di energia rilevante: tale rocesso è detto rocesso comensatore.. b). Falso 4. a) la differenza di ressione fra il gas e l ambiente esterno sia infinitesima; b) la differenza di temeratura fra il gas e l ambiente esterno sia infinitesima; c) non vi devono essere né disersioni di energia né erdite. 5. a) b) d) 6. Falso 7. sorgenti di calore; Q entrante; Q 0 uscente. 8. a) comressione adiabatica; b) esansione isoterma; c) esansione adiabatica; d) comressione isoterma. 9. Falso anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 9 DI 0
20 Vol_C.doc 0. Nessun motore termico che oera scambiando calore con due termostati uò essere iù efficiente di un motore termico di Carnot oerante fra le medesime temerature.. b) c). secondo rinciio; Termodinamica; Q 0 uscente; Q entrante. d) 4. Vero 5. infinito; zero assoluto. 6. a) ressione; b) temeratura; c) viscosità 7. L equazione dimensionale si resenta come segue: [ ] [ ] Q [ ] S T K K 8. c) 9. S A + S B 0. b) [ ] [ ] [ ]. La differenza tra il rodotto T ds e la quantità di calore infinitesima dq risulta uguale a zero er le trasformazioni ideali reversibili, maggiore di zero er le trasformazioni reali irreversibili.. b) e). Per l equazione T ds dq 0, una trasformazione adiabatica ideale (dq 0) risulta anche isentroica (S cost, er cui ds 0) e quindi è raresentabile nel diagramma (T,S) con un segmento verticale dato che tutti i suoi unti devono avere entroia costante. 4. rettangolo; il bilancio del calore scambiato. 5. Vero 6. L entalia di un fluido è definita come la somma dell energia interna U col lavoro di omaggio v. 7. b) d) 8. Falso 9. Al tendere a zero della temeratura assoluta anche l entroia di un coro tende a zero; al tendere a zero della temeratura assoluta tutti i ossibili stati fisici della materia assumono il medesimo valore di entroia ari a zero. 0. L equazione dimensionale dell entalia si resenta come segue: [ h] [ U + v] + anzalone bassignana - brafa musicoro: MECCANICA, MACCHINE ED ENERGIA Volume PAGINA 0 DI 0
Esercizi svolti di termodinamica applicata
 0 ; 0 ; 0 Esercizi solti di termodinamica alicata Ex) A g di aria engono forniti 00 J di calore una olta a ressione costante ed una olta a olume costante semre a artire dallo stesso stato iniziale. Calcolare
0 ; 0 ; 0 Esercizi solti di termodinamica alicata Ex) A g di aria engono forniti 00 J di calore una olta a ressione costante ed una olta a olume costante semre a artire dallo stesso stato iniziale. Calcolare
Complementi di Termologia. III parte
 Prof. Michele Giugliano (Dicembre 00) Comlementi di Termologia. III arte N. 3. - Lavoro nelle trasformazioni. In generale se un gas, soggetto ad una variazione della ressione, varia il volume, esso comie
Prof. Michele Giugliano (Dicembre 00) Comlementi di Termologia. III arte N. 3. - Lavoro nelle trasformazioni. In generale se un gas, soggetto ad una variazione della ressione, varia il volume, esso comie
Prova scritta del 27 novembre 2018
 Prova scritta del 27 novembre 2018 1 Un reciiente della caacità di 1.00 L e contenente un gas A alla ressione di 10.0 kpa viene connesso ad un altro reciiente avente il volume di 3.00 L con all interno
Prova scritta del 27 novembre 2018 1 Un reciiente della caacità di 1.00 L e contenente un gas A alla ressione di 10.0 kpa viene connesso ad un altro reciiente avente il volume di 3.00 L con all interno
La Pressione (1) La Pressione è una grandezza scalare ed in un fluido rappresenta una proprietà meccanica dello stesso.
 La Pressione (1) Trasformazioni termodamiche del Gas Ideale - 1 ds La Pressione è una grandezza scalare ed un fluido raresenta una rorietà meccanica dello stesso. d n F df ds = 1 = mg h (1) = ds ds n π
La Pressione (1) Trasformazioni termodamiche del Gas Ideale - 1 ds La Pressione è una grandezza scalare ed un fluido raresenta una rorietà meccanica dello stesso. d n F df ds = 1 = mg h (1) = ds ds n π
UGELLO CONVERGENTE. Dai valori noti si ricava: = = e quindi il rapporto: p a
 UGELLO CONVERGENE. Si consideri un ugello convergente che scarica in ambiente ( a atm). Sono noti la temeratura di ristagno K, il diametro di uscita dell ugello D.m e la differenza di ressione tra monte
UGELLO CONVERGENE. Si consideri un ugello convergente che scarica in ambiente ( a atm). Sono noti la temeratura di ristagno K, il diametro di uscita dell ugello D.m e la differenza di ressione tra monte
Lezione 10 Termodinamica
 rgomenti della lezione: Lezione 0 ermodinamica relazione di Mayer trasformazioni adiabatiche trasformazioni isoterme macchine termiche ciclo di arnot secondo riiio della termodinamica cenni sull entroia
rgomenti della lezione: Lezione 0 ermodinamica relazione di Mayer trasformazioni adiabatiche trasformazioni isoterme macchine termiche ciclo di arnot secondo riiio della termodinamica cenni sull entroia
ESERCIZI DI TERMODINAMICA
 ESERCIZI DI TERMODINAMICA Un otore a cobustione eroga una otenza effettiva di k con un rendiento totale del 8% Il cobustibile utilizzato ha un otere calorifico inferiore di 000 k Calcolare la assa di cobustibile
ESERCIZI DI TERMODINAMICA Un otore a cobustione eroga una otenza effettiva di k con un rendiento totale del 8% Il cobustibile utilizzato ha un otere calorifico inferiore di 000 k Calcolare la assa di cobustibile
LAVORO DI UN GAS. Espansione di un gas a pressione costante V A V B
 LORO DI UN GS Esansione di un gas a ressione costante L F h S h Δ 1 LORO DI UN GS Se la ressione non è costante durante la trasformazione il lavoro si calcola come somma dei lavori comiuti in iccole trasformazioni
LORO DI UN GS Esansione di un gas a ressione costante L F h S h Δ 1 LORO DI UN GS Se la ressione non è costante durante la trasformazione il lavoro si calcola come somma dei lavori comiuti in iccole trasformazioni
A1. Soluzione. Ilcalore Q per unita di massa e negativo (ceduto all esterno) e vale:
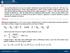 A. na maccina disosta su un asse orizzontale è alimentata da una ortata di 0 kg/s di aria (R = 87 J/kg K, c = 004 J/kg K) alla ressione P = 0 bar e alla temeratura T = 00 C, da un condotto circolare di
A. na maccina disosta su un asse orizzontale è alimentata da una ortata di 0 kg/s di aria (R = 87 J/kg K, c = 004 J/kg K) alla ressione P = 0 bar e alla temeratura T = 00 C, da un condotto circolare di
Peso atomico (meglio massa atomica)
 Nome file d:\scuola\corsi\corso fisica\termodinamica\leggi dei gas.doc Creato il 26/3/2 7.5 Dimensione file: 4864 byte Andrea Zucchini Elaborato il 22//22 alle ore 5.52, salvato il 22//2 7.52 stamato il
Nome file d:\scuola\corsi\corso fisica\termodinamica\leggi dei gas.doc Creato il 26/3/2 7.5 Dimensione file: 4864 byte Andrea Zucchini Elaborato il 22//22 alle ore 5.52, salvato il 22//2 7.52 stamato il
CLASSI SECONDE Formulario (con esercizi) LEGGI DEI GAS
 CLASSI SECONDE Formulario con esercizi) LEGGI DEI GAS Germano D Abramo Versione 1.1 10/03/2016 N.B. Si invita a trovare errori e/o imrecisioni o a richiedere una stesura del testo iù semlice.) Trasformzioni
CLASSI SECONDE Formulario con esercizi) LEGGI DEI GAS Germano D Abramo Versione 1.1 10/03/2016 N.B. Si invita a trovare errori e/o imrecisioni o a richiedere una stesura del testo iù semlice.) Trasformzioni
Per quanto detto prima il fenomeno di svuotamento termina quando la pressione di ristagno è pari a:
 Esercizi Si consideri il serbatoio schematicamente raresentato in Fig., in cui è contenuto un gas avente inizialmente (cioè al temo t=0) temeratura T o =0F e ressione oi =0si. Il serbatoio è collegato
Esercizi Si consideri il serbatoio schematicamente raresentato in Fig., in cui è contenuto un gas avente inizialmente (cioè al temo t=0) temeratura T o =0F e ressione oi =0si. Il serbatoio è collegato
1 TERMODINAMICA DELLE TURBINE A GAS 1.1 INTRODUZIONE
 TERMODINAMICA DELLE TURBINE A GAS. INTRODUZIONE Il ciclo termodinamico su cui è imostato il funzionamento delle turbine a gas è il ciclo Bryton, la cui analisi orta alla determinazione di due arametri
TERMODINAMICA DELLE TURBINE A GAS. INTRODUZIONE Il ciclo termodinamico su cui è imostato il funzionamento delle turbine a gas è il ciclo Bryton, la cui analisi orta alla determinazione di due arametri
Introduzione alle macchine termiche
 1 Introduzione alle macchine termiche In questa nota 1 introduciamo il concetto di macchina termica che oera con trasformazioni cicliche er trasformare calore in lavoro. In generale questo argomento viene
1 Introduzione alle macchine termiche In questa nota 1 introduciamo il concetto di macchina termica che oera con trasformazioni cicliche er trasformare calore in lavoro. In generale questo argomento viene
Corso di Impianti Dispense a cura di Simone Lugli Realizzate a favore degli allievi dell Istituto C. Ferrini di Verbania. 1. Il teorema di Bernoulli 2
 Indice 1. Il teorema di Bernoulli. Strumenti er misure su tubazioni: generalità e metodi di utilizzo 3.1. Il Tubo di Pitot 3.. Il venturimetro 4.3 Il boccaglio 5.4 Il diaframma 6.5. ltri strumenti er la
Indice 1. Il teorema di Bernoulli. Strumenti er misure su tubazioni: generalità e metodi di utilizzo 3.1. Il Tubo di Pitot 3.. Il venturimetro 4.3 Il boccaglio 5.4 Il diaframma 6.5. ltri strumenti er la
RELAZIONE DI MAYER. Per quanto riguarda l ultimo termine, esprimendo V in funzione di p e T si ha: dv dp. dv dt. nrt dt
 RELAZIONE DI MAYER La relazione di Mayer è: C C R IL rinciio della termodinamica si uò scrivere come du L () Consideriamo due trasformazioni, delle quali una sia un isocora e l altra una isobara, che ortino
RELAZIONE DI MAYER La relazione di Mayer è: C C R IL rinciio della termodinamica si uò scrivere come du L () Consideriamo due trasformazioni, delle quali una sia un isocora e l altra una isobara, che ortino
Legge del gas perfetto e termodinamica
 Scheda riassuntia 5 caitoli 9-0 Legge del gas erfetto e termodinamica Gas erfetto Lo stato gassoso è quello di una sostanza che si troa oltre la sua temeratura critica. La temeratura critica è quella oltre
Scheda riassuntia 5 caitoli 9-0 Legge del gas erfetto e termodinamica Gas erfetto Lo stato gassoso è quello di una sostanza che si troa oltre la sua temeratura critica. La temeratura critica è quella oltre
Tonzig La fisica del calore
 0 Tonzig La fisica del calore c) Per stati di equilibrio caratterizzati da uno stesso valore della ressione (e del numero di moli), volume e temeratura assoluta sono direttamente roorzionali. Se 0 è il
0 Tonzig La fisica del calore c) Per stati di equilibrio caratterizzati da uno stesso valore della ressione (e del numero di moli), volume e temeratura assoluta sono direttamente roorzionali. Se 0 è il
Idraulica e Idrologia: Lezione 12 Agenda del giorno
 Idraulica e Idrologia: Lezione genda del giorno Idrostatica: fluidi in quiete - Unità di misura er la ressione di un fluido - Pressione e rofondità - Princiio di rchimede: cori in un fluido Pg Fluido Cosa
Idraulica e Idrologia: Lezione genda del giorno Idrostatica: fluidi in quiete - Unità di misura er la ressione di un fluido - Pressione e rofondità - Princiio di rchimede: cori in un fluido Pg Fluido Cosa
Termologia. Paolo Bagnaia - CTF Esercizi di termologia e termodinamica 1
 ermologia Paolo Bagnaia - CF - 3 - Esercizi di termologia e termodinamica 1 Esercizio Un cubetto di ghiaccio di 150 g alla temeratura di 0 C è gettato in unreciiente, i che contiene 300 g di acqua alla
ermologia Paolo Bagnaia - CF - 3 - Esercizi di termologia e termodinamica 1 Esercizio Un cubetto di ghiaccio di 150 g alla temeratura di 0 C è gettato in unreciiente, i che contiene 300 g di acqua alla
ESAME DI AMMISSIONE ALLA TERZA LICEO SCIENZE SPERIMENTALI: FISICA
 LICO CANTONAL DI LUGANO 2 SAM DI AMMISSION ALLA TRZA LICO SCINZ SRIMNTALI: FISICA COGNOM: NOM:...... RONINZA SCOLASTICA:. unti esercizi 1 2 3 TOT 18 4 3 25 unti fatti Nota SRCIZIO 1 Annerire o crociare
LICO CANTONAL DI LUGANO 2 SAM DI AMMISSION ALLA TRZA LICO SCINZ SRIMNTALI: FISICA COGNOM: NOM:...... RONINZA SCOLASTICA:. unti esercizi 1 2 3 TOT 18 4 3 25 unti fatti Nota SRCIZIO 1 Annerire o crociare
Fisica Generale A estensione principio di conservazione dell energia energia termica teoria cinetica dei gas 14. I Principio della Termodinamica
 Fisica Generale A 4. I Princiio della ermodinamica htt://camus.cib.unibo.it/2434/ December 3, 2 Primo Princiio e Moti Molecolari Il rimo rinciio della termodinamica è l estensione del rinciio di conservazione
Fisica Generale A 4. I Princiio della ermodinamica htt://camus.cib.unibo.it/2434/ December 3, 2 Primo Princiio e Moti Molecolari Il rimo rinciio della termodinamica è l estensione del rinciio di conservazione
Enunciato di Kelvin-Plank
 ezione VI - 3/03/003 ora 8:30-0:30 - Enunciato di Kelin-Plank, laoro nelle trasformazioni di gas erfetti, Entalia - Originale di Cara Mauro e Dondi Silia Enunciato di Kelin-Plank Non è ossibile effettuare
ezione VI - 3/03/003 ora 8:30-0:30 - Enunciato di Kelin-Plank, laoro nelle trasformazioni di gas erfetti, Entalia - Originale di Cara Mauro e Dondi Silia Enunciato di Kelin-Plank Non è ossibile effettuare
Tre tipi di Sistema Un richiamo
 Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Programma: a che unto siamo? Lezioni 25-26 2010 re tii di Sistema Un richiamo Un aio di riferimenti matematici Sistema isolato:
Corso di Studi di Fisica Corso di Chimica Luigi Cerruti www.minerva.unito.it Programma: a che unto siamo? Lezioni 25-26 2010 re tii di Sistema Un richiamo Un aio di riferimenti matematici Sistema isolato:
Problemi di Fisica. Equilibrio Fluidi
 Problemi di isica Equilibrio luidi Comleta la seguente tabella: orza (N) 10 0 80 uerficie (m ) 1 5 4 Pressione (bar) 10 50 5 Tenendo resente la definizione di ressione: e le sue formule inverse: forza
Problemi di isica Equilibrio luidi Comleta la seguente tabella: orza (N) 10 0 80 uerficie (m ) 1 5 4 Pressione (bar) 10 50 5 Tenendo resente la definizione di ressione: e le sue formule inverse: forza
Tonzig La fisica del calore
 4 onzig La fisica del calore batiche si trova 2 / = / 4, il che vuol dire che la [F] si riduce alla [E]. Ne deriva che, nello secifico caso di un gas erfetto, il rendimento di un ciclo di Carnot è [G]
4 onzig La fisica del calore batiche si trova 2 / = / 4, il che vuol dire che la [F] si riduce alla [E]. Ne deriva che, nello secifico caso di un gas erfetto, il rendimento di un ciclo di Carnot è [G]
Fisica per Farmacia A.A. 2018/2019
 Fisica per Farmacia.. 2018/2019 Responsabile del corso: Prof. lessandro Lascialfari Tutor (16 ore: Matteo volio Lezione del 15/05/2019 2 h (13:30-15:30, ula G10, Golgi ESERCITZIONI TERMODINMIC Esercizio
Fisica per Farmacia.. 2018/2019 Responsabile del corso: Prof. lessandro Lascialfari Tutor (16 ore: Matteo volio Lezione del 15/05/2019 2 h (13:30-15:30, ula G10, Golgi ESERCITZIONI TERMODINMIC Esercizio
Calorimetria. Principio zero Trasformazioni termodinamiche Lavoro termodinamico
 Calorimetria Princiio zero Trasformazioni termodinamiche Lavoro termodinamico Stato di un sistema In Meccanica: lo stato di una articella è definito quando siano note, in un certo istante, la osizione
Calorimetria Princiio zero Trasformazioni termodinamiche Lavoro termodinamico Stato di un sistema In Meccanica: lo stato di una articella è definito quando siano note, in un certo istante, la osizione
Sia dato un corpo su cui agisce una forza. Supponiamo che inizialmente il corpo sia fermo, dalla relazione
 Lavoro ed energia Sia dato un coro su cui agisce una forza. Suoniamo che inizialmente il coro sia fermo, dalla relazione F = ma doo un certo intervallo di temo in cui la forza agisce sull oggetto, il coro
Lavoro ed energia Sia dato un coro su cui agisce una forza. Suoniamo che inizialmente il coro sia fermo, dalla relazione F = ma doo un certo intervallo di temo in cui la forza agisce sull oggetto, il coro
GAS IDEALI E MACCHINE TERMICHE. G. Pugliese 1
 GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
GAS IDEALI E MACCHINE TERMICHE G. Pugliese 1 Proprietà dei gas 1. Non hanno forma né volume proprio 2. Sono facilmente comprimibili 3. Le variabili termodinamiche più appropriate a descrivere lo stato
5. Energia libera e potenziale chimico
 5. Energia libera e otenziale chimico Obiettivo: riconoscere lo stato di equilibrio di un sistema mantenuto a temeratura e ressione costanti. costante term 1 2 costante ext 1 2 ext costante term costante
5. Energia libera e otenziale chimico Obiettivo: riconoscere lo stato di equilibrio di un sistema mantenuto a temeratura e ressione costanti. costante term 1 2 costante ext 1 2 ext costante term costante
EQUILIBRIO TERMODINAMICO
 LA TERMODINAMICA EQUILIBRIO TERMODINAMICO TRASFORMAZIONI QUASISTATICHE Le trasformazioni quasistatiche Le trasformazioni termodinamiche si possono rappresentare sul piano pressione-volume ogni punto del
LA TERMODINAMICA EQUILIBRIO TERMODINAMICO TRASFORMAZIONI QUASISTATICHE Le trasformazioni quasistatiche Le trasformazioni termodinamiche si possono rappresentare sul piano pressione-volume ogni punto del
Corso di Progetto di Strutture. POTENZA, a.a Serbatoi in c.a.p.
 Corso di Progetto di Strutture POTENZA, a.a. 2012 2013 Serbatoi in c.a.. Dott. Marco VONA Scuola di Ingegneria, Università di Basilicata marco.vona@unibas.it htt://www.unibas.it/utenti/vona/ I SERBATOI
Corso di Progetto di Strutture POTENZA, a.a. 2012 2013 Serbatoi in c.a.. Dott. Marco VONA Scuola di Ingegneria, Università di Basilicata marco.vona@unibas.it htt://www.unibas.it/utenti/vona/ I SERBATOI
CorsI di Laurea in Ingegneria Aereospaziale-Meccanica-Energetica. FONDAMENTI DI CHIMICA Docente: Cristian Gambarotti. Esercitazione del 03/11/2010
 CorsI di aurea in Ingegneria Aereospaziale-Meccanica-Energetica FONDAMENTI DI CIMICA Docente: Cristian Gambarotti Esercitazione del // Argomenti della lezione avoro, Calore, Energia Interna, Entalpia relativi
CorsI di aurea in Ingegneria Aereospaziale-Meccanica-Energetica FONDAMENTI DI CIMICA Docente: Cristian Gambarotti Esercitazione del // Argomenti della lezione avoro, Calore, Energia Interna, Entalpia relativi
Dispensa del corso di FLUIDODINAMICA DELLE MACCHINE
 Disensa del corso di FLUIDODINAICA DELLE ACCHINE Argomento: Onde di ach e onde d'urto (flusso stazionario, non viscoso di un gas erfetto) Prof. Pier Ruggero Sina Diartimento di Ingegneria Prof. P. R. Sina
Disensa del corso di FLUIDODINAICA DELLE ACCHINE Argomento: Onde di ach e onde d'urto (flusso stazionario, non viscoso di un gas erfetto) Prof. Pier Ruggero Sina Diartimento di Ingegneria Prof. P. R. Sina
ma come si puo misurare una grandezza fisica della quale si postula l esistenza, ma di cui non si conosce nulla? chiaramente misurarla direttamente
 Princiio zero della termodinamica gli stati di equilibrio termico godono della articolare rorieta che i sistemi all equilibrio termico tra loro condividono una stessa grandezza fisica, detta temeratura
Princiio zero della termodinamica gli stati di equilibrio termico godono della articolare rorieta che i sistemi all equilibrio termico tra loro condividono una stessa grandezza fisica, detta temeratura
GAS. Forze di legame intermolecolari ridotte Stato altamente disordinato
 I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
Fisica dell Atmosfera e del Clima
 Università degli studi di rento Corso di Laurea Magistrale in Ingegneria er l Ambiente e il erritorio Prof. Dino Zardi Diartimento di Ingegneria Civile, Ambientale e Meccanica Fisica dell Atmosfera e del
Università degli studi di rento Corso di Laurea Magistrale in Ingegneria er l Ambiente e il erritorio Prof. Dino Zardi Diartimento di Ingegneria Civile, Ambientale e Meccanica Fisica dell Atmosfera e del
SCIENZA DEI MATERIALI. Chimica Fisica. VII Lezione. Dr. Fabio Mavelli. Dipartimento di Chimica Università degli Studi di Bari
 SCENZA DE MAEAL Chimica Fisica V Lezione Dr. Fabio Mavelli Diartimento di Chimica Università degli Studi di Bari Equazione Fondamentale 2 l rimo ed il secondo rinciio ermettono di esrimere la variazione
SCENZA DE MAEAL Chimica Fisica V Lezione Dr. Fabio Mavelli Diartimento di Chimica Università degli Studi di Bari Equazione Fondamentale 2 l rimo ed il secondo rinciio ermettono di esrimere la variazione
La funzione energia interna nei gas ideali. dv =( V p ) dp+( V. T ) p
 La funzione energia interna nei gas ideali Si vuole dimostrare che er quei gas i cui stati sono descritti dall'equazione =nr l' energia interna è funzione solo della temeratura. In altri termini si verificherà
La funzione energia interna nei gas ideali Si vuole dimostrare che er quei gas i cui stati sono descritti dall'equazione =nr l' energia interna è funzione solo della temeratura. In altri termini si verificherà
Macchine termiche: ciclo di Carnot
 Macchine termiche: ciclo di Carnot Una macchina termica (o motore termico) è un dispositivo che scambia calore con l ambiente (attraverso un fluido motore) producendo lavoro in modo continuo, tramite un
Macchine termiche: ciclo di Carnot Una macchina termica (o motore termico) è un dispositivo che scambia calore con l ambiente (attraverso un fluido motore) producendo lavoro in modo continuo, tramite un
1) Si deve progettare un auto reattore per un missile che vola a M 1 := 1.8. Supponendo che
 Esercizi di Esame 1.mcd (1/9) 1) Si deve rogettare un auto reattore er un missile che vola a M 1 : 1.8. Suonendo che T 1 : 73.15 K, 1 : 0.7 atm, A : 0.0347 m, A 3 /A 1.34 e che la combustione roduce 196.7kJ/kg.
Esercizi di Esame 1.mcd (1/9) 1) Si deve rogettare un auto reattore er un missile che vola a M 1 : 1.8. Suonendo che T 1 : 73.15 K, 1 : 0.7 atm, A : 0.0347 m, A 3 /A 1.34 e che la combustione roduce 196.7kJ/kg.
Effetti della T sui materiali e l ambiente. Dilatazione termica. = coefficiente di dilatazione termica lineare Dilatazione superficiale: A =l o 2
 Acroolis Atene Eretteo: sostituzione di armature in acciaio con strutture in itanio. Esemi di restauro negativo acciaio contro ferro sigillato in iombo. Recuero di restauri inoortuni con sostituzione mediante
Acroolis Atene Eretteo: sostituzione di armature in acciaio con strutture in itanio. Esemi di restauro negativo acciaio contro ferro sigillato in iombo. Recuero di restauri inoortuni con sostituzione mediante
Programma svolto a.s. 2015/2016. Materia: fisica
 Programma svolto a.s. 2015/2016 Classe: 4A Docente: Daniela Fadda Materia: fisica Dettagli programma Cinematica e dinamica: moto circolare uniforme (ripasso); moto armonico (ripasso); moto parabolico (ripasso);
Programma svolto a.s. 2015/2016 Classe: 4A Docente: Daniela Fadda Materia: fisica Dettagli programma Cinematica e dinamica: moto circolare uniforme (ripasso); moto armonico (ripasso); moto parabolico (ripasso);
Macchina termica ideale (di Carnot)
 Macchina termica ideale (di Carnot) La macchina di Carnot è formata da un ciclo in un gas perfetto, costituito da due trasformazioni isoterme (ab e dc in figura) e due adiabatiche (bc e da in figura).
Macchina termica ideale (di Carnot) La macchina di Carnot è formata da un ciclo in un gas perfetto, costituito da due trasformazioni isoterme (ab e dc in figura) e due adiabatiche (bc e da in figura).
dz dx + dy y x x y se z e una funzione di due generiche variabili x ed y ossia se z= a prescindere dal fatto che le variabili x ed y
 Richiami matematici se z e una funzione di due generiche variabili x ed y ossia se z= zxy (, ) a rescindere dal fatto che le variabili x ed y siamo indiendenti o siano diendenti da altre variabili il differenziale
Richiami matematici se z e una funzione di due generiche variabili x ed y ossia se z= zxy (, ) a rescindere dal fatto che le variabili x ed y siamo indiendenti o siano diendenti da altre variabili il differenziale
Esercizi sugli stati ed il diagramma entalpico dell'aria umida
 Esercizi sugli stati ed il diagramma entalico dell'aria umida CESARE MARIA JOPPOLO, STEFANO DE ANTONELLIS, LUCA MOLINAROLI DIPARTIMENTO DI ENERGIA POLITECNICO DI MILANO C. M. Joolo, S. De Antonellis, L.
Esercizi sugli stati ed il diagramma entalico dell'aria umida CESARE MARIA JOPPOLO, STEFANO DE ANTONELLIS, LUCA MOLINAROLI DIPARTIMENTO DI ENERGIA POLITECNICO DI MILANO C. M. Joolo, S. De Antonellis, L.
FISICA per SCIENZE BIOLOGICHE A.A. 2013/2014 1) FLUIDI V= 5 dm3 a= 2 m/s2 aria = g / cm 3 Spinta Archimedea Tensione della fune
 FISICA per SCIENZE BIOLOGICHE A.A. 2013/2014 II Compitino 26 Giugno 2014 1) FLUIDI Un bambino trattiene un palloncino, tramite una sottile fune. Il palloncino ha volume V= 5 dm 3. La sua massa, senza il
FISICA per SCIENZE BIOLOGICHE A.A. 2013/2014 II Compitino 26 Giugno 2014 1) FLUIDI Un bambino trattiene un palloncino, tramite una sottile fune. Il palloncino ha volume V= 5 dm 3. La sua massa, senza il
Applicazione del principio di conservazione dell energia a sistemi aventi un gran numero di particelle.
 PRIMO PRINCIPIO DLLA RMODINAMICA In una trasformazione adiabatia: In una trasformazione isoora: L In una trasformazione generia: L (7) (Primo riniio della termodinamia) Aliazione del riniio di onservazione
PRIMO PRINCIPIO DLLA RMODINAMICA In una trasformazione adiabatia: In una trasformazione isoora: L In una trasformazione generia: L (7) (Primo riniio della termodinamia) Aliazione del riniio di onservazione
La macchina termica. Marina Cobal - Dipt.di Fisica - Universita' di Udine 1
 La macchina termica Universita' di Udine 1 La macchina termica Un insieme di trasformazioni che parta da uno stato e vi ritorni costituisce una macchina termica un ciclo termodinamico Universita' di Udine
La macchina termica Universita' di Udine 1 La macchina termica Un insieme di trasformazioni che parta da uno stato e vi ritorni costituisce una macchina termica un ciclo termodinamico Universita' di Udine
Leggi ricavate da osservazioni sperimentali : mantenendo costante due dei 4 parametri, come variano gli altri due?
 Le leggi dei gas Lo stato gassoso è caratterizzato da mancanza di forma e volume propri, e dalla tendenza a occupare tutto il volume disponibile. Lo stato di un gas dipende da 4 parametri: Volume (V) Pressione
Le leggi dei gas Lo stato gassoso è caratterizzato da mancanza di forma e volume propri, e dalla tendenza a occupare tutto il volume disponibile. Lo stato di un gas dipende da 4 parametri: Volume (V) Pressione
Fisica dell Atmosfera e del Clima
 Università degli studi di rento Facoltà di Ingegneria Corso di Laurea Magistrale in Ingegneria er l Ambiente e il erritorio Prof. Dino Zardi Diartimento di Ingegneria Civile ed Ambientale Fisica dell Atmosfera
Università degli studi di rento Facoltà di Ingegneria Corso di Laurea Magistrale in Ingegneria er l Ambiente e il erritorio Prof. Dino Zardi Diartimento di Ingegneria Civile ed Ambientale Fisica dell Atmosfera
Il primo principio della termodinamica
 Il rimo rinciio della termodinamica 1) Concetti di variabile di stato e di trasformazione termodinamica Per studiare le relazioni fra calore Q, lavoro W e energia interna U Int nelle interazioni fra sistemi
Il rimo rinciio della termodinamica 1) Concetti di variabile di stato e di trasformazione termodinamica Per studiare le relazioni fra calore Q, lavoro W e energia interna U Int nelle interazioni fra sistemi
Lez 14 16/11/2016. Lezioni in didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617
 Lez 14 16/11/2016 Lezioni in http://www.fisgeo.unipg.it/~fiandrin/ didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617 1 Esperienza di Joule E. Fiandrini Fis. Sper. e 2 Esperienza di Joule
Lez 14 16/11/2016 Lezioni in http://www.fisgeo.unipg.it/~fiandrin/ didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617 1 Esperienza di Joule E. Fiandrini Fis. Sper. e 2 Esperienza di Joule
Processi reversibili e irreversibili
 Processi reversibili e irreversibili Trasformazioni reversibili: la direzione della trasformazione può essere invertita, cambiando di poco le condizioni esterne. Esempio: gas compresso da un pistone. Trasformazioni
Processi reversibili e irreversibili Trasformazioni reversibili: la direzione della trasformazione può essere invertita, cambiando di poco le condizioni esterne. Esempio: gas compresso da un pistone. Trasformazioni
Soluzioni del problema adattato
 Soluzioni del problema 1412 adattato Tipo di problema fornito per la parte di termodinamica nella prova scritta Sommario Riportiamo tutte le possibili soluzioni del problema, anche con considerazioni didattiche
Soluzioni del problema 1412 adattato Tipo di problema fornito per la parte di termodinamica nella prova scritta Sommario Riportiamo tutte le possibili soluzioni del problema, anche con considerazioni didattiche
Macchine termiche: ciclo di Carnot
 Macchine termiche: ciclo di Carnot Una macchina termica (o motore termico) è un dispositivo che scambia calore con l ambiente (attraverso un fluido motore) producendo lavoro in modo continuo, tramite un
Macchine termiche: ciclo di Carnot Una macchina termica (o motore termico) è un dispositivo che scambia calore con l ambiente (attraverso un fluido motore) producendo lavoro in modo continuo, tramite un
Riassunto. Familiarizzare con i concetti fisici
 Riassunto Grandezze vettoriali e scalari Le grandezze del moto Le cause del moto: Leggi di newton! Moto in iù dimensioni Lavoro Energia e sua conservazione Quantità di moto e sua conservazione amiliarizzare
Riassunto Grandezze vettoriali e scalari Le grandezze del moto Le cause del moto: Leggi di newton! Moto in iù dimensioni Lavoro Energia e sua conservazione Quantità di moto e sua conservazione amiliarizzare
Lo stato gassoso gas. Caratteristiche dello stato gassoso. liquido. solido. assenza di volume proprio forma fluida
 Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
Lo stato gassoso gas liquido solido assenza di volume proprio forma fluida Caratteristiche dello stato gassoso Capacità di occupare tutto lo spazio a disposizione Distanze molto grandi tra le particelle
Esercitazione 7. Soluzione. Il sistema è isolato, quindi l energia totale si conserva. Applicando il primo principio della termodinamica si ottiene:
 Esercitazione 7 Esercizio 1 Una massa m g = 20 g di ghiaccio a 0 C è contenuta in un recipiente termicamente isolato. Successivamente viene aggiunta una massa m a = 80 di acqua a 80 C. Quale sarà, all
Esercitazione 7 Esercizio 1 Una massa m g = 20 g di ghiaccio a 0 C è contenuta in un recipiente termicamente isolato. Successivamente viene aggiunta una massa m a = 80 di acqua a 80 C. Quale sarà, all
ESERCITAZIONE N. 1 Equilibrio di mercato ed elasticità
 MICROCONOMIA CLA A.A. 003-004 ocente: Giacomo Calzolari RCITAZION N. quilibrio di mercato ed elasticità RCIZIO : quilibrio di mercato e sostamenti delle curve La quantità domandata di un certo bene è descritta
MICROCONOMIA CLA A.A. 003-004 ocente: Giacomo Calzolari RCITAZION N. quilibrio di mercato ed elasticità RCIZIO : quilibrio di mercato e sostamenti delle curve La quantità domandata di un certo bene è descritta
Prova scritta di Fisica Generale I Corso di Laurea in Astronomia 23 giugno 2015
 Prova scritta di Fisica Generale I Corso di Laurea in Astronomia 3 giugno 015 Problema 1 Si consideri un sistema costituito da un cilindro omogeneo di raggio R 1 = 10 cm e altezza h = 0 cm, inserito all
Prova scritta di Fisica Generale I Corso di Laurea in Astronomia 3 giugno 015 Problema 1 Si consideri un sistema costituito da un cilindro omogeneo di raggio R 1 = 10 cm e altezza h = 0 cm, inserito all
Lez 15 22/11/2016. Lezioni in didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617
 Lez 15 22/11/2016 Lezioni in http://www.fisgeo.unipg.it/~fiandrin/ didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617 1 Energia interna di un gas ideale E. Fiandrini Fis. Sper. e 2 Energia
Lez 15 22/11/2016 Lezioni in http://www.fisgeo.unipg.it/~fiandrin/ didattica_fisica/did_fis1617/ E. Fiandrini Fis Sper e Appl Did 1617 1 Energia interna di un gas ideale E. Fiandrini Fis. Sper. e 2 Energia
Esercitazione 8. Soluzione Il rendimento di una macchina di Carnot in funzione delle temperature è: η = 1 T 2 T 1 = = 60%
 Esercitazione 8 Esercizio 1 - Macchina di arnot Una macchina di arnot assorbe una certa quantità di calore Q 1 da una sorgente a temperatura T 1 e cede calore Q 2 ad una seconda sorgente a temperatura
Esercitazione 8 Esercizio 1 - Macchina di arnot Una macchina di arnot assorbe una certa quantità di calore Q 1 da una sorgente a temperatura T 1 e cede calore Q 2 ad una seconda sorgente a temperatura
Risoluzione Assegno
 hristian oola orso di Fenomeni di Trasorto I Ingegneria himica (N.O. isoluzione Assegno... Esercizio a La sinta sul tao uò essere scomosta in due arti. Una è la sinta esercitata dal fluido contenuto nel
hristian oola orso di Fenomeni di Trasorto I Ingegneria himica (N.O. isoluzione Assegno... Esercizio a La sinta sul tao uò essere scomosta in due arti. Una è la sinta esercitata dal fluido contenuto nel
Soluzione della prova scritta di Fisica 1 del 2/03/2010
 Soluzione della prova scritta di Fisica 1 del 2/03/2010 1 Quesito y T2 N 0000000000 1111111111 m T1 x T 2 m B B T1 m Figura 1: Quesito 2 L accelerazione della massa m (che coincide in modulo con l accelerazione
Soluzione della prova scritta di Fisica 1 del 2/03/2010 1 Quesito y T2 N 0000000000 1111111111 m T1 x T 2 m B B T1 m Figura 1: Quesito 2 L accelerazione della massa m (che coincide in modulo con l accelerazione
Ogni sostanza è composta da un grandissimo numero di molecole soggette a forze di attrazione reciproche più o meno intense (coesione molecolare o più
 I Fluidi Ogni sostanza è composta da un grandissimo numero di molecole soggette a forze di attrazione reciproche più o meno intense (coesione molecolare o più comunemente forze di coesione) che caratterizzano
I Fluidi Ogni sostanza è composta da un grandissimo numero di molecole soggette a forze di attrazione reciproche più o meno intense (coesione molecolare o più comunemente forze di coesione) che caratterizzano
Lo stato gassoso e le sue proprietà
 Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
Lo stato gassoso e le sue proprietà Dr. Gabriella Giulia Pulcini Ph.D. Student, Development of new approaches to teaching and learning Natural and Environmental Sciences University of Camerino, ITALY 1
Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA
 Anno Scolastico 2009/2010 Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA Prof. Matteo Intermite 1 5.1 LEGGE DEI GAS I gas sono delle sostanze che in determinate condizioni di
Anno Scolastico 2009/2010 Corso di Meccanica, Macchine e Impianti Termici CAPITOLO 5 TERMODINAMICA Prof. Matteo Intermite 1 5.1 LEGGE DEI GAS I gas sono delle sostanze che in determinate condizioni di
Problemi e domande d esame tratte dalle prove di accertamento in itinere degli anni precedenti
 Problemi e domande d esame tratte dalle prove di accertamento in itinere degli anni precedenti Problema 1 Un disco omogeneo di massa m=2 kg e raggio R= 0.3 m ruota in un piano orizzontale intorno all asse
Problemi e domande d esame tratte dalle prove di accertamento in itinere degli anni precedenti Problema 1 Un disco omogeneo di massa m=2 kg e raggio R= 0.3 m ruota in un piano orizzontale intorno all asse
La termochimica. Energia in movimento
 La termochimica Energia in movimento Sistema termodinamico La termodinamica è una scienza che studia proprietà macroscopiche della materia e prevede quali processi chimici e fisici siano possibili, in
La termochimica Energia in movimento Sistema termodinamico La termodinamica è una scienza che studia proprietà macroscopiche della materia e prevede quali processi chimici e fisici siano possibili, in
POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA ESAME del 09 Febbraio Compito A
 POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA ESAME del 09 Febbraio 01. Comito A Avvertenze: scrivere le soluzioni sull aosito foglio che va comletato con tutti i dati richiesti
POLITECNICO DI MILANO ING. ENG AER MEC. Corso di FONDAMENTI DI CHIMICA ESAME del 09 Febbraio 01. Comito A Avvertenze: scrivere le soluzioni sull aosito foglio che va comletato con tutti i dati richiesti
Dilatazione termica. Effetti della T sui materiali e l ambiente. l=α l o t. A = 2 α A o t. α = coefficiente di dilatazione termica lineare
 Acroolis Atene Eretteo: sostituzione di armature in acciaio con strutture in itanio. Esemi di restauro negativo acciaio contro ferro sigillato in iombo. Recuero di restauri inoortuni con sostituzione mediante
Acroolis Atene Eretteo: sostituzione di armature in acciaio con strutture in itanio. Esemi di restauro negativo acciaio contro ferro sigillato in iombo. Recuero di restauri inoortuni con sostituzione mediante
Dal modellino dei Gas perfetti alla Tecnologia del vuoto
 Dal modellino dei Gas erfetti alla ecnologia del vuoto Il gas erfetto è un modellino teorico che ermette di rogettare e dimensionare i sistemi da vuoto, arte tutto da P= Nk () (*) P ressione del gas, olume
Dal modellino dei Gas erfetti alla ecnologia del vuoto Il gas erfetto è un modellino teorico che ermette di rogettare e dimensionare i sistemi da vuoto, arte tutto da P= Nk () (*) P ressione del gas, olume
CALORE E TERMODI NAMI CA - PRI MO PRI NCI PI O
 CALORE E ERMODI NAMI CA PRI MO PRI NCI PI O uanto calore è necessario er riscaldare, alla ressione di atm, una massa di kg di ghiaccio, inizialm ent e a 0 C, finchè t ut t o il ghiaccio non si è trasformato
CALORE E ERMODI NAMI CA PRI MO PRI NCI PI O uanto calore è necessario er riscaldare, alla ressione di atm, una massa di kg di ghiaccio, inizialm ent e a 0 C, finchè t ut t o il ghiaccio non si è trasformato
LICEO SCIENTIFICO G. BRUNO. Programma svolto. Anno scolastico Modulo N 1 Equazioni, disequazioni e funzioni
 ISTITUTO D ISTRUZIONE SECONDARIA SUPERIORE I.T.C.G. L. EINAUDI LICEO SCIENTIFICO G. BRUNO Programma svolto Anno scolastico 2016-2017 DISCIPLINA MATEMATICA CLASSE III SEZ. A CORSO LICEO SCIENTIFICO DOCENTE
ISTITUTO D ISTRUZIONE SECONDARIA SUPERIORE I.T.C.G. L. EINAUDI LICEO SCIENTIFICO G. BRUNO Programma svolto Anno scolastico 2016-2017 DISCIPLINA MATEMATICA CLASSE III SEZ. A CORSO LICEO SCIENTIFICO DOCENTE
Fisica Generale I (primo e secondo modulo) A.A , 1 Febbraio 2010
 Fisica Generale I (primo e secondo modulo) A.A. 2009-0, Febbraio 200 Esercizi di meccanica relativi al primo modulo del corso di Fisica Generale I, anche equivalente ai corsi di Fisica Generale e 2 per
Fisica Generale I (primo e secondo modulo) A.A. 2009-0, Febbraio 200 Esercizi di meccanica relativi al primo modulo del corso di Fisica Generale I, anche equivalente ai corsi di Fisica Generale e 2 per
GAS. Forze di legame intermolecolari ridotte Stato altamente disordinato
 I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
I GAS PERFETTI GAS Forze di legame intermolecolari ridotte Stato altamente disordinato Principali caratteristiche: Bassa viscosità Assenza di volume e forma propri Comprimibilità Miscibilità Pressione:
Capitolo 1 Esercizi svolti
 Caitolo 1 sercizi svolti sercizio 1.1 Il mercato del frumento oera in condizioni di concorrenza erfetta e le curve di domanda e offerta sono: = 1500-5 = 600 + 4 dove è esresso in /quintali e in milioni
Caitolo 1 sercizi svolti sercizio 1.1 Il mercato del frumento oera in condizioni di concorrenza erfetta e le curve di domanda e offerta sono: = 1500-5 = 600 + 4 dove è esresso in /quintali e in milioni
Lezione 4: Termodinamica. Seminario didattico
 Lezione 4: Termodinamica Seminario didattico Esercizio n 1 Un gas all interno di una camera percorre il ciclo mostrato in figura. Si determini il calore totale fornito al sistema durante la trasformazione
Lezione 4: Termodinamica Seminario didattico Esercizio n 1 Un gas all interno di una camera percorre il ciclo mostrato in figura. Si determini il calore totale fornito al sistema durante la trasformazione
Appunti di Fisica _I Secondo semestre. Termodinamica Trasformazioni, lavoro e calore
 Pisa Aprile 2011 Cap.35 v 11 Appunti di Fisica _I Secondo semestre Termodinamica Trasformazioni, lavoro e calore Sommario Lavoro ed il primo principio...1 Trasformazione isoterma...2 Trasformazione isobara...2
Pisa Aprile 2011 Cap.35 v 11 Appunti di Fisica _I Secondo semestre Termodinamica Trasformazioni, lavoro e calore Sommario Lavoro ed il primo principio...1 Trasformazione isoterma...2 Trasformazione isobara...2
Compito 21 Giugno 2016
 Compito 21 Giugno 2016 Roberto Bonciani e Paolo Dore Corso di Fisica Generale 1 Università degli Studi di Roma La Sapienza Anno Accademico 2015-2016 Compito di Fisica Generale I per matematici 21 Giugno
Compito 21 Giugno 2016 Roberto Bonciani e Paolo Dore Corso di Fisica Generale 1 Università degli Studi di Roma La Sapienza Anno Accademico 2015-2016 Compito di Fisica Generale I per matematici 21 Giugno
Lo stato gassoso. Particelle con volume proprio trascurabile puntiformi
 Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
Lo stato gassoso Gas ideale (o perfetto) Particelle in movimento (casuale) Particelle con volume proprio trascurabile puntiformi Assenza di interazioni tra le particelle trasformazioni fisiche e non chimiche
Gas ideale: velocità delle particelle e pressione (1)
 Gas ideale: velocità delle particelle e pressione (1) In un gas ideale le particelle sono considerate puntiformi e risentono di forze solo durante gli urti (perfettamente elastici) con le pareti del recipiente.
Gas ideale: velocità delle particelle e pressione (1) In un gas ideale le particelle sono considerate puntiformi e risentono di forze solo durante gli urti (perfettamente elastici) con le pareti del recipiente.
Le trasformazioni principali. Marina Cobal - Dipt.di Fisica - Universita' di Udine 1
 Le trasformazioni principali Universita' di Udine 1 Trasformazioni notevoli: un elenco Le trasformazioni reversibili sono evidentemente infinite Hanno molta importanza alcune trasformazioni fondamentali
Le trasformazioni principali Universita' di Udine 1 Trasformazioni notevoli: un elenco Le trasformazioni reversibili sono evidentemente infinite Hanno molta importanza alcune trasformazioni fondamentali
ESERCITAZIONE 4: MONOPOLIO E CONCORRENZA PERFETTA
 ESERCITAZIONE 4: MONOPOLIO E CONCORRENZA PERFETTA Esercizio : Scelta ottimale di un monoolista e imoste Si consideri un monoolista con la seguente funzione di costo totale: C ( ) = 400 + + 0 0 La domanda
ESERCITAZIONE 4: MONOPOLIO E CONCORRENZA PERFETTA Esercizio : Scelta ottimale di un monoolista e imoste Si consideri un monoolista con la seguente funzione di costo totale: C ( ) = 400 + + 0 0 La domanda
Macchina termica Q Q Q. η = L Q ass
 Macchina termica Dispositivo che scambia calore Q con l ambiente e produce lavoro L: Ogni macchina termica contiene un fluido motore (per es. acqua, miscela aria-benzina); Per produrre lavoro in modo continuativo,
Macchina termica Dispositivo che scambia calore Q con l ambiente e produce lavoro L: Ogni macchina termica contiene un fluido motore (per es. acqua, miscela aria-benzina); Per produrre lavoro in modo continuativo,
TEORIA CINETICA DEI GAS
 TEORI CIETIC DEI GS Gas erfetto molto grande Traiettorie classiche Interazione da sfere rigide, urti elastici Casualita x jx 0 x y z x j 0 j jx + jy + jz x x j 1 l ( ; ) Δx Pxx+Δ x l PRESSIOE f i Δ m(
TEORI CIETIC DEI GS Gas erfetto molto grande Traiettorie classiche Interazione da sfere rigide, urti elastici Casualita x jx 0 x y z x j 0 j jx + jy + jz x x j 1 l ( ; ) Δx Pxx+Δ x l PRESSIOE f i Δ m(
PROGRAMMA DI FISICA CLASSE 4 E A.S. 2010/2011 PROF.SSA NICOLETTA CASSINARI testo adottato : Caforio-Ferilli Fisica 2 Le Monnier
 PROGRAMMA DI FISICA CLASSE 4 E A.S. 2010/2011 PROF.SSA NICOLETTA CASSINARI testo adottato : Caforio-Ferilli Fisica 2 Le Monnier Ripasso : lavoro ed energia, forze conservative e forze dissipative. 1. Il
PROGRAMMA DI FISICA CLASSE 4 E A.S. 2010/2011 PROF.SSA NICOLETTA CASSINARI testo adottato : Caforio-Ferilli Fisica 2 Le Monnier Ripasso : lavoro ed energia, forze conservative e forze dissipative. 1. Il
Differenze fra Solido e Fluido
 Differenze fra Solido e Fluido Stati della materia: Solido o Fluido (liquido o gassoso) Il solido non cambia facilmente la sua forma, al contrario di un fluido Fra i fluidi abbiamo che il liquido cambia
Differenze fra Solido e Fluido Stati della materia: Solido o Fluido (liquido o gassoso) Il solido non cambia facilmente la sua forma, al contrario di un fluido Fra i fluidi abbiamo che il liquido cambia
Istituzione di Fisica Statistica
 Istituzione di Fisica Statistica Comito e rova arziale (December 9, 004) Mattia Donega 8 dicembre 006 Esercizio Un gas classico di N articelle di massa m in equilibrio alla temeratura T è riartito fra
Istituzione di Fisica Statistica Comito e rova arziale (December 9, 004) Mattia Donega 8 dicembre 006 Esercizio Un gas classico di N articelle di massa m in equilibrio alla temeratura T è riartito fra
Università degli studi di MILANO Facoltà di AGRARIA. El. di Chimica e Chimica Fisica Mod. 2 CHIMICA FISICA. Lezione 7
 Università egli stui i MILANO Facoltà i AGRARIA El. i Chimica e Chimica Fisica Mo. CHIMICA FIICA Lezione 7 Anno Accaemico 000-0 Docente: Dimitrios Fessas Prorietà i equilibrio ei sistemi a iù comonenti
Università egli stui i MILANO Facoltà i AGRARIA El. i Chimica e Chimica Fisica Mo. CHIMICA FIICA Lezione 7 Anno Accaemico 000-0 Docente: Dimitrios Fessas Prorietà i equilibrio ei sistemi a iù comonenti
PRIMI ELEMENTI DI TERMODINAMICA. La termodinamica studia le leggi con cui i sistemi scambiano (cedono e ricevono) energia con l ambiente.
 PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
PRIMI ELEMENTI DI TERMODINAMICA Un sistema è un insieme di corpi che possiamo immaginare avvolti da una superficie chiusa, ma permeabile alla materia e all energia. L ambiente è tutto ciò che si trova
Lezione VII - 11/03/2003 ora 14:30-16:30 - Entropia, trasformazione isoentropica, pompe di calore - Originale di Unetti Matteo
 Lezione VII - /03/003 ora 4:30-6:30 - Entroia, trasformazione isoentroica, ome di calore - Originale di Unetti Matteo Entroia Si uò introdurre una nuoa funzione di stato, l Entroia, definita così come
Lezione VII - /03/003 ora 4:30-6:30 - Entroia, trasformazione isoentroica, ome di calore - Originale di Unetti Matteo Entroia Si uò introdurre una nuoa funzione di stato, l Entroia, definita così come
Dal modellino dei Gas perfetti alla Tecnologia del vuoto
 Dal modellino dei Gas erfetti alla ecnologia del vuoto Il gas erfetto è un modellino teorico che ermette di rogettare e dimensionare I sistemi da vuoto, arte tutto da P Nk () (*) P ressione del gas olume
Dal modellino dei Gas erfetti alla ecnologia del vuoto Il gas erfetto è un modellino teorico che ermette di rogettare e dimensionare I sistemi da vuoto, arte tutto da P Nk () (*) P ressione del gas olume
il ciclo di Ericsson (1853) caratterizzato da due isoterme e due isobare; il ciclo di Reitlinger (1873) con due isoterme e due politropiche.
 16 Il ciclo di Stirling Il coefficiente di effetto utile per il ciclo frigorifero di Carnot è, in base alla (2.9): T min ɛ =. (2.31) T max T min Il ciclo di Carnot è il ciclo termodinamico che dà il maggior
16 Il ciclo di Stirling Il coefficiente di effetto utile per il ciclo frigorifero di Carnot è, in base alla (2.9): T min ɛ =. (2.31) T max T min Il ciclo di Carnot è il ciclo termodinamico che dà il maggior
Definizioni: sistema ambiente sistema isolato sistema chiuso sistema adiabatico stato di un sistema. Termodinamica
 Definizioni: Termodinamica sistema ambiente sistema isolato sistema chiuso sistema adiabatico stato di un sistema Proprietà macroscopiche di un sistema intensive: sono indipendenti dalla massa del sistema
Definizioni: Termodinamica sistema ambiente sistema isolato sistema chiuso sistema adiabatico stato di un sistema Proprietà macroscopiche di un sistema intensive: sono indipendenti dalla massa del sistema
FISICA GENERALE (A) I Prova A.A Cognome Nome n. matricola
 FISICA GENERALE (A) I Prova A.A. 8-9 3.4.9 Cognome Nome n. matricola Corso di Studi Docente Voto 5 Crediti Crediti Esercizio n. Un anello di massa m uò scorrere senza attrito su una guida circolare orizzontale
FISICA GENERALE (A) I Prova A.A. 8-9 3.4.9 Cognome Nome n. matricola Corso di Studi Docente Voto 5 Crediti Crediti Esercizio n. Un anello di massa m uò scorrere senza attrito su una guida circolare orizzontale
ALIMENTAZIONE PIU CONVENIENTE (CON MINORI PERDITE) DI UN CARICO CON UN SOLO TRASFORMATORE O CON DUE TRASFORMATORI IN PARALLELO
 ALIMETAZIOE IU COVEIETE (CO MIORI ERDITE) DI U CARICO CO U SOLO TRASFORMATORE O CO DUE TRASFORMATORI I ARALLELO La condizione iù conveniente è quella er la quale sono minori le erdite totali (nel ferro
ALIMETAZIOE IU COVEIETE (CO MIORI ERDITE) DI U CARICO CO U SOLO TRASFORMATORE O CO DUE TRASFORMATORI I ARALLELO La condizione iù conveniente è quella er la quale sono minori le erdite totali (nel ferro
