CHIMICA ANALITICA II CON LABORATORIO. (AA ) 8 C.F.U. - Laurea triennale in Chimica
|
|
|
- Giuseppina Zamboni
- 4 anni fa
- Visualizzazioni
Transcript
1 CHIMICA ANALITICA II CON LABORATORIO (AA ) 8 C.F.U. - Laurea triennale in Chimica 16
2 Separazione dei picchi e risoluzione Già conosciamo il fattore di selettività o fattore di separazione che è una misura della separazione di due sostanze (A e B) ed è indicato con α: α = K B K A = k B k A = (t R') B (t R ') A Rapporto dei coefficienti di partizione Rapporto dei fattori di ritenzione Rapporto dei tempi di ritenzione corretti (per il tempo morto t M ) Il fattore di selettività α descrive solo la selettività del sistema di fasi impiegato. L efficienza di una colonna dipende anche dal numero di piatti N, e dall entità del fattore di ritenzione (k). Quindi si utilizza la RISOLUZIONE (R S ) per caratterizzare l abilità di una colonna cromatografica a separare due analiti (cioè la selettività). R S si calcola per i picchi gaussiani di A e B, impiegando le ampiezze di base (w b ). R S = Δt w A + w B 2 = tb R - t A R w b con w b w A w B "b" sta per "baseline" segue Introduzione alla cromatografia: separazione e risoluzione 2
3 Poiché è frequente che i picchi in condizioni reali siano NON simmetrici, quindi non gaussiani, è opportuno esprimere R S in termini diversi da w b. Ricordando che il numero di piatti teorici è espresso come: direzione del flusso della f.m. 2 = N 16 t R w b --> si ricava w b (per la sostanza B): w B = 4 t B R TAILING FRONTING Quindi sostituendo w B in R S : t B R - t A R R S = = w B t B R - t A R 4 --> Dipendenza di R S dal numero dei piatti N t B R Dato che il fattore di ritenzione è uguale a: k = t R - t M t M --> si ricava t R : t R = t M (k+1) t B R - t A R R S = = 4 t B R 4 t M (k B +1) - t M (k A +1) = t M (k B +1) k B - k A 4 --> Dipendenza di R S dai fattori di ritenzione k B +1 delle sostanze A e B segue Introduzione alla cromatografia: separazione e risoluzione 3
4 Dato che il fattore di separazione α è uguale a: --> si ricava k A : α = k B k = k A A k B α R S = k k B - k B - A 4 k B +1 = 4 k B +1 k B α α α --> Dipendenza di R S dai fattori di ritenzione delle sostanze A e B = k B (α-1) 4 α (k B +1) = α-1 4 α k B k B +1 Se i fattori di ritenzione di A e B sono simili, quindi k B k A k' e quindi α 1, si può esprimere R S come: R S = α-1 4 k' --> Dipendenza di R S dal fattore di separazione k'+1 Quando la risoluzione R S è nota, il numero di piatti teorici N può esser calcolato dai fattori di separazione e il fattore di ritenzione del componente B, k B. N = 16 R S2 α α k B +1 2 k B segue Introduzione alla cromatografia: separazione e risoluzione 4
5 R S = α-1 4 k' k'+1 La separazione può essere ottimizzata in base alla dipendenza della risoluzione R S da, k, N (o meglio H). Le variabili possono essere modificate in modo indipendente l una dall altra. Il fattore di separazione (collegato alla differenza dei t R ) può essere modificato cambiando il tipo di interazione molecolare (es. cambiando la fase stazionaria); Il fattore di ritenzione k (collegato a t R ) può essere modificato cambiando la T in GC o la composizione della f.m. in LC; Il numero di piatti teorici N può essere migliorato aumentando la lunghezza della colonna o ottimizzando l'altezza dei piatti teorici (H); H è influenzata dalla velocità del flusso (u), dalle dimensioni delle particelle del materiale di impaccamento (d D ), dalla viscosità delle fasi e quindi dai coefficienti di diffusione D S e D M, dallo spessore (d f ) del film di liquido immobilizzato usato come f.s.; Nel caso di picchi simmetrici, egualmente intensi, si parla di risoluzione R S = 1 per la separazione della linea di base, o separazione di 4. Nel caso di picchi a intensità molto diversa o asimmetrici è necessaria una separazione molto maggiore per una completa separazione. Introduzione alla cromatografia: separazione e risoluzione 5
6 Analisi qualitativa in cromatografia I metodi cromatografici sono impiegabili per analisi qualitative, quantitative o per scopi preparativi. L'informazione qualitativa: nei cromatogrammi interni risiede nella posizione della sostanza sulla f.s. (es. in TLC); nei cromatogrammi esterni risiede nel valore del volume o tempo di ritenzione delle diverse sostanze. Sebbene la riproducibilità del tempo o del volume di ritenzione sia minore della precisione delle lunghezze d onda in spettroscopia, comparando i dati di ritenzione con quelli di sostanze standard, può essere stabilita la presenza o assenza di una sostanza nel campione. Per identificare inequivocabilmente una sostanza si può accoppiare la separazione cromatografica con un opportuno rivelatore posto alla fine della colonna, (es. UV per HPLC, MS per GC). Nelle analisi qualitative di una miscela multicomponente, si deve ricordare che la capacità di picchi di una colonna è limitata. La capacità di picchi riflette il numero di picchi che possono essere risolti in una sequenza di picchi in un intervallo definito. Secondo J. Calvin Giddings (Unified Separation Science - Wiley 1991) in cromatografia di eluizione, la capacità di picco n é approssimativamente calcolabile come: n = ln n = ln V R (n) V R (1) t R (n) t R (1) Capacità di picchi n tipiche per numeri definiti di N, in GC, LC e cromatografia su gel, secondo Giddings Capacità di picchi n Numero di piatti teorici N Gel GC LC Se il numero di costituenti il campione eccede la capacità di picchi, allora si ha sovrapposizione dei picchi sotto i quali due o più costituenti eluiscono insieme. Introduzione alla cromatografia: analisi qualitativa 6
7 Analisi quantitativa in cromatografia Per ottenere informazione quantitativa: nelle cromatografie interne si può misurare l intensità complessiva della macchia (spot) di una sostanza sulla f.s. (es. in TLC); nelle cromatografie esterne (cioè su colonna) si effettua una valutazione dell altezza o dell area dei picchi. I metodi cromatografici sono metodi relativi; si esegue una taratura mediante analisi di sostanze standard (si usano sia standard esterni che interni). Nelle cromatografie interne: se si decide di valutare l altezza di picco, si deve garantire che non c è alterazione nella forma del picco a seguito di cambio delle condizioni cromatografiche (nel confrontare il segnale del campione con quello dello standard); poiché se ci sono alterazioni, non c è più proporzione diretta con la concentrazione. Variabili come T della colonna, velocità di flusso, volume d iniezione devono essere precisamente controllati. Inoltre bisogna evitare di sovraccaricare la colonna con una grande quantità di campione. se si decide di valutare l area di picco, le alterazioni di forma dei picchi sono meno rilevanti. Si usano metodi di integrazione numerici, assistiti dal calcolatore. Le aree del picco si possono approssimare, calcolando il prodotto tra l'altezza e l ampiezza a mezza altezza (area = h w h ). Picchi molto stretti possono generare problemi nell'integrazione dell'area poiché è difficile collocare la posizione esatta di inizio e fine del picco. Introduzione alla cromatografia: analisi quantitativa 7
8 GASCROMATOGRAFIA
9 INTRODUZIONE I composti da analizzare sono vaporizzati nel sistema di iniezione ed eluiti attraverso una colonna con l aiuto di un gas come fase mobile. La fase mobile è usata soltanto come gas di trasporto (carrier gas) il che significa che non ci sono interazioni chimiche significative tra analiti e f.m.. Le fasi stazionarie possono essere liquide (partizione liquido/gas (GLC detta anche GC) che viene utilizzata per analisi di composti organici) o solide (adsorbimento GSC- "gassolid chromatography"; es. analisi di gas permanenti e C1-C3) - nelle CROMATOGRAFIE PER ADSORBIMENTO la fase stazionaria è solida e le sostanze si separano a seconda della loro affinità di adsorbimento sulla fase solida; - nelle CROMATOGRAFIE DI PARTIZIONE la fase stazionaria è un film liquido supportato su solido e le sostanze si separano in dipendenza dei loro coefficienti di partizione tra la fase mobile e la fase stazionaria. Le analisi gas cromatografiche sono adatte per analiti volatili, termicamente stabili, non polari, o che possono esser resi tali da opportune reazioni ( DERIVATIZZAZIONE). Gascromatografia: introduzione 9
10 ESEMPIO per GSC: Chromatographia May 1982, Volume 15, Issue 5, pp Separation of mixtures of permanent gases and light hydrocarbons on spherical carbon molecular sieves by gassolid chromatography P. KuszA. AndrysiakJ. Bobiński
11 Derivatizzazione La derivatizzazione consiste nella modifica per reazione chimica di un composto in modo da produrre un nuovo composto su cui sia possibile effettuare una analisi gas cromatografica. Si derivatizza per: Consentire l'analisi di composti che, per esempio, non siano sufficientemente volatili o stabili per analisi GC; Migliorare l'andamento del cromatogramma o la possibilità di rivelare un determinato composto. Molti composti non producono un cromatogramma utilizzabile (ad es. molteplicità di picchi o un picco unico molto largo), oppure è difficile rivelare il composto a causa della sua natura. Quindi è necessario effettuare una opportuna derivatizzazione dello stesso prima di effettuare l'analisi GC. Con la derivatizzazione si può ottenere: Un aumento della volatilità (es. analisi degli zuccheri) per esempio per eliminazione (mascheramento) di gruppi polari OH, NH ed SH; Aumento della rivelabilità, ad es. per steroidi/colesterolo; Aumento della stabilità dei composti; Aumento della sensibilità nel caso di rivelatore ECD (Electron Capture Detection). L'introduzione di gruppi rivelabili tramite ECD come gli acil-alogenuri, permette la rivelazione di sostanze "cieche" all'ecd. segue Gascromatografia: derivatizzazione 11
12 In genere il motivo principale per cui i composti vengono derivatizzati è per renderli più volatili. Di solito le molecole poco volatili sono grandi, oppure sono piccole ma possiedono molti gruppi polari che ne diminuiscono la volatilità. Nel secondo caso è abbastanza semplice aumentare la volatilità della molecola perchè basta "mascherare" i gruppi polari tramite opportune reazioni. Questo risultato si può ottenere con tre tipi di reazioni: Silanizzazione (metodo più usato); Alchilazione; Acilazione. Silanizzazione Consente di rimpiazzare gli idrogeni attivi con gruppi TMS (trimetilsilil-). Questa reazione avviene per attacco nucleofilo SN2. Migliore è il gruppo uscente migliore sarà la resa della silanizzazione. La reazione deve avvenire in solventi anidri e non contenenti alcol, poiché essi reagirebbero per primi inficiando al procedura di silanizzazione. Il Bis(trimethylsilyl)acetamide ("BSA", Me 3 SiNC(OSiMe 3 )Me è un efficiente agente silanizzante. La reazione del BSA con gruppi alcolici dà come prodotti il corrispondente trimetilsilil-etere e N- (trimetilsilil)acetamide come sottoprodotto: ROH + Me 3 SiNC(OSiMe 3 )Me ROSiMe 3 + Me 3 SiN(H)C(O)Me segue Gascromatografia: derivatizzazione 12
13 Dati di ritenzione e coefficiente di partizione Per tenere conto di pressione e temperatura, nella teoria si usa il volume di ritenzione (V R e V M ) piuttosto che il tempo di ritenzione (nella pratica invece si usano i tempi). Se F è il flusso del gas carrier (ml di carrier per minuto): V R = F t R V M = F t M t M si può determinare anche con iniezione di metano aggiunto al carrier o aria Il volume di ritenzione corretto si esprime come: Il volume di ritenzione corretto è caratteristico di una sostanza ed è correlato, attraverso il volume della f.s. (V S ), V R = V R - V M al coefficiente di partizione: V R = K V S La resistenza della colonna comporta pressioni più elevate all ingresso che all uscita (differenza di P in colonna); in considerazione della comprimibilità dei gas, il flusso di gas aumenta all aumentare della differenza di pressione. Per descrivere il volume di ritenzione indipendentemente dalle cadute di pressione si può usare un fattore correttivo j (di Martin), V N = j V R Il volume di ritenzione specifico V g dipende da V N, dalla massa della fase stazionaria (in g) W S, dalla temperatura con j = 3 2 p i p p i p della colonna T (in K): V g = V N W S 273 T È meno influenzato dalle condizioni di analisi, ma spesso si preferisce impiegare V R o valori di ritenzione relativi. Gascromatografia: ritenzione e coefficiente di partizione 13
14 La separazione in fase gassosa B H = C M u + + C u S u B = 2 k D D M coefficiente di DIFFUSIONE LONGITUDINALE C M = f(d D 2, d c 2 ) D M coefficiente di TRASFERIMENTO DI MASSA "da e verso" la fase mobile C S = q k d 2 f 2 t (1+k) 2 D d k = S (1+k) 2 coefficiente di TRASFERIMENTO DI MASSA "da e verso" la fase stazionaria Variabili importanti per descrivere l efficienza delle colonne sono: Velocità lineare della fase mobile Coefficiente di diffusione nella f.m. Coefficiente di diffusione nella f.s. Diametro del materiale di impaccamento Spessore del rivestimento liquido della f.s. Tempo di desorbimento dell analita Diametro della colonna Fattore di ritenzione della sostanza Costanti Dipendenza funzionale ("funzione di") u D M D S d D d f t d d c k k D, q f N e H vengono impiegati per valutare l efficacia di separazione di diverse colonne. La diffusione longitudinale (B) è relativamente più rilevante in GC che in altre cromatografie (coefficiente diffusione nei gas circa volte maggiori che nei liquidi). Quindi il minimo nella funzione H(u) è più appiattito e posizionato verso velocità lineari più elevate. segue Gascromatografia: la separazione 14
15 Il potere risolvente di una colonna per uno specifico problema analitico può esser meglio descritto dalla efficienza di separazione (teoria dei piatti e modelli cinetici non bastano ). Si considerano le tensioni di vapore degli analiti e la loro interazione con la f.s.: considerando le leggi di Raoult e Henry, Herington ottenne la relazione seguente per descrivere l efficienza di separazione: V lg g2 = lg p 0 + lg γ V g1 p 0 2 γ 0 2 [A] = p A K H Legge di Henry : A dove: - [A] è la concentrazione del gas nel liquido, - p A è la pressione parziale del gas e - K AH è la costante di Henry che viene espressa in mol l -1 atm -1. Legge di Raoult: p A = X A p A dove (a una determinata T): - X A è la frazione molare di A nella fase liquida; - p A è la pressione parziale del gas e - p A0 è la pressione di vapore di A puro. Dove V g2 e V g1 sono volumi di ritenzione specifici per i componenti 1 e 2; p 10 componenti pure; 10 e 20 sono i coefficienti di attività a diluizione infinita. e p 20 sono le tensioni di vapore delle Se si ricercano i tempi di ritenzione necessari per separare i due costituenti, si applicano le seguenti relazioni: lg t R 2 lg p 0 + lg γ t R 1 p 0 2 γ 0 2 t R 2 p 0 1 p 0 γ 0 1 t R 1 2 γ 0 2 La separazione tra due sostanze è primariamente determinata dalle volatilità relative; le pressioni di vapore dipendono ovviamente da T. I coefficienti di attività sono espressione delle interazioni tra analiti e f.s. e determinano la selettività della fase stazionaria; sono disponibili circa 1000 diverse fasi liquide. Le differenze nelle pressioni di vapore sono alla base della separazione tra composti chimicamente correlati (serie omologhe); sostanze con stessa T eb, sono separabili in base a diversi coefficienti di attività. Gascromatografia: la separazione 15
16 La strumentazione La strumentazione può variare rispetto alle seguenti componenti: Tipo di carrier gas usato; Regolatore del gas; Sistema di iniezione del campione; Colonna cromatografica; Rivelatore Il flusso e le pressioni del carrier gas sono aggiustati con regolatori di flusso e pressione e il gas è diretto attraverso l iniettore alla colonna cromatografica. Il campione è introdotto in uno speciale iniettore o direttamente iniettato in colonna (i campioni liquidi vengono vaporizzati). Gli analiti sono separati nella colonna che è mantenuta in un forno a temperatura controllata. Usualmente si impiega un grandiente di temperatura per migliorare la separazione. La strumentazione moderna è controllata da computer. Gascromatografia: la strumentazione 16
17 Gas di trasporto Il gas di trasporto (carrier): ha come funzione principale trasferire gli analiti da iniettore a detector (passando attraverso la colonna); non deve interagire con le molecole del campione. In teoria qualsiasi gas inerte e sufficientemente puro (99.995%); le impurezze presenti possono essere H 2 O e O 2. In pratica si utilizza He o H 2 o N 2 ; Il gas viene flussato attraverso setacci molecolari o letto adsorbente per rimuovere H 2 O, prima di entrare nel sistema gascromatografico; Il flusso è assicurato dalla pressione in eccesso da una bombola, così che non sia necessaria una pompa. Il flusso deve essere costante per riproducibilità; Lavorando in condizioni isoterme, è sufficiente impostare la pressione dell alimentazione della colonna usando un riduttore di pressione a due stadi. Nel caso di un metodo a temperatura programmata, un regolatore di flusso dev essere aggiunto per tener conto dei cambiamenti della resistenza del fluido. Per misurare la velocità del flusso, all ingresso si può inserire un rotametro, o un flussimetro a bolle di sapone all uscita della colonna; Per colonne impaccate il flusso di gas di trasporto varia nell intervalllo tra 25 e 150 ml min -1, per capillari varia tra 1 e 25 ml min -1. segue Gascromatografia: gas di trasporto 17
18 Il gas di trasporto non influenza la selettività della separazione, B ma ha un effetto su risoluzione, tempo di analisi e sensibilità; H = C M u + + C u S u I parametri caratterizzanti il carrier gas sono: Massa molare che determina l effetto delle collisioni con le molecole di analita in fase gassosa. Se si ha MM elevata, le collisioni rallenteranno di più la migrazione degli analiti in colonna; essi stazioneranno per più tempo nella f.m. in colonna, il che aumenta la diffusione longitudinale e quindi l allargamento dei picchi. La densità di un gas (e quindi la pressione) ha un effetto simile. Maggiore la densità, maggiori le collisioni tra le molecole e l allargamento dei picchi. E opportuno mantenere la pressione più bassa possibile che però garantisca un flusso ragionevole di gas lungo la colonna; La viscosità del gas determina la minima pressione possibile applicabile al sistema. La pressione da utilizzare dipende anche dalla lunghezza e dal diametro interno della colonna. Si possono ottenere H (altezza piatti teorici) ottimali e simili con carrier gas diversi, ma i tempi di analisi cambiano. H(u) ha un minimo simile per He, H 2, N 2. Per He, H 2 si può aumentare u (velocità della fase mobile) con piccolo cambiamento di H (= aumento, cioè peggioramento della risoluzione). La separazione più veloce si ha con H 2, poiché possiede piccola MM e viscosità. Gascromatografia: gas di trasporto 18
19 Sistemi di iniezione del campione (liquido) Per l analisi quantitativa la scelta della tecnica e delle condizioni d iniezione può essere critica. Di solito nel GC vengono iniettati campioni liquidi e il liquido deve essere vaporizzato (o nell iniettore o nel primo tratto della colonna). Tipi di iniettore per campioni liquidi sono: split/splitless injector on-column injector programmable temperature injector Per colonne capillari i volumi di liquido iniettati maggiori. variano tra 0,5 e pochi μl, ma si possono anche iniettare volumi Per colonne impaccate i volumi sono dell ordine dei μl Per gas si impiegano sistemi di iniezione dedicati. Gascromatografia: sistemi iniezione 19
20 Iniezione in modalità split (I) Nell iniezione split solo una parte del campione è trasferita in colonna dal carrier gas.; la maggior parte è eliminata (venting) attraverso uno suddivisione del flusso (split) verso lo scarico. Il setto alla testa dell'iniettore è attraversato dalla siringa (a punta obliqua) che inietta il campione in un liner; Il campione viene vaporizzato all'interno del liner; Al fondo dell iniettore c è una valvola di splittaggio; Per un iniezione split, il campione è iniettato nel liner caldo dell iniettore, con la valvola di splittaggio aperta. La maggior parte del campione vaporizzato viene trasportato allo scarico, una piccola parte entra in colonna (20:1-100:1, misurato da flussi di carrier gas, di solito controllati tramite software o predisposti, nella vecchia strumentazione, tramite valvole manuali e uso di un flussimetro). Quando il solvente è iniettato, 1-2 μl di liquido formano μl di vapore, e cambiano la pressione all'interno dell'iniettore. Il quantitativo di vapore formatosi dipende dal volume iniettato e dal tipo di solvente. Gascromatografia: sistemi iniezione segue 20
21 Iniezione in modalità split (II) I parametri da ottimizzare/variabili: Temperatura dell'iniettore (es. tra 150 C e 250 C); Rapporto di splittaggio; Volume ed eventuali materiali di impaccamento (es. lana di vetro) nel liner; Pressione e velocità di flusso del gas di trasporto. Una temperatura elevata vaporizza rapidamente il campione; Per assicurare un evaporazione rapida e omogenea del campione in fondo al liner si pone della lana di vetro deattivata, per rallentare il liquido iniettato; Durante l iniezione la temperatura del forno che contiene la colonna deve essere sufficientemente elevata da impedire la ricondensazione del campione vaporizzato; L iniettore split genera picchi affilati ed è relativamente facile da impiegare; Non è ottimale per le analisi quantitative, in quanto il rapporto di split cambia anche con piccole variazioni nelle condizioni d iniezione; Componenti più volatili sono meglio trasferite in colonna rispetto a componenti meno volatili della miscela iniettata; Non è adeguato per effettuare analisi di composti in tracce (ppb). Gascromatografia: sistemi iniezione 21
22 Iniezione in modalità splitless L intero campione è trasferito in colonna (valvola di split chiusa durante l iniezione); La valvola è aperta dopo un tempo predeterminato (periodo splitless), che dipende da velocità e pressione del carrier gas, dal quantitativo di campione e dal tipo di solvente; Il trasferimento del vapore di solvente in colonna richiede del tempo, per cui l'intervallo di tempo di chiusura della valvola split dev essere tale da consentire che la maggior parte del campione passi in colonna (anche s per 1-2 μl). Poiché il trasferimento dei vapori richiede tempo, la zona in cui si trova il campione è ampia e richiede un processo di riconcentrazione: E' un ottimo sistema per effettuare analisi quantitativa anche di componenti in tracce (ppb) se gli analiti non sono molto volatili la riconcentrazione può essere effettuata mantenendo la temperatura del forno abbastanza bassa in modo che gli analiti rimangano intrappolati nella f.s. della colonna (ma T comunque sufficientemente alta da prevenire la ricondensazione in colonna); se gli analiti sono volatili la T del forno deve essere ancora più bassa per consentire la ricondensazione del solvente. Questo tipo di ricondensazione può essere utilizzata per riconcentrare gli analiti. Criticità: Effetto matrice: componenti non volatili presenti nella matrice possono disturbare il processo di vaporizzazione; Effetto memoria: è causato da costituenti rimasti nell iniettore da iniezioni precedenti che entrano in colonna generando "picchi fantasma" (cioè non relativi al campione che si sta analizzando in quel momento) Gascromatografia: sistemi iniezione 22
23 Liner per iniettori split/splitless Es. comparazione dell'utilizzo di un liner per iniezione split e uno per splitless in una iniezione di miscela di alcani in iniettore splitless. Si nota che la forma e l'altezza del picco del composto più volatile che eluisce per primo (t R più basso) è peggiore se si utilizza il liner non corretto (cioè per split) nella modalità splitless. Gascromatografia: sistemi iniezione 23
SCHEMA DI UN GASCROMATOGRAFO
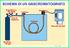 SCHEMA DI UN GASCROMATOGRAFO Regolatore a due Stadi Iniettore Rivelatore Gas di Trasporto Colonna Raccolta dei Dati Bombola del gas GC 2 14/15 1 REQUISITI DEL GAS DI TRASPORTO Filtro molecolare di 5 Angstrom
SCHEMA DI UN GASCROMATOGRAFO Regolatore a due Stadi Iniettore Rivelatore Gas di Trasporto Colonna Raccolta dei Dati Bombola del gas GC 2 14/15 1 REQUISITI DEL GAS DI TRASPORTO Filtro molecolare di 5 Angstrom
Chromatography is a mature technique now. Gary Christian, Analytical Chemistry,
 Chromatography is a mature technique now. Gary Christian, nalytical Chemistry, 6th Ed. (Wiley) Descrizione generale della cromatografia I metodi cromatografici sono accomunati dalla separazione di sostanze
Chromatography is a mature technique now. Gary Christian, nalytical Chemistry, 6th Ed. (Wiley) Descrizione generale della cromatografia I metodi cromatografici sono accomunati dalla separazione di sostanze
GASCROMATOGRAFIA INTRODUZIONE
 GASCROMATOGRAFIA INTRODUZIONE La Gascromatografia è una tecnica analitica utile per separare componenti o soluti di una miscela, sulla base delle quantità relative di ogni soluto, distribuite fra un carrier
GASCROMATOGRAFIA INTRODUZIONE La Gascromatografia è una tecnica analitica utile per separare componenti o soluti di una miscela, sulla base delle quantità relative di ogni soluto, distribuite fra un carrier
Cromatografia. cromatogramma
 Cromatografia Il termine cromatografia racchiude una serie di metodi analitici impiegati per separare e quantificare singolarmente i diversi componenti presenti in miscele di analiti anche molto complesse.
Cromatografia Il termine cromatografia racchiude una serie di metodi analitici impiegati per separare e quantificare singolarmente i diversi componenti presenti in miscele di analiti anche molto complesse.
INIETTORI PER COLONNE CAPILLARI
 INIETTORI PER COLONNE CAPILLARI Nessun tipo di iniettore è adatto per tutti i tipi di campioni gas, liquidi, solidi (% ppt.) Tutti gli iniettori hanno vantaggi e svantaggi Devono essere studiati e testati
INIETTORI PER COLONNE CAPILLARI Nessun tipo di iniettore è adatto per tutti i tipi di campioni gas, liquidi, solidi (% ppt.) Tutti gli iniettori hanno vantaggi e svantaggi Devono essere studiati e testati
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
La frazione lipidica TRIGLICERIDI
 Dott. Raffaele Marrone raffaele.marrone@unina.it La frazione lipidica TRIGLICERIDI 1 TRANSESTERIFICAZIONE reazione di sostituzione nucleofila GAS CROMATOGRAFIA La tecnica cromatografica consiste nello
Dott. Raffaele Marrone raffaele.marrone@unina.it La frazione lipidica TRIGLICERIDI 1 TRANSESTERIFICAZIONE reazione di sostituzione nucleofila GAS CROMATOGRAFIA La tecnica cromatografica consiste nello
GASCROMATOGRAFIA (UNA TECNICA DI SEPARAZIONE)
 GASCROMATOGRAFIA (UNA TECNICA DI SEPARAZIONE) Cromatografo Registratore Cromatogramma GC 1 14/15 1 COLONNE GC (IMPACCATE) Fase Mobile (Gas di trasporto) Supporto Solido Fase Stazionaria Liquida GC 1 14/15
GASCROMATOGRAFIA (UNA TECNICA DI SEPARAZIONE) Cromatografo Registratore Cromatogramma GC 1 14/15 1 COLONNE GC (IMPACCATE) Fase Mobile (Gas di trasporto) Supporto Solido Fase Stazionaria Liquida GC 1 14/15
cromatografia Esplorando le proteine
 Cromatografia Flavia Frabetti Tecnici di laboratorio 2010/2011 Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per
Cromatografia Flavia Frabetti Tecnici di laboratorio 2010/2011 Esplorando le proteine Un passaggio indispensabile negli studi di biochimica che necessitano di conoscere la sequenza aa di una proteina per
CROMATOGRAFIA DOTT. JOANNA IZABELA LACHOWICZ
 CROMATOGRAFIA DOTT. JOANNA IZABELA LACHOWICZ RISOLUZIONE DELLA COLONNA R= R= R= ΔZ ½(W A +W B ) 2ΔZ (W A +W B ) 2[(t R ) B (t R ) A ] (W A +W B ) RISOLUZIONE E PARAMETRI DELLA SEPARAZIONE ϒ- fattore della
CROMATOGRAFIA DOTT. JOANNA IZABELA LACHOWICZ RISOLUZIONE DELLA COLONNA R= R= R= ΔZ ½(W A +W B ) 2ΔZ (W A +W B ) 2[(t R ) B (t R ) A ] (W A +W B ) RISOLUZIONE E PARAMETRI DELLA SEPARAZIONE ϒ- fattore della
TIPI di CROMATOGRAFIA
 Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
Metodo di separazione che si basa sulla distribuzione degli analiti tra una fase mobile e una fase stazionaria. TIPI di CROMATOGRAFIA Eluizione degli analiti può avvenire: Capillarità Gravità Pressione
CHIMICA ANALITICA II CON LABORATORIO. (AA ) 8 C.F.U. - Laurea triennale in Chimica
 CHIMICA ANALITICA II CON LABORATORIO (AA 2018-19) 8 C.F.U. - Laurea triennale in Chimica 15 Il cromatogramma Principalmente per le cromatografie su colonna si usa la tecnica dell'eluizione (eluente è
CHIMICA ANALITICA II CON LABORATORIO (AA 2018-19) 8 C.F.U. - Laurea triennale in Chimica 15 Il cromatogramma Principalmente per le cromatografie su colonna si usa la tecnica dell'eluizione (eluente è
CHIMICA ANALITICA II CON LABORATORIO. (AA ) 8 C.F.U. - Laurea triennale in Chimica
 CHIMICA ANALITICA II CON LABORATORIO (AA 2016-17) 8 C.F.U. - Laurea triennale in Chimica 10 Fondamenti teorici / cromatografia su colonna Lo sviluppo di un cromatogramma Tecnica di eluizione (eluente è
CHIMICA ANALITICA II CON LABORATORIO (AA 2016-17) 8 C.F.U. - Laurea triennale in Chimica 10 Fondamenti teorici / cromatografia su colonna Lo sviluppo di un cromatogramma Tecnica di eluizione (eluente è
CHIMICA ANALITICA II CON LABORATORIO. (AA ) 8 C.F.U. - Laurea triennale in Chimica
 CHIMICA ANALITICA II CON LABORATORIO (AA 2016-17) 8 C.F.U. - Laurea triennale in Chimica 11 Teoria della cromatografia Esaminiamo l effetto di allargamento dei picchi lungo la colonna; l ampiezza del picco
CHIMICA ANALITICA II CON LABORATORIO (AA 2016-17) 8 C.F.U. - Laurea triennale in Chimica 11 Teoria della cromatografia Esaminiamo l effetto di allargamento dei picchi lungo la colonna; l ampiezza del picco
Esercitazione 4: determinazione della concentrazione di sodio e potassio nelle urine mediante spettroscopia di emissione in fiamma
 Esercitazione 4: determinazione della concentrazione di sodio e potassio nelle urine mediante spettroscopia di emissione in fiamma Apparato strumentale Sodio e potassio vengono determinati in campioni
Esercitazione 4: determinazione della concentrazione di sodio e potassio nelle urine mediante spettroscopia di emissione in fiamma Apparato strumentale Sodio e potassio vengono determinati in campioni
Cromatografia liquida ad alta risoluzione HPLC
 Cromatografia liquida ad alta risoluzione HPLC LC classica HPLC (fase La moderna cromatografia in fase liquida, confrontata con la tecnica classica, è caratterizzata da: -colonne di diametro Inferiore
Cromatografia liquida ad alta risoluzione HPLC LC classica HPLC (fase La moderna cromatografia in fase liquida, confrontata con la tecnica classica, è caratterizzata da: -colonne di diametro Inferiore
TERMODINAMICA. t R = t M + t R. t R = t M (1 +k) t R = t M (1 +K c /β) GC 3 14/15 1
 TERMODINAMICA t R = t M + t R t R = t M (1 +k) t R = t M (1 +K c /β) GC 3 14/15 1 t O ALLARGAMENTO DELLA BANDA (H) t 1 t Iniziale A metà Alla fine GC 3 14/15 HETP Colonne Impaccate (VanDeemter - 1956):
TERMODINAMICA t R = t M + t R t R = t M (1 +k) t R = t M (1 +K c /β) GC 3 14/15 1 t O ALLARGAMENTO DELLA BANDA (H) t 1 t Iniziale A metà Alla fine GC 3 14/15 HETP Colonne Impaccate (VanDeemter - 1956):
ISIS A PONTI Gallarate
 4 A TCB 1 IL CROMATOGRAMMA: E il tracciato che descrive l andamento del segnale del rivelatore in funzione del tempo o del volume di eluente a partire dall istante in cui la miscela viene introdotta nella
4 A TCB 1 IL CROMATOGRAMMA: E il tracciato che descrive l andamento del segnale del rivelatore in funzione del tempo o del volume di eluente a partire dall istante in cui la miscela viene introdotta nella
Sostanze non volatili possono essere derivatizzate
 Gascromatografia Permette la separazione di sostanze gassose o gassificabili variando la temperatura. Sono sostanze a basso peso molecolare, di natura poco polare, assolutamente non ionica. Eventualmente
Gascromatografia Permette la separazione di sostanze gassose o gassificabili variando la temperatura. Sono sostanze a basso peso molecolare, di natura poco polare, assolutamente non ionica. Eventualmente
Gas-cromatografia. onna.
 Gas-cromatografia La fase mobile è un gas. Le sostanze da separare (liquidi, solidi, gas) devono essere portate ad una temperatura sufficiente a renderle gassose o comunque portarle allo stato di vapore.
Gas-cromatografia La fase mobile è un gas. Le sostanze da separare (liquidi, solidi, gas) devono essere portate ad una temperatura sufficiente a renderle gassose o comunque portarle allo stato di vapore.
CHIMICA ANALITICA II CON LABORATORIO. (AA ) 8 C.F.U. - Laurea triennale in Chimica
 CHIMICA ANALITICA II CON LABORATORIO (AA 2018-19) 8 C.F.U. - Laurea triennale in Chimica 14 INTRODUZIONE ALLA CROMATOGRAFIA INTRODUZIONE Le tecniche di separazione cromatografica sono state all'inizio
CHIMICA ANALITICA II CON LABORATORIO (AA 2018-19) 8 C.F.U. - Laurea triennale in Chimica 14 INTRODUZIONE ALLA CROMATOGRAFIA INTRODUZIONE Le tecniche di separazione cromatografica sono state all'inizio
ESTRAZIONE PURIFICAZIONE. Modificazione chimica ANALISI STRUMENTALE
 Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
Procedura per l analisi quali/quantitativa. Analita puro Composto di riferimento Curva di calibrazione Singolo-Più punti Campione biologico ESTRAZIONE PURIFICAZIONE Modificazione chimica ANALISI STRUMENTALE
ANALISI QUALITATIVA E QUANTITATIVA
 ANALISI QUALITATIVA E QUANTITATIVA 1. QUALITATIVA - Cosa è presente Cromatografia- comparare i t R s Spettroscopia - MS, IR, UV 2. QUANTITATIVA - Quantità presente nel campione Altezza del picco Area del
ANALISI QUALITATIVA E QUANTITATIVA 1. QUALITATIVA - Cosa è presente Cromatografia- comparare i t R s Spettroscopia - MS, IR, UV 2. QUANTITATIVA - Quantità presente nel campione Altezza del picco Area del
Chi siamo? Missione: semplificare la tecnica GC e portarla in reparto
 Chi siamo? Dal 1989 produce GC da processo Ambientale per analisi VOC in emissione/immisione Converting: Sicurezza nelle macchine da stampa, LEL Gestione ricircolo dell aria e recupero energetico Controllo
Chi siamo? Dal 1989 produce GC da processo Ambientale per analisi VOC in emissione/immisione Converting: Sicurezza nelle macchine da stampa, LEL Gestione ricircolo dell aria e recupero energetico Controllo
2 ZEPPA G. BELVISO S.
 Appunti di Tecniche avanzate per il controllo degli alimenti Parte 2 ZEPPA G. BELVISO S. Università degli Studi di Torino Il termine cromatografia indica un insieme di tecniche che hanno lo scopo di separare
Appunti di Tecniche avanzate per il controllo degli alimenti Parte 2 ZEPPA G. BELVISO S. Università degli Studi di Torino Il termine cromatografia indica un insieme di tecniche che hanno lo scopo di separare
TIPI DI CROMATOGRAFIE
 Corso di Chimica Analitica TIPI DI CROMATOGRAFIE Prof. Paola Gramatica Fasi in successione: 2) Separazione dei componenti la miscela Dopo l isolamento della miscela da analizzare, se ne devono separare
Corso di Chimica Analitica TIPI DI CROMATOGRAFIE Prof. Paola Gramatica Fasi in successione: 2) Separazione dei componenti la miscela Dopo l isolamento della miscela da analizzare, se ne devono separare
1 INTRODUZIONE 1.1 La cromatografia [1]
![1 INTRODUZIONE 1.1 La cromatografia [1] 1 INTRODUZIONE 1.1 La cromatografia [1]](/thumbs/63/48965705.jpg) 1 INTRODUZIONE 1.1 La cromatografia [1] Con il termine cromatografia s intende un processo chimico-fisico che permette di separare le molecole di una miscela. Il principio base della cromatografia è l'equilibrio
1 INTRODUZIONE 1.1 La cromatografia [1] Con il termine cromatografia s intende un processo chimico-fisico che permette di separare le molecole di una miscela. Il principio base della cromatografia è l'equilibrio
CORSO ANALISI CHIMICA Cromatografia: parametri U.D.2 ITIS VIOLA A.S. 2016/2017 CROMATOGRAFIA. PARTE GENERALE: parametri
 CROMATOGRAFIA PARTE GENERALE: parametri Schema Dalla combinazione dei meccanismi e dei supporti, si possono avere numerose varianti di tecniche cromatografiche 2 RIPASSO 1. Descrivi cosa si intente per
CROMATOGRAFIA PARTE GENERALE: parametri Schema Dalla combinazione dei meccanismi e dei supporti, si possono avere numerose varianti di tecniche cromatografiche 2 RIPASSO 1. Descrivi cosa si intente per
TECNICHE CROMATOGRAFICHE
 TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
TECNICHE CROMATOGRAFICHE Le tecniche cromatografiche permettono di separare gli analiti presenti in una miscela complessa. Tutti i sistemi cromatografici sono costituiti da una fase stazionaria, che puo
CROMATOGRAFIA IONICA (IC)
 CROMATOGRAFIA IONICA (IC) CROMATOGRAFIA CROMATOGRAFIA IONICA RESINE A SCAMBIO IONICO Struttura Meccanismo di scambio STRUMENTAZIONE IC SOPPRESSORE A MEMBRANA PROTOCOLLO DI ANALISI CROMATOGRAFIA Analisi
CROMATOGRAFIA IONICA (IC) CROMATOGRAFIA CROMATOGRAFIA IONICA RESINE A SCAMBIO IONICO Struttura Meccanismo di scambio STRUMENTAZIONE IC SOPPRESSORE A MEMBRANA PROTOCOLLO DI ANALISI CROMATOGRAFIA Analisi
FARMAFFARI Via Cascina Venina, 7 ASSAGO (MI) / Via C.Conti Rossini, 26 ROMA Telefono
 RELAZIONE TECNICA Caratterizzazione chimico fisica di un filtro per sigaretta (dispositivo SMOKAT) (brevetto n. BO2014A000560 102014902301094-102017000039687) Introduzione Il dispositivo SMOKAT è oggetto
RELAZIONE TECNICA Caratterizzazione chimico fisica di un filtro per sigaretta (dispositivo SMOKAT) (brevetto n. BO2014A000560 102014902301094-102017000039687) Introduzione Il dispositivo SMOKAT è oggetto
Università degli Studi di Urbino
 Università degli Studi di Urbino Facoltà di Scienze e Tecnologie Effetto della temperatura nella preparazione e nell'uso di nano-colonne HPLC di Fabiana Capriotti Relatore: Achille Cappiello A. A. 2008-09
Università degli Studi di Urbino Facoltà di Scienze e Tecnologie Effetto della temperatura nella preparazione e nell'uso di nano-colonne HPLC di Fabiana Capriotti Relatore: Achille Cappiello A. A. 2008-09
fase stazionaria fase mobile
 Cromatografia Insieme di tecniche che hanno lo scopo di separare una miscela nei suoi componenti, per permetterne il riconoscimento qualitativo e quantitativo. Sono basate sulla distribuzione dei vari
Cromatografia Insieme di tecniche che hanno lo scopo di separare una miscela nei suoi componenti, per permetterne il riconoscimento qualitativo e quantitativo. Sono basate sulla distribuzione dei vari
CROMATOGRAFIA. Tecniche di purificazione
 CROMATOGRAFIA Tecniche di purificazione La cromatografia è tra i metodi fisici più impiegati per la separazione e la purificazione dei composti organici. Principio base (valido per tutte le tecniche cromatografiche)
CROMATOGRAFIA Tecniche di purificazione La cromatografia è tra i metodi fisici più impiegati per la separazione e la purificazione dei composti organici. Principio base (valido per tutte le tecniche cromatografiche)
Introduzione alla Chimica Analitica
 Corso di Chimica Ambientale Introduzione alla Chimica Analitica Prof. Paola Gramatica http://dipbsf.uninsubria.it/qsar dipbsf.uninsubria.it/qsar/ Education paola.gramatica @ uninsubria.it Prof. Paola Gramatica
Corso di Chimica Ambientale Introduzione alla Chimica Analitica Prof. Paola Gramatica http://dipbsf.uninsubria.it/qsar dipbsf.uninsubria.it/qsar/ Education paola.gramatica @ uninsubria.it Prof. Paola Gramatica
ESERCIZI GASCROMATOGRAFIA
 ESERCIZI GASCROMATOGRAFIA A SPUNTI DI RIFLESSIONE 1. Che cosa si intende per sililazione di un supporto a base di gel di silice e quali sono i vantaggi che derivano da tale trattamento? 2. Spiegare per
ESERCIZI GASCROMATOGRAFIA A SPUNTI DI RIFLESSIONE 1. Che cosa si intende per sililazione di un supporto a base di gel di silice e quali sono i vantaggi che derivano da tale trattamento? 2. Spiegare per
CROMATOGRAFIA DOTT. JOANNA IZABELA LACHOWICZ
 CROMATOGRAFIA DOTT. JOANNA IZABELA LACHOWICZ Soltanto 23% delle sostanze possono essere separate nella GC Usando liquidi possiamo aumentare uso della cromatografia TIPI DI CROMATOGRAFIA RIPARTIZIONE
CROMATOGRAFIA DOTT. JOANNA IZABELA LACHOWICZ Soltanto 23% delle sostanze possono essere separate nella GC Usando liquidi possiamo aumentare uso della cromatografia TIPI DI CROMATOGRAFIA RIPARTIZIONE
La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione.
 Tecniche di analisi chimica Prof. Marcello Romagnoli Titolazione La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione. Una quantità nota del
Tecniche di analisi chimica Prof. Marcello Romagnoli Titolazione La titolazione è un metodo di analisi chimica per la misura della concentrazione di una data sostanza in soluzione. Una quantità nota del
L approccio analitico
 L approccio analitico la sequenza analitica Estrazione della frazione aromatica Introduzione in un sistema cromatografico Separazione dei composti dell aroma Riconoscimento e quantificazione L approccio
L approccio analitico la sequenza analitica Estrazione della frazione aromatica Introduzione in un sistema cromatografico Separazione dei composti dell aroma Riconoscimento e quantificazione L approccio
!"#$%&'"($%)*+%(,-#$*+*%(+"..*%/0".1&"%/"##*%',#&2$,3$%,+-"3$.4*
 !"#$%&'"($%)*+%(,-#$*+*%(+"..*%/0".1&"%/"##*%',#&2$,3$%,+-"3$.4* Filtrazione nel pallone ed evaporazione del solvente tramite rotavapor Cromatografia 5%6*(,/$%.+,6"(,-+"7$.$%8*3-,3,%&($#$22"($%)*+%#"%'*)"+"2$,3*%*%)&+$7$."2$,3*%/*$%.,6),'($%,+-"3$.$%9"'"3/,'$%'&##"%/$'(+$9&2$,3*%'*#*(($8"%/$%&3"%,%)$:%','("32*%(+"%/&*%7"'$;!Fase
!"#$%&'"($%)*+%(,-#$*+*%(+"..*%/0".1&"%/"##*%',#&2$,3$%,+-"3$.4* Filtrazione nel pallone ed evaporazione del solvente tramite rotavapor Cromatografia 5%6*(,/$%.+,6"(,-+"7$.$%8*3-,3,%&($#$22"($%)*+%#"%'*)"+"2$,3*%*%)&+$7$."2$,3*%/*$%.,6),'($%,+-"3$.$%9"'"3/,'$%'&##"%/$'(+$9&2$,3*%'*#*(($8"%/$%&3"%,%)$:%','("32*%(+"%/&*%7"'$;!Fase
CROMATOGRAFIA. Definizioni
 CROMATOGRAFIA Definizioni La cromatografia è una tecnica che permette di separare ed analizzare (sia per scopi qualitativi che quantitativi) miscele incognite liquide o gassose. Tutte le tecniche cromatografiche
CROMATOGRAFIA Definizioni La cromatografia è una tecnica che permette di separare ed analizzare (sia per scopi qualitativi che quantitativi) miscele incognite liquide o gassose. Tutte le tecniche cromatografiche
CROMATOGRAFIA. Cromatografia su colonna classica
 CROMATOGRAFIA Michail Semenovich Tswett (1872-1919), botanico russo, studioso dei pigmenti vegetali Miscela di idrocarburi Carbonato di calcio Esperimento fondamentale Fase 1: il campione viene caricato
CROMATOGRAFIA Michail Semenovich Tswett (1872-1919), botanico russo, studioso dei pigmenti vegetali Miscela di idrocarburi Carbonato di calcio Esperimento fondamentale Fase 1: il campione viene caricato
IL PROBLEMA ANALITICO
 IL PROBLEMA ANALITICO COSA CERCARE? COME TROVARLO? 1. TRATTAMENTO CAMPIONE 2. ESTRAZIONE 3. PURIFICAZIONE 4. DETERMINAZIONE QUALI-QUANTITATIVA STORIA Cromatografia = colore + grafia 1906 Michael Tswett,
IL PROBLEMA ANALITICO COSA CERCARE? COME TROVARLO? 1. TRATTAMENTO CAMPIONE 2. ESTRAZIONE 3. PURIFICAZIONE 4. DETERMINAZIONE QUALI-QUANTITATIVA STORIA Cromatografia = colore + grafia 1906 Michael Tswett,
Abbiamo visto che per efficienza di una colonna si intende la sua capacità di mantenere compatti i picchi lungo il percorso e quindi all uscita.
 Cromatografia 4 1 Abbiamo visto che per efficienza di una colonna si intende la sua capacità di mantenere compatti i picchi lungo il percorso e quindi all uscita. Tale grandezza, in omaggio al parallelismo
Cromatografia 4 1 Abbiamo visto che per efficienza di una colonna si intende la sua capacità di mantenere compatti i picchi lungo il percorso e quindi all uscita. Tale grandezza, in omaggio al parallelismo
Introduzione all analisi cromatografica
 Introduzione all analisi cromatografica La cromatografia La cromatografia è un metodo analitico largamente utilizzato per la separazione, l identificazione e la determinazione quantitativa dei componenti
Introduzione all analisi cromatografica La cromatografia La cromatografia è un metodo analitico largamente utilizzato per la separazione, l identificazione e la determinazione quantitativa dei componenti
CROMATOGRAFIA. Principio. Promemoria! I componenti di una miscela sono separati
 CROMATOGRAFIA Principio I componenti di una miscela sono separati Promemoria! Dopo la separazione, i componenti raggiungono un rivelatore che dà luogo ad un segnale proporzionale alla loro concentrazione.
CROMATOGRAFIA Principio I componenti di una miscela sono separati Promemoria! Dopo la separazione, i componenti raggiungono un rivelatore che dà luogo ad un segnale proporzionale alla loro concentrazione.
IL CROMATOGRAMMA. I parametri fondamentali del cromatogramma. Costante di distribuzione o coefficiente di distribuzione
 IL CROMATOGRAMMA Tutte le tecniche cromatografiche, ad eccezione della cromatografia su colonna a bassa pressione e della TLC, si concludono con la registrazione di un cromatogramma, cioè di un tracciato
IL CROMATOGRAMMA Tutte le tecniche cromatografiche, ad eccezione della cromatografia su colonna a bassa pressione e della TLC, si concludono con la registrazione di un cromatogramma, cioè di un tracciato
CROMATOGRAFIA E SPETTROMETRIA DI MASSA DI COMPOSTI ORGANICI
 DIPARTIMENTO DI SCIENZE CHIMICHE Corso di laurea magistrale in Chimica organica e bioorganica Anno accademico 2017/2018-1 anno CROMATOGRAFIA E SPETTROMETRIA DI MASSA DI COMPOSTI ORGANICI CHIM/06-6 CFU
DIPARTIMENTO DI SCIENZE CHIMICHE Corso di laurea magistrale in Chimica organica e bioorganica Anno accademico 2017/2018-1 anno CROMATOGRAFIA E SPETTROMETRIA DI MASSA DI COMPOSTI ORGANICI CHIM/06-6 CFU
SERATE CHIMICHE - Cromatografia - Chimica Analitica
 SERATE CHIMICHE - Cromatografia - Chimica Analitica CROMATOGRAFIA Introduzione e accenni Storici La cromatografia è una tecnica di separazione, che permette di dividere i vari componenti di una miscela
SERATE CHIMICHE - Cromatografia - Chimica Analitica CROMATOGRAFIA Introduzione e accenni Storici La cromatografia è una tecnica di separazione, che permette di dividere i vari componenti di una miscela
3021 Ossidazione dell antracene ad antrachinone
 ssidazione dell antracene ad antrachinone Ce IV (NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Riferimento in letteratura: Tse-Lok Ho et al., Synthesis 97, 6; Classificazione Tipo di reazione e classi
ssidazione dell antracene ad antrachinone Ce IV (NH ) (N ) 6 C H CeH 8 N 8 8 C H 8 (78.) (58.) (8.) Riferimento in letteratura: Tse-Lok Ho et al., Synthesis 97, 6; Classificazione Tipo di reazione e classi
Analisi Chimica Relazione
 Titolo Sbarbada Davide 5 /CH I.S.I.I. Marconi -PC- Pagina 1 di 6 05/04/2006 Gascromatografia Obiettivo Analisi Chimica Relazione Effettuare l analisi di una miscela di alcoli mediante gascromatografia
Titolo Sbarbada Davide 5 /CH I.S.I.I. Marconi -PC- Pagina 1 di 6 05/04/2006 Gascromatografia Obiettivo Analisi Chimica Relazione Effettuare l analisi di una miscela di alcoli mediante gascromatografia
TRADUZIONE DEL METODO HJ PER INTUVO
 TRADUZIONE DEL METODO HJ679-2013 PER INTUVO Traduzione di un metodo per colonne con d.i. di 530 µm in metodi per colonne da 250 µm o da 320 µm per il sistema GC Agilent Intuvo 9000 Introduzione Il metodo
TRADUZIONE DEL METODO HJ679-2013 PER INTUVO Traduzione di un metodo per colonne con d.i. di 530 µm in metodi per colonne da 250 µm o da 320 µm per il sistema GC Agilent Intuvo 9000 Introduzione Il metodo
con C A concentrazione del gas disciolto La PA è quindi funzione lineare della concentrazione. La pressione parziale è: P A = Y * Ptot.
 ASSORBIMENTO E una operazione unitaria la cui finalità è l eliminazione di un soluto volatile contenuto in una miscela gassosa. Il solvente liquido scende dall alto mentre la miscela gassosa entra dal
ASSORBIMENTO E una operazione unitaria la cui finalità è l eliminazione di un soluto volatile contenuto in una miscela gassosa. Il solvente liquido scende dall alto mentre la miscela gassosa entra dal
Sviluppo e convalida di un metodo analitico
 Sviluppo e convalida di un metodo analitico Sviluppo del metodo analitico Esistono molteplici ragioni per lo sviluppo di un nuovo metodo analitico tra cui: mancanza di un metodo per l analisi di un determinato
Sviluppo e convalida di un metodo analitico Sviluppo del metodo analitico Esistono molteplici ragioni per lo sviluppo di un nuovo metodo analitico tra cui: mancanza di un metodo per l analisi di un determinato
2. SISTEMA DI PURIFICAZIONE CROMATOGRAFICA A MEDIA PRESSIONE (Biotage).
 1. APPARECCHIO PER REAZIONI A MICROONDE (Cem). Apparecchio per reazioni a microonde con sistema di sfiato automatico delle sovrappressioni, che consente di condurre reazioni che superano i 300 psi (20
1. APPARECCHIO PER REAZIONI A MICROONDE (Cem). Apparecchio per reazioni a microonde con sistema di sfiato automatico delle sovrappressioni, che consente di condurre reazioni che superano i 300 psi (20
PROPRIETÁ DEI LIQUIDI
 PROPRIETÁ DEI LIQUIDI Viscosità: resistenza di un fluido al flusso, ossia scorrimento relativo delle molecole Una semplice misura (indiretta) è il tempo di efflusso di un dato volume di liquido attraverso
PROPRIETÁ DEI LIQUIDI Viscosità: resistenza di un fluido al flusso, ossia scorrimento relativo delle molecole Una semplice misura (indiretta) è il tempo di efflusso di un dato volume di liquido attraverso
DICLOROMETANO (METILENE CLORURO) urinario in GC/MS spazio di testa Codice GC18010
 DICLOROMETANO (METILENE CLORURO) urinario in GC/MS spazio di testa Codice GC18010 BIOCHIMICA Il diclorometano (o cloruro di metilene) è un composto chimico appartenente alla categoria degli alogenuri alchilici.
DICLOROMETANO (METILENE CLORURO) urinario in GC/MS spazio di testa Codice GC18010 BIOCHIMICA Il diclorometano (o cloruro di metilene) è un composto chimico appartenente alla categoria degli alogenuri alchilici.
In laboratorio si devono osservare delle norme necessarie ad evitare incidenti che talvolta possono rivelarsi estremamente pericolosi.
 In laboratorio si devono osservare delle norme necessarie ad evitare incidenti che talvolta possono rivelarsi estremamente pericolosi. 1. E ovviamente vietato fumare. 2. Non distrarsi in nessun caso, nè
In laboratorio si devono osservare delle norme necessarie ad evitare incidenti che talvolta possono rivelarsi estremamente pericolosi. 1. E ovviamente vietato fumare. 2. Non distrarsi in nessun caso, nè
Scelta della matrice e prelievo del campione. Laboratorio. Preparazione del campione. Separazione delle sostanze in esame. Trattamento pre-analisi
 Scelta della matrice e prelievo del campione Laboratorio Preparazione del campione Separazione delle sostanze in esame Trattamento pre-analisi Analisi strumentale Valutazione critica del risultato aggiunta
Scelta della matrice e prelievo del campione Laboratorio Preparazione del campione Separazione delle sostanze in esame Trattamento pre-analisi Analisi strumentale Valutazione critica del risultato aggiunta
Un modello per il gas ideale
 Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
Un modello per il gas ideale Un gas ideale consiste di particelle (atomi o molecole) che hanno le seguenti proprietà 1. Il volume proprio delle particelle è trascurabile rispetto al volume occupato dal
14. Transizioni di Fase_a.a. 2009/2010 TRANSIZIONI DI FASE
 TRANSIZIONI DI FASE Fase: qualsiasi parte di un sistema omogenea, di composizione chimica costante e in un determinato stato fisico. Una fase può avere le stesse variabili intensive (P, T etc) ma ha diverse
TRANSIZIONI DI FASE Fase: qualsiasi parte di un sistema omogenea, di composizione chimica costante e in un determinato stato fisico. Una fase può avere le stesse variabili intensive (P, T etc) ma ha diverse
Il riscaldamento può essere effettuato con un bagno ad acqua, ad olio, un mantello scaldante, tenendo in considerazione che deve essere effettuato
 DISTILLAZIONE La distillazione è una tecnica di purificazione che permette la separazione di liquidi o di solidi bassofondenti che fondono senza alterazione chimica. Si basa fondamentalmente sull equilibrio
DISTILLAZIONE La distillazione è una tecnica di purificazione che permette la separazione di liquidi o di solidi bassofondenti che fondono senza alterazione chimica. Si basa fondamentalmente sull equilibrio
H.P.L.C. High Performance Liquid Chromatography
 Lezione 16 14.12.2015 H.P.L.C. High Performance Liquid Chromatography cromatografia liquida fase mobile allo stato liquido strumento costituito da: 1) riserva di fase mobile 2) filtro 3) sistema di pompaggio
Lezione 16 14.12.2015 H.P.L.C. High Performance Liquid Chromatography cromatografia liquida fase mobile allo stato liquido strumento costituito da: 1) riserva di fase mobile 2) filtro 3) sistema di pompaggio
Distribuzione e Temperatura. Pressione di Vapore. Evaporazione
 Evaporazione Le molecole del Liquido hanno una distribuzione di energia cinetica. Una frazione di molecole della superficie del liquido ha energia cinetica sufficiente per sfuggire all attrazione attrazione
Evaporazione Le molecole del Liquido hanno una distribuzione di energia cinetica. Una frazione di molecole della superficie del liquido ha energia cinetica sufficiente per sfuggire all attrazione attrazione
REGISTRO DELLE LEZIONI 2005/2006. Tipologia. Addì Tipologia. Addì Tipologia
 Presentazione del corso. Modalità di svolgimento della prova di esame. Introduzione all'analisi organica qualitativa. Analisi organica qualitativa: comportamento alla calcinazione. Saggio di Laissagne
Presentazione del corso. Modalità di svolgimento della prova di esame. Introduzione all'analisi organica qualitativa. Analisi organica qualitativa: comportamento alla calcinazione. Saggio di Laissagne
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta)
 Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
Cromatografia Dal greco chroma : colore, graphein : scrivere 1903 Mikhail Twsett (pigmenti vegetali su carta) E il termine generico che indica una serie di tecniche di separazione di molecole simili in
GASCROMATOGRAFIA. 9 ottobre 2014 Giornata di Studio Sistemi di analisi
 GASCROMATOGRAFIA GASCROMATOGRAFIA Un Gascromatografo è un analizzatore basato su microprocessore che misura le concentrazioni di un ampia gamma di sostanze quali: idrocarburi, idrogeno, azoto, ossigeno,
GASCROMATOGRAFIA GASCROMATOGRAFIA Un Gascromatografo è un analizzatore basato su microprocessore che misura le concentrazioni di un ampia gamma di sostanze quali: idrocarburi, idrogeno, azoto, ossigeno,
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia. Corso di Analisi Chimico-Tossicologica.
 Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
Università Degli Studi di Cagliari Facoltà Farmacia Corso di laurea in Tossicologia Corso di Analisi Chimico-Tossicologica Distillazione La distillazione La distillazione consiste nel vaporizzare un liquido
PROPRIETA DELLE SOLUZIONI
 1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
1 11 PROPRIETA DELLE SOLUZIONI 2 SOLUZIONI IDEALI H mix = 0 le interazioni fra le molecole di soluto e di solvente puri sono paragonabili a quelle fra soluto e solvente; durante il processo di dissoluzione
S = f(c) c x = f -1 (s x )
 CHIMICA ANALITICA SI INTERESSA DI METODI STRUMENTI PER DETERMINARE LA COMPOSIZIONE CHIMICA DI UN SISTEMA. LESSICO ANALITA = SOSTANZA DA DETERMINARE (SPECIE). MATRICE = TUTTO IL RESTO DEL CAMPIONE INTERFERENTE
CHIMICA ANALITICA SI INTERESSA DI METODI STRUMENTI PER DETERMINARE LA COMPOSIZIONE CHIMICA DI UN SISTEMA. LESSICO ANALITA = SOSTANZA DA DETERMINARE (SPECIE). MATRICE = TUTTO IL RESTO DEL CAMPIONE INTERFERENTE
REGISTRO DELLE LEZIONI
 UNIVERSITÀ DEGLI STUDI DI GENOVA Dipartimento di Chimica e Chimica Industriale Corso di laurea in Chimica e Tecnologie Chimiche REGISTRO DELLE LEZIONI dell' INSEGNAMENTO o MODULO UFFICIALE Nome: CHIMICA
UNIVERSITÀ DEGLI STUDI DI GENOVA Dipartimento di Chimica e Chimica Industriale Corso di laurea in Chimica e Tecnologie Chimiche REGISTRO DELLE LEZIONI dell' INSEGNAMENTO o MODULO UFFICIALE Nome: CHIMICA
GLI STATI DI AGGREGAZIONE DELLA MATERIA. Lo stato liquido
 GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato liquido Lo stato liquido Liquidi: energia dei moti termici confrontabile con quella delle forze coesive. Limitata libertà di movimento delle molecole, che
GLI STATI DI AGGREGAZIONE DELLA MATERIA Lo stato liquido Lo stato liquido Liquidi: energia dei moti termici confrontabile con quella delle forze coesive. Limitata libertà di movimento delle molecole, che
A cura di P.I. Antonio Caprai e-mail: caprai@iirg.pi.cnr.it tel. ++39 050 3152391
 CONSIGLIO NAZIONALE DELLE RICERCHE ISTITUTO INTERNAZIONALE PER LE RICERCHE GEOTERMICHE 56127 PISA (Italy) Via G. Moruzzi, 1 - Tel. 0503152381 0503152383 0503152384 Fax 050312562322 05031562323 e-mail:
CONSIGLIO NAZIONALE DELLE RICERCHE ISTITUTO INTERNAZIONALE PER LE RICERCHE GEOTERMICHE 56127 PISA (Italy) Via G. Moruzzi, 1 - Tel. 0503152381 0503152383 0503152384 Fax 050312562322 05031562323 e-mail:
LA SPETTROMETRIA DI MASSA
 LA SPETTROMETRIA DI MASSA Tecnica che consente di caratterizzare e identificare composti sconosciuti e noti in base alla determinazione della loro massa molecolare e alla loro caratterizzazione strutturale
LA SPETTROMETRIA DI MASSA Tecnica che consente di caratterizzare e identificare composti sconosciuti e noti in base alla determinazione della loro massa molecolare e alla loro caratterizzazione strutturale
ACETATO DI METILE urinario in GC-FID Codice GC02510
 ACETATO DI METILE urinario in GC-FID Codice GC02510 BIOCHIMICA L acetato di metile, a temperatura ambiente si presenta come un liquido volatile e incolore; è un composto molto infiammabile ed irritante.
ACETATO DI METILE urinario in GC-FID Codice GC02510 BIOCHIMICA L acetato di metile, a temperatura ambiente si presenta come un liquido volatile e incolore; è un composto molto infiammabile ed irritante.
CROMATOGRAFIA. Michail Semenovich Tswett ( ), botanico russo, studioso dei pigmenti vegetali. Esperimento fondamentale. Carbonato di calcio
 CROMATOGRAFIA D.C. Harris, Elementi di chimica analitica, Zanichelli, 1 a ed. italiana, 1999, capitoli 16-18 R. Cozzi, P. Protti, T. Ruaro, Analisi Chimica Strumentale, Zanichelli, 1997, volume C. 1 Michail
CROMATOGRAFIA D.C. Harris, Elementi di chimica analitica, Zanichelli, 1 a ed. italiana, 1999, capitoli 16-18 R. Cozzi, P. Protti, T. Ruaro, Analisi Chimica Strumentale, Zanichelli, 1997, volume C. 1 Michail
Schema a blocchi di uno spettrofluorimetro
 MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
MONOCROMATORE EMISSIONE EM Schema a blocchi di uno spettrofluorimetro MONOCROMATORE ECCITAZIONE SORGENTE EXC RIVELATORE (TUBO FOTOMOLTIPLICATORE) Anche il DNA assorbe nell UV Cosa determina l assorbanza
Il diagramma di stato presenta una concavità verso il basso. Distillando miscele che si trovano a sinistra dell azeotropo, cioè più diluite, la
 Il diagramma di stato presenta una concavità verso il basso. Distillando miscele che si trovano a sinistra dell azeotropo, cioè più diluite, la distillazione procede sino al valore massimo di concentrazione
Il diagramma di stato presenta una concavità verso il basso. Distillando miscele che si trovano a sinistra dell azeotropo, cioè più diluite, la distillazione procede sino al valore massimo di concentrazione
Solventi (eluenti) per cromatografia :)"#$#%#*1#5"#%+!()*/$'"=%3.$#-.#5"#
 Solventi (eluenti) per cromatografia!"#$#%&'%(#"$)*')%+,'-.#*/%&'%'&$)./$01$'%/%0/--)%(2#23 4'.*)#-/5) 6#"$/.*)$1$)%&'%./$0)5') 6)*1#5# 4*)$)7)$,') 8'.*)$),#"/5) 8'#"'*%#"#$#!"'*#%/.#"/") 9.#")5# :'$'&'5/!"/5)*)
Solventi (eluenti) per cromatografia!"#$#%&'%(#"$)*')%+,'-.#*/%&'%'&$)./$01$'%/%0/--)%(2#23 4'.*)#-/5) 6#"$/.*)$1$)%&'%./$0)5') 6)*1#5# 4*)$)7)$,') 8'.*)$),#"/5) 8'#"'*%#"#$#!"'*#%/.#"/") 9.#")5# :'$'&'5/!"/5)*)
4013 Sintesi del benzalacetofenone da benzaldeide e acetofenone
 4013 Sintesi del benzalacetofenone da benzaldeide e acetofenone montmorillonite KSF/ + + H 2 C 8 H 8 C 7 H 6 C 15 H 12 (120.2) (106.1) (208.3) Classificazione Tipo di reazione e classi di sostanze Reazione
4013 Sintesi del benzalacetofenone da benzaldeide e acetofenone montmorillonite KSF/ + + H 2 C 8 H 8 C 7 H 6 C 15 H 12 (120.2) (106.1) (208.3) Classificazione Tipo di reazione e classi di sostanze Reazione
Estrazione con solvente 18/01/2010. Laboratorio di chimica. Prof. Aurelio Trevisi
 Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
Laboratorio di chimica Prof. Aurelio Trevisi Estrazione con solvente SCOPO: Estrarre mediante cicloesano lo iodio da una soluzione idroalcolica L estrazione con solventi si basa sulla diversa affinità
SCHEMA DI UN GASCROMATOGRAFO. He, Ar, N 2, H 2
 GASCROMATOGRAFIA La fase mobile è un gas. Le sostanze da separare (liquidi, solidi, gas) devono essere portate ad una temperatura sufficiente a renderle gassose o comunque portarle allo stato di vapore.
GASCROMATOGRAFIA La fase mobile è un gas. Le sostanze da separare (liquidi, solidi, gas) devono essere portate ad una temperatura sufficiente a renderle gassose o comunque portarle allo stato di vapore.
Seminario di Cacciatore Rosalia
 Un organismo vivente è un sistema chimico complesso nel quale la materia organica viene sintetizzata, riprodotta, trasformata e decomposta in un incessante ed intenso susseguirsi di reazioni e processi
Un organismo vivente è un sistema chimico complesso nel quale la materia organica viene sintetizzata, riprodotta, trasformata e decomposta in un incessante ed intenso susseguirsi di reazioni e processi
METILISOBUTILCHETONE (4 metil-2 pentanone) urinario in GC/MS spazio di testa Codice GC10510
 METILISOBUTILCHETONE (4 metil-2 pentanone) urinario in GC/MS spazio di testa Codice GC10510 BIOCHIMICA Il metilisobutilchetone è un liquido incolore ed infiammabile che viene utilizzato in laboratorio
METILISOBUTILCHETONE (4 metil-2 pentanone) urinario in GC/MS spazio di testa Codice GC10510 BIOCHIMICA Il metilisobutilchetone è un liquido incolore ed infiammabile che viene utilizzato in laboratorio
QUESTIONARIO TECNICO
 DIREZIONE GENERALE Via Caduti del Lavoro, 40 60131 ANCONA Tel. 071/2132720 - Fax 071/2132740 e-mail: arpam.direzionegenerale@ambiente.marche.it http://arpa.marche.it QUESTIONARIO TECNICO ALLEGATO D GASCROMATOGRAFO
DIREZIONE GENERALE Via Caduti del Lavoro, 40 60131 ANCONA Tel. 071/2132720 - Fax 071/2132740 e-mail: arpam.direzionegenerale@ambiente.marche.it http://arpa.marche.it QUESTIONARIO TECNICO ALLEGATO D GASCROMATOGRAFO
Fulvio Prof. Magni Corso di laurea di Tecnici di Laboratorio BioMedico III anno. Scopo
 Scienze Tecniche di Medicina e di Laboratorio Fulvio Prof. Magni Corso di laurea di Tecnici di Laboratorio BioMedico III anno Scopo Messa a punto di un metodo analitico per valutazioni: - Qualitative -
Scienze Tecniche di Medicina e di Laboratorio Fulvio Prof. Magni Corso di laurea di Tecnici di Laboratorio BioMedico III anno Scopo Messa a punto di un metodo analitico per valutazioni: - Qualitative -
CORSO DI CHIMICA. Esercitazione del 7 Giugno 2016
 CORSO DI CHIMICA Esercitazione del 7 Giugno 2016 25 ml di una miscela di CO e CO 2 diffondono attraverso un foro in 38 s. Un volume uguale di O 2 diffonde nelle stesse condizioni in 34,3 s. Quale è la
CORSO DI CHIMICA Esercitazione del 7 Giugno 2016 25 ml di una miscela di CO e CO 2 diffondono attraverso un foro in 38 s. Un volume uguale di O 2 diffonde nelle stesse condizioni in 34,3 s. Quale è la
PRINCIPIO DISTILLAZIONE
 DISTILLAZIONE Operazione unitaria di separazione più impiegata nell'industria. L'agente di separazione è il calore => non contamina la miscela da separare. PRINCIPIO Fornire calore a una miscela liquida
DISTILLAZIONE Operazione unitaria di separazione più impiegata nell'industria. L'agente di separazione è il calore => non contamina la miscela da separare. PRINCIPIO Fornire calore a una miscela liquida
AMPICILLINA SODICA PREPARAZIONE INIETTABILE. Ampicillina sodica polvere sterile per preparazioni iniettabili
 1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
1 0 1 0 1 0 1 0 1 001/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. La monografia è stata completamente revisionata per armonizzarla con le corrispondenti
1. Perché le sostanze si sciolgono?
 1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
1. Perché le sostanze si sciolgono? Le soluzioni sono miscugli omogenei i cui costituenti conservano le loro proprietà. Nelle soluzioni il solvente è il componente in maggiore quantità. Il soluto è il
La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici
 La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici Materia = tutto ciò che possiede una massa ed occupa uno spazio Energia =
La Termodinamica è la disciplina che si occupa dello studio degli scambi di energia e di materia nei processi fisici e chimici Materia = tutto ciò che possiede una massa ed occupa uno spazio Energia =
ACETONE Urinario in GC/MS spazio di testa Codice GC10110
 ACETONE Urinario in GC/MS spazio di testa Codice GC10110 BIOCHIMICA L acetone, o dimetil chetone, è un prodotto che rientra nella biochimica fisiologica: modeste quantità si formano come prodotto del metabolismo
ACETONE Urinario in GC/MS spazio di testa Codice GC10110 BIOCHIMICA L acetone, o dimetil chetone, è un prodotto che rientra nella biochimica fisiologica: modeste quantità si formano come prodotto del metabolismo
DIETILCHETONE (3-pentanone) Urinario in GC/MS spazio di testa Codice GC11010
 DIETILCHETONE (3-pentanone) Urinario in GC/MS spazio di testa Codice GC11010 BIOCHIMICA Il Dietilchetone è un liquido incolore ed infiammabile che viene utilizzato in laboratorio come solvente organico
DIETILCHETONE (3-pentanone) Urinario in GC/MS spazio di testa Codice GC11010 BIOCHIMICA Il Dietilchetone è un liquido incolore ed infiammabile che viene utilizzato in laboratorio come solvente organico
Capitolo 14 Le proprietà delle soluzioni
 Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
Capitolo 14 Le proprietà delle soluzioni 1. Perché le sostanze si sciolgono 2. Soluzioni acquose ed elettroliti 3. La concentrazione delle soluzioni 4. L effetto del soluto sul solvente: le proprietà colligative
AMOXICILLINA CAPSULE
 0 0 0 0 0 00/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. Caratteri: è stato inserito granulato di colore bianco o paglierino su informazioni di
0 0 0 0 0 00/FU Aprile 00 Commenti entro il Settembre 00 NOTA: Armonizzata con la versione revisionata della B.P. Caratteri: è stato inserito granulato di colore bianco o paglierino su informazioni di
Sommario della lezione 18. Proprietà colligative
 Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
Sommario della lezione 18 Proprietà colligative Interazioni soluto-solvente Interazioni soluto-solvente La solubilità di un soluto in un particolare solvente dipende da: la natura delle particelle di solvente
4004 Sintesi del gamma-decalattone da 1-ottene ed estere etilico dell acido iodoacetico
 4004 Sintesi del gamma-decalattone da 1-ottene ed estere etilico dell acido iodoacetico + I CH 2 CH 3 Cu + CH 3 CH 2 I C 8 H 16 C 4 H 7 I 2 C 10 H 18 2 (112.2) (214.0) (63.6) (170.3) C 2 H 5 I (156.0)
4004 Sintesi del gamma-decalattone da 1-ottene ed estere etilico dell acido iodoacetico + I CH 2 CH 3 Cu + CH 3 CH 2 I C 8 H 16 C 4 H 7 I 2 C 10 H 18 2 (112.2) (214.0) (63.6) (170.3) C 2 H 5 I (156.0)
La Concentrazione. C i = m i / M,
 La Concentrazione La concentrazione, C i, di un composto chimico i all interno di un sistema a più componenti, definisce il rapporto C i = m i / M, dove m i è la massa di i e M = ( i m i ) è la massa totale
La Concentrazione La concentrazione, C i, di un composto chimico i all interno di un sistema a più componenti, definisce il rapporto C i = m i / M, dove m i è la massa di i e M = ( i m i ) è la massa totale
