SPETTROSCOPIA DI RISONANZA MAGNETICA NULCEARE: H NMR
|
|
|
- Luisa Pasquali
- 5 anni fa
- Visualizzazioni
Transcript
1 SPETTROSCOPIA DI RISONANZA MAGNETICA NULCEARE: 1 H NMR
2 1x x10 14 Radio frequenze MHz 1
3 Tutti i nuclei possiedono una carica e in alcuni di essi questa carica, ruotando sull asse nucleare, produce un dipolo magnetico µ. Se il nucleo viene immerso in un campo magnetico esterno uniforme il nucleo può assumere diverse orientazioni
4 Stati nucleari di spin: ciascun nucleo che ha numero di massa (M) e/ o numero atomico (N) dispari è dotato di spin (il numero di spin I determina il numero di orientazioni (2I+1) che il nucleo può assumere in un campo magnetico esterno uniforme) 2I+1 1 H, 13 C, 31 P: M dispari I=1/2 12 C, 16 O, 32 S: M e N (6,8,16) pari I=0 2 H, 14 N: M pari, N (1,7) dispari I=1
5 Numeri di protoni pari dispari pari dispari Numero di neutroni pari dispari dispari pari I (numero di spin) 0 1 o 2 o 3 o. 1/2 o 3/2 o 5/2 o.. 1/2 o 3/2 o 5/2 o.. I = 0 il nucleo non possiede momento angolare, né momento magnetico: non dà spettri NMR
6
7 Il momento magnetico nucleare µ non è perfettamente allineato col campo, ma continua ad oscillare attorno al campo magnetico applicato Bo compiendo un moto di precessione simile a quello di una trottola.
8 La frequenza alla quale avviene la precessione è nota come frequenza di Larmor ν 0 = γb 0 /2π γ = rapporto giromagnetico dipende dal nucleo in esame Equazione fondamentale dell NMR ν = γ B 0 / 2π
9 ν 0 = γb 0 /2π E = hc = hν λ la frequenza di risonanza è direttamente proporzionale all energia
10 ν 0 = γb 0 /2π B 0 (Tesla) ν 1 H (MHz) ν 13 C (MHz)
11 Nucleo I µ γ (10 8 rad/ Ts) ν (MHz)* Abbondanza isotopica naturale 1 H 1/ C 1/ N F 1/ P 1/ *frequenze di risonanza NMR in un campo magnetico applicato di Tesla I= Numero quantico di spin µ = γih/2π momento magnetico nucleare γ = rapporto giromagnetico dipende dal nucleo in esame ν = γ B 0 /2π
12
13 Preparazione del campione Generalmente si opera in soluzione sciogliendo il campione (10-20 mg) in un opportuno solvente (0.6 ml). Si utilizzano solventi deuterati per non avere interferenze del solvente. Il solvente più comunemente usato è il CDCl 3. Possono essere usati anche acetone-d 6, benzene-d 6, metanolod 4 e D 2 O.
14 Tutti gli strumenti superiori ai 100MHz si basano su magneti superconduttori raffreddati ad elio e funzionano con la tecnica ad impulsi FT (Fourier Transform) Attualmente si usano spettrometri FT in cui il campione viene immerso in un campo magnetico intenso (9.4T 400MHZ) in modo da avere un elevato potere risolutivo e maggiore sensibilità. Il campione viene inserito tra le espansioni del magnete e tenuto in rotazione attorno al suo asse (~15giri/ s) per avere un campo omogeneo in tutto il campione.
15 FT NMR: tutte le frequenze della zona di interesse sono irradiate contemporaneamente Si opera con la tecnica degli impulsi in un determinato intervallo di tempo. In questo modo si riesce ad irradiare l intero intervallo di frequenze desiderato. Al termine dell impulso i nuclei ritornano allo stato fondamentale emettendo radiofrequenze caratteristiche. Il segnale che si ottiene è il FID (Free Induction Decay) il quale viene convertito mediante l operazione matematica della trasformata di Fourier nello spettro NMR.
16 CHEMICAL SHIFT Fino a questo punto saremmo portati a credere che per ogni tipo di nucleo ci sia UNA SOLA frequenza di risonanza, definita dalla relazione: ν 1 = γ B 0 / 2π Se fosse cosi, l NMR non sarebbe poi tanto interessante per il chimico. Ma, avendo a che fare con molecole e non con nuclei isolati, le frequenze di risonanza sono fortemente influenzate dagli atomi e dagli elettroni vicini al nucleo in esame. In altri termini: NUCLEI CON DIVERSO INTORNO CHIMICO HANNO FREQUENZE DI RISONANZA DIVERSE. L importanza dell NMR non e quindi nell abilita di differenziare tra diversi elementi, ma tra nuclei che abbiano intorni chimici differenti.
17 CHEMICAL SHIFT In una molecola gli H sono circondati da elettroni e la loro circolazione crea un campo magnetico opposto a B 0 e quindi scherma il nucleo. Il grado di schermatura dipende da diversi fattori ð diverse frequenze di risonanza per nuclei in intorni chimici diversi. Le differenze di frequenza ( Hz) sono dell ordine di 1 ppm se si confrontano con la frequenza con cui viene irradiato (400 MHz) e pertanto è conveniente riferirlo ad un composto standard. Caratteristiche dello standard: ð Contenere nuclei magnetici di un solo tipo, con lo stesso intorno elettronico, in modo che il suo spettro NMR consista in una sola linea. ð Contenere molti nuclei dello stesso tipo in modo da avere un segnale intenso anche quando è in piccola quantità. ð Cadere in una regione dello spettro lontana. ð Essere chimicamente inerte.
18 il campo magnetico applicato causa un movimento degli elettroni nella nube elettronica, che produce un campo magnetico indotto che scherma il nucleo. L effetto schermante è tanto maggiore quanto maggiore è la densità elettronica intorno al nucleo. Perciò i protoni circondati da una alta densità elettronica risuonano a frequenza inferiore di protoni circondati da una bassa densità elettronica. ν eff = γ B 0 (1-σ) σ costante di schermo
19 Definizione di chemical shift Quello che è collegato alla struttura della molecola non è quindi la frequenza assoluta di risonanza (che dipende dal campo magnetico applicato), ma il chemical shift. Visto che il chemical shift è una differenza di frequenza, è necessaria una frequenza di riferimento rispetto a cui misurare la differenza. Come frequenza di riferimento si è scelta la frequenza di risonanza del tetrametilsilano (TMS) Il chemical shift è misurato rispetto al TMS
20 La scala dei δ Per rendere il chemical shift indipendente da B 0 si usa la scala dei δ, definita come nell equazione di seguito riportata. La differenza di frequenza è divisa per la frequenza assoluta, e poiché entrambe queste grandezze sono proporzionali a B 0, il loro rapporto è indipendente da B 0. Il fattore 10 6 è usato perché le variazioni di frequenza di risonanza sono molto piccole rispetto alle frequenze stesse.
21 La scala dei δ: esempio Consideriamo per esempio un protone che, in uno spettrometro in cui i protoni risuonano a 300 MHz, ha un chemical shift di 390 Hz. Lo stesso protone, in uno spettrometro con B 0 maggiore, in cui i protoni risuonano a 500 MHz, avrà un chemical shift di 650 Hz. Se usiamo la scala dei δ, vediamo che in entrambi i casi il chemical shift del protone sarà di 1.3 ppm.
22 Il chemical shift protonico La maggior parte dei protoni di una molecola organica risuonano in un intervallo di 10 ppm, tra δ 0 e δ 10. Il principale fattore che determina il chemical shift di un protone è la densità elettronica del relativo idrogeno: atomi elettronegativi legati nelle vicinanze dell idrogeno riducono la sua densità elettronica, e quindi l effetto schermante degli elettroni, per cui il chemical shift aumenta. TMS 10 δ (ppm) Frequenza maggiore Minore schermatura Nuclei deschermati (campi bassi) 0 Frequenza minore Maggiore schermatura Nuclei schermati (campi alti)
23 Il chemical shift protonico I protoni olefinici (legati a carboni sp 2 ) hanno chemical shift molto più alto dei protoni legati a carboni sp 3, con valori tipici di δ 5-6. Questo può essere spiegato in base alla maggiore elettronegatività dei carboni sp 2, che riduce la densità elettronica sugli idrogeni olefinici. Questa spiegazione però non è sufficiente, poiché i protoni degli alchini, che sono legati a carboni sp ancora più elettronegativi, risuonano invece a δ 2-3. La densità elettronica sul protone non è quindi l unico effetto che influenza il chemical shift, come vedremo nella prossima lezione.
24 TMS (tetrametilsilano) 12 H equivalenti unico segnale H 3 C CH 3 Si CH 3 CH 3 Per uniformità nel riportare i dati NMR è stata introdotta l unità chemical shift (δ) espressa in ppm (unità adimensionale) ν A - ν δ = TMS 10 6 δ = ν 0 ν Α è la frequenza a cui risuona il protone in esame ν TMS è la frequenza a cui risuona il TMS ν 0 è la frequenza di risonanza del nucleo che si sta studiando ( 1 H, 13 C) al valore di B 0 dello strumento che si usa x = 1.2 ppm
25 I tre idrogeni del metile sono equivalenti
26 Equivalenza Chimica : due nuclei sono chimicamente equivalenti (o isocroni) se hanno la stessa frequenza di risonanza. Due nuclei sono equivalenti se sono INTERSCAMBIABILI attraverso una qualsivoglia operazione di simmetria o mediante un processo chimico rapido.
27 Equivalenza chimica
28 Equivalenza chimica H Cl H Cl Protoni omotopici interscambiabili attraverso un operazione C 2 (rotazione di 180 intorno ad un asse). Se uno o l altro dei due protoni viene sostituito ad es. con D, ottengo la stessa molecola Questi protoni sono isocroni, hanno lo stesso chemical shift H 3 C H H COOH Protoni enantiotopici interscambiabili attraverso un operazione σ (riflessione attraverso un piano di simmetria). Se uno o l altro dei due protoni viene sostituito ad es. con D, ottengo due enantiomeri. Anche questi protoni hanno lo stesso chemical shift. H 3 C HO H H H COOH Protoni diastereotopici non possono essere scambiati in virtù di un elemento di simmetria. Ciascuno possiede un proprio spostamento chimico se si eccettua una sovrapposizione casuale. I protoni diastereotopici geminali accoppiano tra loro. Se uno o l altro dei due protoni viene sostituito ad es. con D, ottengo due diastereoisomeri
29 INTENSITA DEL SEGNALE L area sottesa ad un segnale di risonanza e proporzionale al numero dei nuclei che danno origine a tale segnale O O
30
31 9H CH 3 H 3 C CH 3 O O CH 3 3H
32 FATTORI CHE INFLUENZANO IL CHEMICAL SHIFT ð Elettronegatività degli atomi adiacenti ð Ibridizzazione degli atomi adiacenti ð Induzione magnetica dovuta ad un sistema di elettroni π adiacente Un C ibridizzato sp 2 è più elettronegativo di uno sp 3 (ha maggiore carattere s)
33 CH 3 -X All aumentare dell elettronegatività di X aumenta il chemical shift, ma l effetto diminuisce all aumentare della distanza. CH 3 -X Elettronegatività di X δ CH 3 F CH 3 OH CH 3 Cl CH 3 Br CH 3 I (CH 3 ) 4 C (CH 3 ) 4 Si
34 INTERVALLI DI CHEMICAL SHIFT PROTONICI DELLE PRINCIPALI CLASSI DI COMPOSTI ORGANICI Tipo di 1 H δ Tipo di 1 H δ RCH R(C=O)OCH RCH 2 R R(C=O)OCH 2 R R 3 CH RCH 2 I R 2 C=CRCHR RCH 2 Br RC CH RCH 2 Cl ArCH RCH 2 F ArCH 2 R R 2 C=CH ROH R 2 C=CHR RCH 2 OH ArH RCH 2 OR R(C=O)H R 2 NH R(C=O)OH R(C=O)CH R(C=O)CH 2 R
35 δ (ppm)
36 EFFETTO DELL IBRIDIZZAZIONE SUL CHEMICAL SHIFT Tipo di 1 H δ RCH 3, R 2 CH 2, R 3 CH R 2 C=C(R)CHR RC CH R 2 C=CHR, R 2 C=CH RCHO
37 Corrente diamagnetica: è la circolazione degli elettroni intorno ad un nucleo sotto l influenza di un campo magnetico applicato Schermaggio: l effetto, prodotto da un aumento di densità elettronica attorno a un nucleo, che provoca un assorbimento di questo a campi alti cioè frequenze minori (il segnale risulta spostato sulla parte destra dello spettro) Il campo magnetico di cui risente il nucleo è minore: la risonanza avviene a frequenze minori (se si facesse una scansione del campo magnetico bisognerebbe applicare un campo più alto) Deschermaggio: l effetto, prodotto da una diminuzione di densità elettronica attorno a un nucleo, che provoca un assorbimento di questo a campi bassi cioè frequenze maggiori (il segnale risulta spostato sulla parte sinistra dello spettro)
38 ANISOTROPIA DIAMAGNETICA Composti organici contenenti legami π Alcheni ppm Alchini ppm Aromatici ppm Aldeidi ( ppm) Lo schermaggio e il deschermaggio dipendono dall orientazione della molecola rispetto al campo magnetico esterno. Per composti insaturi lo spazio è suddiviso in regioni caratterizzate da campi magnetici più intensi o meno intensi. Nei composti aromatici si ha un elevato deschermaggio a causa della struttura ciclica (corrente d anello) che produce un campo magnetico indotto particolarmente intenso.
39 B o nucleo schermato B o nucleo schermato linee di flusso del c.m. indotto C C nucleo deschermato nucleo deschermato Gli H sono esposti ad un campo che è la somma di B 0 e B i : B eff = B 0 +B i La frequenza di risonanza sarà maggiore effetto deschermante
40 nucleo schermato nucleo schermato Gli H sono esposti ad un campo che è inferiore a B 0 : B eff = B 0 -B i La frequenza di risonanza sarà inferiore effetto schermante
41
42 MOLTEPLICITA accoppiamento spin-spin Il fenomeno responsabile della molteplicità del segnale è detto accoppiamento spin-spin ed è dovuto all influenza sul campo magnetico di cui risente il nucleo in esame dell orientazione degli spin degli altri nuclei nelle immediate vicinanze. H a H b C C Il c.s. di H a è influenzato dal fatto che lo spin di H b sia allineato con o contro il campo magnetico esterno (e viceversa). Il risultato dell accoppiamento è una suddivisione del segnale in due picchi.
43 Hb
44 1:2:1
45 Molteplicità del segnale di H a in presenza di H b H a C C H a H b C C 1 1 H a H b C C H b H a H b C C H b H b δ H a
46 Molteplicità del segnale NMR O 6H 4H Regola (n + 1)
47 Intensità relative per semplici multipletti n Molteplicità n+1 Intensità relative Nome del multipletto Singoletto (s) 1 2 1:1 Doppietto (d) 2 3 1:2:1 Tripletto (t) 3 4 1:3:3:1 Quartetto (q) 4 5 1:4:6:4:1 Quintetto 5 6 1:5:10:10:5:1 Sestetto 6 7 1:6:15:20:15:6:1 Settetto 7 8 1:7:21:35:35:21:7:1 Ottetto 8 9 1:8:28:56:70:56:28:8:1 Ennetto
48 H a H b C C H a H b C C H b H a H a B 0 ββ αβ βα J ab αα J ab J ab H a H b C C H b H b B 0 βββ H a αββ βαβ ββα ααβ αβα βαα ααα J ab J ab J ab
49 J = costante di accoppiamento (Hz) La differenza di frequenza in Hz tra i picchi che costituiscono il doppietto (o il tripletto o il quartetto, regola n+1) è proporzionale all efficacia delll accoppiamento
50 Patterns caratteristici
51
52 Multipletti Quando un protone, o un gruppo di protoni magneticamente equivalenti, interagisce con più di un gruppo di protoni il segnale avrà la forma di un multipletto di multipletti. dd: doppio doppietto td: tripletto di doppietti
53
54 tt : tripletto di tripletti
55 Sistema AMX
56 I profili di splitting semplici sono prodotti dall accoppiamento di protoni che possiedono spostamenti chimici molto differenti Δν/J > 9-10 cioè la differenza di chemical shift è circa 10 volte il valore della costante di accoppiamento questi sistemi vengono detti del primo ordine e seguono la regola n+1.
57 Accoppiamento del secondo ordine sistema AB Quando Δν/J diventa piccolo i doppietti si avvicinano l uno all altro, i due picchi interni aumentano di intensità e quelli esterni diminuiscono di intensità (sistema AB). Quando la differenza di spostamento chimico diventa zero, i picchi centrali vanno in coalescenza, trasformandosi in un unico picco e i segnali esterni scompaiono: i protoni sono equivalenti.
58 J dipende esclusivamente dai campi magnetici interni alla molecola e non dipende né dall intensità del campo magnetico esterno né dalla radiofrequenza applicata. J viene espresso in Hertz. Generalmente l accoppiamento perde importanza oltre il terzo legame, a meno che non sia presente una tensione d anello, una delocalizzazione (sistemi aromatici o coniugati) o un sistema di quattro legami successivi disposti a W. H a H b 3 J C C costante di accoppiamento vicinale H b 2 J C H b costante di accoppiamento geminale 4 J- 5 J costante di accoppiamento long range
59 Equazione di Karplus Relazione della J vicinale dall angolo diedro La costante di accoppiamento vicinale dipende dall angolo diedro tra i due protoni (ma non solo, anche i sostituenti contano). Come si vede nel grafico, è piccola per idrogeni in gauche (Φ=60 ), ed è grande per idrogeni anti (Φ=180 ). 3 J = A + B cos 2 Φ + C cos2φ in cui A, B e C sono costanti con valori empirici per le singole situazioni:
60
61
62 La stereochimica di un doppio legame può essere determinata misurando le costanti di accoppiamento tra i protoni vinilici. Quando il doppio legame è contenuto in un ciclo la 3 J tra i due protoni vinilici riflette la grandezza del ciclo.
63 H 3 C H C H H H H b C C C OH a H H H b H a appare come un singolettto e non come un tripletto in quanto il protone ossidrilico H a è scambiato rapidamente tra le molecole di alcol o con molecole di H 2 O eventualmente presenti nel campione. Uso di solventi come DMSO-d 6 o diluizioni rallentano lo scambio e si osserva la molteplicità. I legami idrogeno riducono la densità elettronica intorno al protone ossidrilico, spostando pertanto il picco a frequenze maggiori.
64 EQUIVALENZA CHIMICA Concetto semplice: un insieme di spin (nuclei) sono chimicamente equivalenti quando: a) sono la stessa specie isotopica b) hanno lo stesso intorno chimico; cioè quando è possibile con una operazione di simmetria scambiarli ottenendo sempre lo stesso composto nuclei chimicamente equivalenti hanno lo stesso chemical shift, sono isocroni. Il contrario NON è sempre vero! (isocronia accidentale) Per motivi quantomeccanici l accoppiamento tra nuclei chimicamente equivalenti non è osservabile.
65 EQUIVALENZA MAGNETICA Si parla di equivalenza magnetica solo quando la molecola contiene più di un gruppo di spins chimicamente equivalenti. Es. H a F a I due atomi di idrogeno sono chimicamente equivalenti così come i due atomi di 19 F. H b F b I due atomi 1 H sono anche magneticamente equivalenti?
66 EQUIVALENZA MAGNETICA Si parla di equivalenza magnetica solo quando la molecola contiene più di un gruppo di spins chimicamente equivalenti. Es. H a F a I due atomi di idrogeno sono chimicamente equivalenti così come i due atomi di 19 F. H b F b I due atomi 1 H sono anche magneticamente equivalenti? La risposta è NO, perchè per esempio H a accoppia con F a con una costante dalla costante che ha con F b (J cis J trans )
67 J HF circa 50 Hz EQUIVALENZA MAGNETICA
68 quindi due nuclei che sono chimicamente sono anche magneticamente equivalenti se le loro proprietà magnetiche sono uguali e per esempio se le costanti di accoppiamento con un altro sistema di spin sono uguali. Es. EQUIVALENZA MAGNETICA O H H a H a ' H a e H a sono chimicamente equivalenti H b e H b sono chimicamente equivalenti H b H b ' H a e H b sono magneticamente equivalenti? CH 3 Risposta: confronta J Ha,Hb con J Ha,Hb
69
70 Range di assorbimento di protoni legati ad eteroatomi Alcoli ppm Fenoli ppm Acidi ppm RNH 2, R 2 NH ppm Ar-NH ppm RCONH ppm RCONHR ppm Per concentrazioni 5-10% in CDCl 3 Il legame H provoca uno shift a chemical shift più alti (cioè a campi bassi, frequenze maggiori) perché diminuisce la densità di carica.
71 Numero di insaturazioni C W H X N Y O Z U.N. = W-1/2X+1/2Y+0Z+1 3-pentanone W: n. atomi tetravelenti X: n. atomi monovalenti Y: n. atomi trivalenti Z: n. atomi bivalenti C 5 H 10 O 1.2 ppm (tripletto) 2.5 ppm (quartetto) O
72 ESERCIZI
73 C 4 H 8 O ppm (quartetto) 1.97 ppm (singoletto) 1.2 ppm (tripletto) O O
74 Acetato di etile C 4 H 8 O ppm (quartetto) 1.97 ppm (singoletto) 1.20 ppm (tripletto) O O
75 C 7 H ppm 2.3 ppm (singoletto)
76 Toluene C 7 H ppm 2.3 ppm (singoletto)
77 C 8 H 8 O 2.2 ppm (singoletto) 10 ppm (singoletto) 7.6 ppm
78 4-metilbenzaldeide C 8 H 8 O 2.2 ppm (singoletto) 10 ppm (singoletto) 7.6 ppm CHO
79 C 10 H 14 O 6.9 ppm, sistema AB 3.6 (singoletto) 2.7 (settetto) 1.6 (doppietto)
80 4-isopropil-1-metossibenzene C 10 H 14 O 6.9 ppm, sistema AB 3.6 (singoletto) 2.7 (settetto) 1.6 (doppietto) OCH 3
81 CHO OCH 3 4-metossi-benzaldeide
82 acido 4-metilbenzoico COOH
83
84 2-metil-2-butanolo OH
85
86 3-metil-2-butanolo OH
87
88 2-metil-1-butanolo OH
89
90 Isopropil etil etere O
91 2-metilbutanale CHO
92 3-metilbutanale CHO
93 Per esercizi sull 1 H-NMR
Risonanza Magnetica Nucleare NMR
 Risonanza Magnetica Nucleare NMR Numeri quantici di spin di alcuni nuclei Gli isotopi più abbondanti di C e O non hanno spin Element 1 H 2 H 12 C 13 C 14 N 16 O 17 O 19 F N.ro quantico di Spin 1/2 1 0
Risonanza Magnetica Nucleare NMR Numeri quantici di spin di alcuni nuclei Gli isotopi più abbondanti di C e O non hanno spin Element 1 H 2 H 12 C 13 C 14 N 16 O 17 O 19 F N.ro quantico di Spin 1/2 1 0
L effetto del sostituente (induttivo e coniugativo) modifica:
 L effetto del sostituente (induttivo e coniugativo) modifica: 1 la densità elettronica del centro di reazione influenza la REATTIVITA Se da un atomo di ad un altro cambia la distribuzione degli elettroni
L effetto del sostituente (induttivo e coniugativo) modifica: 1 la densità elettronica del centro di reazione influenza la REATTIVITA Se da un atomo di ad un altro cambia la distribuzione degli elettroni
Informazioni che si possono ricavare da uno spettro protonico
 Informazioni che si possono ricavare da uno spettro protonico Per interpretare uno spettro 1 H NMR bisogna: 1) Contare il numero di picchi che corrispondono agli idrogeni fisicamente diversi nella molecola.
Informazioni che si possono ricavare da uno spettro protonico Per interpretare uno spettro 1 H NMR bisogna: 1) Contare il numero di picchi che corrispondono agli idrogeni fisicamente diversi nella molecola.
LO SPETTRO ELETTROMAGNETICO
 LO SPETTRO ELETTROMAGNETICO 1 LO SPETTRO ELETTROMAGNETICO cresce Visibile Raggi γ Raggi X UV IR Micro onde cresce Onde radio Medio corte medie e lunghe Eccitazione dei nuclei atomici Lontano Vicino Lontano
LO SPETTRO ELETTROMAGNETICO 1 LO SPETTRO ELETTROMAGNETICO cresce Visibile Raggi γ Raggi X UV IR Micro onde cresce Onde radio Medio corte medie e lunghe Eccitazione dei nuclei atomici Lontano Vicino Lontano
Massa: sono isomeri strutturali: M + è lo stesso (anche se il resto dello spettro è un po diverso).
 Massa: sono isomeri strutturali: M + è lo stesso (anche se il resto dello spettro è un po diverso). UV-vis: un alcano ha solo elettroni σ: la transizione elettronica richiede una radiazione di energia
Massa: sono isomeri strutturali: M + è lo stesso (anche se il resto dello spettro è un po diverso). UV-vis: un alcano ha solo elettroni σ: la transizione elettronica richiede una radiazione di energia
Spettroscopia NMR Interazioni spin-spin
 Spettroscopia NMR Interazioni spin-spin meno schermato più schermato H sch H sch H eff H eff Energia relativa Energia assorbita B 0 Accoppiamento tra nuclei Energia relativa Energia assorbita H A Accoppiamento
Spettroscopia NMR Interazioni spin-spin meno schermato più schermato H sch H sch H eff H eff Energia relativa Energia assorbita B 0 Accoppiamento tra nuclei Energia relativa Energia assorbita H A Accoppiamento
γ= rapporto magnetogirico
 Proprietà magnetiche dei nuclei I nuclei (massa + carica) sono in rotazione (spin) Metodi Fisici in Chimica Organica - NMR z µ p y x Alla rotazione (spin) è associato un momento angolare, p p = h I( I
Proprietà magnetiche dei nuclei I nuclei (massa + carica) sono in rotazione (spin) Metodi Fisici in Chimica Organica - NMR z µ p y x Alla rotazione (spin) è associato un momento angolare, p p = h I( I
γ= rapporto magnetogirico
 Proprietà magnetiche dei nuclei I nuclei (massa + carica) sono in rotazione (spin) Metodi Fisici in Chimica Organica - NMR z µ p y x Alla rotazione (spin) è associato un momento angolare, p p = h I( I
Proprietà magnetiche dei nuclei I nuclei (massa + carica) sono in rotazione (spin) Metodi Fisici in Chimica Organica - NMR z µ p y x Alla rotazione (spin) è associato un momento angolare, p p = h I( I
Proprietà magnetiche dei nuclei. Alla rotazione (spin) è associato un momento angolare, p. = hm. gli stati di spin sono quantizzati
 Proprietà magnetiche dei nuclei I nuclei (massa + carica) sono in rotazione (spin) Metodi Fisici in Chimica Organica - NMR z µ p y x Alla rotazione (spin) è associato un momento angolare, p p = h I( I
Proprietà magnetiche dei nuclei I nuclei (massa + carica) sono in rotazione (spin) Metodi Fisici in Chimica Organica - NMR z µ p y x Alla rotazione (spin) è associato un momento angolare, p p = h I( I
Metodi Spettroscopici: NMR
 Metodi Spettroscopici: NMR Massa: sono isomeri strutturali: M + è lo stesso (anche se il resto dello spettro è un po diverso). UV-vis: un alcano ha solo elettroni σ: la transizione elettronica richiede
Metodi Spettroscopici: NMR Massa: sono isomeri strutturali: M + è lo stesso (anche se il resto dello spettro è un po diverso). UV-vis: un alcano ha solo elettroni σ: la transizione elettronica richiede
La molecola è: CH 3 CH 2 CH 2 CH 2 CH 3
 ESERCIZI DI NMR La molecola è: CH 3 CH 2 CH 2 CH 2 CH 3 Lo spettro presenta solo segnali a campi molto alti relativi a H legati a C sp 3 di tipo alchilico e tutti primari o secondari. Di conseguenza si
ESERCIZI DI NMR La molecola è: CH 3 CH 2 CH 2 CH 2 CH 3 Lo spettro presenta solo segnali a campi molto alti relativi a H legati a C sp 3 di tipo alchilico e tutti primari o secondari. Di conseguenza si
NUCLEI NMR ATTIVI E SPIN
 NUCLEI NMR ATTIVI E SPIN I diversi nuclei risuonano a campi magnetici (e frequenze) molto diversi La frequenza caratteristica a cui risuonano i nuclei dello standard è Ξ Per un nucleo specifico, le variazioni
NUCLEI NMR ATTIVI E SPIN I diversi nuclei risuonano a campi magnetici (e frequenze) molto diversi La frequenza caratteristica a cui risuonano i nuclei dello standard è Ξ Per un nucleo specifico, le variazioni
Benzil Acetato. Linea dell integrale. La linea dell integrale rappresenta una quantità proporzionale al numero di H. Rapporto tra le altezze
 Benzil Acetato La linea dell integrale rappresenta una quantità proporzionale al numero di Linea dell integrale 55 : 22 : 33 = 5:2:3 Rapporto tra le altezze Accoppiamento Spin-Spin Accoppiamento SPIN-SPIN
Benzil Acetato La linea dell integrale rappresenta una quantità proporzionale al numero di Linea dell integrale 55 : 22 : 33 = 5:2:3 Rapporto tra le altezze Accoppiamento Spin-Spin Accoppiamento SPIN-SPIN
BREVE INTRODUZIONE ALLA SPETTROSCOPIA NMR
 Mauro Tonellato BREVE INTRODUZIONE ALLA SPETTROSCOPIA NMR www.pianetachimica.it Breve introduzione teorica alla Spettroscopia NMR I nuclei degli atomi che possiedono un numero dispari di protoni, un numero
Mauro Tonellato BREVE INTRODUZIONE ALLA SPETTROSCOPIA NMR www.pianetachimica.it Breve introduzione teorica alla Spettroscopia NMR I nuclei degli atomi che possiedono un numero dispari di protoni, un numero
Aspetti salienti. 1.Problema di sensibilità 2.Accoppiamenti diretti 1 J e 2 J C(H) 3.Disaccoppiamento 4.Chemical shift
 13 C NMR Aspetti salienti 1.Problema di sensibilità 2.Accoppiamenti diretti 1 J e 2 J C(H) 3.Disaccoppiamento 4.Chemical shift 1. PROBLEMA DELLA SENSIBILITA 12 C non è NMR-attivo: I = 0 13 C possiede spin,
13 C NMR Aspetti salienti 1.Problema di sensibilità 2.Accoppiamenti diretti 1 J e 2 J C(H) 3.Disaccoppiamento 4.Chemical shift 1. PROBLEMA DELLA SENSIBILITA 12 C non è NMR-attivo: I = 0 13 C possiede spin,
+ ε (deschermo) ε (schermo) α β α. B o
 Il fenomeno dell accoppiamento di spin Nuclei non equivalenti possono interagire attraverso i loro momenti di spin Ai fini della indagine strutturale di molecole incognite è necessario sario non solo considerare
Il fenomeno dell accoppiamento di spin Nuclei non equivalenti possono interagire attraverso i loro momenti di spin Ai fini della indagine strutturale di molecole incognite è necessario sario non solo considerare
06/04/2017 METODI SPETTROSCOPICI - 3. Risonanza magnetica elettronica (EPR O ESR) CHIMICA ANALITICA UNIVERSITÀ DEGLI STUDI DI TERAMO
 UNIVERSITÀ DEGLI STUDI DI TERAMO CL in BIOTECNOLOGIE Anno Accademico 2016/2017 CHIMICA ANALITICA METODI SPETTROSCOPICI - 3 La risonanza magnetica elettronica è una branca della spettroscopia nella quale
UNIVERSITÀ DEGLI STUDI DI TERAMO CL in BIOTECNOLOGIE Anno Accademico 2016/2017 CHIMICA ANALITICA METODI SPETTROSCOPICI - 3 La risonanza magnetica elettronica è una branca della spettroscopia nella quale
Parametri da cui dipendono le costanti di accoppiamento
 Parametri da cui dipendono le costanti di accoppiamento 2 J: può essere negativa o positiva 2 J 12-15 z se Csp 3 ; 2-4 z se Csp 2 Metodi Fisici in Chimica Organica - NMR 3 J: è di solito positiva a) angolo
Parametri da cui dipendono le costanti di accoppiamento 2 J: può essere negativa o positiva 2 J 12-15 z se Csp 3 ; 2-4 z se Csp 2 Metodi Fisici in Chimica Organica - NMR 3 J: è di solito positiva a) angolo
Spettroscopia di Risonanza Magnetica Nucleare
 Spettroscopia di Risonanza Magnetica Nucleare TIPO DI SPETTROSCOPIA INTERVALLO DI LUNGHEZZA D ONDA TIPO DI TRANSIZIONE QUANTICA ULTRAVIOLETTO-VISIBILE 180-780 nm Elettroni di legame INFRAROSSO 0,75-300
Spettroscopia di Risonanza Magnetica Nucleare TIPO DI SPETTROSCOPIA INTERVALLO DI LUNGHEZZA D ONDA TIPO DI TRANSIZIONE QUANTICA ULTRAVIOLETTO-VISIBILE 180-780 nm Elettroni di legame INFRAROSSO 0,75-300
Spettroscopia di Risonanza Magnetica Nucleare (NMR)
 È basata sulle interazioni tra la componente magnetica di una radiazione elettromagnetica, dell ordine delle radiofrequenze, con i nuclei delle molecole poste in un forte campo magnetico. 1 L isotopo più
È basata sulle interazioni tra la componente magnetica di una radiazione elettromagnetica, dell ordine delle radiofrequenze, con i nuclei delle molecole poste in un forte campo magnetico. 1 L isotopo più
La molecola è il benzene. Lo spettro è semplicissimo, i sei idrogeni sono omotopici e quindi danno un unico segnale a 7.4 ppm nella tipica zona degli
 La molecola è il benzene. Lo spettro è semplicissimo, i sei idrogeni sono omotopici e quindi danno un unico segnale a 7.4 ppm nella tipica zona degli idrogeni aromatici La molecola è l etilbenzene Lo
La molecola è il benzene. Lo spettro è semplicissimo, i sei idrogeni sono omotopici e quindi danno un unico segnale a 7.4 ppm nella tipica zona degli idrogeni aromatici La molecola è l etilbenzene Lo
Chemical shifts di protoni (CH 3, CH 2 o CH) in posizione α rispetto ad un sostituente
 Chemical shifts di protoni (C 3, C 2 o C) in posizione α rispetto ad un sostituente 32 (continua) 33 Chemical shifts dei protoni di benzeni monosostituiti 34 (contunua) 35 La conseguenza della NON dipendenza
Chemical shifts di protoni (C 3, C 2 o C) in posizione α rispetto ad un sostituente 32 (continua) 33 Chemical shifts dei protoni di benzeni monosostituiti 34 (contunua) 35 La conseguenza della NON dipendenza
SISTEMI DI SPIN E COSTANTE DI ACCOPPIAMENTO. Corso Metodi Fisici in Chimica Organica Prof. Renzo LUISI Uniba. vietata la vendita
 SISTEMI DI SPIN E COSTANTE DI ACCOPPIAMENTO Accoppiamento di spin Definizione dei sistemi di spin Nuclei chimicamente non-equivalenti vengono identificati dalle lettere A, B, C. X..etc. L attribuzione
SISTEMI DI SPIN E COSTANTE DI ACCOPPIAMENTO Accoppiamento di spin Definizione dei sistemi di spin Nuclei chimicamente non-equivalenti vengono identificati dalle lettere A, B, C. X..etc. L attribuzione
Risonanza Magnetica Nucleare
 Risonanza Magnetica Nucleare Il fenomeno della risonanza magnetica nucleare è legato ad una proprietà p di alcuni nuclei quale lo spin. Lo spin è una proprietà fondamentale come la carica e la massa. Protoni,
Risonanza Magnetica Nucleare Il fenomeno della risonanza magnetica nucleare è legato ad una proprietà p di alcuni nuclei quale lo spin. Lo spin è una proprietà fondamentale come la carica e la massa. Protoni,
La molecola è ClCH 2 CH 2 CH 2 CH 3 Ci sono tre segnali caratteristici: -1 ppm tripletto il CH 3 terminale ha un leggerissimo spostamento verso campi
 La molecola è ClCH 2 CH 2 CH 2 CH 3 Ci sono tre segnali caratteristici: -1 ppm tripletto il CH 3 terminale ha un leggerissimo spostamento verso campi più bassi del solito CH 3 (che cade in genere sotto
La molecola è ClCH 2 CH 2 CH 2 CH 3 Ci sono tre segnali caratteristici: -1 ppm tripletto il CH 3 terminale ha un leggerissimo spostamento verso campi più bassi del solito CH 3 (che cade in genere sotto
La molecola è la piridina. Lo spettro presenta tre segnali dovuti agli H: Ha (2), Hb (2) e Hc (1).
 La molecola è la piridina. b c b Lo spettro presenta tre segnali dovuti agli : a (2), b (2) e c (1). a a In questa particolare molecola l effetto elettron attrattore dell piridinico è alto nelle posizioni
La molecola è la piridina. b c b Lo spettro presenta tre segnali dovuti agli : a (2), b (2) e c (1). a a In questa particolare molecola l effetto elettron attrattore dell piridinico è alto nelle posizioni
Spettroscopia di Risonanza Magnetica Nucleare (NMR)
 È basata sulle interazioni tra la componente magnetica di una radiazione elettromagnetica, dell ordine delle radiofrequenze, con i nuclei delle molecole poste in un forte campo magnetico. Permette di ottenere
È basata sulle interazioni tra la componente magnetica di una radiazione elettromagnetica, dell ordine delle radiofrequenze, con i nuclei delle molecole poste in un forte campo magnetico. Permette di ottenere
NMR e Fenomeni Dinamici
 NMR e Fenomeni Dinamici L NMR è molto utile per lo studio di fenomeni dinamici come equilibri, scambi intere intramolecolari,, studi conformazionali,, isomerizzazioni configurazionali etc. Alla base dell
NMR e Fenomeni Dinamici L NMR è molto utile per lo studio di fenomeni dinamici come equilibri, scambi intere intramolecolari,, studi conformazionali,, isomerizzazioni configurazionali etc. Alla base dell
Lo spettro 13 C NMR. La spettroscopia
 Lo spettro 13 C NMR La spettroscopia 13 C NMR presenta un problema connesso a due fattori: 1. Il rapporto giromagnetico basso [γ(c) = 7.095.10-27 JT -1 ; γ(h) = 28.212.10-27 JT -1 ] determina una piccola
Lo spettro 13 C NMR La spettroscopia 13 C NMR presenta un problema connesso a due fattori: 1. Il rapporto giromagnetico basso [γ(c) = 7.095.10-27 JT -1 ; γ(h) = 28.212.10-27 JT -1 ] determina una piccola
Risonanza magnetica di spin: ESR (o EPR) nucleare: RMN/NMR
 Risonanza magnetica di spin: ESR (o EPR) nucleare: RMN/NMR 1944-prima osservazione della ESR 1938-prima osservazione della NMR Tecniche spettroscopiche oggi standard Applicazioni di caratterizzazione e
Risonanza magnetica di spin: ESR (o EPR) nucleare: RMN/NMR 1944-prima osservazione della ESR 1938-prima osservazione della NMR Tecniche spettroscopiche oggi standard Applicazioni di caratterizzazione e
Spettroscopia NMR (Risonanza Magnetica Nucleare)
 Spettroscopia NMR (Risonanza Magnetica Nucleare) studia l assorbimento della radiazione a radiofrequenze da parte di molecole quando i loro atomi sono orientati da un campo magnetico applicato. rispetto
Spettroscopia NMR (Risonanza Magnetica Nucleare) studia l assorbimento della radiazione a radiofrequenze da parte di molecole quando i loro atomi sono orientati da un campo magnetico applicato. rispetto
La spettroscopia NMR può dare una un grande numero di informazioni sulla struttura di molecola organiche. Esempio di uno spettro NMR
 La spettroscopia di risonanza magnetica nucleare (NMR, dall inglese Nuclear Magnetic Resonance) sfrutta la differenza di energia che i vari stati di spin nucleari possono assumere in presenza di un campo
La spettroscopia di risonanza magnetica nucleare (NMR, dall inglese Nuclear Magnetic Resonance) sfrutta la differenza di energia che i vari stati di spin nucleari possono assumere in presenza di un campo
ACCOPPIAMENTO DI SPIN
 ACCOPPIAMENTO DI SPIN ACCOPPIAMENTO INDIRETTO (SCALARE) Interazione magnetica fra nuclei Mediato dagli elettroni di legame Misurato dalla J (Hz) costante di accoppiamento Termine di contatto di Fermi Contatto
ACCOPPIAMENTO DI SPIN ACCOPPIAMENTO INDIRETTO (SCALARE) Interazione magnetica fra nuclei Mediato dagli elettroni di legame Misurato dalla J (Hz) costante di accoppiamento Termine di contatto di Fermi Contatto
Risonanza Magnetico Nucleare
 Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Risonanza Magnetico Nucleare 21/3/2005 RMN ovvero NMR Spettroscopia RMN permette di - acquisire immagini 2D e 3D di parti del corpo umano ottima risoluzione
Dipartimento di Fisica a.a. 2004/2005 Fisica Medica 2 Risonanza Magnetico Nucleare 21/3/2005 RMN ovvero NMR Spettroscopia RMN permette di - acquisire immagini 2D e 3D di parti del corpo umano ottima risoluzione
Gli accoppiamenti di spin. e i sistemi di spin nucleari
 Gli accoppiamenti di spin e i sistemi di spin nucleari l momento magnetico di un nucleo interagisce con i momenti magnetici dei nuclei vicini. sistono due tipi di interazioni: nterazione diretta, anisotropa
Gli accoppiamenti di spin e i sistemi di spin nucleari l momento magnetico di un nucleo interagisce con i momenti magnetici dei nuclei vicini. sistono due tipi di interazioni: nterazione diretta, anisotropa
1. PRINCIPI GENERALI IL METODO A IMPULSI
 1. PRINCIPI GENERALI IL METODO A IMPULSI LA RADIAZIONE EM CAMPO ELETTRICO OSCILLANTE CAMPO MAGNETICO OSCILLANTE Radiofrequenze n = 40-1000 MHz (In pratica: 300 1000 MHz) Lo Spin Nucleare I I = 0, 1/2,
1. PRINCIPI GENERALI IL METODO A IMPULSI LA RADIAZIONE EM CAMPO ELETTRICO OSCILLANTE CAMPO MAGNETICO OSCILLANTE Radiofrequenze n = 40-1000 MHz (In pratica: 300 1000 MHz) Lo Spin Nucleare I I = 0, 1/2,
rappresenta la cinetica del processo: se è grande il processo è lento
 Conseguenze del principio di indeterminazione in sistemi coinvolgenti processi cinetici: a) scambio chimico; b) rotazioni impedite attorno a legami; c) tautomerie; d) inversioni di spin ω t 1 2π se i processi
Conseguenze del principio di indeterminazione in sistemi coinvolgenti processi cinetici: a) scambio chimico; b) rotazioni impedite attorno a legami; c) tautomerie; d) inversioni di spin ω t 1 2π se i processi
Spettroscopia 13 C NMR
 L analisi degli spettri 13 C NMR non differisce molto da quella dell 1 H. La principale differenza risiede nella minore sensibilità osservata nella registrazione degli d spettri 13 C che pertanto richiedono
L analisi degli spettri 13 C NMR non differisce molto da quella dell 1 H. La principale differenza risiede nella minore sensibilità osservata nella registrazione degli d spettri 13 C che pertanto richiedono
Esercitazione n. 8 - Aspetti generali di reazioni e meccanismi
 Esercitazione n. 8 Aspetti generali di reazioni e meccanismi 1. Dare una definizione dei seguenti termini: coordinata di reazione; stadio di una reazione; stato di transizione, reagente radicalico; scissione
Esercitazione n. 8 Aspetti generali di reazioni e meccanismi 1. Dare una definizione dei seguenti termini: coordinata di reazione; stadio di una reazione; stato di transizione, reagente radicalico; scissione
Chimica Fisica III A.A Prof.ssa Marilena Di Valentin. Spettroscopia di Risonanza Magnetica Nucleare
 Chimica Fisica A.A. 07-08 Prof.ssa Marilena Di Valentin Spettroscopia di Risonanza Magnetica ucleare Spettroscopia MR: un metodo fondamentale in chimica, fisica, biologia e medicina PREM OBEL: 944 Physics
Chimica Fisica A.A. 07-08 Prof.ssa Marilena Di Valentin Spettroscopia di Risonanza Magnetica ucleare Spettroscopia MR: un metodo fondamentale in chimica, fisica, biologia e medicina PREM OBEL: 944 Physics
H C H H 3 C CH 3. INFORMAZIONI CHE OTTENGO DALLO SPETTRO NMR (ES.: 1 H NMR) Accoppiamento scalare o indiretto J coupling. singoletto.
 INFORMAZIONI E OTTENGO DALLO SPETTRO NMR (ES.: 1 NMR) Accoppiamento scalare o indiretto J coupling 3 O 3 singoletto quadrupletto tripletto INFORMAZIONI E OTTENGO DALLO SPETTRO NMR (ES.: 1 NMR) AOPPIAMENTO
INFORMAZIONI E OTTENGO DALLO SPETTRO NMR (ES.: 1 NMR) Accoppiamento scalare o indiretto J coupling 3 O 3 singoletto quadrupletto tripletto INFORMAZIONI E OTTENGO DALLO SPETTRO NMR (ES.: 1 NMR) AOPPIAMENTO
LABORATORIO DI CHIMICA INORGANICA Barbara Milani tel
 LABORATORIO DI CHIMICA INORGANICA Barbara Milani milaniba@units.it tel. 040 5583956 Ricevimento: venerdì dalle 15.00 alle 17.00 oppure previo appuntamento Libri di testo: gli stessi proposti dal Prof.
LABORATORIO DI CHIMICA INORGANICA Barbara Milani milaniba@units.it tel. 040 5583956 Ricevimento: venerdì dalle 15.00 alle 17.00 oppure previo appuntamento Libri di testo: gli stessi proposti dal Prof.
Risonanza magnetica nucleare
 Risonanza magnetica nucleare Università di Firenze Corso di Tecnologie Biomediche Lezione del 31 ottobre 2003 Leonardo Bocchi Principi fisici Premessa Modello classico Visualizzazione semplificata Equazione
Risonanza magnetica nucleare Università di Firenze Corso di Tecnologie Biomediche Lezione del 31 ottobre 2003 Leonardo Bocchi Principi fisici Premessa Modello classico Visualizzazione semplificata Equazione
Introduzione alla Risonanza Magnetica Nucleare
 Chimica Fisica III - Modulo B A.A. 203-204 Dott.ssa Marilena Di Valentin con la collaborazione del Dott. Marco Ruzzi Introduzione alla Risonanza Magnetica ucleare Testo di riferimento: Capitolo 4 Peter
Chimica Fisica III - Modulo B A.A. 203-204 Dott.ssa Marilena Di Valentin con la collaborazione del Dott. Marco Ruzzi Introduzione alla Risonanza Magnetica ucleare Testo di riferimento: Capitolo 4 Peter
Introduzione all NMR / MRI. 19 aprile 2010 Corso di Biotecnologie
 Introduzione all NMR / MRI 19 aprile 2010 Corso di Biotecnologie NMR e MRI, stessa fisica, diversi obiettivi NMR come tecnica spettroscopica Spettroscopia: misura (diretta o indiretta) di assorbimento
Introduzione all NMR / MRI 19 aprile 2010 Corso di Biotecnologie NMR e MRI, stessa fisica, diversi obiettivi NMR come tecnica spettroscopica Spettroscopia: misura (diretta o indiretta) di assorbimento
Spettrometria di Risonanza Magnetica Nucleare
 Spettrometria di Risonanza Magnetica Nucleare Tipo di spettroscopia Intervallo di lunghezza d onda Intervallo di numeri d onda (cm -1 ) Tipo di transizione quantica Emissione raggi γ 0.005-1.4Å - nucleare
Spettrometria di Risonanza Magnetica Nucleare Tipo di spettroscopia Intervallo di lunghezza d onda Intervallo di numeri d onda (cm -1 ) Tipo di transizione quantica Emissione raggi γ 0.005-1.4Å - nucleare
NMR Stato Solido. Non distruttivo. Studio di materiali. Polimeri insolubili, membrane cellulari, materiali ceramici, legno, ossa
 NMR Stato Solido Non distruttivo Solidi cristallini, amorfi, polveri Studio di materiali Polimeri insolubili, membrane cellulari, materiali ceramici, legno, ossa Non richiede preparazione del campione,
NMR Stato Solido Non distruttivo Solidi cristallini, amorfi, polveri Studio di materiali Polimeri insolubili, membrane cellulari, materiali ceramici, legno, ossa Non richiede preparazione del campione,
Identificazione di un composto organico:
 Identificazione di un composto organico: Laboratorio di Chimica Organica II? O O NO 2 Identificazione di un composto organico: Laboratorio di Chimica Organica II? Analisi elementare: formula bruta (C x
Identificazione di un composto organico: Laboratorio di Chimica Organica II? O O NO 2 Identificazione di un composto organico: Laboratorio di Chimica Organica II? Analisi elementare: formula bruta (C x
Esercizio 2 Soluzione
 Esercizio 2 Soluzione Poiché il testo non ci fornisce la formula molecolare del composto incognito, per prima cosa dobbiamo ricavarla a partire dai dati dell analisi elementare. Con questa tecnica otteniamo
Esercizio 2 Soluzione Poiché il testo non ci fornisce la formula molecolare del composto incognito, per prima cosa dobbiamo ricavarla a partire dai dati dell analisi elementare. Con questa tecnica otteniamo
Classi di composti: derivati carbonilici
 Classi di composti: derivati carbonilici Bande di controllo/conferma zona di stiramento del carbonile 59 Tabella sinottica della posizione della banda di stiramento del carbonile e della posizione delle
Classi di composti: derivati carbonilici Bande di controllo/conferma zona di stiramento del carbonile 59 Tabella sinottica della posizione della banda di stiramento del carbonile e della posizione delle
Esperimenti FT-NMR a impulsi
 Vettore magnetizzazione netta M 0 per un nucleo immerso in un campo magnetico B 0, per indurre la transizione l impulso RF è applicato lungo la direzione dell asse x. Il campo magnetico alternante applicato
Vettore magnetizzazione netta M 0 per un nucleo immerso in un campo magnetico B 0, per indurre la transizione l impulso RF è applicato lungo la direzione dell asse x. Il campo magnetico alternante applicato
L interazione Zeeman nucleare
 L interaione Zeeman nucleare 1 Hamiltoniano di spin: Lo stato di una particella (nucleo o elettrone) è di una particella è descritta da una funione d onda che include le variabili spaiali (coordinate delle
L interaione Zeeman nucleare 1 Hamiltoniano di spin: Lo stato di una particella (nucleo o elettrone) è di una particella è descritta da una funione d onda che include le variabili spaiali (coordinate delle
Risonanza magnetica nucleare protonica (NMR - PMR)
 Risonanza magnetica nucleare protonica (NMR - PMR) Basi fisiche I nuclei degli atomi hanno un movimento di rotazione intorno a se stessi (spin). Posto che ogni carica dotata di moto genera un campo magnetico,
Risonanza magnetica nucleare protonica (NMR - PMR) Basi fisiche I nuclei degli atomi hanno un movimento di rotazione intorno a se stessi (spin). Posto che ogni carica dotata di moto genera un campo magnetico,
SPETTROSCOPIA DI RISONANZA MAGNETICA NUCLEARE. Studio dell Equilibrio Cheto-Enolico 2,4- pentadione 3-metil-2,4-pentadione
 SPETTRSCPIA DI RISNANZA MAGNETICA NUCLEARE Studio dell Equilibrio Cheto-Enolico 2,4- pentadione 3-metil-2,4-pentadione 1 La risonanza magnetica nucleare è una tecnica spettroscopica che permette lo studio
SPETTRSCPIA DI RISNANZA MAGNETICA NUCLEARE Studio dell Equilibrio Cheto-Enolico 2,4- pentadione 3-metil-2,4-pentadione 1 La risonanza magnetica nucleare è una tecnica spettroscopica che permette lo studio
ν [Hz] δ [ppm] = ν rif [MHz]
![ν [Hz] δ [ppm] = ν rif [MHz] ν [Hz] δ [ppm] = ν rif [MHz]](/thumbs/72/68052460.jpg) EMIAL SIFT SPSTAMENT IMI sizione del segnale di risonanza dei protoni di una molecola) pettrometria NMR non sarebbe molto utile se tutti i protoni risuonassero alla stessa uenza!! toni all interno di una
EMIAL SIFT SPSTAMENT IMI sizione del segnale di risonanza dei protoni di una molecola) pettrometria NMR non sarebbe molto utile se tutti i protoni risuonassero alla stessa uenza!! toni all interno di una
INTRODUZIONE ALLA SPETTROSCOPIA NMR
 Mauro Tonellato INTRODUZIONE ALLA SPETTROSCOPIA NMR www.pianetachimica.it Basi teoriche della spettroscopia NMR www.pianetachimica.it Premessa La spettroscopia di Risonanza Magnetica Nucleare (NMR) è una
Mauro Tonellato INTRODUZIONE ALLA SPETTROSCOPIA NMR www.pianetachimica.it Basi teoriche della spettroscopia NMR www.pianetachimica.it Premessa La spettroscopia di Risonanza Magnetica Nucleare (NMR) è una
Aromaticità Un composto si definisce aromatico se possiede un anello di elettroni chiuso.
 Aromaticità Un composto si definisce aromatico se possiede un anello di elettroni chiuso. E anche detto aromatico, quando tramite i seguenti criteri soddisfa la regola di ückel: 1. I composti aromatici
Aromaticità Un composto si definisce aromatico se possiede un anello di elettroni chiuso. E anche detto aromatico, quando tramite i seguenti criteri soddisfa la regola di ückel: 1. I composti aromatici
ESERCIZI NMR. 1. La realizzazione di un tomografia (imaging) NMR è più o meno pericolosa per la persona di una tomografia PET?
 ESERCIZI NMR A SPUNTI DI RIFLESSIONE 1. La realizzazione di un tomografia (imaging) NMR è più o meno pericolosa per la persona di una tomografia PET? 2. Come si spiega il fatto che l adozione della tecnica
ESERCIZI NMR A SPUNTI DI RIFLESSIONE 1. La realizzazione di un tomografia (imaging) NMR è più o meno pericolosa per la persona di una tomografia PET? 2. Come si spiega il fatto che l adozione della tecnica
COMPOSTI CARBONILICI
 MPSTI ABNILII Il gruppo funzionale carbonilico rappresenta la specie chimica di più facile identificazione nello spettro I: grazie alla sua caratteristica banda di assorbimento (stretta e molto intensa)
MPSTI ABNILII Il gruppo funzionale carbonilico rappresenta la specie chimica di più facile identificazione nello spettro I: grazie alla sua caratteristica banda di assorbimento (stretta e molto intensa)
delle interazioni accoppiate dell intorno dei due atomi nell ambito della molecola.
 FATTORI CHE INFLUENZANO LA FREQUANZA DI ASSORBIMENTO Torniamo ora alla legge di Hooke: : abbiamo detto che questa relazione ci permette di conoscere la frequenza alla quale assorbirà un oscillatore di
FATTORI CHE INFLUENZANO LA FREQUANZA DI ASSORBIMENTO Torniamo ora alla legge di Hooke: : abbiamo detto che questa relazione ci permette di conoscere la frequenza alla quale assorbirà un oscillatore di
Processi di rilassamento. Mx,y
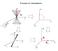 Processi di rilassamento M0 Mz Mx,y Mz Mx,y Rilassamento trasversale Rilassamento longitudinale Spin-spin, adiabatico Spin-reticolo, non adiabatico dm z M M0 = z dt T1 dm x,y Eqz. di Bloch Mz(t)=M0+[Mz(0)-M0]*exp(-t/T1)
Processi di rilassamento M0 Mz Mx,y Mz Mx,y Rilassamento trasversale Rilassamento longitudinale Spin-spin, adiabatico Spin-reticolo, non adiabatico dm z M M0 = z dt T1 dm x,y Eqz. di Bloch Mz(t)=M0+[Mz(0)-M0]*exp(-t/T1)
Lo spettro 1 H NMR. 2. i protoni non sono simmetrici rispetto ad un piano di simmetria. Possono essere equivalenti o non-equivalenti.
 Lo spettro 1 H NMR Protoni magneticamente equivalenti e non-equivalenti. Come si è detto nell'introduzione alla spettroscopia NMR, uno spettro al protone ( 1 H NMR) è costituito da tanti segnali quanti
Lo spettro 1 H NMR Protoni magneticamente equivalenti e non-equivalenti. Come si è detto nell'introduzione alla spettroscopia NMR, uno spettro al protone ( 1 H NMR) è costituito da tanti segnali quanti
RISONANZA MAGNETICA NUCLEARE (N.M.R.) o IMAGING A RISONANZA MAGNETICA (M.R.I.)
 RISONANZA MAGNETICA NUCLEARE (N.M.R.) o IMAGING A RISONANZA MAGNETICA (M.R.I.) e una tecnica non invasiva impiega radiazioni a bassa frequenza (non ionizzanti!) ν 10-100 MHz (radiofrequenze) sfrutta la
RISONANZA MAGNETICA NUCLEARE (N.M.R.) o IMAGING A RISONANZA MAGNETICA (M.R.I.) e una tecnica non invasiva impiega radiazioni a bassa frequenza (non ionizzanti!) ν 10-100 MHz (radiofrequenze) sfrutta la
Risonanza Magnetica Nucleare (NMR)
 Risonanza Magnetica Nucleare (NMR) La spettroscopia di risonanza magnetica nucleare (NMR, dall inglese Nuclear Magnetic Resonance) sfrutta la differenza di energia che i vari stati di spin nucleari possono
Risonanza Magnetica Nucleare (NMR) La spettroscopia di risonanza magnetica nucleare (NMR, dall inglese Nuclear Magnetic Resonance) sfrutta la differenza di energia che i vari stati di spin nucleari possono
Assorbimenti di alcani (stretching. Corso Metodi Fisici in Chimica Organica Prof. Renzo LUISI Uniba. vietata la vendita
 Assorbimenti di alcani (stretching C-H) Corso Metodi Fisici in Chimica rganica Prof. Renzo LUISI Uniba. vietata la vendita Analisi di spettri: ALCANI (C-H) 4000 3500 3000 2500 2000 1500 1300 1000 700 500
Assorbimenti di alcani (stretching C-H) Corso Metodi Fisici in Chimica rganica Prof. Renzo LUISI Uniba. vietata la vendita Analisi di spettri: ALCANI (C-H) 4000 3500 3000 2500 2000 1500 1300 1000 700 500
SPETTROSCOPIA UV-VIS LEZIONE 9
 SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
SPETTROSCOPIA UV-VIS LEZIONE 9 RADIAZIONE ELETTROMAGNETICA La radiazione elettromagnetica è la propagazione nello spazio e nel tempo dell energia elettromagnetica tramite onde e corpuscoli. natura ondulatoria:
Principi di Base di MR
 Principi di Base di MR Spin Proprietà fondamentale come la massa e la carica elettrica Protoni, elettroni e neutroni hanno tutti spin ½ Quando posta in un campo magnetico B 0, una particella con spin può
Principi di Base di MR Spin Proprietà fondamentale come la massa e la carica elettrica Protoni, elettroni e neutroni hanno tutti spin ½ Quando posta in un campo magnetico B 0, una particella con spin può
Lezione n. 27 / 28 NMR. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 27 / 28 Principi delle spettroscopie magnetiche Proprietà magnetiche della materia NMR 02/03/2008 Antonino Polimeno 1 Proprietà magnetiche
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 27 / 28 Principi delle spettroscopie magnetiche Proprietà magnetiche della materia NMR 02/03/2008 Antonino Polimeno 1 Proprietà magnetiche
ψ = Il carbonio (Z=6) - 2 elettroni equivalenti nello stato 2p - la funzione d onda globale deve essere antisimmetrica tripletto di spin, S=1
 s 1s s 1s p + p o p - configurazione elettronica del C nello stato fondamentale di tripletto di spin [He] (s) (p) p + p o p - configurazione elettronica del C nello stato eccitato di singoletto di spin
s 1s s 1s p + p o p - configurazione elettronica del C nello stato fondamentale di tripletto di spin [He] (s) (p) p + p o p - configurazione elettronica del C nello stato eccitato di singoletto di spin
Aldeidi e chetoni. 1) Rottura α 2) Rottura i. Più pronunciate nei chetoni. 3) Rottura β con trasposizione di H in γ (McLafferty)
 Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Aldeidi e chetoni Hanno potenziale di ionizzazione inferiore a quello degli alcooli dunque lo ione molecolare è più intenso e più facilmente osservabile anche in aldeidi e chetoni superiori. 1) Rottura
Mauro Tonellato SPETTROSCOPIA NMR. Indice
 Mauro Tonellato SPETTRSPIA NMR Indice 1. Introduzione 2 2. Spostamento himico 10 3. Area dei Picchi 19 4. Accoppiamento di Spin: Molteplicità 20 5. Albero di Frazionamento 25 6. Accoppiamento di Spin tra
Mauro Tonellato SPETTRSPIA NMR Indice 1. Introduzione 2 2. Spostamento himico 10 3. Area dei Picchi 19 4. Accoppiamento di Spin: Molteplicità 20 5. Albero di Frazionamento 25 6. Accoppiamento di Spin tra
FORMAZIONE DI LEGAMI. Il legame chimico si definisce quando fra due atomi esistono delle forze che danno luogo alla formazione di un aggregato.
 FORMAZIONE DI LEGAMI Il legame chimico si definisce quando fra due atomi esistono delle forze che danno luogo alla formazione di un aggregato. Presa r come distanza internucleare si osserva che l'energia
FORMAZIONE DI LEGAMI Il legame chimico si definisce quando fra due atomi esistono delle forze che danno luogo alla formazione di un aggregato. Presa r come distanza internucleare si osserva che l'energia
FENOMENI CHE CAUSANO ALLARGAMENTO DI RIGA NEGLI SPETTRI NMR. Nuclei con momento di quadrupolo; Sostanze paramagnetiche; Processi di scambio.
 FENOMENI HE USNO LLRGMENTO DI RIG NEGLI SPETTRI NMR Nuclei con momento di quadrupolo; Sostanze paramagnetiche; Processi di scambio. Sostanze paramagnetiche Le sostanze paramagnetiche sono caratterizzate
FENOMENI HE USNO LLRGMENTO DI RIG NEGLI SPETTRI NMR Nuclei con momento di quadrupolo; Sostanze paramagnetiche; Processi di scambio. Sostanze paramagnetiche Le sostanze paramagnetiche sono caratterizzate
RMN elementi di base
 RMN elementi di base Carpi 3 aprile 2009 Marco Serafini m.serafini@ausl.mo.it Campo magnetico Campo magnetico terrestre valore medio: 0.05 mt (0.5 Gauss) Magneti permanenti intensità: 5-300 mt (50-3000)
RMN elementi di base Carpi 3 aprile 2009 Marco Serafini m.serafini@ausl.mo.it Campo magnetico Campo magnetico terrestre valore medio: 0.05 mt (0.5 Gauss) Magneti permanenti intensità: 5-300 mt (50-3000)
ESERCIZI SPETTROMETRIA DI MASSA
 ESERCIZI SPETTROMETRIA DI MASSA A SPUNTI DI RIFLESSIONE 1. In cosa differiscono le tecniche soft da quelle strong? 2. Con quali tecniche si hanno maggiori probabilità di ottenere ioni molecolari? 3. Per
ESERCIZI SPETTROMETRIA DI MASSA A SPUNTI DI RIFLESSIONE 1. In cosa differiscono le tecniche soft da quelle strong? 2. Con quali tecniche si hanno maggiori probabilità di ottenere ioni molecolari? 3. Per
Bassa Energia Alta Energia
 L assorbimento di fotoni causa variazioni nelle vibrazioni molecolari hν Bassa Energia Alta Energia Vibrazioni Molecolari Atomi legati si muovono nello spazio Un ciclo vibrazionale ogni ~10-15 secondi
L assorbimento di fotoni causa variazioni nelle vibrazioni molecolari hν Bassa Energia Alta Energia Vibrazioni Molecolari Atomi legati si muovono nello spazio Un ciclo vibrazionale ogni ~10-15 secondi
Selezione per le Olimpiadi Internazionali della Chimica 2011 Fase nazionale Soluzione dei problemi a risposta aperta. :.. Xe O..
 Selezione per le limpiadi Internazionali della himica 2011 ase nazionale Soluzione dei problemi a risposta aperta 3. REATTIVITÀ E RMA DELLE MLELE: composti dello Xenon a) Le reazioni bilanciate richieste
Selezione per le limpiadi Internazionali della himica 2011 ase nazionale Soluzione dei problemi a risposta aperta 3. REATTIVITÀ E RMA DELLE MLELE: composti dello Xenon a) Le reazioni bilanciate richieste
ESERCIZI ESERCIZI. il basso d. aumenta lungo un periodo da sinistra verso
 ESERCIZI 1) L elettronegatività di un elemento: a è l energia che esso libera acquistando un elettrone e trasformandosi in ione negativo b è l energia necessaria per trasformarlo in ione positivo c indica
ESERCIZI 1) L elettronegatività di un elemento: a è l energia che esso libera acquistando un elettrone e trasformandosi in ione negativo b è l energia necessaria per trasformarlo in ione positivo c indica
Lezione n. 26. Principi generali della spettroscopia IR. 02/03/2008 Antonino Polimeno 1
 Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 26 Principi generali della spettroscopia IR 02/03/2008 Antonino Polimeno 1 Spettroscopia infrarossa (1) - La spettroscopia infrarossa studia
Chimica Fisica - Chimica e Tecnologia Farmaceutiche Lezione n. 26 Principi generali della spettroscopia IR 02/03/2008 Antonino Polimeno 1 Spettroscopia infrarossa (1) - La spettroscopia infrarossa studia
CENNI DI NMR DINAMICO. - Testo consigliato: Stradi
 CENNI DI NMR DINAMICO - Testo consigliato: Stradi La branca della spettroscopia NMR indicata con il termine di NMR dinamico si occupa dell effetto dei processi di scambio chimico (in senso ampio) sugli
CENNI DI NMR DINAMICO - Testo consigliato: Stradi La branca della spettroscopia NMR indicata con il termine di NMR dinamico si occupa dell effetto dei processi di scambio chimico (in senso ampio) sugli
INTERPRETAZIONE DEGLI SPETTRI IR
 INTERPRETAZIONE DEGLI SPETTRI IR Anche se non esistono gruppi di regole per la interpretazione completa degli spettri infrarossi, si è trovato che possono essere utili alcune linee-guida generali. 1. Cominciare
INTERPRETAZIONE DEGLI SPETTRI IR Anche se non esistono gruppi di regole per la interpretazione completa degli spettri infrarossi, si è trovato che possono essere utili alcune linee-guida generali. 1. Cominciare
UNIVERSITA DEGLI STUDI DI PARMA
 UNIVERSITA DEGLI STUDI DI PARMA FACOLTA DI FARMACIA Corso di laurea specialistica in Chimica e Tecnologia Farmaceutiche TESI SPERIMENTALE APPROCCI SINTETICI A SUBSTRATI ARRICCHITI IN 13 C E D COME POTENZIALI
UNIVERSITA DEGLI STUDI DI PARMA FACOLTA DI FARMACIA Corso di laurea specialistica in Chimica e Tecnologia Farmaceutiche TESI SPERIMENTALE APPROCCI SINTETICI A SUBSTRATI ARRICCHITI IN 13 C E D COME POTENZIALI
NMR e Biologia strutturale
 NMR e Biologia strutturale Forza di Lorentz F qv B Legge di Biot-Savart Legge di Ampére Magnetismo Il magnetismo è una proprietà della materia Generato da cariche in movimento, come elettroni Le proprietà
NMR e Biologia strutturale Forza di Lorentz F qv B Legge di Biot-Savart Legge di Ampére Magnetismo Il magnetismo è una proprietà della materia Generato da cariche in movimento, come elettroni Le proprietà
LO SPETTRO ELETTROMAGNETICO
 LO SPETTRO ELETTROMAGNETICO cresce cresce Raggi γ Raggi X UV IR Micio onde Onde radio Medio corte medie lunghe Processo: Eccitazione dei nuclei atomici Lontano Vicino Lontano Transizione degli e-interni
LO SPETTRO ELETTROMAGNETICO cresce cresce Raggi γ Raggi X UV IR Micio onde Onde radio Medio corte medie lunghe Processo: Eccitazione dei nuclei atomici Lontano Vicino Lontano Transizione degli e-interni
Spettroscopia. 05/06/14 SPET.doc 0
 Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
Spettroscopia 05/06/14 SPET.doc 0 Spettroscopia Analisi del passaggio di un sistema da uno stato all altro con scambio di fotoni Spettroscopia di assorbimento Spettroscopia di emissione: In entrambi i
STUDIO DELLA FASE MARTENSITICA TRAMITE NMR
 STUDIO DELLA FASE MARTENSITICA TRAMITE NMR Corso IUSS Modelli costitutivi per materiali avanzati a.a. 2009/2010 Presentazione di Andrea Capozzi e Stefano Pirotta SOMMARIO PARTE 1: Spettroscopia NMR Introduzione
STUDIO DELLA FASE MARTENSITICA TRAMITE NMR Corso IUSS Modelli costitutivi per materiali avanzati a.a. 2009/2010 Presentazione di Andrea Capozzi e Stefano Pirotta SOMMARIO PARTE 1: Spettroscopia NMR Introduzione
Legame chimico: covalente polare Legame covalente polare
 Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
Legame chimico: covalente polare Legame covalente polare Il passaggio dal legame covalente al legame ionico è il risultato di una distribuzione elettronica non simmetrica. Il simbolo δ (lettera greca delta
L accoppiamento indiretto spin-spin
 L accoppiamento indiretto spin-spin Stefano Chimichi Università di Firenze stefano.chimichi@unifi.it Stefano Chimichi, 2008 Spin-Spin Splitting nella Spectroscopia NMR Ovvero non tutti i picchi sono singoletti!
L accoppiamento indiretto spin-spin Stefano Chimichi Università di Firenze stefano.chimichi@unifi.it Stefano Chimichi, 2008 Spin-Spin Splitting nella Spectroscopia NMR Ovvero non tutti i picchi sono singoletti!
L ONDA ELETTROMAGNETICA UNITA DI MISURA E DEFINIZIONI. ν ν. λ =
 IR: Teoria Campo elettrico L ONDA ELETTROMAGNETICA Lunghezza d onda Direzione di propagazione Campo magnetico Lunghezza d onda (cm) Numero d onda (cm -1 ) UNITA DI MISURA E DEFINIZIONI c λ = ν ν ν = =
IR: Teoria Campo elettrico L ONDA ELETTROMAGNETICA Lunghezza d onda Direzione di propagazione Campo magnetico Lunghezza d onda (cm) Numero d onda (cm -1 ) UNITA DI MISURA E DEFINIZIONI c λ = ν ν ν = =
CARATTERIZZAZIONE RILASSOMETRICA DI VINI ED ACETI
 Università degli Studi di Torino Facoltà di Scienze M.F.N Corso di Laurea Magistrale in Chimica Clinica, Forense e dello Sport TESI DI LAUREA CARATTERIZZAZIONE RILASSOMETRICA DI VINI ED ACETI Candidato:
Università degli Studi di Torino Facoltà di Scienze M.F.N Corso di Laurea Magistrale in Chimica Clinica, Forense e dello Sport TESI DI LAUREA CARATTERIZZAZIONE RILASSOMETRICA DI VINI ED ACETI Candidato:
ACIDI CARBOSSILICI Gli acidi carbossilici presentano tre bande caratteristiche dovute al gruppo funzionale COOH
 ACIDI CABOSSILICI Gli acidi carbossilici presentano tre bande caratteristiche dovute al gruppo funzionale COOH OH C O Presenta infatti le bande di assorbimento caratteristiche dei due gruppi: C=O e OH
ACIDI CABOSSILICI Gli acidi carbossilici presentano tre bande caratteristiche dovute al gruppo funzionale COOH OH C O Presenta infatti le bande di assorbimento caratteristiche dei due gruppi: C=O e OH
Genesi del segnale RM
 Genesi del segnale RM imaging RM si fonda sul segnale ricavato all applicazione di radiofrequenze ( RF ) su nuclei di rogeno ( H ) immersi in un campo magnetico static CMS ). ali nuclei sono dotati di
Genesi del segnale RM imaging RM si fonda sul segnale ricavato all applicazione di radiofrequenze ( RF ) su nuclei di rogeno ( H ) immersi in un campo magnetico static CMS ). ali nuclei sono dotati di
PROPRIETÀ MAGNETICHE DELLA MATERIA. ovvero: comportamento della materia in presenza di un campo magnetico
 PROPRIETÀ MAGNETICHE DELLA MATERIA ovvero: comportamento della materia in presenza di un campo magnetico dinamometro Fenomenologia All'interno di un solenoide percorso da corrente si crea un campo magnetico
PROPRIETÀ MAGNETICHE DELLA MATERIA ovvero: comportamento della materia in presenza di un campo magnetico dinamometro Fenomenologia All'interno di un solenoide percorso da corrente si crea un campo magnetico
Teorie Acido-Base. valutazione degli acidi
 Teorie Acido-Base valutazione degli acidi Teoria di Brønsted-Lowry Acidi donano ioni H + Basi accettano ioni H + CH 3 C 2 H + H 2 CH 3 C 2 + H 3 + acido acetico CH 3 NH 2 + H 2 CH 3 NH 3+ + H metilammina
Teorie Acido-Base valutazione degli acidi Teoria di Brønsted-Lowry Acidi donano ioni H + Basi accettano ioni H + CH 3 C 2 H + H 2 CH 3 C 2 + H 3 + acido acetico CH 3 NH 2 + H 2 CH 3 NH 3+ + H metilammina
ATOMO. Legge della conservazione della massa Legge delle proporzioni definite Dalton
 Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
Democrito IV secolo A.C. ATOMO Lavoisier Proust Legge della conservazione della massa Legge delle proporzioni definite Dalton (808) Teoria atomica Gay-Lussac volumi di gas reagiscono secondo rapporti interi
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO
 La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
La teoria atomica moderna: il modello planetario L ELETTRONE SI MUOVE LUNGO UN ORBITA INTORNO AL NUCLEO La luce La LUCE è una forma di energia detta radiazione elettromagnetica che si propaga nello spazio
Mauro Tonellato SPETTROSCOPIA NMR. Indice
 Mauro Tonellato SPETTRSPIA NMR Indice 1. Introduzione 2 2. Spostamento himico 10 3. Area dei Picchi 19 4. Accoppiamento di Spin: Molteplicità 20 5. Albero di Frazionamento 25 6. Accoppiamento di Spin tra
Mauro Tonellato SPETTRSPIA NMR Indice 1. Introduzione 2 2. Spostamento himico 10 3. Area dei Picchi 19 4. Accoppiamento di Spin: Molteplicità 20 5. Albero di Frazionamento 25 6. Accoppiamento di Spin tra
STRUTTURA ATOMICA. tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica
 STRUTTURA ATOMICA tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica il nucleo è composto da protoni e neutroni che hanno massa = 1 nella scala dei pesi atomici
STRUTTURA ATOMICA tutti gli atomi hanno un nucleo carico positivamente che possiede quasi tutta la massa atomica il nucleo è composto da protoni e neutroni che hanno massa = 1 nella scala dei pesi atomici
