Daniela Carotti. Dipartimento di Scienze Biochimiche III piano - stanza 310.
|
|
|
- Aurelio Mantovani
- 7 anni fa
- Visualizzazioni
Transcript
1 Daniela Carotti Dipartimento di Scienze Biochimiche III piano - stanza daniela.carotti@uniroma1.it
2 organismo cellula componenti biochimiche acqua ioni carboidrati riserva di energia ruolo strutturale lipidi riserva di energia ruolo strutturale ormoni proteine enzimi ormoni movimento trasporto recettori ruolo strutturale acidi nucleici DNA conservazione dell informazione mrnatrasporto dell informazione trna decodifica dell informazione
3 globuli rossi fibroblasti ci fanno respirare ci fanno stare in piedi miociti neuroni ci fanno sentire ci fanno muovere Le cellule sono macchine chimiche che degradano molecole nutritive traendone Energia, che usano per sintetizzare biomolecole, compiere lavoro meccanico, trasportare molecole o ioni, trasferire l informazione genetica.
4 Il metabolismo è la somma di tutte le trasformazioni chimiche che avvengono in un organismo o in una cellula Il catabolismo è l insieme delle reazioni che portano alla scissione di molecole complesse (ricche di energia) in sostanze più semplici (povere di energia). Rilascia energia Nutrienti contenenti energia Carboidrati Grassi Proteine Molecole complesse Carboidrati Grassi Proteine Attività cellulari catabolismo anabolismo E Prodotti di scarto poveri di energia CO 2 H 2 O NH 3 Molecole semplici L anabolismo è l insieme delle reazioni che portano alla formazione di molecole complesse a partire da molecole più semplici. Richiede energia
5 Quali sono le molecole che scindiamo per ottenere energia? 6 6 Acido oleico Energia Lavoro
6 Elettroforesi bidimensionale di proteine di E.coli
7
8 Proteine Le proteine sono macromolecole a peso molecolare variabile da a oltre dalton Sono costituite da H, C, O e N; il contenuto di N è il 16% del peso secco ed è costante Nelle proteine possono trovarsi S e P in quantità variabile Sono polimeri lineari costituiti dall unione di un grande numero di unità elementari: gli amminoacidi Ciascuna proteina ha una propria struttura tridimensionale che la rende capace di svolgere specifiche funzioni biologiche
9 Amminoacidi Hanno almeno un gruppo amminico e un gruppo carbossilico -NH 2 -COOH alanina CH 3 CH COOH NH 2 CH 2 NH 2 CH 2 COOH In natura esistono più di 300 amminoacidi, ma soltanto 20 sono incorporati nelle proteine dei mammiferi perché sono gli unici codificati dal DNA
10 Amminoacidi alanina CH 3 CH 2 NH 2 CH NH 2 CH 2 COOH COOH α β Acido 3-aminopropanoico CH 3 CH 2 CH COOH NH 2 CH 3 CH CH 2 COOH NH 2 neurotrasmettitore CH 2 NH 2 CH 2 CH 2 COOH α β γ Acido aminobutirrico In catene più lunghe il gruppo aminico può essere in posizione α, β, γ, ecc. AMINOACIDI naturali sintetici proteici non proteici
11 Gli amminoacidi proteici hanno alcune caratteristiche comuni il gruppo R è diverso per i vari amminoacidi e costituisce la catena laterale o radicale Hanno tutti un atomo di idrogeno H R Cα NH 2 COOH Sono tutti α- amimnoacidi perché il gruppo amminico e il gruppo carbossilico sono legati all atomo di carbonio α Ci sono anche aa liberi, cioè non associati a proteine, con funzioni specializzate: neurotrasmettitori, ormoni CH 3 CH 2 COOH β α Il carbonio α è quello più vicino alla funzione più ossidata
12 Gli amminoacidi sono molecole otticamente attive In tutti gli amminoacidi proteici il carbonio α è asimmetrico (tranne nella glicina) cioè è legato con quattro gruppi chimici diversi Funzione più ossidata in alto NH 2 α H α NH 2 R L amimnoacido R D - amimnoacido Tutti gli amminoacidi proteici sono L-aminoacidi
13
14 Proprietà acido-base Quando un amminoacido viene sciolto in H 2 O diventa uno ione dipolare (zwitterione)) che può agire sia come acido (donatore di protoni) che come base (accettore di protoni) Le sostanze che hanno questa doppia natura si definiscono anfòtere o anfoliti il gruppo carbossilico si dissocia H R Cα COO - NH 3 + ph fisiologico circa 7,4 il gruppo amminico si protona
15 La natura del gruppo -R conferisce proprietà diverse a ciascun amminoacido
16 Le proteine animali contengono tutti gli aminoacidi essenziali Le proteine vegetali sono povere o prive di alcuni aminoacidi essenziali es.: il mais è povero di lisina e triptofano
17 Classificazione basata sulla conformazione PROTEINE FIBROSE: hanno una disposizione spaziale caratterizzata da lunghe catene disposte parallelamente a formare strutture allungate lineari o planari. Sono insolubili collageno mioglobina PROTEINE GLOBULARI: la catena polipeptidica si ripiega nello spazio in modo da assumere una forma pseudosferica. Sono solubili
18 PROTEINE Classificazione basata sulla composizione chimica 1.Proteine semplici se costituite solo da amminoacidi 2. Proteine coniugate se alla proteina è legato un gruppo non proteico, indicato con il termine di GRUPPO PROSTETICO Glicoproteine Lipoproteine Nucleoproteine Metalloproteine Fosfoproteine Cromoproteine
19 PROTEINE Classificazione delle proteine basata sulla funzione Proteine responsabili di catalisi enzimatica Proteine di trasporto Proteine di deposito Proteine di difesa Proteine responsabili del movimento Proteine di sostegno meccanico Proteine deputate alla trasmissione dei segnali
20 LEGAME PEPTIDICO È UN LEGAME COVALENTE MOLTO FORTE idrolisi acida o basica HCl 6M o NaOH 4M per 24 ore a 120 C sottovuoto idrolisi enzimatica Enzimi proteolitici a 37 C
21 L unità base ripetuta lungo la catena principale è (NH CαH C=O) Le catene laterali degli aminoacidi sporgono all esterno della catena e non partecipano mai alla formazione del legame peptidico
22 La rotazione è permessa solo intorno al legame N-C α (angolo φ, phi) e al legame C α -C (angolo ψ, psi)
23 Lo scheletro di una catena polipeptidica può essere immaginato come una serie di piani rigidi consecutivi che hanno in comune un punto di rotazione costituito dal carbonio α, da cui sporgono le catene laterali dei diversi amminoacidi
24 Teoricamente φ e ψ possono avere qualsiasi valore compreso tra -180 e +180 Molte combinazioni di angoli (φ, ψ) per gli amminoacidi non sono permesse, a causa delle collisioni steriche fra atomi della catena principale e/o delle catene laterali Si delimitano così solo 3 regioni ben definite corrispondenti alle coppie di valori consentiti
25 Le proteine sono organizzate secondo quattro livelli strutturali Struttura primaria: è la sequenza lineare degli aminoacidi dal N terminale al C terminale Struttura secondaria: conformazioni regolari dovute principalmente ripiegamento della catena polipeptidica su se stessa Struttura terziaria: ripiegamento della catena Struttura quaternaria: associazioni tra più catene polipetidiche
26 STRUTTURA PRIMARIA Sequenza degli aminoacidi, cioè l ordine con cui si succedono nella catena polipeptidica Lys-Arg-Glu-Glu-Gly-Gly-Asp-Ser-Lys-Thr-Ala-Ala La sequenza degli aminoacidi non è casuale ma rigorosamente definita dal codice genetico del DNA La struttura primaria stabilisce le strutture successive che la proteina può avere Due proteine con la stessa composizione aminoacidica ma con sequenza diversa sono due proteine diverse Alterazioni della sequenza aminoacidica di una proteina possono provocare la perdita della attività
27 Struttura secondaria La struttura secondaria descrive la conformazione della catena principale di ciascun residuo aminoacidico di quel tratto rispetto a quelli adiacenti Si formano tratti ordinati di struttura secondaria quando una serie di residui aminoacidici vicini adottano angoli φ e ψ simili α-elica struttura β a foglietto ripiegato La STRUTTURA SECONDARIA STRUTTURA SECONDARIA si riferisce alla disposizione regolare della catena polipeptidica in una direzione dello spazio
28 α - Elica E determinata dall avvolgimento elicoidale della catena polipeptidica intorno ad un asse immaginario L avvolgimento è regolare e destrorso L a-elica è stabilizzata dai legami H i che si formano tra i gruppi -C=O e HN- di legami peptidici che si trovano su due spire adiacenti legami intramolecolari
29 Le catene laterali degli aminoacidi sono proiettate all esterno dell elica la struttura ad α-elica viene interrotta dalla presenza della prolina e di aminoacidi con R troppo ingombranti
30 La STRUTTURA BETA è caratterizzata dal ripiegamento a zig-zag zag della catena polipeptidica I beta sheet sono pieghettati: i carboni alfa del legame peptidico si alternano tra sopra e sotto il piano del foglio E stabilizzata da legami H che si formano tra i gruppi CO e NH di legami peptidici di catene adiacenti legami intermolecolari
31 Ripiegamento nello spazio dell intera catena polipeptidica: catena principale e catene laterali Struttura terziaria tratti a struttura disordinata (random coiled) tratti ad α-elica tratti con struttura beta
32 Legami che stabilizzano la struttura terziaria interazioni idrofobiche forze di Van der Waals legami idrogeno catena polipeptidica ponti disolfuro legami ionici
33 Nella struttura terziaria quasi tutte le catene idrofobiche si trovano all'interno e quasi tutte le catene laterali idrofile sull'esterno della proteina ad interagire con l'acqua Le proteine globulari sono compatte in modo da escludere del tutto l'acqua dal loro core idrofobico
34 STRUTTURA QUATERNARIA Associazione di più catene polipeptidiche che vengono dette SUBUNITA Le subunità possono essere uguali (struttura quaternaria OMOGENEA) o diverse (struttura quaternaria ETEROGENEA) Le forze che tengono associati i monomeri sono le stesse che stabilizzano la struttura terziaria
35 Le proteine sono organizzate secondo quattro livelli strutturali Struttura primaria: è la sequenza lineare degli aminoacidi dal N terminale al C terminale Legame covalente: legame peptidico Legami idrogeno tra C=O e NH Legami tra le catene laterali Struttura secondaria: conformazioni regolari dovute principalmente ripiegamento della catena polipeptidica su se stessa Struttura terziaria: ripiegamento della catena Legami deboli: legami idrogeno legami idrofobici legami ionici Struttura quaternaria: associazioni tra più catene polipetidiche
36 Le proteine quando perdono la loro organizzazione strutturale perdono la funzionalità Si dice che le proteine sono denaturate
37 Le proteine denaturate formano degli agglomerati molecolari insolubili, determinati dalla formazione di legami aspecifici
38 Collageno E la proteina più abbondante nel nostro organismo: costituisce circa il 25-30% delle nostre proteine
39 COLLAGENO L unità fondamentale del collageno è il TROPOCOLLAGENO Il TROPOCOLLAGENO (15A x 3000A) è formato da tre catene polipeptidiche avvolte tra loro a costituire una TRIPLA ELICA con andamento destrorso Ogni catena ha una struttura elicoidale sinistrorsa: passo 8,6 A residui per giro 3 incremento per residuo 2,8 A
40 Il collageno è costituito da: glicina 33% prolina e idrossiprolina 33% altri aa 33% x è Sequenza ripetitiva (GLY - x - y) n in genere una prolina o una idrossiprolina La prolina induce una curvatura nella catena polipetidica Non è una struttura ad α elica
41 La tripla elica e e stabilizzata da legami idrogeno tra le catene Le tre catene sono sfalsate: i residui di Gly non sono mai in corrispondenza Gli anelli pirrolidinici delle proline e delle idrossiproline sono rivolti all esterno Le catene laterali ingombranti degli altri AA sono rivolte all esterno Struttura della tripla elica collageno vista da una delle estremità
42 Le molecole di tropocollageno si associano in fibre La catena laterale di alcuni aminoacidi viene modificata con una reazione enzimatica che richiede la vitamina C Nella fibrilla, le molecole di tropocollageno sono unite da legami trasversali (legami crociati) RESISTENZA MECCANICA
43 Amido omopolisaccaride contenente glucosio amilosio 10-20% ,000 unità di glucosio amilopectina 80-90% 10 6 unità di glucosio granuli di amido da semi di pisello colorati con lo iodio
44 Glucosio poliidrossi aldeide nuovo ossidrile, di natura riducente
45 Gli aldosi
46 Glucosio Fruttosio poliidrossi aldeide poliidrossi chetone
47 Fruttosio poliidrossi chetone
48 I chetosi
49 Come due molecole di glucosio si legano fra di loro legame α(1-4) 4)glicosidico legame β(1-4) 4)glicosidico
50 Disaccaridi saccarosio lattosio glucosio fruttosio galattosio glucosio legame 1-41 α-glicosidico legame 1-41 β-glicosidico
51 Polisaccaridi Legame α(1-6) glicosidico Legame α(1-4) glicosidico Amido (piante) Glicogeno (animali)
52 Cellulosa parete cellulare microfibrille di cellulosa nella parete cellulare cellule legame 1-4 β-glicosidico E un omopolisaccaride lineare molecole di cellulosa Non possiamo ricavare glucosio dalla cellulosa perché non siamo in grado di scindere i legami 1-41 β glicosidici quando sono presenti in un polimero
53 glucosio fruttosio monosaccaridi saccarosio lattosio disaccaridi amido glicogeno polisaccaridi
54 trigliceridi glicerolo CH 2 CH CH 2 CH 2 CH CH 2 OH OH OH H 2 OO O C H 2 OO O C H 2 OO O (CH ) n 2 CH 3 legame estere (CH ) n 2 CH 3 C (CH 2) n CH 3 O + 3 HO C (CH 2) n CH 3 acido grasso
55 Acidi grassi R CH 2 CH 2 CH 2 CH 2 COO - δ γ β α Le catene di atomi di C, catene alifatiche, possono essere lunghe anche atomi di C Acidi grassi insaturi R CH 2 CH CH CH 2 COO - H H H C C C C cis H trans
56 olio burro liquido a temperatura ambiente Ricco in acidi grassi insaturi solido a temperatura ambiente Ricco in acidi grassi saturi
57 Fosfolipidi O CH 2 O C O (CH ) n 2 CH 3 CH CH 2 O O C O (CH ) n 2 CH 3 CP (CH O 2CH ) n 2 CH 3 COO - O - NH 3 + acido fosfatidil fosfatidico serina
58 Fosfolipidi
59 Colesterolo
60
61 Struttura della membrana cellulare fosfogliceride sfingomielina colesterolo testa idrofilica coda idrofobica
62
Introduzione alla biologia della cellula. Lezione 2 Le biomolecole
 Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
Introduzione alla biologia della cellula Lezione 2 Le biomolecole Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono
AMMINOACIDI E PROTEINE
 AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
AMMINOACIDI E PROTEINE 1 AMMINOACIDI Gli amminoacidi sono composti organici composti da atomi di carbonio, idrogeno, ossigeno e azoto e in alcuni casi anche da altri elementi come lo zolfo. Gli amminoacidi
CARBOIDRATI C H O ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO
 CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
CARBOIDRATI ZUCCHERO SACCARIDE GLUCIDE CARBOIDRATO C H O carboidrati C n H 2n O n H C O C O Il glucosio è un monosaccaride con 6 atomi di carbonio GLUCOSIO Forma ciclica Forma lineare a ph 7 circa lo 0,0026%
Composti organici. I composti organici. Atomi e molecole di carbonio. Atomi e molecole di carbonio. Gruppi funzionali. Isomeri
 I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
I composti organici Atomi e molecole di carbonio Carboidrati Lipidi Proteine Acidi nucleici Composti organici Materiale composto da biomolecole - Formate in buona parte da legami ed anelli di carbonio.
Proprietà comuni. Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici
 Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Gli aminoacidi Proprietà comuni Il gruppo α-carbossilico b è un acido più forte del gruppo carbossilico degli acidi alifatici paragonabili Il gruppo α-aminico è un acido più forte (o una base più debole
Struttura degli amminoacidi
 AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE AMMINOACIDI, PEPTIDI E PROTEINE Le proteine sono macromolecole costituite dall unione di un grande numero di unità elementari: gli amminoacidi
Valitutti, Falasca, Tifi, Gentile. Chimica. concetti e modelli.blu
 Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Valitutti, Falasca, Tifi, Gentile Chimica concetti e modelli.blu 2 Capitolo 10 Le basi della biochimica 3 Sommario 1. Le molecole biologiche si dividono in quattro classi 2. I carboidrati sono il «carburante»
Biologia. Lezione 09/11/2010
 Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
Biologia Lezione 09/11/2010 Tutte le molecole contenute nelle cellule sono costituite da composti del carbonio Zuccheri Lipidi Proteine Acidi nucleici Polimeri Sono macromolecole formate da unità (MONOMERI)
scaricato da www.sunhope.it Proteine semplici costituite dai soli amminoacidi
 Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
Proteine semplici costituite dai soli amminoacidi Proteine coniugate costituite dagli amminoacidi + porzioni di natura non amminoacidica dette GRUPPI PROSTETICI Le Proteine coniugate prive del gruppo prostetico
L ACQUA E LE SUE PROPRIETÀ
 L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
L ACQUA E LE SUE PROPRIETÀ L acqua è una sostanza indispensabile per tutte le forme di vita. Ogni molecola di acqua (H2O) è formata da due atomi di idrogeno e un atomo di ossigeno, uniti tramite due legami
 http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
http://digilander.libero.it/glampis64 Idrogeno, ossigeno, carbonio e azoto costituiscono il 99% delle cellule. I composti del carbonio sono chiamati composti organici o molecole organiche. I composti organici
La struttura delle proteine
 La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La struttura delle proteine Funzioni delle proteine Strutturali Contrattili Trasporto Riserva Ormonali Enzimatiche Protezione Struttura della proteina Struttura secondaria: ripiegamento locale della catena
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) L atomo del carbonio (C).. C. Atomo tetravalente. C C C C Gli idrocarburi I legami del carbonio 109.5 gradi
CARBOIDRATI SEMPLICI
 CARBOIDRATI Dal greco glucos =dolce Glucidi Zuccheri Sostanze formate acqua e carbonio Hanno forma molecolare (CH₂O)n 1 CARBOIDRATI SEMPLICI Monosaccaridi, una sola unità di poliidrossi aldeide o di poliidrossi
CARBOIDRATI Dal greco glucos =dolce Glucidi Zuccheri Sostanze formate acqua e carbonio Hanno forma molecolare (CH₂O)n 1 CARBOIDRATI SEMPLICI Monosaccaridi, una sola unità di poliidrossi aldeide o di poliidrossi
LE PROTEINE. SONO Polimeri formati dall unione di AMMINOACIDI (AA) Rende diversi i 20 AA l uno dall altro UN ATOMO DI C AL CENTRO
 LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
LE PROTEINE SONO Polimeri formati dall unione di ATOMI DI C, H, N, O CHE SONO AMMINOACIDI (AA) Uniti tra loro dal Legame peptidico 20 TIPI DIVERSI MA HANNO STESSA STRUTTURA GENERALE CON Catene peptidiche
sono le unità monomeriche che costituiscono le proteine hanno tutti una struttura comune
 AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
AMINO ACIDI sono le unità monomeriche che costituiscono le proteine sono 20 hanno tutti una struttura comune sono asimmetrici La carica di un amino acido dipende dal ph Classificazione amino acidi Glicina
Formazione del legame peptidico:
 Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
Formazione del legame peptidico: Planare, ha una forza intermedia tra il legame semplice ed il legame doppio. 2^ lezione N R C C O O O + R N R C O C O O N R C C N C C O Ogni piano delle unità peptidiche
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE
 CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
CORSO DI BIOCHIMICA PER INGEGNERIA BIOMEDICA I ESERCITAZIONE 1) Che tipo di ibridazione ha il carbonio coinvolto nel doppio legame degli alcheni? Descrivi brevemente. Alcheni Ibridazione sp 2 2s p x p
Immagini e concetti della biologia
 Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Sylvia S. Mader Immagini e concetti della biologia 2 A3 Le molecole biologiche 3 Il carbonio è l elemento di base delle biomolecole Una cellula batterica può contenere fino a 5000 tipi diversi di composti
Chimotripsina Una proteina globulare. Glicina Un amminoacido
 Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Chimotripsina Una proteina globulare Glicina Un amminoacido - In teoria un numero enorme di differenti catene polipeptidiche potrebbe essere sintetizzato con i 20 amminoacidi standard. 20 4 = 160.000 differenti
Le macromolecole dei tessuti - 1
 Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
Le macromolecole dei tessuti - 1 Che cosa sono le proteine? Sono macromolecole complesse ad alta informazione Sono costituite da una o più catene polipeptidiche Ogni catena peptidica è composta da centinaia
BIOMOLECOLE LE BASI DELLA BIOCHIMICA. Capitolo 1 Dal Carbonio agli OGM PLUS
 BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
BIOMOLECOLE LE BASI DELLA BIOCHIMICA Capitolo 1 Dal Carbonio agli OGM PLUS BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici Proteine BIOMOLECOLE Carboidrati Lipidi Acidi Nucleici - monosaccaridi - disaccaridi
Aminoacidi. Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α
 Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Aminoacidi Gli α-aminoacidi sono molecole con almeno due gruppi funzionali legati al carbonio α 1 Isomeria ottica Tutti gli AA, esclusa la glicina, presentano almeno un atomo di carbonio asimmetrico, il
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
Amminoacidi Peptidi Proteine Amminoacidi-Peptidi-Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Stereoisomeri: composti con la stessa connessione tra gli atomi, ma con una differente
I materiali della vita
 I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
I materiali della vita I componenti chimici dei viventi Il corpo dei viventi è formato da relativamente pochi elementi chimici e in percentuale diversa da quella del mondo non vivente. Le molecole dei
Capitolo 3 Le biomolecole
 apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
apitolo 3 Le biomolecole opyright 2006 Zanichelli editore I composti organici e i loro polimeri 3.1 La diversità molecolare della vita è basata sulle proprietà del carbonio Un atomo di carbonio può formare
Diagramma di Ramachandran
 Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Chimica Biologica A.A. 2010-2011 Diagramma di Ramachandran Diagramma di Ramachandran Catena polipeptidica La formazione in successione di legami peptidici genera la cosiddetta catena principale o scheletro
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici STRUTTURA TERZIARIA La struttura tridimensionale
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
STRUTTURA E FUNZIONE DELLE PROTEINE PROTEINE 50% DEL PESO SECCO DI UNA CELLULA STRUTTURA intelaiatura citoscheletrica strutture cellulari impalcatura di sostegno extracellulare FUNZIONE catalisi enzimatica
LE PROTEINE -struttura tridimensionale-
 LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
LE PROTEINE -struttura tridimensionale- Struttura generale di una proteina Ceruloplasmina Cosa sono??? Sono biopolimeri con forme ben definite. composti da molteplici amminoacidi, legati con legami peptidici
I composti organici. Il carbonio e i composti organici
 I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
I composti organici Il carbonio e i composti organici COSA SONO I COMPOSTI ORGANICI? I composti organici sono composti in cui uno o più atomi di carbonio (C) sono uniti tramite un legame covalente ad atomi
H N H R N H R N R R N R H H H
 AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
AMMINE Sono derivati dell ammoniaca (NH 3 ) nei quali uno o più atomi di idrogeno sono sostituiti da altrettanti radicali alchilici (R-, come ad esempio il gruppo -CH 3 ). Come l ammoniaca anche le ammine
Legami chimici. Covalente. Legami deboli
 Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
Legami chimici Covalente Legami deboli Legame fosfodiesterico Legami deboli Legami idrogeno Interazioni idrofobiche Attrazioni di Van der Waals Legami ionici Studio delle macromolecole Lipidi
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici
 I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
I composti organici della vita: carboidrati, lipidi, proteine e acidi nucleici La seta della tela di ragno è un insieme di macromolecole, dette proteine. Sono le caratteristiche fisico-chimiche di queste
LE MOLECOLE BIOLOGICHE
 LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
LE MOLECOLE BIOLOGICHE Le cellule contengono quattro famiglie principali di molecole organiche Zuccheri (monosaccaridi) - forniscono una fonte di energia - subunità dei polisaccaridi Amminoacidi - subunità
La chimica della pelle
 La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
La chimica della pelle 1 Gli amminoacidi Queste unità hanno la particolare caratteristica di contenere nella stessa molecola un gruppo acido (- COOH) ed uno basico (- NH 2 ), legati tra loro attraverso
LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche:
 LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
LEZIONE n 1 LE MACROMOLECOLE BIOLOGICHE Le cellule contengono 4 famiglie principali di molecole organiche: macromolecole Macromolecole macromolecole I componenti chimici di una cellula -Le macromolecole
30/10/2015 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE
 LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
LIVELLI DI ORGANIZZAZIONE STRUTTURALE DELLE PROTEINE 1 CARATTERISTICHE DEL LEGAME PEPTIDICO lunghezza intermedia tra un legame singolo e uno doppio ibrido di risonanza per il parziale carattere di doppio
Funzioni delle proteine
 Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
Funzioni delle proteine ENZIMI Proteine di trasporto Proteine di riserva Proteine contrattili o motili Proteine strutturali Proteine di difesa Proteine regolatrici Proteine di trasporto Emoglobina Lipoproteine
CHIMICA ORGANICA. 2 a D. Novembre Scuola Secondaria di Primo Grado «Bonazzi Lilli» IC PG 14. Ponte Felcino Perugia.
 CHIMICA ORGANICA 2 a D Novembre 2014 Scuola Secondaria di Primo Grado «Bonazzi Lilli» IC PG 14 Ponte Felcino Perugia Manuela Casasoli IL CARBONIO La chimica organica studia i composti organici in cui il
CHIMICA ORGANICA 2 a D Novembre 2014 Scuola Secondaria di Primo Grado «Bonazzi Lilli» IC PG 14 Ponte Felcino Perugia Manuela Casasoli IL CARBONIO La chimica organica studia i composti organici in cui il
LE PROTEINE SINTESI PROTEICA. funzione delle proteine nel nostro organismo
 LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
LE PTEIE Le proteine sono sostanze organiche presenti in tutte le cellule di tutti gli organismi viventi Le proteine sono costituite da,,,, (S) Struttura delle proteine Le proteine sono macromolecole (
BIOMOLECOLE. I mattoni delle cellule.
 BIMLECLE I mattoni delle cellule PRINCIPALI GRUPPI FUNZINALI I gruppi funzionali sono gruppi di atomi, uniti da legami covalenti, che conferiscono alla molecola di cui fanno parte un comportamento chimico
BIMLECLE I mattoni delle cellule PRINCIPALI GRUPPI FUNZINALI I gruppi funzionali sono gruppi di atomi, uniti da legami covalenti, che conferiscono alla molecola di cui fanno parte un comportamento chimico
PROTEINE DEFINIZIONE:
 Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Cap.4 Le PROTEINE DEFINIZIONE: Macromolecole formate di AA della serie L uniti tra loro da un legame peptidico. FUNZIONI DELLE PROTEINE Enzimi Proteine di riconoscimento Proteine di trasporto Proteine
Le idee della chimica
 G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
G. Valitutti A.Tifi A.Gentile Seconda edizione Copyright 2009 Zanichelli editore Capitolo 25 Le basi della biochimica 1. I carboidrati 2. I lipidi 3. Gli amminoacidi, i peptidi e le proteine 4. La struttura
LA CHIMICA DELLA VITA
 LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
LA CHIMICA DELLA VITA L elemento presente in tutte le molecole caratteristiche degli esseri viventi è IL CARBONIO Il carbonio ha numero atomico 6 (Z=6). Ha valenza 4: ai suoi atomi mancano 4 elettroni
ACIDI GRASSI INSATURI
 LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
LIPIDI ACIDI GRASSI SATURI ACIDI GRASSI INSATURI TRIGLICERIDI TRIGLICERIDI Grassi neutri o lipidi semplici glicerolo + 1 acido grasso monogliceride glicerolo + 2 acidi grassi digliceride glicerolo + 3
Chimica Biologica A.A α-elica foglietto β reverse turn
 Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
Chimica Biologica A.A. 2010-2011 α-elica foglietto β reverse turn Str. Secondaria sperimentalmente osservata: Si distinguono fondamentalmente tre tipi di strutture secondarie: α elica foglietto β reverse
LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI PROTEINE. sono ACIDI NUCLEICI. molecole complesse = POLIMERI. formate dall'unione di
 LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
LE BIOMOLECOLE LE BIOMOLECOLE DETTE ANCHE MOLECOLE ORGANICHE; CARBOIDRATI LE BIOMOLECOLE sono LIPIDI PROTEINE ACIDI NUCLEICI molecole complesse = POLIMERI formate dall'unione di molecole semplici = MONOMERI
Formazione. di un peptide.
 Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
Formazione. di un peptide. Quando due aminoacidi si uniscono si forma un legame peptidico. In questo caso il dipeptide glicilalanina (Gly-Ala) viene mostrato come se si stesse formando in seguito a eliminazione
I composti organici e i loro polimeri
 I ARBIDRATI I composti organici e i loro polimeri La diversità molecolare della vita è basata sulle proprietà del ARBNI. Un atomo di carbonio può formare quattro legami covalenti. Questi legami gli permettono
I ARBIDRATI I composti organici e i loro polimeri La diversità molecolare della vita è basata sulle proprietà del ARBNI. Un atomo di carbonio può formare quattro legami covalenti. Questi legami gli permettono
SOLUZIONI DEGLI ESERCIZI
 Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
Dal carbonio agli OGM Biochimica e biotecnologie SOLUZIONI DEGLI ESERCIZI Capitolo 0 Il mondo del carbonio 1. b, e 2. d 3. 7 4. 5. 6. 7. a) Isomeria di posizione; b) i due composti non sono isomeri; c)
CPIA 1 FOGGIA punto di erogazione San Severo. Prof.ssa ANNA LUCIA L. CANCELLIERE
 CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
CPIA 1 FOGGIA punto di erogazione San Severo Prof.ssa ANNA LUCIA L. CANCELLIERE Sono delle grandi molecole che troviamo nel mondo dei viventi sia come molecole costituenti gli organismi viventi che come
Carboidrati. Principale ciclo energetico della biosfera si basa sul metabolismo dei carboidrati
 Carboidrati Principale ciclo energetico della biosfera si basa sul metabolismo dei carboidrati Carboidrati: funzioni Fornire energia chimica Sostegno (parete cellulare vegetale) Protezione (parete batterica)
Carboidrati Principale ciclo energetico della biosfera si basa sul metabolismo dei carboidrati Carboidrati: funzioni Fornire energia chimica Sostegno (parete cellulare vegetale) Protezione (parete batterica)
2. La chimica della vita Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA
 Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA Simbolo Numero atomico % in organismi viventi Elementi che costituiscono circa il 96% del peso degli organismi viventi O 8 65.0 C 6 18.5
Tutta la MATERIA è soggetta alle leggi della CHIMICA e della FISICA Simbolo Numero atomico % in organismi viventi Elementi che costituiscono circa il 96% del peso degli organismi viventi O 8 65.0 C 6 18.5
Costituzione dei viventi
 Costituzione dei viventi La materia e costituita da elementi chimici in forma pura o in combinazioni dette composti 25 dei 92 elementi naturali sono costituenti essenziali dei viventi 4 (C, O,, N) costituiscono
Costituzione dei viventi La materia e costituita da elementi chimici in forma pura o in combinazioni dette composti 25 dei 92 elementi naturali sono costituenti essenziali dei viventi 4 (C, O,, N) costituiscono
Amminoacidi Peptidi Proteine
 Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Amminoacidi Peptidi Proteine Amminoacidi: Struttura generale COOH H NH 2 Centro chiralico Gli amminoacidi nelle molecole proteiche sono tutti stereoisomeri L IDROFOBOCI IDROFOBOCI IDROFILICI Secondo gruppo
Organizzazione della materia
 Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
Organizzazione della materia Elementi: sostanze che non possono essere scisse in altre più semplici mediante reazioni chimiche ordinarie. Atomo: è la porzione più piccola di un elemento, formato da 3 particelle
α-cheratine (α-elica) collageni e cheratine β-cheratine (conformazione β) M.N. Gadaleta
 Per la scoperta delle conformazioni più comuni delle catene polipeptidiche cioè α-elica e β-conformazione è stato particolarmente importante lo studio delle cheratine, proteine fibrose, e l analisi della
Per la scoperta delle conformazioni più comuni delle catene polipeptidiche cioè α-elica e β-conformazione è stato particolarmente importante lo studio delle cheratine, proteine fibrose, e l analisi della
F. Fogolari Milano, Marzo
 Biomolecole - 1 Federico Fogolari Dipartimento Scientifico e Tecnologico Universita di Verona Ca Vignal 1, Strada Le Grazie 15 37134 Verona, Italy tel. ++39-045-8027906 fax. ++39-045-8027929 email: fogolari@sci.univr.it
Biomolecole - 1 Federico Fogolari Dipartimento Scientifico e Tecnologico Universita di Verona Ca Vignal 1, Strada Le Grazie 15 37134 Verona, Italy tel. ++39-045-8027906 fax. ++39-045-8027929 email: fogolari@sci.univr.it
Disaccaridi: cellobiosio e maltosio
 Disaccaridi: cellobiosio e maltosio I disaccaridi contengono un legame glicosidico tra il carbonio anomerico di uno zucchero e un ossidrile qualunque di un secondo zucchero. Il legame può essere a o b.
Disaccaridi: cellobiosio e maltosio I disaccaridi contengono un legame glicosidico tra il carbonio anomerico di uno zucchero e un ossidrile qualunque di un secondo zucchero. Il legame può essere a o b.
COMPORTAMENTO ANFOTERO DEGLI AA
 Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
Proprietà acido-basiche degli aminoacidi FORMA NON IONICA Non esiste a nessun valore di ph FORMA ZWITTERIONICA È la forma prevalente a ph 7 COMPORTAMENTO ANFOTERO DEGLI AA CARICA NETTA +1 CARICA NETTA
Struttura delle Proteine
 Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Chimica Biologica A.A. 2010-2011 Struttura delle Proteine Marco Nardini Dipartimento di Scienze Biomolecolari e Biotecnologie Università di Milano Macromolecole Biologiche Struttura Proteine Proteine:
Costituenti chimici della materia vivente
 Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
Costituenti chimici della materia vivente Le macromolecole biologiche Macromolecole (dal greco macros = grande) biologiche. Classi di composti biologici multifunzionali: Polisaccaridi proteine acidi
saccaridi glucidi (CH O) poli-idrossi chetoni aldeidi monosaccaridi oligo- e poli-saccaridi il glucosio amido cellulosa
 I carboidrati I carboidrati (o saccaridi o glucidi) hanno formula bruta (CH 2 O) n, dove n è maggiore di 3. Chimicamente sono poli-idrossi chetoni o aldeidi ed esistono sia in forma semplice (monosaccaridi)
I carboidrati I carboidrati (o saccaridi o glucidi) hanno formula bruta (CH 2 O) n, dove n è maggiore di 3. Chimicamente sono poli-idrossi chetoni o aldeidi ed esistono sia in forma semplice (monosaccaridi)
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA)
 La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
La chimica della vita: i composti organici. CARBOIDRATI LIPIDI PROTEINE ACIDI NUCLEICI (DNA, RNA) POLIMERI Le cellule sintetizzano un enorme numero di grosse molecole a partire da una ristretta serie di
1. Le biomolecole: Struttura e funzione delle proteine
 1. Le biomolecole: Struttura e funzione delle proteine Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) Le biomolecole Biomolecola:
1. Le biomolecole: Struttura e funzione delle proteine Corso 240/350: Didattica di biochimica e biologia molecolare con laboratorio (2 CFU) 16 ore) Marco Scocchi ( BIO/10-11) Le biomolecole Biomolecola:
LIPIDI. Steroidi Acidi grassi Trigliceridi Fosfolipidi Prostaglandine Vitamine liposolubili
 LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dal fatto di di non essere solubili in in acqua ma solubili in in solventi non polari aprotici. 1. 1. Acidi grassi 2. 2. Trigliceridi 3.
LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dal fatto di di non essere solubili in in acqua ma solubili in in solventi non polari aprotici. 1. 1. Acidi grassi 2. 2. Trigliceridi 3.
Amminoacidi. Struttura base di un a-amminoacido
 Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Amminoacidi Struttura base di un a-amminoacido Forma non ionizzata Forma ionizzata, sale interno (zwitterione) Il carbonio α di tutti gli α-amminoacidi (tranne la glicina) è asimmetrico (=chirale) D-alanina
Monosaccaridi essenziali
 Monosaccaridi essenziali Questi monosaccaridi sono normalmente assunti con la dieta e sono utilizzati per la biosintesi di glicoproteine etc. Ad esempio dall acido N-acetil-D-neuramminico hanno origine
Monosaccaridi essenziali Questi monosaccaridi sono normalmente assunti con la dieta e sono utilizzati per la biosintesi di glicoproteine etc. Ad esempio dall acido N-acetil-D-neuramminico hanno origine
I carboidrati. (CH 2 O)n n>3. Mono-, oligo-, polisaccaridi. n = 3 triosi n = 4 tetrosi n = 5 pentosi n = 6 esosi
 I carboidrati (CH 2 O)n n>3 Mono-, oligo-, polisaccaridi n = 3 triosi n = 4 tetrosi n = 5 pentosi n = 6 esosi I monosaccaridi sono derivati aldeidici e chetonici di alcoli poliossidrilici a catena lineare,
I carboidrati (CH 2 O)n n>3 Mono-, oligo-, polisaccaridi n = 3 triosi n = 4 tetrosi n = 5 pentosi n = 6 esosi I monosaccaridi sono derivati aldeidici e chetonici di alcoli poliossidrilici a catena lineare,
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH
 Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Presentano un gruppo amminico ( N 2 ) ed un gruppo carbossilico ( COO) nella stessa molecola C 3 N 2 C α * COO Acido 2-ammino propanoico (acido α-ammino propionico) STPA-Chimica Organica
Amminoacidi (1) Acido 2-ammino propanoico (acido α-ammino propionico) α * NH 2 CH 3 COOH. ) ed un gruppo carbossilico ( COOH) nella stessa molecola
 Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
Amminoacidi (1) Presentano un gruppo amminico ( NH 2 ) ed un gruppo carbossilico ( COOH) nella stessa molecola CH 3 NH 2 C H α * COOH Acido 2-ammino propanoico (acido α-ammino propionico) 1 Amminoacidi
MEMBRANE. struttura: fosfolipidi e proteine
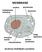 MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
MEMBRANE struttura: fosfolipidi e proteine I lipidi sono sostanze di origine biologica insolubili in acqua. Vi fanno parte: trigliceridi, fosfolipidi, colesterolo, sfingolipidi, alcoli alifatici, cere,
LIPIDI. Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici
 LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici 1.Acidi grassi 2.Trigliceridi 3.Fosfolipidi 4.Prostaglandine
LIPIDI Classe eterogenea di di sostanze organiche caratterizzate dall essere insolubili in in acqua ma solubili in in solventi non polari aprotici 1.Acidi grassi 2.Trigliceridi 3.Fosfolipidi 4.Prostaglandine
9) Scrivere un disaccaride formato dal β-d-galattosio e dall α-d-n-acetil-glucosammina legati da un legame glicosidico β(1-4).
 CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
CARBOIDRATI - AMMINOACIDI - PROTEINE 1) Scrivere la proiezione di Fisher del D-ribosio e del D-glucosio. La lettera D a cosa si riferisce? Disegnare inoltre il disaccaride ottenuto dalla condensazione
STRUTTURA E FUNZIONE DELLE PROTEINE
 STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
STRUTTURA E FUNZIONE DELLE PROTEINE Le PROTEINE sono i biopolimeri maggiormente presenti all interno delle cellule, dal momento che costituiscono dal 40 al 70% del peso secco. Svolgono funzioni biologiche
LEZIONE 2 COMPOSTI DEL CARBONIO: MACROMOLECOLE:
 LEZIONE 2 COMPONENTI CHIMICI DELLA CELLULA ACQUA COMPOSTI DEL CARBONIO: MACROMOLECOLE: ZUCCHERI ACIDI GRASSI PROTEINE NUCLEOTIDI percentuale di abbondanza relativa I componenti chimici di una cellula organismi
LEZIONE 2 COMPONENTI CHIMICI DELLA CELLULA ACQUA COMPOSTI DEL CARBONIO: MACROMOLECOLE: ZUCCHERI ACIDI GRASSI PROTEINE NUCLEOTIDI percentuale di abbondanza relativa I componenti chimici di una cellula organismi
24.1 La sostanze di importanza biologica sono per la maggior parte composti organici
 24 BIOCHIMICA 24.1 La sostanze di importanza biologica sono per la maggior parte composti organici La biochimica è la disciplina che studia in modo sistematico le sostanze chimiche nei sistemi viventi,
24 BIOCHIMICA 24.1 La sostanze di importanza biologica sono per la maggior parte composti organici La biochimica è la disciplina che studia in modo sistematico le sostanze chimiche nei sistemi viventi,
I Composti Organici. Le Biomolecole
 I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
I Composti Organici I composti organici sono molecole tutte contenenti carbonio. Essi comprendono. 1. composti di interesse energetico che sono gli Idrocarburi ( i derivati del petrolio), 2. composti a
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale.
 Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Lipidi: funzioni. Strutturale. Riserva energetica. Segnale. Lipidi:classificazione. Saponificabili Non saponificabili Semplici Complessi Prostaglandine Steroidi Cere Trigliceridi Fosfogliceridi Sfingolipidi
Amminoacidi - Peptidi - Proteine. Emoglobina
 Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Amminoacidi - Peptidi - Proteine Emoglobina 1 Emoglobina Gli amminoacidi sono le sostanze di base che costituiscono le proteine. Ogni proteina è caratterizzata da una precisa sequenza di mattoni di amminoacidi.
Irrancidimento (ossidazione) degli acidi grassi insaturi
 Irrancidimento (ossidazione) degli acidi grassi insaturi Aldeidi STPA-Chimica rganica Alcuni saggi sui grassi numero di acidità (titolazione in presenza di fenolftaleina con base forte diluita a temperatura
Irrancidimento (ossidazione) degli acidi grassi insaturi Aldeidi STPA-Chimica rganica Alcuni saggi sui grassi numero di acidità (titolazione in presenza di fenolftaleina con base forte diluita a temperatura
BIOLOGIA GENERALE. Alessandro Massolo Dip. Biologia Animale e Genetica c/o Prof. F. Dessì-Fulgheri (Via Romana 17) massolo@unifi.
 Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Biologia generale Massolo Alessandro massolo@unifi.it; Tel. 347-9403330 BIOLOGIA GENERALE Facoltà di Scienze della Formazione Scienze della Formazione Primaria Alessandro Massolo Dip. Biologia Animale
Indice generale 1. Introduzione alla biochimica 2. Acqua, ph, acidi, basi, sali, tamponi
 Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
Indice generale 1. Introduzione alla biochimica 1 Unità di misura 1 Energia e calore 3 Struttura dell atomo 3 Tavola periodica degli elementi 4 Legami chimici 8 Legami covalenti 8 Legami non covalenti
I composti più importanti dal punto di vista biologico, detti anche. BIOMOLECOLE, appartengono a quattro classi: carboidrati, proteine,
 I composti più importanti dal punto di vista biologico, detti anche BIMLELE, appartengono a quattro classi: carboidrati, proteine, acidi nucleici e lipidi. arboidrati: polimeri di monosaccaridi Proteine:
I composti più importanti dal punto di vista biologico, detti anche BIMLELE, appartengono a quattro classi: carboidrati, proteine, acidi nucleici e lipidi. arboidrati: polimeri di monosaccaridi Proteine:
LIVELLI DI STRUTTURA DELLE PROTEINE
 FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
FUNZIONI E STRUTTURA DELLE PROTEINE PROF.SSA AUSILIA ELCE Indice 1 INTRODUZIONE -------------------------------------------------------------------------------------------------------------- 3 2 LIVELLI
Livello di organizzazione degli esseri viventi
 Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Livello di organizzazione degli esseri viventi _Organismo; _Apparato; _Organo; _Tessuti; _Cellule; _Organelli cellulari; _Molecole. Atomo, elemento, molecola, composto, formula, legame, elettronegativita.
Liceo Scientifico Statale" A.ROMITA" CLASSE: 2C PROGRAMMA DI CHIMICA. ARGOMENTI: LA MOLE. La mole:unità di quantità e di sostanza.
 Liceo Scientifico Statale" A.ROMITA" CLASSE: 2C PROGRAMMA DI CHIMICA. ARGOMENTI: LA MOLE. La mole:unità di quantità e di sostanza. La costante di Avogadro. La massa molare. Relazione tra massa di una sostanza
Liceo Scientifico Statale" A.ROMITA" CLASSE: 2C PROGRAMMA DI CHIMICA. ARGOMENTI: LA MOLE. La mole:unità di quantità e di sostanza. La costante di Avogadro. La massa molare. Relazione tra massa di una sostanza
INDICE PARTE I CHIMICA. Autori Introduzione
 INDICE Autori Introduzione XI XIII PARTE I CHIMICA Capitolo 1 STRUTTURA DELL ATOMO 3 1.1 Teorie atomiche 3 1.2 Costituenti dell atomo 4 1.3 Numeri quantici 4 1.4 Tipi di orbitali 5 1.5 Aufbau 6 1.6 Sistema
INDICE Autori Introduzione XI XIII PARTE I CHIMICA Capitolo 1 STRUTTURA DELL ATOMO 3 1.1 Teorie atomiche 3 1.2 Costituenti dell atomo 4 1.3 Numeri quantici 4 1.4 Tipi di orbitali 5 1.5 Aufbau 6 1.6 Sistema
MACROMOLECOLE. Polimeri (lipidi a parte)
 MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
MACROMOLECOLE Monomeri Polimeri (lipidi a parte) Le caratteristiche strutturali e funzionali di una cellula o di un organismo sono determinate principalmente dalle sue proteine. Ad esempio: Le proteine
che è caratteristico degli alcoli (es CH 3 -CH 2 -OH etanolo) gruppo carbonilico che si trova in composti detti chetoni;
 LE BIOMOLECOLE 1. IL CARBONIO E I SUOI COMPOSTI Il carbonio è l'elemento base del mondo vivente. Ciò si deve alla sua particolare capacità di formare 4 legami covalenti, in genere molto forti, o con altri
LE BIOMOLECOLE 1. IL CARBONIO E I SUOI COMPOSTI Il carbonio è l'elemento base del mondo vivente. Ciò si deve alla sua particolare capacità di formare 4 legami covalenti, in genere molto forti, o con altri
Cellula batterica. ioni, piccole molecole 4% Fosfolipidi 2% DNA 1% RNA 6%
 Le macromolecole, assieme, costituiscono la maggior parte del contenuto secco degli organismi viventi Cellula batterica ioni, piccole molecole 4% Fosfolipidi 2% DNA 1% RNA 6% CLASSIFICAZIONE DEI CARBOIDRATI:
Le macromolecole, assieme, costituiscono la maggior parte del contenuto secco degli organismi viventi Cellula batterica ioni, piccole molecole 4% Fosfolipidi 2% DNA 1% RNA 6% CLASSIFICAZIONE DEI CARBOIDRATI:
RUOLI BIOLOGICI DELLE PROTEINE. Biochimica
 RUOLI BIOLOGICI DELLE PROTEINE Biochimica Il collagene una proteina strutturale Il collagene è un componente principale di tessuti quali la pelle, i capelli, i tendini, le ossa, il cartilagine, i vasi
RUOLI BIOLOGICI DELLE PROTEINE Biochimica Il collagene una proteina strutturale Il collagene è un componente principale di tessuti quali la pelle, i capelli, i tendini, le ossa, il cartilagine, i vasi
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA. Angela Chambery Lezione 6
 Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 6 La struttura secondaria delle proteine Concetti chiave: Il carattere planare di un gruppo peptidico limita la flessibilitàconformazionale
Corso di Laurea in Farmacia Insegnamento di BIOCHIMICA Angela Chambery Lezione 6 La struttura secondaria delle proteine Concetti chiave: Il carattere planare di un gruppo peptidico limita la flessibilitàconformazionale
Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone
 Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
I carboidrati sono detti anche idrati del carbonio, generati cioè da atomi di carbonio e acqua.
 LEZIONE DI CHIMICA: BIOMOLECOLE Glucidi ( carboidrati o zuccheri) I carboidrati sono detti anche idrati del carbonio, generati cioè da atomi di carbonio e acqua. Sono fonte di energia per l organismo e
LEZIONE DI CHIMICA: BIOMOLECOLE Glucidi ( carboidrati o zuccheri) I carboidrati sono detti anche idrati del carbonio, generati cioè da atomi di carbonio e acqua. Sono fonte di energia per l organismo e
Definizione Composti quaternari: C H O N S P Fe Mg I
 PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
PROTIDI Definizione Composti quaternari: C H O N S P Fe Mg I ORIGINE cellulare ogni cellula sintetizza le sue prote CARATTERISTICHE insolubili in acqua sensibili a variazioni di ph coagulano in presenza
Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone
 Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
Carboidrati Carboidrati puri : zucchero e amido nei cibi, cellulosa nel legno, carta e cotone Glucosio Carboidrati modificati: membrane cellulari, acidi nucleici, Da carbonio idrato: glucosio= C 6 H 12
LIPIDI. I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi.
 LIPIDI I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi. I lipidi sono composti idrofobi perché non sono solubili in acqua ma
LIPIDI I lipidi (la parola deriva dal greco lìpos, grasso) sono un gruppo di sostanze grasse presente in tutti gli organismi viventi. I lipidi sono composti idrofobi perché non sono solubili in acqua ma
le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. STRUTTURA TERZIARIA
 STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
STRUTTURA TERZIARIA le porzioni con strutture secondarie sono avvicinate e impaccate mediante anse e curve della catena. Le proteine globulari dopo aver organizzato il proprio scheletro polipeptidico con
